β—pH曲线在发动机冷却液评定中的应用
许扬++徐小鹏++汪玉瑄++李艳慧

摘要:使用储备碱度和由“β-pH曲线”得到的缓冲范围、终点pH值评价发动机冷却液缓冲能力及其对金属腐蚀倾向。分析全有机型发动机冷却液与混合型发动机冷却液的β-pH曲线,得到缓冲能力及其对金属腐蚀倾向特点,提出使用注意事项。考察分析国内外16个主流品牌发动机冷却液的β-pH曲线,总结国内外发动机冷却液缓冲能力及其对金属腐蚀倾向的差别。
关键词:发动机冷却液;β-pH曲线;缓冲范围;储备碱度;金属腐蚀倾向
中图分类号:TE626.32文献标识码:A
Application of β-pH Curve in the Evaluation of Engine Coolant
XU Yang, XU Xiao-peng, WANG Yu-xuan, LI Yan-hui
(China FAW Corporation Limited R&D Center, Changchun 130011, China)
Abstract:Buffering capacity and metal corrosion tendency of engine coolant were evaluated using reserve alkalinity, buffer area and the finish pH obtained through the β-pH curve. The β-pH curves of Organic Additive Technology (OAT)coolants and hybrid coolants were analyzed to get the characteristics of the buffering capacity and the metal corrosion tendency, and matters needing attention of using were proposed. The β-pH curves of 16 major engine coolant brands at home and abroad were inspected and analyzed, and the difference of buffering capacity and metal corrosion tendency between the domestic engine coolant and the foreign engine coolant was summarized.
Key words:engine coolant; β-pH curve; buffer area; reserve alkalinity; metal corrosion tendency
0引言
随着长寿命发动机冷却液的推出,发动机冷却液的金属腐蚀性和长期性能稳定性受到更多关注。现行的发动机冷却液实验室评定方法(参照GB 29743技术要求和试验方法)中,通常采用玻璃器皿腐蚀和储备碱度对发动机冷却液的长寿命进行评价。但在实际操作中,玻璃器皿腐蚀试验试验周期长、试验结果影响因素多等原因导致无法进行快速准确评定;储备碱度是对三乙醇胺、硼酸盐、磷酸盐等常见缓冲试剂[1]含量的表征,对于不含常见缓冲试剂的全有机型发动机冷却液可能失去了实际意义。
按照金属腐蚀热力学理论,每一种金属均存在其特有的Pourbaix图(电位-pH图)[2],通过Pourbaix图,可以得到金属的腐蚀区与钝化区对应的腐蚀电位区间和溶液pH值范围,在不采取控制腐蚀电位的方法时,溶液pH值范围决定了金属的腐蚀倾向,当溶液的pH值位于钝化区内,金属腐蚀倾向较小,反之腐蚀倾向较大。
发动机冷却液在使用过程中因受自身酸化、酸性气体介入等因素影响,pH值不断下降,为减少金属腐蚀倾向,发动机冷却液需要必要的缓冲能力,以维持pH值在金属钝化区内。为考察发动机冷却液pH值变化情况,使用定量的盐酸模拟发动机冷却液酸化过程,参照分析化学中缓冲容量概念[3],绘制“β-pH曲线”,计算发动机冷却液缓冲范围,结合储备碱度及加入定量盐酸后的终点pH值,评价发动机冷却液缓冲能力,通过对比Pourbaix图中金属钝化区pH值范围,对金属腐蚀情况进行预判。
1试验部分
1.1试验样品
50%乙二醇水溶液、22个国内外主流品牌发动机冷却液。
2试验讨论
2.150%乙二醇水溶液的缓冲能力
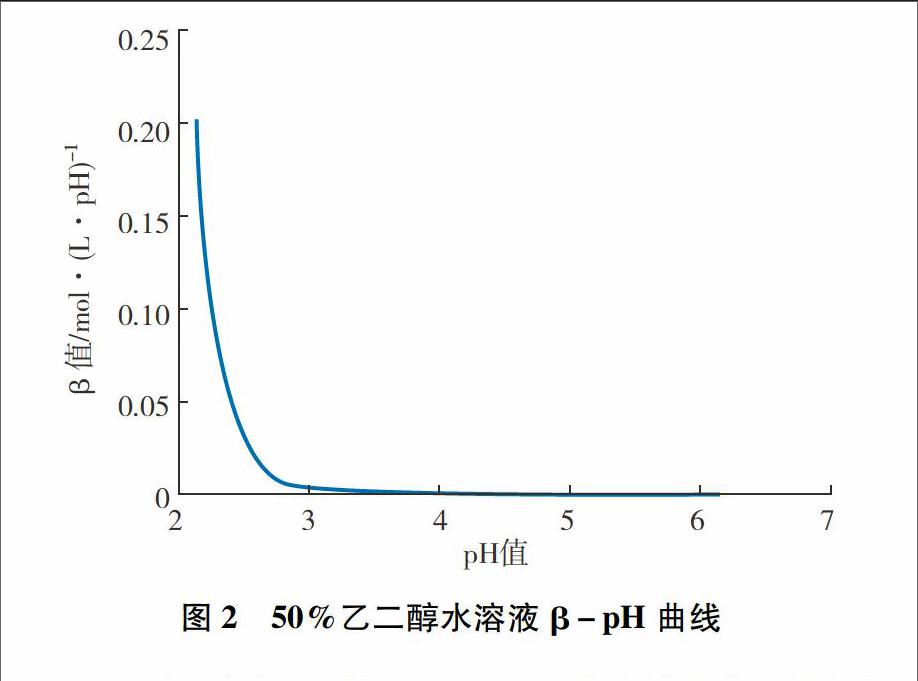
将50%乙二醇水溶液按照1.3配制试验液,记录pH滴定曲线,按照1.4数据处理方法绘制β-pH曲线,如图1、图2所示。
由图1、图2可知, 50%乙二醇水溶液经过稀释后,初始pH值在6.0以上,理论上可以通过滴定得到储备碱度,显然此时的储备碱度没有实际意义。由pH滴定曲线绘制得到的“β-pH曲线”表示50%乙二醇水溶液缓冲能力随pH值变化的情况,β越大,缓冲能力越强,pH值变化越小。当pH>3时,β≈0,此时50%乙二醇水溶液基本没有缓冲能力,pH值快速下降;当pH<3时,由于前期H+积累,试验液中H+浓度较大,盐酸提供的H+对试验液的pH值影响变小,β值快速增大,pH值变化缓慢,尽管此时β随pH值减小而快速上升,但不能体现发动机冷却液抵抗酸化的缓冲能力。
综上所述,50%乙二醇水溶液没有缓冲能力,储备碱度没有实际意义;β-pH曲线可以直观表现50%乙二醇水溶液在酸化过程中缓冲能力变化情况,间接说明pH值变化的快慢程度;发动机冷却液酸化后能够达到的最小pH值为2~3。
2.2发动机冷却液β-pH曲线
2.2.1全有机型发动机冷却液β-pH曲线
选取添加剂相同牌号不同的-35号、-45号、-50号全有机型发动机冷却液作为试验样品,按照1.3、1.4进行试验及数据处理,绘制β-pH曲线,如图3所示。
图3全有机型发动机冷却液β-pH曲线
由图3可知,配方相同牌号不同的三个全有机型发动机冷却液有相近的β-pH曲线,冰点越低,相同pH值下的β越大。从β-pH曲线变化趋势来看,在发动机冷却液酸化过程中,β持续增大,pH值持续下降,从pH≈6开始,β随pH值减小而快速上升,pH值变化较小,加入10 mL盐酸后,试验液pH值在5附近,冰点越高,pH值越小。
计算3个发动机冷却液的储备碱度、弱碱性环境下的缓冲范围,并记录终点pH值,见表1。
表1全有机型发动机冷却液缓冲能力
发动机冷却液储备碱度(pH)/mL1)缓冲范围/pH终点pH值2)OAT-35号6.00(5.52)4.80OAT-45号7.43(5.48)5.06OAT-50号7.48(5.54)5.12注:1)储备碱度单位中的pH表示计算储备碱度时的pH值,下同。
2)终点pH值为加入10 mL盐酸后试验液pH值,下同。
结合图3、表1可知,试验样品均具有较高的储备碱度,但在弱碱性环境下没有缓冲范围。当发动机冷却液发生酸化,溶液中的pH值调节剂与产生的H+发生中和反应,但pH值调节剂不具备缓冲能力,pH值将随H+增多而快速下降,当pH值超出表2中由Pourbaix图得到的金属钝化态pH值范围后,金属腐蚀倾向将会增大。
表2金属钝化态pH值范围(25℃)
金属种类钝化态pH值范围铝4~8.5铜7~12.5铁8.5~12.5铅/焊锡7.5~9.5
由于图3中终点pH值没有达到2~3,说明全有机型发动机冷却液自身在弱酸性环境中体现一定缓冲作用,但弱酸性环境下铁的腐蚀倾向相对较大,长时间的弱酸性环境将使铁质发动机腐蚀成水锈,进入发动机冷却系统,提高发动机冷却液中铁离子浓度,引起其他金属的腐蚀。因此,在不采取必要的腐蚀防护技术和严格的发动机冷却液监测程序的情况下,全有机型发动机冷却液不适合在铁质发动机的冷却系统中使用。
由于全有机型发动机冷却液存在弱碱性环境下pH快速下降的特点,加入pH<7的蒸馏水将引起pH值下降、β下降,pH值快速下降,各金属的腐蚀倾向增大。因此,在使用过程中要严格控制发动机冷却系统的密封性,如出现发动机冷却液严重泄露,应及时更换。
2.2.2混合型发动机冷却液β-pH曲线
选取添加剂相同牌号不同的-25号、-35号、-45号重负荷混合型发动机冷却液作为试验样品,按照1.3、1.4进行试验及数据处理,绘制β-pH曲线,如图4所示。
由图4可知,配方相同牌号不同的三个重负荷混合型发动机冷却液有相近的β-pH曲线,冰点越低,相同pH值下的β越大。从曲线的变化趋势来看,在pH≈6.5~10时,β-pH曲线出现凸峰,并在pH=8.3附近存在极值,此阶段pH值变化非常缓慢;从pH≈6开始,β缓慢上升,pH值缓慢下降,加入定量盐酸后,pH值达到3~4,冰点越高,pH值越小。
计算3个发动机冷却液的储备碱度、弱碱性环境下的缓冲范围,并记录终点pH值,见表3。
表3重负荷混合型发动机冷却液缓冲能力
发动机冷却液储备碱度
(pH)/mL 缓冲范围/pH终点pH值HEC-2-256.80(5.53)6.82~9.793.41HEC-2-357.99(5.49)6.50~9.714.10HEC-2-458.38(5.53)6.65~9.964.34由图4、表3可得,试验样品储备碱度较高,在弱碱性环境下共有的缓冲范围为6.8~9.7,在pH≈83时,β为极值,此时发动机冷却液pH值保持时间长。与表2对比,pH=8.3时,所有金属均能达到钝化态,金属腐蚀倾向较小,该发动机冷却液理论上可以在较长时间内对金属进行保护。
图4中β在弱碱性环境下出现极值,终点pH值接近2~3,表明混合型发动机冷却液在弱碱性环境下具有很强的缓冲能力,但当缓冲试剂消耗完,β上升缓慢,相比于全有机型发动机冷却液的pH值下降较快,缓冲能力差。因此,混合型发动机冷却液更适合使用在弱碱性环境下,当发动机冷却液酸化加强,缓冲试剂消耗完,金属腐蚀倾向将迅速增大。
混合型发动机冷却液因具有缓冲剂,pH值在较长时间内变化较小,但随发动机冷却液不断酸化,当pH值超出该发动机冷却液缓冲范围时,pH值将迅速下降,金属腐蚀倾向明显增大。因此,当发动机冷却液发生蒸发或泄露时,可以补加蒸馏水,但过多的补加将使缓冲剂严重稀释,缓冲容量下降,应及时补加同品牌发动机冷却液。
2.2.3国外主流品牌发动机冷却液β-pH曲线
选取8个国外主流品牌发动机冷却液作为试验样品,按照1.3、1.4进行试验及数据处理,绘制β-pH曲线,如图5所示。
图5国外主流品牌发动机冷却液β-pH曲线
由图5可知,8个国外主流品牌发动机冷却液β-pH曲线呈现三种形式。A7发动机冷却液的β-pH曲线与混合型发动机冷却液(如图4)相似,A4、A8发动机冷却液的β-pH曲线与50%乙二醇水溶液(如图2)相似,其余5个国外主流品牌发动机冷却液的β-pH曲线与全有机型发动机冷却液(如图3)相似。
A7发动机冷却液的β-pH曲线在pH≈5.5~8.5时出现凸峰,在pH=6.8附近出现极值,从pH≈5.5开始,β随pH值减小而快速上升,表明A7添加了一定量的缓冲试剂,使发动机冷却液pH值可以长时间维持在6~8之间,为金属提供长时间的保护,但pH值超出缓冲剂的缓冲范围后,pH值快速下降,增大金属腐蚀风险。
A4、A8发动机冷却液在pH>5.5时,β≈0,在pH≈3.5~5.5时A4的β-pH曲线出现凸峰,在pH=4.5附近出现极值,发动机冷却液此时体现出一定的缓冲能力;A8发动机冷却液从pH≈5开始,β随pH值减小而快速上升,升高过程中没有凸峰。A4、A8发动机冷却液在加入10 mL盐酸溶液后,终点pH值达到2~3之间,与图2比对可知,此时发动机冷却液已无抵抗酸化的能力,金属腐蚀倾向很大。
其余5个发动机冷却液在pH>6时,β较小,发动机冷却液缓冲能力体现不明显,从pH≈6开始,β随pH值减小而快速上升,但上升程度Δβ不同,如A3终点pH≈5,Δβ=0.08 mol/L·pH,A6终点pH≈4.5,Δβ=0.04 mol/L·pH, 发动机冷却液体现出不同的缓冲能力。由于终点pH值没有达到2~3之间,发动机冷却液中还有抵抗酸化的物质,但此时pH值过低,金属腐蚀倾向增大。
试验中发现,A1、A2发动机冷却液在接近终点时出现混浊,添加剂少量析出,如图6所示。析出的添加剂为弱酸性,短时间内增大了复合玻璃电极表面电极膜H+含量,pH值出现快速下降,表现为β下降,随着搅拌的继续,析出的添加剂分散到溶液中,pH值波动变小,β再次上升,在β-pH曲线上表现为出现凸峰。
计算8个发动机冷却液的储备碱度、弱碱性环境下的缓冲范围,并记录终点pH值,见表4。
由表4,国外主流品牌发动机冷却液的储备碱度普遍较小;除A4、A7发动机冷却液外,没有明显的缓冲范围,而A4的缓冲范围在酸性区域,对金属腐蚀保护较弱;除A4、A7发动机冷却液外,加入10 mL盐酸后终点pH值在4~5之间。从储备碱度、缓冲范围和终点pH值三方面来评价,A7发动机冷却液具有较好缓冲能力,理论上能够对金属起到长期的腐蚀防护作用。
2.2.4国内主流品牌发动机冷却液β-pH曲线
选取8个国内主流品牌发动机冷却液作为试验样品,按照1.3、1.4进行试验及数据处理,绘制β-pH曲线,如图7所示。
由图7可知,8个国内主流品牌发动机冷却液β-pH曲线呈现三种形式。B5发动机冷却液β-pH曲线类似于全有型发动机冷却液(如图3),B3、B4发动机冷却液β-pH曲线类似于50%乙二醇水溶液(如图2),其余5个发动机冷却液的β-pH曲线与混合型发动机冷却液(如图4)相似。
B5发动机冷却液为全有机型发动机冷却液,在pH>6时,β≈0,发动机冷却液在弱碱性条件下无明显缓冲作用;在pH=5.5时,有大量添加剂析出,静置后出现白色沉淀,如图8(c)所示,在β-pH曲线上体现为β出现突跃;终点pH值约为4.5,表明此发动机冷却液中的添加剂在弱酸性条件下能够抵御pH值快速波动,但此时的缓冲作用对金属腐蚀防护作用很小。
B3、B4发动机冷却液的β-pH曲线存在两个凸峰,分别在pH=7.0~9.5与pH=4.0~5.0,在pH=8.2附近与pH=4.5附近出现极值,弱碱性环境下形成的凸峰为缓冲剂作用结果,弱酸性环境下的凸峰为添加剂析出产生的结果(如图8(a)、(b)所示);终点pH值达到2~3之间,此时发动机冷却液没有缓冲能力。从B3、B4发动机冷却液的β-pH曲线来看,凸峰出现的位置基本相同,终点pH值基本相同,可以初步认为两个发动机冷却液使用相同的缓冲剂体系。
其余5个发动机冷却液的β-pH曲线与图4相似,但缓冲范围不同。在pH=7.0~9.5时,β-pH曲线有凸峰,在pH=8.2附近出现极值,由于缓冲剂加入量不同,凸峰高度不同,终点pH值不同,如B6发动机冷却液的峰值最大(β=0.0234 mol/L·pH),终点pH值为5.22,B1发动机冷却液峰值最小(β=0.00394 mol/L·pH),终点pH值为3.99。
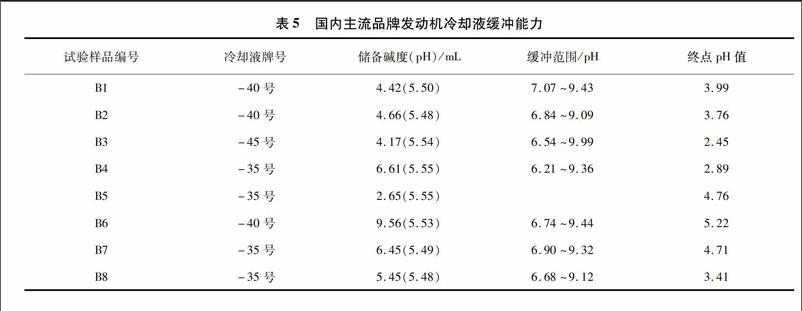
计算8个发动机冷却液的储备碱度、弱碱性环境下的缓冲范围,并记录终点pH值,见表5。
由表5可得,国内主流品牌发动机冷却液的储备碱度普遍较大,B6发动机冷却液以其高储备碱度、适宜的缓冲范围、较高的终点pH值,表现出非常好的缓冲能力,发动机冷却液在长时间内对金属腐蚀倾向小。
对比表4与表5,从储备碱度来看,国外主流品牌发动机冷却液普遍小于国内主流品牌发动机冷却液;从缓冲范围来看,国外主流品牌发动机冷却液普遍没有缓冲范围,国内主流品牌发动机冷却液缓冲范围通常为pH=7~9;从终点pH值来看,国外主流品牌发动机冷却液普遍为4~5,国内主流品牌发动机冷却液通常为3~5。
国外主流品牌发动机冷却液中,A7发动机冷却液具有较高的储备碱度和适宜的缓冲范围,可以满足发动机冷却液较长时间的使用寿命,而在国内主流品牌发动机冷却液中,B6发动机冷却液具有更高的储备碱度,缓冲范围在偏碱性区域,更有利于对金属腐蚀的防护,缓冲能力与金属腐蚀防护能力优于A7发动机冷却液。
3结论
通过分析发动机冷却液储备碱度与β-pH曲线,得到以下结论:
(1)“储备碱度”概念存在局限性,对于全有机型发动机冷却液可能失去实际意义。
(2)使用10 mL盐酸模拟乙二醇水溶液的酸化过程,发动机冷却液pH值最小为2~3。
(3)储备碱度与β-pH曲线相结合,可以更全面的表征发动机冷却液缓冲能力,通过对比缓冲范围与金属钝化态pH值范围可以对金属腐蚀倾向进行预判。
(4)全有机型发动机冷却液使用过程中,需要严格控制发动机冷却系统密封性。出现发动机冷却液泄露时,不能添加蒸馏水,要整体更换发动机冷却液。
(5)混合型发动机冷却液使用过程中,如遇到发动机冷却液泄露或蒸发,可以采用补加蒸馏水的方式暂时解决,但当发动机冷却液pH值超过其缓冲范围时,应及时更换。
(6)大部分国外主流品牌发动机冷却液储备碱度较低,没有缓冲范围,终点pH值在4~5之间,β-pH曲线类似于全有机型发动机冷却液。
(7)大部分国内主流品牌发动机冷却液储备碱度较高,缓冲范围在7~9之间,终点pH值为3~5,β-pH曲线类似于混合型发动机冷却液。
4研究展望
发动机冷却液缓冲范围虽然一定程度上预测了金属腐蚀倾向,但缓蚀剂的加入会改变金属腐蚀热力学相图,金属钝化态的pH值范围发生变化,仅从储备碱度和β-pH曲线无法得到相关信息。因此,对于金属腐蚀倾向的预判还需要进一步考察缓蚀剂对于金属钝化态pH值范围的影响,结合长时间的腐蚀试验结果得到准确的结论。
参考文献:
[1] ASTM D1121-98 Standard Test Method for Reserve Alkalinity of Engine Coolants and Antirusts[S].
[2] 张天胜,张浩,高红,等.缓蚀剂 [M].2版.北京:化学工业出版社,2008:37-39.
[3] 邹明珠,许宏鼎,于桂荣,等.化学分析 [M].2版.长春:吉林大学出版社,2001:81.

