奥卡西平致Stevens-Johnson综合征和中毒性表皮坏死松解症的特点及基因相关性分析Δ
陈 晨,江 祎,师少军,刘易慧#(.华中科技大学同济医学院附属协和医院药学部,武汉 4300;.武汉市新洲区人民医院药学部,武汉 43400)
奥卡西平致Stevens-Johnson综合征和中毒性表皮坏死松解症的特点及基因相关性分析Δ
陈 晨1*,江 祎2,师少军1,刘易慧1#(1.华中科技大学同济医学院附属协和医院药学部,武汉 430022;2.武汉市新洲区人民医院药学部,武汉 431400)
目的:探讨奥卡西平致Stevens-Johnson综合征(SJS)和中毒性表皮坏死松解症(TEN)的临床特点及其基因多态性。方法:计算机检索中国知网(CNKI)、万方、维普、PubMed、EMBase、SpringerLink等数据库,对有关奥卡西平引起严重皮肤不良反应的个案报道文献进行整理和分析。结果:收集文献12篇,获取奥卡西平引发SJS/TEN的病例报道13例。奥卡西平的严重皮肤不良反应发生于男性多于女性,不良反应大多发生在用药后1~14 d,经过糖皮质激素、抗过敏药物等治疗均能痊愈,没有致死性病例报道。8例患者进行了基因型检测,其中6例患者为HLA-B*1502阳性,2例为HLA-B*1518/B*4001(HLA-B*1502的变异)。结论:应当严密监测奥卡西平的不良反应,注意患者用药教育与随访,必要情况下通过检测HLA-B*1502基因可指导临床合理使用奥卡西平,优化临床用药方案。
奥卡西平(Oxcarbazepine,商品名:Trileptal),是一种新型抗癫痫药。美国食品与药物管理局(FDA)于2000年批准其用于治疗成人及4~6岁儿童的部分性癫痫发作,作为单药治疗或辅助治疗。自奥卡西平上市以来,其药品不良反应(ADR)Stevens-Johnson综合征(SJS)和中毒性表皮坏死松解症(TEN)的发生率比预计的要高出3~10倍,且起病过程急,病势、病情严重,且病死率极高,尤其是TEN。2005年,美国新的药品说明书中已增加了该药品有严重的皮肤过敏反应的警告。近年来多项研究显示,芳香族抗癫痫药(AED)诱发的严重皮肤不良反应(cADRs)与人类白细胞抗原(Human leucocyte antigen,HLA)B家族的基因具有强相关性,显示该疾病存在基因易感性[1]。并且不同种族人群的HLA基因位点不同。在中国、泰国及东南亚地区其他国家,HLA-B*1502基因与卡马西平诱导的SJS/TEN呈现出强相关性[2-6],奥卡西平次之。本文通过对国内外奥卡西平引起SJS和TEN的案例报道进行统计分析,为进一步增强医护人员对奥卡西平安全性的认知,促进临床合理用药提供参考。
1 资料来源
通过计算机分别以“Oxcarbazepine”and“Stevens-Johnson syndrome”or“Toxic epidermal necrolysis”or“Severe cutanous adverse drug reactions”or“Severe drug eruption”为英文关键词、“奥卡西平”and“Stevens-Johnson综合征”or“史-约综合征”or“史蒂文-约翰逊氏综合征”or“中毒性表皮坏死松解症”or“严重皮肤药品不良反应”or“重症药疹”为中文关键词,分别检索PubMed、EMBase、SpringerLink、维普中文科技期刊数据库、中国知网全文数据库(CNKI)等数据库,检索时间自建库起至2016年6月21日。同时,根据需要追溯查出与本研究有关的全部文献并获取全文。
将检索到的文献依据以下标准严格筛选:排除因用药差错所致不良事件,排除文献中未说明和未验证到可能是由奥卡西平引起的;排除未明确诊断为SJS/TEN的报道;排除个案汇总性质的二次综述性文献;排除有一稿多投或抄袭嫌疑的病例报道;排除重复报道案例。
2 方法
阅读纳入文献,分别统计患者年龄、性别、过敏史及用药史、用法用量、基因型文献来源,以及ADR临床表现、出现时间、治疗措施与转归情况等项目。
3 结果
3.1 基本情况
通过主题词结合关键词的形式,共检索出相关文献20篇,通过筛选共得到涉及SJS/TEN个案报道的文献12篇[7-18],其中中文文献4篇,英文文献8篇,发表时间为2007-2016年,提取有效病例13例。其中,男性患者9例(69.23%),女性患者4例(30.77%);平均年龄(29.8± 25.5)岁,最小3岁,最大81岁,具体见表1。
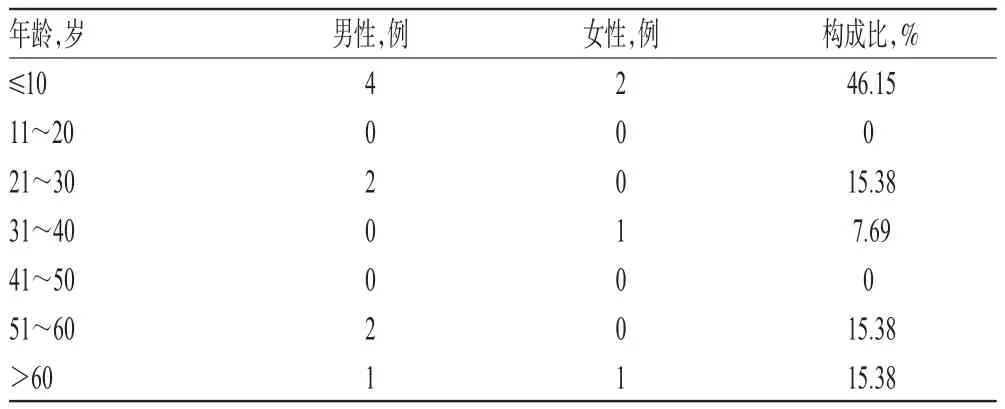
表1 发生SJS/TEN患者的年龄和性别分布Tab 1 Distribution of age and gender of SJS/TEN patients
3.2 原患疾病与过敏史
13例奥卡西平所致SJS/TEN病例中,原患疾病为癫痫的患者10例,三叉神经痛2例,病毒性脑炎1例。1例患者既往有药物过敏史(具体致敏药物不详),1例明确无过敏史,其余患者过敏史文献中未交待,具体见表2。
3.3 用药情况
奥卡西平说明书推荐起始剂量为每日600 mg(8~10 mg/kg),分2次给药。为了获得理想的效果,可以每隔1周增加日剂量,每次增加剂量不超过600 mg。每日维持剂量范围在600~2 400 mg,绝大多数患者对每日900 mg的剂量即有效果。本研究纳入的13例患者中,除1例未报道具体用法用量以外,其余12例用药剂量均在150~1 200 mg/d范围内,多低于常规推荐剂量,单次增加剂量也低于600 mg/d。联合用药的有4例,联用药物有苯妥英钠、左乙拉西坦、托吡酯、甲钴胺片和阿奇霉素。4例患者停用奥卡西平后更换为其他抗癫痫药物(拉莫三嗪、左乙拉西坦、托吡酯),皮损未见加剧。
3.4 SJS/TEN发生时间分布
奥卡西平ADR发生时间最快出现在用药1 d后,最迟为用药40 d(连续用药10 d)后,大多分布在14 d以内。由表2中的数据可知,奥卡西平引起cADRs的损害多为迟发型,但是往往在用药初期就有所表现,应引起临床医护人员的高度重视。
3.5 临床表现
SJS是通过药物或其他抗原引起人类组织相容性复合物限制性表达,从而激发细胞毒性T细胞引起的特定变应性反应;表现为严重渗出性多形性红斑,累及黏膜,进一步发展出现水疱、皮肤黏膜溃疡及脱落、TEN等。因此临床上常认为SJS和TEN是同一种疾病的不同表现形式,皮肤脱落少于体表面积10%为SJS,大于30%为TEN,介于10%~30%者为SJS与TEN共存,表2中最后一个病例即表现为SJS/TEN重叠[18]。由表2还可以看出,除皮肤黏膜的变化外,SJS/TEN也常伴发热、结膜出血以及心肾等多脏器全身性损害,疾病进展较快。
3.6 治疗与转归
13例患者中,除4篇文献未进行相关描述外,其余9例患者均给予停药及对症治疗,其中8例给予了激素和抗过敏药物治疗,2例使用了丙种球蛋白。13例患者中,1例痊愈,7例缓解,5例未描述。13例患者治疗时间不等,最短10 d,最长1个月,具体见表2。
3.7 基因相关性
13例患者中,共有8例进行了基因型测定,其中6例表现为HLA-B*1502阳性,2例为HLA-B*1518/B*4001(HLA-B*1518/B*4001为HLA-B*1502的变异)。
4 讨论
4.1 奥卡西平致cADRs的临床特点和治疗手段
研究数据表明,SJS发病率约为每百万人1.2~7例,约20%发生于儿童,男性多于女性[19]。统计表1中奥卡西平致ADR的性别比例发现,男性明显多于女性,这与文献数据一致。但是年龄分布上无明显区别,可能与本次纳入病例数较少有关。
分析发现,即使按照说明书推荐剂量,也依然可能发生严重的ADR,表明奥卡西平诱发SJS/TEN与用药剂量无明显相关性。国内外研究也指出,奥卡西平引起SJS/TEN的预后同样与药物的类型及剂量无关,反而受药物使用时间影响较大[20-21]。轻型药疹患者在出现皮疹时需及时停用致敏药物,能避免疾病的继续恶化。本研究中的1例患者在出现皮疹后并未及时停药,导致ADR进一步加重[7],与文献报道一致。
SJS和TEN的治疗目前以激素冲击治疗和抗过敏治疗为主,但TEN患者全身应用皮质激素至今仍有争议,因其可能增加脓毒血症并发症的风险,除非在大面积皮肤损害发生之前使用。严重患者在进行相关治疗的基础上,可早期经验性预防性抗感染[22]。同时还需加强皮肤护理、营养支持等措施,并注意眼部和其他器官的并发症。
很多个案报道分析了静脉注射免疫球蛋白对TEN的治疗作用。French LE等[23]对8个非对照临床研究综述后发现,8项研究中有6项认为注射免疫球蛋白对治疗TEN有益,尤其是在疾病的早期给予足够剂量时(>2 g/kg)。
4.2 奥卡西平诱发SJS/TEN的基因相关性
分析13例患者的发病地区可以发现,SJS/TEN地域分布上以亚洲为主,这种地域差异性可能与人种和基因型相关。目前已经明确,在汉族人群中,卡马西平诱发SJS/TEN与HLA-B*1502等位基因呈100%相关,但是综述发现奥卡西平引起SJS/TEN的病例中,尚存在其他基因型,证明奥卡西平可能存在其他相关的等位基因,如HLA-B*1518/B*4001。Song JS等[24]报道了卡马西平的另一个可能相关基因位点为HLA-A*3101,但奥卡西平尚未见关于此基因型的相关报道。奥卡西平是卡马西平的10-酮基衍生物,由于具有不同的代谢通路,被认为比卡马西平安全。在整个人群中,估计每年奥卡西平诱导的SJS/TEN几率为每百万人中0.5~6例[25],在台湾地区的汉族人群中奥卡西平致SJS相对风险较卡马西平低30~40倍。与卡马西平相比较,奥卡西平相对安全且ADR少,因此已作为部分性发作伴或不伴继发全身强直-阵挛发作的一线用药。
4.3 临床用药注意事项
奥卡西平是卡马西平的结构类似物,两者存在交叉过敏现象。卡马西平过敏者有25%~30%对奥卡西平过敏,如服用卡马西平出现剥脱性皮炎者,应避免服用奥卡西平。对于有药物过敏史的患者,尤其是卡马西平过敏的患者,用药过程中应特别注意观察患者有无发生过敏反应。如有服用卡马西平出现严重过敏史者,应避免服用奥卡西平。
英国药品和健康产品管理局(MHRA)在2013年11月发布的药品安全警示中提示,不同抗癫痫药的特征不同,在不同厂商产品之间转换使用抗癫痫药可能导致ADR发生或癫痫失控[26]。刘宁等[27]的综述研究也显示有多例将卡马西平转换为奥卡西平治疗后出现皮疹的案例,特别是转换比例过高的患者。本研究表明,使用奥卡西平发生SJS/TEN的患者度过急性期后,换用拉莫
三嗪、左乙拉西坦和托吡酯治疗原发疾病,并未产生新发的ADR,这与前述研究认为抗癫痫药物之间的转换易导致严重不良反应的观点相悖,但也可能是由于不同转换药物和转换比例的差异性所致。相关问题还有待进一步考察研究。

表2 13例奥卡西平SJS/TEN案例报道统计表Tab 2 Statistical table for 13 cases reports of SJS/TEN induced by oxcarbazepine
13例患者中有4例同时联用了其他药物,包括苯妥英钠、左乙拉西坦、托吡酯、甲钴胺和阿奇霉素。根据李里等[28]的分析,奥卡西平可升高苯妥英钠、苯巴比妥和丙戊酸钠血药浓度20%~30%,降低拉莫三嗪、卡马西平和托吡酯的谷浓度,但没有明显证据证明苯妥英钠可以升高奥卡西平的血药浓度。唑吡酯是细胞色素P450酶(CYP450)的温和诱导剂,Nallani SC等[29]发现只有高浓度的托吡酯对CYP3A4才存在诱导作用,常规剂量的唑吡酯对肝药酶的作用非常微弱。左乙拉西坦的蛋白结合率低(<10%),经人体吸收后仅34%被代谢,且不能通过CYP450、葡萄糖苷酸转移酶(UGT)或环氧化水解酶与其他药物发生药动学相互作用[30],因此药物相互作用较小。甲钴胺主要用于治疗周围神经病变,和奥卡西平的作用机制、代谢途径均有很大差异,两者不存在明显的相互作用。综上所述,以上4种药物均不会升高奥卡西平的血药浓度,因此可以排除联用这些药物导致ADR的发生。
阿奇霉素和奥卡西平均为肝药酶抑制剂,梁艳龙等[14]认为阿奇霉素可升高奥卡西平血药浓度,且患儿在患脑炎后半年内对抗癫痫药物敏感性高,可能也是导致ADR发生的原因。因此,在临床使用中应尽量避免联用。
5 结语
奥卡西平由于疗效肯定、安全性较高,在临床上的应用越来越广泛。但是其引起cADRs的机制尚不明确,本文概述了近10年来国内外文献关于奥卡西平引发SJS/TEN临床表现和防治措施的报道,旨在引起临床工作者的关注。在奥卡西平的临床应用中做好ADR监测和防治工作:用药前询问患者家族史和药物过敏史;用药剂量正规化、合理化;尽量减少联合用药;用药期间定期密切观察患者情况,有条件者可以进行基因检测,HLA-B*1502和HLA-B*1518阳性患者尽量避免使用,阴性患者在使用中也需谨慎,监测患者各项生理指标和血药浓度。若出现轻微的ADR可视病情减量服药,严重的ADR须停药并对症治疗。
[1] Chung WH,Hung SI,Hong HS,et al.Medical genetics:a marker for Stevens-Johnson syndrome[J].Nature,2004,428(6982):486.
[2] Alfirevic A,Jorgensen AL,Williamson PR,et al.HLA-B locus in Caucasian patients with carbamazepine hypersensitivity[J].Pharmacogenomics,2006,7(6):813-818.
[3] Mehta TY,Prajapati LM,Mittal B,et al.Association of HLA-B*1502 allele and carbamazepine-induced Stevens-Johnson syndrome among Indians[J].Indian J Dermatol Venereol Leprol,2009,75(6):579-582.
[4] Locharernkul C,Loplumlert J,Limotai C,et al.Carbamazepine and phenytoin induced Stevens-Johnson syndrome is associated with HLA-B*1502 allele in Thai population[J].Epilepsia,2008,49(12):2087-2091.
[5] Chang CC,Too CL,Murad S,et al.Association of HLAB* 1502 allele with carbamazepine-induced toxic epidermal necrolysis and Stevens-Johnson syndrome in the multiethnic Malaysian population[J].Int J Dermatol,2011,50(2):221-224.
[6]Man CB,Kwan P,Baum L,et al.Association between HLAB*1502 allele and antiepileptic drug-induced cutaneous reactions in Han Chinese[J].Epilepsia,2007,48(5):1015-1018.
[7] 张丽,周权.奥卡西平致严重药疹反应1例[J].天津药学,2007,19(5):34.
[8]Chen Y,Chu CY,Hsiao CH.Oxcarbazepine-induced Stevens-Johnson syndrome in a patient with HLA-B*1502 genotype[J].J Eur Acad Dermatol Venereol,2009,23(6):702-703.
[9] Lin LC,Lai PC,Yang SF,et al.Oxcarbazepine-induced Stevens-Johnson syndrome:a case report[J].Kaohsiung J Med Sci,2009,25(2):82-86.
[10] Hung SI,Chung WH,Liu ZS,et al.Common risk allele in aromatic antiepileptic-drug induced Stevens-Johnson syndrome and toxic epidermal necrolysis in Han Chinese [J].Pharmacogenomics,2010,11(3):349-356.
[11] 何学莲,王芳琳,吴革菲,等.奥卡西平诱发的Stevens-Johnson综合征的临床特点及基因表达[J].实用儿科临床杂志,2011,26(5):360-362.
[12] Wal P,Wal A,Pandey U,et al.Genetic predisposition to oxcarbazepine induced Stevens-Johnson syndrome[J].Indian J Crit Care Med,2011,15(3):173-175.
[13] Sharma SR,Sharma N,Yeolekar ME.Oxcarbazepine-induced Stevens Johnson syndrome:a rare case report[J]. Indian Dermatol Online J,2011,2(1):13-15.
[14] 王菊莉,陶英贤,曹洪涛,等.奥卡西平诱发Stevens-Johnson综合征1例报道[J].山西医科大学学报,2013,44(6):501-502.
[15] 梁艳龙,郝小生,王江涛,等.儿童奥卡西平致Stevens-Johnson综合征1例报告[J].中风与神经疾病杂志,2014,31(4):365.
[16] Sun D,Yü CH,LIU ZS,et al.Association of HLA-B* 1502 and*1511 allele with antiepileptic drug-induced Stevens-Johnson syndrome in central China[J].J Huazhong Univ Sci Technolog Med Sci,2014,34(1):146-150.
[17] Guleria VS,Sharda C,Rana T,et al.Oxcarbazepine induced toxic epidermal necrolysis:a rare case report[J].Indian J Pharmacol,2015,47(4):459-461.
[18] Poletti-Jabbour J,Wiegering-RospigliosiA,Pereyra-Elías R,et al.Carbamazepine and oxcarbazepine:reflections afteran oxcarbazepine-induced Stevens-Johnson syndrome/toxic epidermal necrolysis overlap[J].Eur J Clin Pharmacol,2016,72(8):1031-1032.
[19] Finkelstein Y,Soon GS,Acuna P,et al.Recurrence and outcomes of Stevens-Johnson syndrome and toxic epidermal necrolysis in children[J].Pediatrics,2011,128(4):723-728.
[20] Chia FL,Leong KP.Severe cutaneous adverse reactions to drugs[J].Current Opinion in Internal Medicine,2007,6(5):304-309.
[21] 陈子怡,周列民,周珏倩,等.抗癫痫药物所致重型药疹及危险因素分析[J].医学信息,2006,19(11):1989-1990.
[22] 吝战权,关欣,沈司京,等.临床药师参与卡马西平致重症型多形红斑1例的临床实践[J].中国药房,2011,22(38):3645-3646.
[23] French LE,Trent JT,Kerdel FA.Use of intravenous immunoglobulin in toxic epidermal necrolysis and Stevens-Johnson syndrome:our current understanding[J].Int Immunopharmacol,2006,6(4):543-549.
[24] Song JS,Kang ES,Joo EY,et al.Absence of HLA-B* 1502 and HLA-A*3101 Alleles in 9 Korean patients with antiepileptic drug-induced skin rash:a preliminary study [J].Ann Lab Med,2014,34(5):372-375.
[25] Dogan EA,Usta BE,Bilgen R,et al.Efficacy,tolerability and side effects of oxcarbazepine monotherapy:a prospective study in adult and elderly patients with newly diagnosed parial epilepsy[J].Epilepsy Behav,2008,13(1):156-161.
[26]CFDA.英国警示在不同抗癫痫药之间转换使用的潜在风险[EB/OL].(2014-01-08)[2016-09-10].http://www. cfda.gov.cn/WS01/CL0389/96361_1.html.
[27] 刘宁,齐晓涟.奥卡西平致皮疹7例分析[J].医药导报,2010,29(5):959-961.
[28] 李里,淑华,朱雨岚,等.新型抗癫痫药之间及其与传统抗癫痫药的相互作用和机制[J].中国新药杂志,2007,16(2):102-113.
[29] Nallani SC,Glauser TA,Hariparsad N,et al.Dose dependent induction of cytochrome P450(CYP)3A4 and activation of pregnane X receptor by topiramate[J].Epilepsia,2003,44(12):1521-1528.
[30] Anderson GD,Saneto RP.Modified-release formulations of second-generation antiepileptic drugs:pharmacokinetic and clinical aspects[J].CNS Drugs,2015,29(8):669-681.
Analysis of the Characteristics and Gene Relationship of Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis Induced by Oxcarbazepine
CHEN Chen1,JIANG Yi2,SHI Shaojun1,LIU Yihui1(1.Dept.of Pharmacy,Union Hospital,Tongji Medical College,Huazhong University of Science and Technology,Wuhan 430022,China;2.Dept.of Pharmacy,Wuhan Xinzhou District People’s Hospital,Wuhan 431400,China)
OBJECTIVE:To investigate the clinical characteristics and gene polymorphism of oxcarbazepine(OXC)-induced Stevens-Johnson syndrome(SJS)and toxic epidermal necrolysis(TEN).METHODS:Retrieved from CNKI,Wanfang,VIP,PubMed,EMBase,SpringerLink and other databases,case reports about OXC-induced severe ADR were summarized and analyzed.RESULTS:Twelve literatures were collected,and 13 case reports about OXC-induced SJS/TEN were obtained.Male had more OXC-induced severe skin ADR than female.ADR mostly occurred during 1-14 d after medication.All patients were cured with treatment of glucocorticoid and antiallergy,without death case.Genotyping for 8 patients were performed and 6 of them showed the presence of HLA-B*1502 allele.While HLA-B alleles of 2 patients were HLA-B*1518/B*4001,which was the variation of HLA-B*1502.CONCLUSIONS:OXC-induced ADR should be monitored closely.Great importance should be attached to patient education and follow-up program.HLA-B*1502 gene detection should be performed to guide rational use of OXC and optimize clinical drug use plan.
Oxcarbazepine;Stevens-Johnson syndrome;Toxic epidermal necrolysis;HLA-B*1502 gene
R971+.6;R969.3
A
1001-0408(2017)05-0620-06
2016-09-14
2016-10-31)
国家科技支撑计划子课题(No.2013BAI06B04)
*药师,硕士。研究方向:临床药学。电话:027-85351703。E-mail:cenzi1987@163.com
#通信作者:主管药师,博士。研究方向:临床药学。电话:027-85351703。E-mail:kafkaliu@163.com
DOI10.6039/j.issn.1001-0408.2017.05.12
关键词奥卡西平;Stevens-Johnson综合征;中毒性表皮坏死松解症;HLA-B*1502

