不同产地百合药材中8种活性成分的分析与评价
张黄琴+严辉+钱大玮+朱振华+郭盛+郭兰萍+唐志书+段金廒

[摘要]該研究采用UPLCTQMS联用技术,对百合中8种成分进行分析测定。35个批次百合药材中王百合苷E、王百合苷F、王百合苷C及王百合苷B的质量分数分别在0604 0×10-1~1862×10-1,0680 0×10-2~4475×10-2,0700 0×10-3~2965×10-1,0170 0×10-1~4724 mg·g-1;绿原酸、咖啡酸、原儿茶醛及阿魏酸的质量分数分别在6827×10-3~1607×10-3,0111 0×104~7971×10-3,0593 7×10-3~2962×10-3,2606×10-2~4589×10-2 mg·g-1。进行主成分分析,绘制PCA(principal components analysis)得分图及VIP图,35批百合药材被分成以产地为区分的2组,2个主产地百合样品中,阿魏酸和咖啡酸在2个产地的百合中含量差异较大,其他6种成分含量在两产地间相差较小。通过主成分分析的F综合评分,可将样品进行排序,结果发现,在综合排名的前10位,有8种百合为安徽霍山百合。建立基于的UPLCTQMS用于百合多指标的质量评价方法,具有准确、高效、便捷等优点,为百合药材质量控制提供依据。
[关键词]百合; 含量测定; UPLCTQMS; 主成分分析; 相关性分析
Analysis and evaluation of eight active ingredients in
Lilium lancifolium from different regions
ZHANG Huangqin1, YAN Hui1, QIAN Dawei1*, ZHU Zhenhua1, GUO Sheng1,
GUO Lanping2, TANG Zhishu3, DUAN Jinao1
(1Jiangsu Collaborative Innovation Center of Chinese Medicinal Resources Industrialization, National and Local Collaborative
Engineering Center of Chinese Medicinal Resources Industrialization and Formulae Innovative Medicine, Nanjing University of
Chinese Medicine, Nanjing 210023, China;
2State Key Laboratory Breeding Base of Daodi Herbs, China Academy of Chinese Medical Sciences, Beijing 100700, China;
3Shanxi Collaborative Innovation Center of Chinese Medicinal Resources Industrialization, Shanxi University of Chinese Medicine,
Xianyang 712083, China)
[Abstract]This study established a rapid UPLCTQMS/MS method for determination of eight active ingredients in Lilium lancifolium The contents range of regaloside E, F, C and B are as follows: 0604 0×10-11862×10-1, 0680 0×10-24475×10-2, 0700 0×10-32965×10-1, 0170 0×10-14724 mg·g-1; the contents of chlorogenic acid, caffeic acid, protocatechualdehyde and ferulic acid, within the range of 6827×10-31607×10-3, 0011 1×10-37971×10-3, 0593 7×10-32962×10-3, 2606×10-24589×10-2 mg·g-1, respectively According to PCA (principal components analysis) plotting, 35 batches can be divided into two categories, namely Anhui Huoshan and Hunan Longshan The main different elements between these two categories are caffeic acid and ferulic acid according to the VIP (variable importance in the projection) points figure Based on comprehensive principal component values, there are eight batches of L lancifolium from Huoshan among the comprehensive ranking of ten The UPLCTQMS method for simultaneous analysis of eight active ingredients is accurate, efficient and convenient. This result can provide scientific basis for quality control of L lancifolium
[Key Words]Lilium lancifolium; determination; UPLCTQMS; principal components analysis; correlation analysis
百合药材为百合科植物卷丹Lilium lancifolium Thunb、百合L brownii F E Brown var viridulum Baker或细叶百合L pumilum DC的干燥肉质鳞叶[1]。其味甘,性寒,有养阴润肺、清心安神、止咳祛痰之功。用于治疗阴虚燥咳、劳嗽咳血、肺痈、老年人慢性支气管炎、神经衰弱、失眠心悸、精神恍惚等症[23]。现代研究表明,百合含酚性甘油酯类、有机酸类、生物碱类、甾体皂苷类和黄酮类等活性成分,其中酚性甘油酯类化合物,包括王百合苷E、王百合苷F、王百合苷C、王百合苷B、1O阿魏酰甘油等,具有抗氧化、抗肿瘤、抗增殖、免疫调节等作用[46]。目前有关百合中有效成分的分析方法主要是采用HPLCUV测定薯蓣皂苷元等皂苷类成分;总多糖及总黄酮的含量测定多运用紫外可见分光光度法;其元素含量采用ICPAES,ICPMS测定;亦有应用LCMS测定百合中酚性甘油酯的含量的报道[714],但所报道的测定方法中,每一种方法只针对单一结构类型的成分进行测定,并且其中单黄酮成分及另一类活性成分有机酸的含量测定方法尚未见报道。本文建立了应用UPLCTQ/MS同时测定百合中特征性成分酚性甘油酯、黄酮及有机酸类成分的分析方法,通过一次测定即能完成百合中3类活性成分的含量分析,是一个较全面快速的百合质量评价方法。并用于目前我国百合药材的主产地湖南龙山、安徽霍山[1517]栽培品种卷丹的分析评价。为百合药材的质量控制与临床用药提供依据。
1材料
11仪器
ACQUITY UPLC系统(二元高压泵,自动进样器,柱温箱,二极管阵列检测器,Waters公司);Xevo TQ/MS质谱系统(Waters公司);MassLynxTM质谱工作站(Waters公司);ML204电子分析天平(1/10万)、MS105电子分析天平(1/1万)(梅特勒托尼多仪器有限公司);Millipore Q纯水系统(美国Millipore公司);KQ250E型超声波清洗器(昆山禾创超声仪器有限公司);Anke GL16G Ⅱ型离心机(上海安亭科学仪器厂)。
12试药与试剂
王百合苷E、王百合苷F、王百合苷C、王百合苷B均为本实验室从百合药材中分离自制,其化学结构经1HNMR,13CNMR及ESIMS分析确认,纯度经HPLCUV检测均大于98%。乙腈、甲醇、甲酸(TEDIA)、绿原酸、咖啡酸、原儿茶醛、阿魏酸(成都普菲德生物科技有限公司)。
百合样品为实地采集,经南京中医药大学段金廒教授鉴定为百合科植物卷丹L lancifolium的干燥肉质鳞叶,共采集了35批百合样品,其中S1~S18为湖南龙山百合,S19~S35为安徽霍山百合,凭证标本存放于江苏省中药资源产业化过程协同创新中心。
2方法
21供试品溶液的制备
取各批次百合药材供试品(40目)约05 g,精密称定,置于具塞锥形瓶,加50%甲醇20 mL,称重,静置2 h,室温超声30 min,称重,以50%甲醇补足失重,摇匀,离心10 min(13 000 r·min-1)。取上清液适量,经022 μm的微孔滤膜滤过后,取续滤液作为供试品溶液。以干燥品计算供试品各类成分的含量。
22对照品溶液的制备
分别取绿原酸、咖啡酸、原儿茶醛、阿魏酸、王百合苷E、王百合苷F、王百合苷C、王百合苷B对照品适量,精密称定,用甲醇溶解配制成对照品储备液;取适量各成分储备液,加甲醇稀释定容,配制成混合对照品溶液,其中各成分质量浓度分别为0484 0,0436 0,0420 0,0620 0,0638 0,0717 0,1064,2010 g·L-1的混合对照品储备液。取上述混合对照品溶液用甲醇稀釋成6份不同浓度的混标工作液。
23UPLCTQMS分析条件
色谱分析条件:Waters ACQUITY UPLC BEH C18(21 mm ×100 mm,17 μm)色谱柱;柱温35 ℃。流动相乙腈(A),01%甲酸水溶液(B),梯度洗脱(0 ~ 2 min,3% A;2 ~ 6 min,3%~ 10% A;6 ~ 9 min,10%~15% A。流速04 mL·min-1;进样量 2 μL。
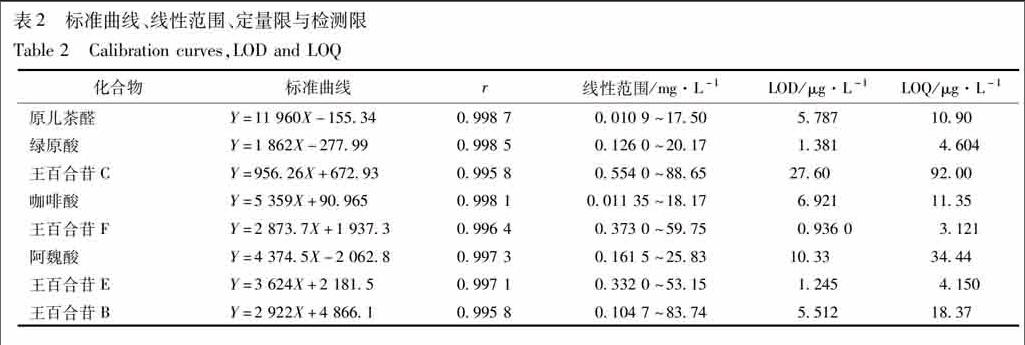
质谱检测条件ESI源;扫描方式ESI+,ESI-模式;多反应检测(MRM);毛细管电压30 kV;锥孔电压30 V;萃取电压30 V;离子源温度150 ℃;脱溶剂气温度500 ℃;锥孔气流量50 L·h-1;脱溶剂气流量1 000 L·h-1,辅助气流015 mL·min-1。各类成分的质谱参数见表1,色谱图见图1。
张黄琴等:不同产地百合药材中8种活性成分的分析与评价
24线性试验及方法学考察
241标准曲线与定量限
精密量取22项下混标工作液按23项下的分析条件进行测定。以被测化合物的峰面积(Y)对浓度(X)进行线性回归,并按信噪比(S/N)为10和3分别计算被测组分的定量限(LOQ)和检测限(LOD)。结果见表2,各成分线性良好,r均在0995 8以上。
242精密度试验
取中浓度混合对照品溶液,在上述色谱条件下分别在1日内重复进样6次和在连续3日内重复进样3次以测定所分析的化学成分的峰面积,以各指标成分含量的RSD来评价日内及日间精密度。
结果见表3,各成分日内精密度RSD≤28%,日间精密度RSD≤30%。
243重复性试验
取S1号样品6 份,按照21项下方法制备供试品溶液,分别进样分析,以样品中各指标成分含量的 RSD 值来评价其重复性。结果见表3,重复性RSD≤31%。
244稳定性试验
取S1号样品6 份,按照21项下方法制备供试品溶液,置于4 ℃保存,分别于0,2,4,8,12,24 h分别取样,进行UPLCMS/MS分析,以各指标成分含量,计算RSD,考察方法的稳定性。结果见表3,稳定性RSD≤35%。
245加样回收率试验
取025 g已知含量的样品9份(S1),每份精密称定,加入样品中各成分量的80%,100%,120%的对照品,各平行3份,按照供试品溶液的制备方法处理并按上述条件测定,计算平均回收率和RSD。结果见表3,平均加样回收率9521%~1060%,RSD≤41%均符合分析要求。
25数据处理
将测得数据导入EZ info软件(Waters公司),进行主成分分析(principal components analysis,PCA),得各样品的得分图。采用偏最小二乘法(partial least squares method,PLS)分析得到各指标的VIP值,依据VIP值的大小判断各个指标对分类的重要程度。利用SPSS得出各指标的综合因子,根据综合得分,给出各批次的排名。相关性分析使用SPSS210。
3结果
31样品测定
各样品按21项下的方法制得供试品溶液。取各供试品溶液,按23项下的条件进样测定,测定结果见表4。百合样品中王百合苷E的范围为0604 0×10-1~1862×10-1 mg·g-1;王百合苷F的范围为0680 0×10-2~4475×10-2 mg·g-1;王百合苷C的范围为0700 0×10-3~2965×10-1 mg·g-1;王百合苷B的范围为0170 0×10-1~4724 mg·g-1;绿原酸的范围为6827×10-3~1607×10-3 mg·g-1;咖啡酸的范围为0111 0×10-4~7971×10-3 mg·g-1;原儿茶醛的范围为0593 7×10-3~2962×10-3 mg·g-1;阿魏酸的范围为2606×10-2~4589×10-2 mg·g-1。
32各项指标间的主成分分析
将测得百合中8种成分进行分析,应用EZ info,SPSS 210统计软件对原始数据进行标准化处理。
321EZ info软件绘制PCA得分图及VIP图
将测定数据导入EZ info(Waters公司)软件进行主成分分析,通过降维建立包含第1个主成分
t[1]与第2个主成分t[2]二维空间的PLSDA分类模型,见图2。第1个主成分轴是原始数据矩阵方差最大方向,第2个主成分轴是方差次大方向,降维时,最大限度保留有用信息,寻找能够使不同产地样品得到最大分离的方向。由图2分析得出,以8种物质含量为变量,进行主成分分析,绘制PCA得分图,35批百合药材被分成以产地为区分的2组。
采用偏最小二乘法分析得到各个指标的VIP值,见图3,阿魏酸、咖啡酸的VIP值均大于1,表明这2种成分在2个产地的百合中含量差异性较大;绿原酸,原儿茶醛,RegC,RegE,RegB,RegF的VIP值较小,表明这些成分含量在2个产地间相差较小。
322SPSS软件进行主成分分析
为比较不同批次百合药材的质量差异,用SPSS进行主成分分析,根据综合因子,给出各批次的排名。
3221主成分筛选及其贡献率主成分的特征值及贡献率是选择主成分的依据,见表5,描述了主成
分分析初始值对原有变量的总体描述情况。从表中可知前2个主成分的累积方差贡献率达到8536%,因此选择前2个主成分,它们基本代表百合样品中此8种成分的信息。
经方差最大正交旋转后的因子载荷矩阵,用以鉴别有实际意义的因子见表6。从中可以看到第1个主因子和王百合苷E、王百合苷F、王百合苷C、王百合苷B、绿原酸呈高度正相關;第2个主因子和咖啡酸、阿魏酸呈高度正相关。因为总方差85%以上的贡献来自前2个主因子,所以可以认为王百合苷E、王百合苷F、王百合苷C、王百合苷B、绿原酸、咖啡酸、阿魏酸是百合的特征成分。
3222计算因子得分因子得分系数矩阵,根据主成分计算公式可以得到前2个主成分与原来8项指标的线性组合:F1=0210 RegE+0210 RegF+0211 RegC+0196 RegB+0204绿原酸-0029咖啡酸+0061原儿茶醛-0031阿魏酸;F2=-0036RegE+0019 RegF-0016RegC-0040 RegB+0103绿原酸+0428咖啡酸+0260原儿茶醛+0426阿魏酸;计算综合得分F=0574 1F1+0279 5F2,见表7。
按综合评价函数计算得出不同样品的综合得分(F)及得分排名见表8。综合排序的名次越前,表明就该8项指标而言,该样品的质量较好,反之,质量就较差。
根据主成分分析结果,在综合排名的前10位,有8种百合为安徽霍山百合。初步判断,以该8种成分为评价指标时,安徽霍山百合质量略好于湖南龙山。
33各项指标间的相关性分析
百合药材中该8项指标的相关性见表9。结果显示,不同产地百合中该8项指标之间有RegFRegE、RegC绿原酸、阿魏酸咖啡酸等共12对呈显著正相关;且无呈显著负相关对。
4讨论
41供试品溶液制备方法的确定
在正式实验前,对提取溶剂及料液比分别做了相关单因素考察。在溶剂倍量一定时,分别用30%,50%,80%甲醇、乙醇进行提取;在溶剂体积分数确定时,分别考察了20,40,60,80倍量料液比提取百合药材,经过进样分析得出以50%的甲醇为提取溶剂,料液比为40倍时,提取效果最好。
42分析方法的选择
本实验测得百合样品中酚性甘油酯类、有机酸类及黄酮类成分量低至千分之几,如绿原酸的为0000 682 7%~0007 971%。HPLC与UPLC虽对百合样品中成分均有紫外吸收,但检测灵敏度较低,而各类成分含量均较低,因此本研究选择灵敏度高的UPLCTQMS分析方法同时测定百合药材中的8种成分。
43不同产地百合药材的质量评价
运用主成分分析法对药材多指标进行综合评价,是一个科学、合理、全面的评价药材质量的统计方法[18]。本研究中,首先为研究2个产地百合药材组分上的差异,对2个产地共35批百合药材中8个成分进行分析,对于该类复杂数据,利用主成分分析对数据降维处理得PCA得分图及VIP图,图2可以清楚、直观地看出,百合样品被分成以产地为区分的2组,图3反映出阿魏酸、咖啡酸的VIP均大于1,表明这两种成分在2个产地的百合中含量差异性较大,由此可以基本判定2个产地的划分是以阿魏酸和咖啡酸为指标的。随之,为比较不同批次百合药材的质量差异,用SPSS进行主成分分析,根据综合因子,给出各批次的排名,在综合排名的前10位,有8种百合为安徽霍山百合。初步判断,以该8种成分为评价指标时,安徽霍山百合质量略好于湖南龙山。
相关性分析旨在研究2个变量之间的变化趋势[19],本研究对百合药材中的8个成分进行了相关性分析,由相关性分析结果可知,4种酚性甘油酯类成分含量相互间均有极大的相关性,提示该4种酚性甘油酯类成分在百合药材中的含量是相互促进的,某种酚性甘油酯含量高,其余的也会协同升高。
同时值得注意的是,酸类成分中绿原酸的含量与4种酚性甘油酯类成分含量也成高度相关,这一特点的具体原因有待实验的进一步探讨。
百合药材中除了含量较高的多糖及皂苷类,本文所测的这几类成分亦是百合的特征性成分与活性成分。酚性甘油酯是百合的特征性成分亦是其功效成分,研究表明酚性甘油酯类有一定的抗氧化活性,与百合养阴润肺、清心安神、止咳祛痰等功效紧密相关。黄酮类成分、有机酸类也具有较好的生物活性[9,13]。雖然这些成分的含量较低,却亦是其主要的功效成分。故本文所建立的同时测定百合中这3类成分的方法,可以为全面评价百合药材的质量提供一种切实可行的参考。
[参考文献]
[1]中国药典一部[S] 2015: 132.
[2]黄燕萍 百合的研究现状[J] 中国药业, 2010, 19(8):88
[3]丁敬敏, 叶爱英, 姚成 ICPAES法测定百合中的微量元素[J] 广东微量元素科学, 2008, 15(4):37
[4]聂慧, 严辉, 钱大玮,等 加工方法对百合质量的影响研究[J] 中国现代中药, 2013, 15(4):308
[5]Luo J, Li L, Kong L Preparative separation of phenylpropenoid glycerides from the bulbs of Lilium lancifolium, by highspeed countercurrent chromatography and evaluation of their antioxidant activities[J] Food Chem, 2012, 131(3):1056
[6]Cheng W Y, Kuo Y H, Huang C JIsolation and identification of novel estrogenic compounds in Yam Tuber (Dioscorea alata cv. Tainung No2)[J]. J Agric Food Chem, 2007, 55(18):7350.
[7]高淑怡, 李卫民, 高英 HPLC法测定百合、卷丹、细叶百合中3种甾体皂苷的含量[J] 中药新药与临床药理, 2012, 23(6):675
[8]傅春燕, 刘永辉, 李明娟,等 HPLC测定中药百合中2个甾体皂苷的含量[J] 天然产物研究与开发, 2012, 24(9):1250
[9]胡文彦 江苏产宜兴百合活性研究与质量评价[D] 镇江: 江苏大学, 2007
[10]傅春燕, 刘永辉, 李明娟,等 紫外可见分光光度法测定不同产地龙牙百合中皂苷含量[J] 广东微量元素科学, 2011, 18(5):55
[11]高彦宁, 周日宝, 童巧珍,等 不同来源百合中总皂苷元含量的比较研究[J] 湖南中医药大学学报, 2007, 27(3):16
[12]曲伟红, 周日宝, 童巧珍,等 百合产地加工方法对百合质量影响的研究[J] 湖南中医杂志, 2004(4):73
[13]聂慧, 严辉, 钱大玮,等 百合药材UPLC特征图谱及特征峰QTOFMS分析研究[J] 中药材, 2013, 36(7):1087
[14]聂慧 百合药材质量影响因素探讨[D]镇江:江苏大学, 2014
[15]杨茜 龙山县百合种植现状及增产提质政策与技术研究[D]. 长沙: 湖南农业大学, 2014
[16]潘清平,周日宝,贺又舜,等龙山县百合种植基地概况[J] 中医药导报, 2003, 9(6):56
[17]张黄琴, 严辉, 钱大玮,等 不同产地百合药材中无机元素的分析与评价[J] 中国现代中药, 2016, 18(8):960
[18]严辉,段金廒,钱大玮,等我国不同产地当归药材质量的分析与评价[J]中草药,2009, 40(12):1988
[19]雷连娣,欧阳荔,刘雅琼,等不同产地黄芪中元素分布特征及相关性分析[J]中国中药杂志,2008, 33(3):255
[责任编辑丁广治]
[收稿日期]20160922
[基金项目]中央本级重大增减支项目(2060302);国家自然科学基金项目(81373978)
[通信作者]*钱大玮,研究员,硕士生导师,Tel: (025) 85811916,Email: qiandwnj@126com

