健康人群全身动态13N-NH3·H2O PET/CT显像13N-NH3·H2O的生物分布及辐射吸收剂量评估
张芳玲,易 畅,余冬兰,赵彬良,史新冲,张祥松*
(1.中山大学附属第一医院影像科,2.设备科,广东 广州 510080)
健康人群全身动态13N-NH3·H2O PET/CT显像13N-NH3·H2O的生物分布及辐射吸收剂量评估
张芳玲1,易 畅1,余冬兰2,赵彬良1,史新冲1,张祥松1*
(1.中山大学附属第一医院影像科,2.设备科,广东 广州 510080)
目的 探讨健康人群13N-NH3·H2O PET/CT显像中13N-NH3·H2O的生物分布和主要器官的辐射吸收剂量。方法 对5名健康志愿者在注射666~814 MBq13N-NH3·H2O后进行全身PET/CT扫描,获得每名受试者的连续动态图像。通过CT二维轴位图像手动勾画ROI,并在PET图像中找出相应层面,按照医学内照射剂量计算(MIRD)方法评估13N-NH3·H2O的吸收剂量。结果 心脏、肝及双肾13N-NH3·H2O摄取最高,其次为胰腺、脑组织、脾脏和胃。心脏的吸收剂量最高,为(7.14±3.63)×10-3mGy/MBq。受试者全身辐射吸收剂量为(2.11±0.44)×10-3mGy/MBq,全身有效剂量为(6.58±1.23)×10-3mSv/MBq。结论13N-NH3·H2O作为重要的心肌显像示踪剂,用于人体全身PET/CT显像的辐射剂量是安全的。
正电子发射型体层摄影术;辐射剂量;健康人;13N-NH3·H2O
13N-NH3·H2O是一种测定心脏和脑组织等局部血流量的示踪剂[1-2],作为氮代谢的主要物质,其在谷氨酰胺合成中也具有重要作用。既往曾有学者[3-4]对13N-NH3·H2O在人体部分组织器官的辐射剂量进行研究,但受限于研究设备(均为SPECT),不可全身连续动态扫描。目前关于PET/CT人体13N-NH3·H2O显像辐射剂量的研究主要为动物实验,少数临床研究的样本量也均相对较小,且多为单纯PET扫描,而非PET/CT[5-6]。本研究对5名健康志愿者进行全身动态13N-NH3·H2O PET/CT成像,以医学内照射剂量计算方法(medical internal radiation dosimetry method, MIRD)对人体主要组织器官进行辐射剂量评估,以期为临床安全应用13N-NH3·H2O提供参考依据。
1 资料与方法
1.113N-NH3·H2O的制备 采用在线合成法,以Cyclone-10/5回旋加速器(IBA)通过[16O(p,α)13N]核反应产生13N-NH3,并在13N-NH3中加入少量乙醇,防止13N氧化。13N-NH3·H2O的放化纯度达99%,总合成时间≤10 min。
1.2 一般资料 征集健康志愿者共5名(表1),男3名,女2名,年龄57~78岁,平均(65.0±8.2)岁,既往身体健康,常规体格检查、血液及尿液分析等实验室检查、精神科检查均正常。本研究经我院医学伦理委员会批准,所有受试者均签署知情同意书。
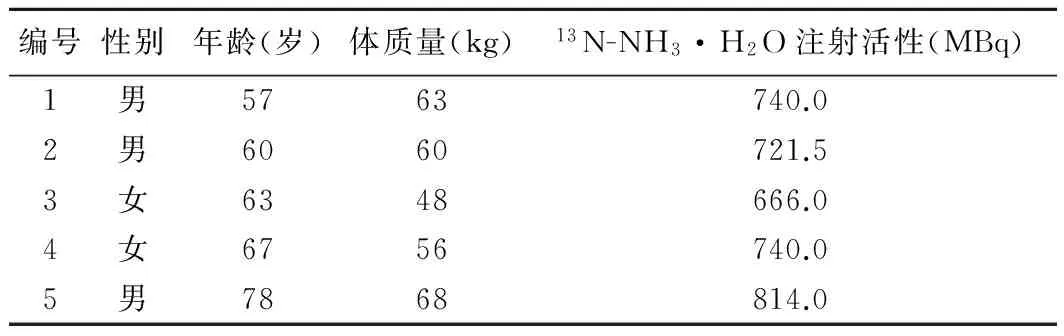
表1 5名健康志愿者的一般资料及13N-NH3·H2O的注射活性
1.3 仪器与方法 采用Philips Gemini GXL 16 PET/CT扫描仪。所有受试者在注射放射性同位素前至少禁食8 h。经低剂量CT(low dose CT, ldCT)扫描对图像进行衰减校正。CT扫描参数:峰值电压140 kV,管电流50 mAs,螺距0.813,球管旋转时间0.5 s。对受试者注射666~814 MBq的13N-NH3·H2O后分别进行5次连续全身动态扫描。依据每名受试者的身高,选择9或10种检查床位置(视野15 cm)。前2次二维模式全身扫描每次检查扫描时间为1 min,随后2次扫描时间增加至1 min 10 s,最后1次扫描时间为1 min 30 s。每名受试者1~5次扫描的开始时间分别为13N-NH3·H2O 注射后0.5、12.5、25、40和55 min。全身图像重建采用二维有序子集最大期望算法(OSEM),进行4次迭代,包含15个子集,高斯滤波5.14 mm,变焦为1。
1.4 图像分析 将所有图像数据均传至Philips Gemini工作站。测量分析的源器官包括脑、甲状腺、双肺、心脏、肝、胆囊、胃、双肾、胰腺、脾及骨髓。并将肌肉组织纳入生物分布分析,另对膀胱进行辐射吸收剂量分析。骨髓摄取以脊柱和股骨头为参考,心脏和胃的ROI分别设定于心壁和胃壁。除骨髓和膀胱外,其余所有ROI的选择均以CT作为参考,在第1次扫描的PET二维轴位图像中进行手工勾画。由于放射性药物的排泄可导致膀胱大小和形态发生变化,因此膀胱的ROI在每次扫描中均需重新勾画;骨髓的ROI在冠状位图像中进行勾画。分别获得各脏器的时间-放射性活度曲线(time-activity curves, TAC);计算每个源器官的累积活度,以进行辐射吸收剂量分析。剩余活性为每个时间点全身总活性减去所有已知源器官的活性[7]。
1.4.1 放射性滞留时间 每个源器官不同时间点的衰减活性以放射性摄取活度分数(percentage of the injected dose, %ID)表示,%ID=各源器官的活度/总的注射活度×100%;并通过TAC的曲线下面积(area under the curve, AUC)估算源器官的放射性滞留时间。采用Matlab 7.0软件,采用非线性最小二乘回归算法,单指数或双指数函数迭代,获得各源器官衰减校正的TAC,从零至无穷大积分获得的AUC,即为放射性滞留时间[8]。获得的膀胱%ID包括尿液的总活性,故收集每名受检者的尿液并测量其活性,从膀胱总活性中减去尿液活性,获得校正的膀胱活性。虽然每名受试者的排泄时间为注射13N-NH3·H2O后71~87 min,但因时间间隔较短(仅6~7 min),本研究假设最后1次扫描至排泄之前膀胱的总活性恒定。膀胱的放射性滞留时间为TAC中零至最后1次扫描的时间加最后1次扫描至自然衰退的时间[9]。
1.4.2 吸收剂量 靶器官的辐射吸收剂量参照标准70 kg成年男性的吸收分数计算。采用标准MIRD算法,S因子的值通过查表格获得[10]。计算靶器官的平均总吸收剂量(mean total absorbed dose,Dk),Dk=∑[τ0s(rk←r0)],其中τ0为源器官的滞留时间,rk为靶器官,ro为源器官。有效剂量(effective dose, ED)计算公式:E=∑WtHt,其中Wt为靶器官的权重因子,Ht为靶器官的剂量当量,Ht=WRDk,WR为辐射的权重因子。由于伽马射线和13N激发的正电子的权重因子为1,因此Ht数值等同于Dk。
2 结果
在13N-NH3·H2O注射前及研究结束后5名受试者的生命体征均平稳。其中1名受试者不同时间13N-NH3·H2O的生物分布见图1,其心脏、肝及双肾可见较高的放射性浓聚;胰腺、骨髓、双肺、脾、胆囊、胃和脑呈中等浓聚;甲状腺摄取随时间延长而减低,膀胱摄取随时间增加。
各器官衰减校正的TAC见图2。放射性摄取活度最高者为肝,其最高峰出现在第1帧采集中,峰值%ID为(26.10±7.76)%。双肺、脑、双肾、骨髓、心脏、胃、脾的峰值%ID出现在注射13N-NH3·H2O后0.5 min左右。膀胱的累计活度符合双指数曲线,由此估计通过膀胱排泄的%ID,获得膀胱的峰值%ID为(0.84±0.66)%。
5名受试者的源器官平均放射性滞留时间见表2。全身13N-NH3·H2O滞留时间为(8.29±2.30)×10-2h,肝的滞留时间最长,甲状腺的滞留时间最短。
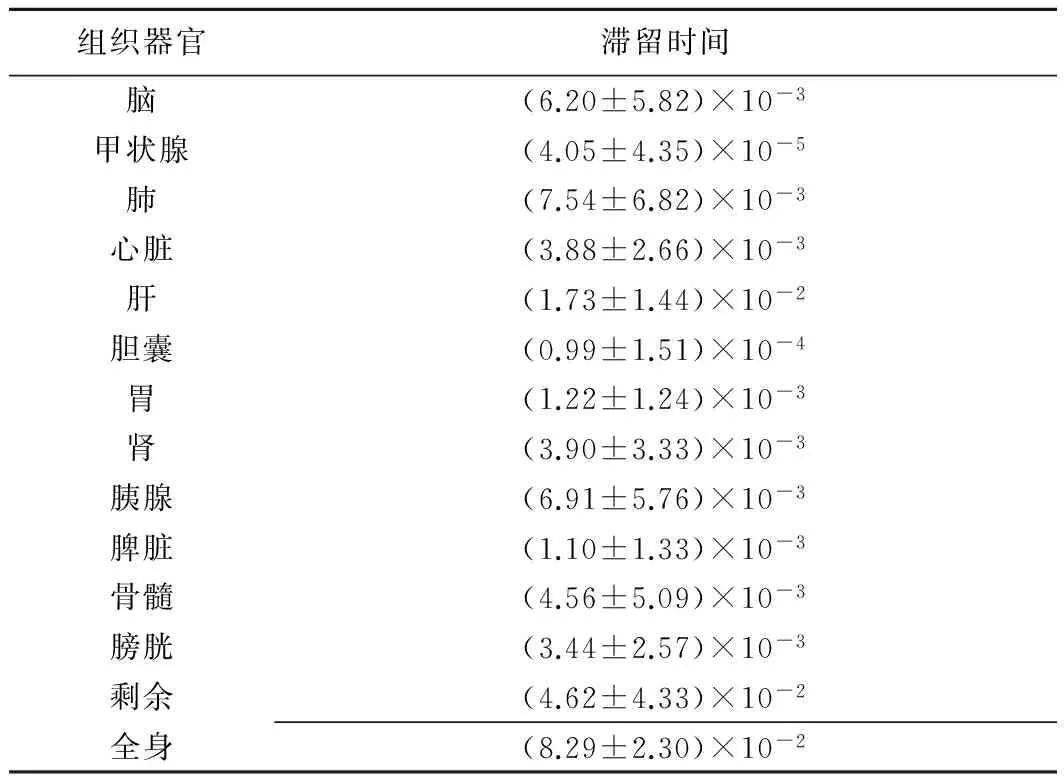
表2 源器官13N-NH3·H2O滞留时间(h,n=5)
每名受试者单个靶器官的辐射吸收剂量见表3。心脏的吸收剂量最高,为(7.14±3.63)×10-3mGy/MBq,其次为双肾[(6.02±3.53)×10-3mGy/MBq]、骨髓[(5.30±3.13)×10-3mGy/MBq]、肝[(4.94±2.83)×10-3mGy/MBq],甲状腺的吸收剂量较低,为(1.50±0.79)×10-3mGy/MBq。受试者全身吸收剂量为(2.11±0.44)×10-3mGy/MBq,全身ED为(6.58±1.23)×10-3mSv/MBq。每名受试者单次13N-NH3·H2O PET/CT扫描辐射吸收剂量为555~740 MBq,ED为3.65~4.87 mSv。
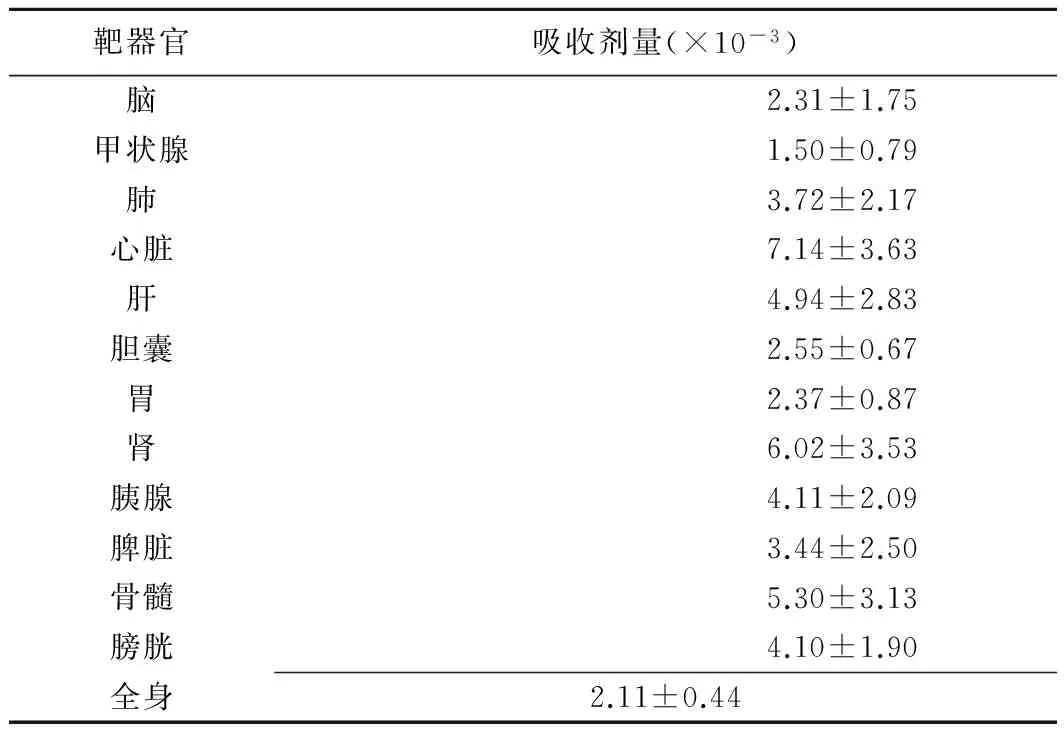
表3 靶器官13N-NH3·H2O辐射吸收剂量(mGy/MBq,n=5)
3 讨论
本研究基于健康志愿者全身PET/CT动态显像评估13N-NH3·H2O的生物分布和辐射吸收剂量,发现心脏的吸收剂量在所有脏器中最高[(7.14±3.63)×10-3mGy/MBq],可能因笔者假定包括血池在内所有放射性均为心壁的摄取,高估了心壁的实际吸收剂量。13N-NH3·H2O通过肾脏及肝胆系统排泄,使双肾及肝的吸收剂量较高[11],分别为(6.02±3.53)×10-3mGy/MBq和(4.94±2.83)×10-3mGy/MBq。本研究结果显示,受试者全身吸收剂量为(2.11±0.44)×10-3mGy/MBq,与Lockwood[3]研究报道的0.001 5 mGy/MBq相似。本研究发现,尽管最后1次扫描膀胱有很强的放射性,但排尿后其吸收剂量减低,为(4.10±1.90)×10-3mGy/MBq,可能由于13N半衰期短及排尿所致。而Lockwood[3]研究报道,膀胱壁在所有器官中吸收剂量最高,为0.05 rad/mCi,推测原因是其忽略了尿液的影响,且采用伽马照相机和直线扫描仪,而非PET/CT显像,此外Lockwood[3]的研究中对全身分布仅取某一时间点进行评估。Stabin[4]研究报道,13N-NH3·H2O全身ED为2.0×10-3mSv/MBq,膀胱壁吸收剂量最高(8.1×10-3mSv/MBq),其次为双肾(4.6×10-3mSv/MBq)、脑(4.2×10-3mSv/MBq)及肝(4.0×10-3mSv/MBq)。本研究结果与Stabin[4]的研究不同,可能是由受试者种族差异、检查前禁食与否、辐射剂量测量方法不同(是否考虑排泄因素)、设备不同及数据采集方法不同所致。由于骨髓免疫细胞的增殖,中轴骨13N-NH3·H2O吸收剂量显著,具体机制有待进一步研究。
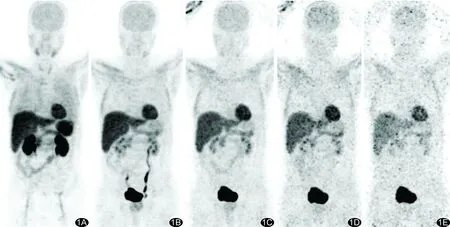
图1 受试者男,60岁,连续5次全身PET最大密度投影图,分别于13N-NH3·H2O注射后0.5(A)、12.5(B)、25(C)、40(D)、55 min(E)采集图像
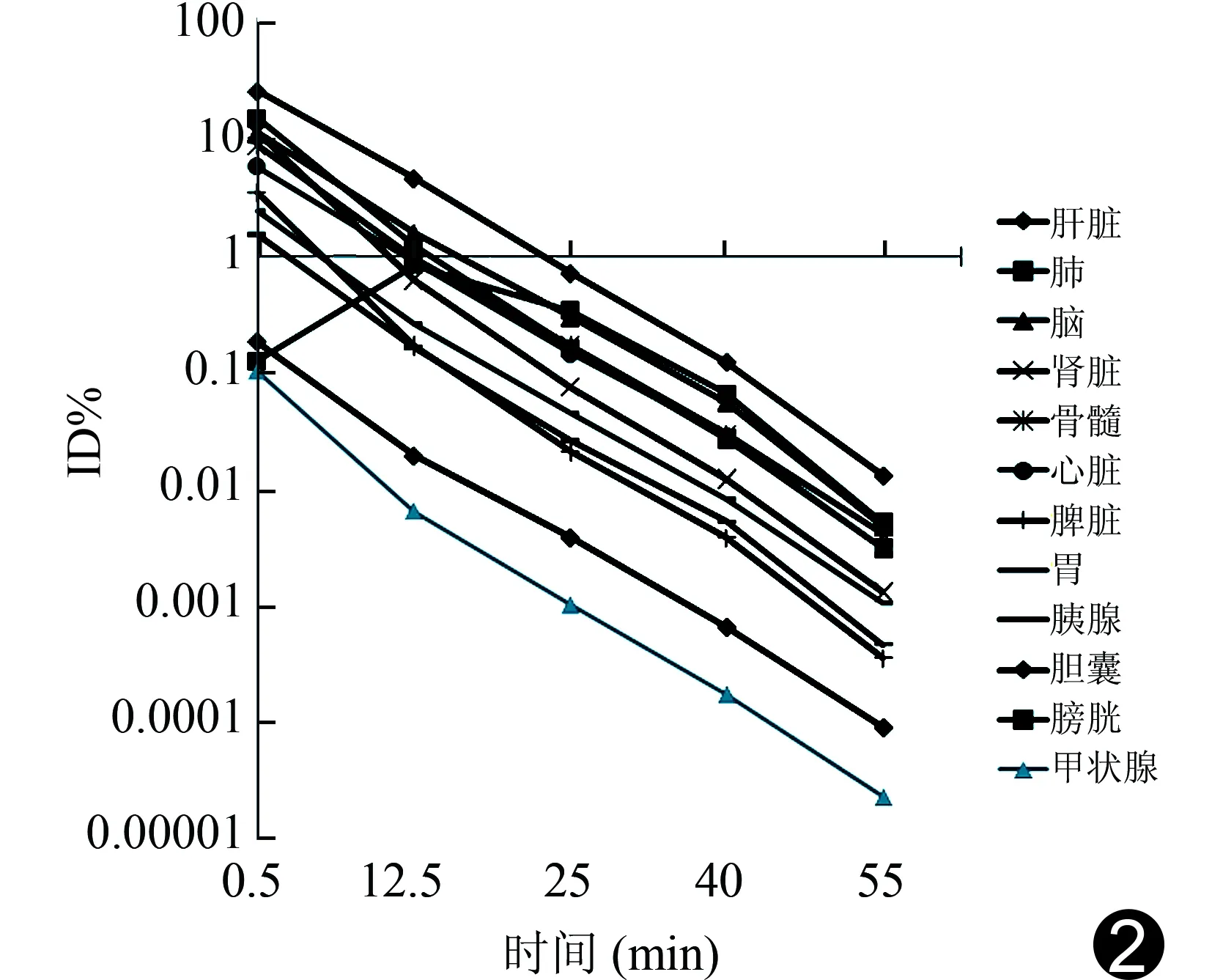
图2 衰减校正的源器官13N-NH3·H2O ID%随时间的变化曲线
NH3·H2O是谷氨酰胺循环的原料,与谷氨酰胺代谢有关。生理状态下,谷氨酰胺主要在骨骼肌、双肺及脂肪组织中合成[12],因此肌肉的13N-NH3·H2O摄取高。本研究中尽管肉眼观察双肺并无高摄取,但其滞留时间[(7.54±6.82)×10-3h]较高。此外,谷氨酰胺合成酶催化谷氨酸和氨水合成谷氨酰胺,参与谷氨酰胺生物合成,可能是13N-NH3·H2O生物分布的标志[13]。谷氨酰胺合成酶主要存在于脑、双肾和肝脏,在肌肉和脂肪组织中表达相对较少,本研究提示13N-NH3·H2O的摄取与谷氨酰胺合成酶的分布基本一致。本研究发现,注射后12.5 min时13N-NH3·H2O的生物分布趋于稳定,随后13N-NH3·H2O迅速从血管排出,随时间缓慢聚集于心、肝、脑、膀胱。
辐射剂量指南中指出,每项研究中健康志愿者的ED不得超过10 mSv[14],或每项PET研究中特定器官的吸收剂量应限制在50 mSv以内[15]。本研究的常规单次13N-NH3·H2O PET/CT扫描辐射吸收剂量为555~740 MBq,ED为3.65~4.87 mSv,符合上述标准。
本研究的主要不足为样本量小,仅5名健康志愿者,因此研究结果的偏倚较大。此外,辐射剂量的计算采用MATLAB代码和电子数据表,而非FDA批准的程序(OLINDA),可能会影响到数据的质量。由于对部分受试者的扫描范围未包括生殖腺,因此生殖腺的辐射剂量评估暂未纳入本研究。
总之,本研究对5名健康受试者进行全身动态PET/CT成像,以MIRD法分析13N-NH3·H2O人体生物分布和辐射剂量,发现全身13N-NH3·H2O PET/CT显像相对安全。
[1] Clark JC, Aigbirdhio FI. Chemistry of nitrogen-13 and oxygen-15//Welch MJ. Redvanly CS. Handbook of radio-pharmaceuticals. Chichester: Wiley, 2003:119-140.
[2] Shi X, Zhang X, Yi C, et al. [13N]Ammonia positron emission tomographic/computed tomographic imaging targeting glutamine synthetase expression in prostate cancer. Mol Imaging, 2014,13. doi: 10.2310/7290.2014:00048.
[3] Lockwood AH. Positron emission tomography in the study of hepatic encephalopathy. Metab Brain Dis, 2002,17(4):431-435.
[4] Stabin MG. Radiopharmaceuticals for nuclear cardiology: Radiation dosimetry, uncertainties and risk. J Nucl Med, 2008,49(9):1555-1563.
[5] 易畅,张祥松,史新冲,等.探讨13N-氨水动态心肌灌注显像定量分析方法.中国医学影像技术,2012,28(2):273-276.
[6] 唐刚华,王明芳,唐小兰,等.由动物实验估算人体内13N-NH3·H2O辐射吸收剂量.辐射研究与辐射工艺学报,2004,22(2):97-100.
[7] Cropley VL, Fujita M, Musachio JL, et al. Whole-body biodistribution and estimation of radiation-absorbed doses of the dopamine D1 receptor radioligand11C-NNC 112 in humans. J Nucl Med, 2006,47(1):100-104.
[8] Seltzer MA, Jahan SA, Sparks R, et al. Radiation dose estimates in humans for C-11-acetate whole-body PET. J Nucl Med, 2004,45(7):1233-1236.
[9] Huang T, Wang H, Tang G, et al. Human radiation dose estimation of11C-CFT using whole-body PET. Clin Nucl Med, 2012,37(12):1159-1162.
[10] Tang G, Wang M, Tang X, et al. Pharmacokinetics and radiation dosimetry estimation of O-(2-[18F]fluoroethyl)-L-ty- rosine as oncologic PET tracer. Appl Radiat Isot, 2003,58(2):219-225.
[11] Keiding S, Sørensen M, Bender D, et al. Brain metabolism of13N-ammonia during acute hepatic encephalopathy in cirrhosis measured by positron emission tomography. Hepatology, 2006,43(1):42-50.
[12] Cooper AJ.13N as a tracer for studying glutamate metabolism. Neurochem Int, 2011,59(4):456-464.
[13] Krajewski WW, Collins R, Holmberg-Schiavone L, et al. Crystal structures of mammalian glutamine synthetases illustrate substrate-induced conformational changes and provide opportunities for drug and herbicide design. J Mol Biol, 2008,375(1):217-228.
[14] International Commission on Radiological Protection. The 2007 recommendations of the International Commission on Radiological Protection. ICRP publication 103. Ann ICRP, 2007,37(2-4):1-332.
[15] Food and Drug Administration. CFR-Code of Federal Regulations Title 21, part 361. [2016-06-01]. http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CF RPart=361&showFR=1
国家自然科学基金(81271599)。
张芳玲(1990—),女,广西桂林人,硕士,医师。研究方向:肿瘤的多种示踪剂联合显像。E-mail: flyzfl@126.com
张祥松,中山大学附属第一医院影像科,510080。E-mail: sd_zh@ vip.tom.com
2016-06-08
2016-12-27
R3; R817
A
1003-3289(2017)03-0478-05

