食用油中3-氯-1,2-丙二醇酯的研究进展
王永瑞,张京星,魏长庆
(1.石河子大学食品学院,新疆石河子 832000;2.石河子大学食品学院,新疆石河子 832000;3.石河子大学食品学院,新疆石河子 832000)
食用油中3-氯-1,2-丙二醇酯的研究进展
王永瑞1,2,张京星3,魏长庆1,*
(1.石河子大学食品学院,新疆石河子 832000;2.石河子大学食品学院,新疆石河子 832000;3.石河子大学食品学院,新疆石河子 832000)
近些年国际上关于食用油污染物——3-氯-1,2丙二醇酯的话题屡见不鲜。作为一种对于人体具有潜在危害的非营养成分,研究食用油中3-氯-1,2丙二醇脂的形成机理以及危害对食用油的安全性有着重要的意义。本文主要阐述食用油中的污染物——3-氯-1,2丙二醇脂的来源、检测方法、形成机理以及去除方法。
食用油,3-氯-1,2丙二醇酯,检测方法,形成机理,去除方法
3-氯-1,2-丙二醇酯作为一种食用油中的污染物,自1980年Velíšek等在用酸水解蔬菜蛋白过程中首次检测出以来,有关于3-氯-1,2-丙二醇酯的报道屡见不鲜[1]。随着检测技术以及检测方法的改进和发展,在我们日常生活中所食用的各类食用油以及含油类食品中均检测出了3-氯-1,2-丙二醇酯[2-5]。Zelinková等[6-7]则在几类婴幼儿成长奶粉也检测到了不等浓度的3-氯-1,2-丙二醇酯,这引起了科学界广泛的关注。虽然关于3-氯-1,2-丙二醇酯的毒理学还尚不清楚,没有直接的证据证明其对人体的健康存在安全隐患,但是可以确定的是3-氯-1,2-丙二醇酯的水解产物3-氯-1,2-丙二醇具有一定的毒性。鉴于3-氯-1,2-丙二醇对于小鼠肾脏以及睾丸的致癌性,国际癌症研究机构已将3-氯-1,2-丙二醇列为一种可能的人体致癌物,隶属于2类B组致癌物[8]。因此,关于3-氯-1,2-丙二醇酯的研究对食用油及其油类产品的安全性有着重要的意义。
1 食用油中3-氯-1,2-丙二醇酯的来源
3-氯-1,2-丙二醇酯是7类氯丙醇酯中的一类(图1),也是食品中含量最多的一类氯丙醇酯。食用油的主要成分是丙三醇酯,又称甘油酯(即甘油单酯,甘油二酯,甘油三酯),3-氯丙醇酯就是甘油酯的3号碳原子上的原子团被氯元素取代后所形成的物质。
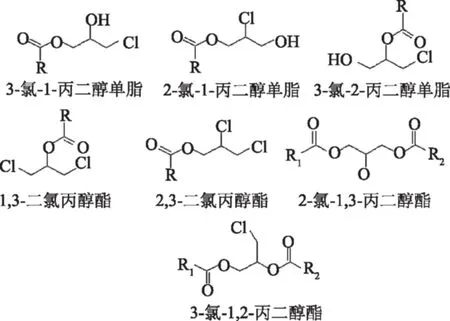
图1 七类氯丙醇酯Fig.1 Seven chloropropanediol esters
1.1 食用油精炼过程中3-氯-1,2-丙二醇酯的变化
未精炼的食用油是几乎不含有3-氯-1,2-丙二醇酯。Abd Razak等[9]收集了马来西亚不同油脂精炼厂的油样本检测结果显示,在未精炼的原油中近80%的样品中没有检测到3-氯-1,2-丙二醇酯,10%样品检测出3-氯-1,2-丙二醇酯的含量高于检出限0.25 mg/kg。漂白后的油脂则有50%高于0.25 mg/kg。而完全精炼后的油脂样品则全部含有3-氯-1,2-丙二醇酯,99%的样品3-氯-1,2丙二醇酯的含量高于0.25 mg/kg。精炼后则发现了高含量的3-氯-1,2-丙二醇酯,这说明3-氯-1,2-丙二醇酯主要在精炼过程中形成。经过研究表明,3-氯-1,2-丙二醇酯主要是来源于油脂精炼的脱臭环节。200 ℃以上高温条件下的脱臭环节除去易挥发物质的同时也形成了3-氯-1,2-丙二醇酯[10]。
1.2 不同前体物质对于3-氯-1,2-丙二醇酯生成的影响
Shimizu等[11]的研究表明,3-氯-1,2-丙二醇酯的形成与甘油三酯、甘油二酯、甘油单酯有关,且生成的3-氯-1,2-丙二醇酯大部分来源于甘油二酯和甘油单酯。Zhang等[12]构建化学模型将甘油三硬脂酸酯分别与NaCl、KCl、FeCl2、CuCl2、ZnCl2、FeCl3以及干HCl气体和有机含氯化合物六氯环己烷在模拟油脂精炼条件下反应生成3-氯-1,2-丙二醇酯的研究表明,仅有FeCl2、FeCl3可以和甘油三酯反应生成3-氯-1,2-丙二醇酯。与此同时,Freudenstein等[13]模拟油脂加工中的除臭阶段研究前体物质对于3-氯-1,2-丙二醇酯生成的影响,结果表明甘油二酯、甘油单酯能增加3-氯-1,2-丙二醇酯生成的可能,然而精炼后卵磷脂却对3-氯-1,2-丙二醇酯的生成没有影响。这都表明3-氯-1,2-丙二醇酯的前体物质主要是甘油二酯、甘油单酯,而甘油三酯不易形成3-氯-1,2-丙二醇酯。并且Mogol等[14]还发现,相比较其它精炼过的油脂,烤制饼干使用精炼后的橄榄油有利于3-氯-1,2-丙二醇酯的生成,这说明在食物深加工过程中,不同种类的食用油对于3-氯-1,2-丙二醇酯的生成也有很大影响[15]。
对于3-氯-1,2-丙二醇酯的另一种前体物质氯元素则可能来源于油料中自身带有的氯盐或者是食用油精炼过程中使用的水溶液中带有的氯盐,主要是NaCl。并且Freudenstein等[13]研究表明除NaCl以外,其他含氯化合物如MgCl2、FeCl2、FeCl3以及氯化四丁基胺等氯盐的存在很大程度上也导致了3-氯-1,2-丙二醇酯的形成。
2 食用油中3-氯-1,2-丙二醇酯的形成影响因素
水分含量、加热温度以及加热时间对于3-氯-1,2-丙二醇酯的生成有着重要的影响。在食用油深炸过程中随着水分含量、温度的增加,3-氯-1,2-丙二醇酯生成量在增加。有研究表明在160 ℃下,加热2 h时生成的3-氯-1,2-丙二醇酯含量是最高的。而当加热时间大于2 h时,会使3-氯-1,2-丙二醇酯发生降解,从而导致3-氯-1,2-丙二醇酯的生成量减少。由于3-氯-1,2-丙二醇酯主要的前体物质是甘油二酯和甘油单酯,而水含量的增加会促进甘油三酯水解为甘油二酯以及甘油单酯,这也使得3-氯-1,2-丙二醇酯生成量在增加[16]。Mogol等[14]的研究发现在饼干烤制过程中,3-氯丙醇及其酯的零级动力学程中的反应速率常数随温度上升而增大。在180~220 ℃之间每上升20 ℃率常数增大约1.4倍,这说明高温环境是影响3-氯-1,2-丙二醇酯生成的重要因素。Li等[17]使用2,6-二叔丁基-4-甲基苯酚(BHT)、丁基羟基茴香醚(BHA)、叔丁基对苯二酚(TBHQ)、没食子酸丙酯(PG)、L-抗坏血酸棕榈酸酯(AP),α生育酚(VE)等抗氧化剂在化学模型以及油模型中抑制3-氯-1,2-丙二醇酯的生成,其研究结果表明这些抗氧化剂无论是在化学模型还是油模型中都展现了对于3-氯-1,2-丙二醇酯生成的抑制能力,且叔丁基对苯二酚(TBHQ)的抑制能力最强,这说明3-氯-1,2-丙二醇酯的生成受抗氧化剂的影响。Zhang等人[12]的研究结果表明由于Fe3+以及Fe2+的催化能力,能促进甘油三硬脂酸酯生成3-氯-1,2-丙二醇酯。
3 3-氯-1,2-丙二醇酯的检测方法及检测仪器
3.1 3-氯-1,2-丙二醇酯的检测方法
对于食用油中3-氯-1,2-丙二醇酯的检测方法还没有建立确切的标准方法,但是目前测定3-氯-1,2-丙二醇酯的方法大体上分为两种:直接法和间接法。直接法顾名思义即直接检测3-氯-1,2-丙二醇酯,间接法则是先通过将3-氯-1,2-丙二醇酯水解成3-氯丙二醇和脂肪酸,通过测定3-氯丙二醇对3-氯-1,2-丙二醇酯定性或者定量。直接法虽然可以有效的测定多种单个脂肪酸酯,但需要这些昂贵的单个脂肪酸酯以及他们的参考标准,而间接法更很容易操作并适用于常规分析,因此目前主要采用间接法测定食用油中的3-氯-1,2-丙二醇酯[18-19]。
3.2 3-氯-1,2-丙二醇酯的测定流程
食用油中3-氯-1,2-丙二醇酯的间接法测定主要分为三个步骤:3-氯-1,2-丙二醇酯的水解,衍生化,衍生化产物的仪器分析。

表1 3-氯1,2-丙二醇及其内标物衍生产物的特征离子峰
3.2.1 3-氯-1,2-丙二醇酯的水解 目前对于3-氯-1,2-丙二醇酯的水解主要有三种方法:1、酸水解,水解时向含有3-氯-1,2-丙二醇酯的脂肪样品中加入硫酸/甲醇溶液于40 ℃作用下加热16 h。2、碱水解,是鉴于甲醇钠可以和脂肪酸乙酯发生酯交换反应,据此提出了甲醇/甲醇钠溶液水解3-氯-1,2-丙二醇酯的方法。由于碱性水解时间短,条件温和,并且在碱性条件下即使有氯离子的存在也不会有新3-氯-1,2-丙二醇酯的生成,所以最常用的是碱水解[20]。3、酶水解,在含有3-氯-1,2-丙二醇酯的脂肪样品中加入脂肪酶后23 ℃加热24 h,3-氯-1,2-丙二醇酯会水解成3-氯-1,2-丙二醇。
3.2.2 3-氯-1,2-丙二醇酯的水解产物的衍生化 衍生化的作用主要是把难于分析的3-氯-1,2-丙二醇酯转化为与其化学结构相似但易于分析的物质,便于量化和分离。3-氯-1,2-丙二醇酯的水解产物3-氯-1,2-丙二醇的衍生化试剂主要有苯硼酸(PBA)、七氟丁酰咪唑(HFBI)、三氟乙酸酐以及丙酮等,最常用的是七氟丁酰咪唑和苯硼酸[21]。其中3-氯-1,2-丙二醇酯水解后生成的3-氯-1,2-丙二醇与七氟丁酰咪唑反应生成2,3,4-七氟丁酸3-氯-1,2-丙二醇二酯,机理如图2所示[22]。而3-氯-1,2-丙二醇酯水解后生成的3-氯-1,2-丙二醇与苯硼酸反应生成苯硼酸3-氯-1,2-丙二醇二酯,机理如图3所示[23-24]。
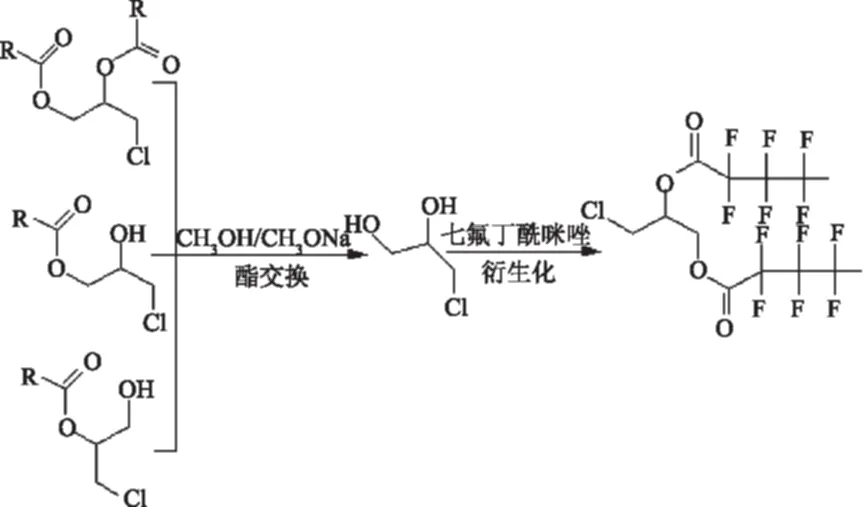
图2 七氟丁酰咪唑衍生3-氯1,2-丙二醇的机理Fig.2 The derivative mechanism of 3-Monochloro-1,2-propanediol by HFBI
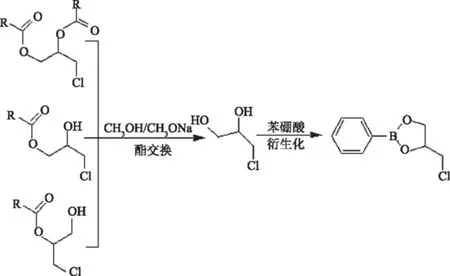
图3 苯硼酸衍生3-氯1,2-丙二醇的机理Fig.3 The derivative mechanism of 3-Monochloro-1,2-propanediol by phenylboric acid
3.2.3 衍生化产物的仪器分析 目前已报道分析仪器有:气相色谱-质谱联用(GC-MS),气相色谱-质谱/质谱(GC-MS/MS),液相色谱-飞行时间质谱联用(LC-TOF-MS),全二维气相色谱-飞行时间质谱联用(GC×GC/TOF-MS),超高压液相色谱串联四级杆飞行时间质谱(UPLC/Q-TOF-MS/MS)等等,最常用的检测仪器是GC-MS[25]。一般使用内标物d5-3-氯-1,2-丙二醇酯对于3-氯-1,2-丙二醇进行定量,相应的用七氟丁酰咪唑以及苯硼酸衍生的衍生产物对应的质谱定性定量离子峰如表1所示[24,26]。
4 食用油中3-氯-1,2-丙二醇酯的形成机理
对于3-氯-1,2-丙二醇酯形成的机理还正处于研究当中,此前一共存在两种猜想,都是以甘油三酯为前体,都是采用SN2亲核取代方式。一种是甘油三酯的一个酯基部分直接被氯原子取代形成3-氯-1,2-丙二醇酯(图4),另一种则是一个酯基水解形成甘油二酯,然后发生水解的位置再被氯原子取代形成3-氯-1,2-丙二醇酯,鉴于氯的亲水疏油性,则第二种猜想的可能性会更高(图5)[27-28]。
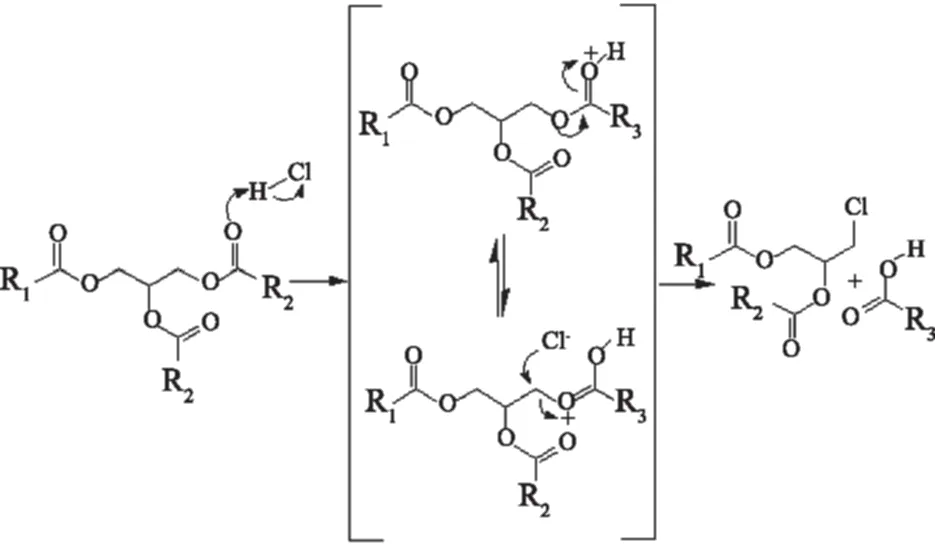
图4 甘油三酯发生亲核取代生成3-氯1,2-丙二醇酯的可能机理Fig.4 Proposed formation mechanism of 3-Monochloro-1,2-propanediol ester through nucleophilic reaction of triglyceride
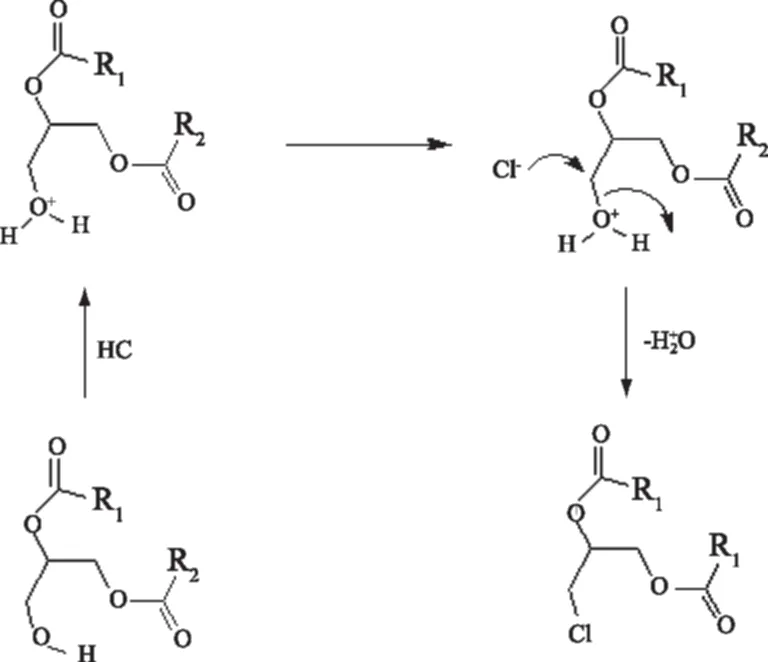
图5 甘油二酯发生亲核取代形成3-氯1,2-丙二醇酯的可能机理Fig.5 Proposed formation mechanism of 3-Monochloro-1,2-propanediol ester through nucleophilic reaction of diglyceride
在此基础上又提出了在路易斯酸的存在下,甘油三酯的其中一个酯基部分水解后形成的甘油二酯。在氯离子进攻碳原子之前,甘油二酯先形成了中间产物,如酰氧鎓离子或缩水甘油脂离子进而形成了3-氯丙醇酯。目前大多数报道普遍认为是先形成了酰氧鎓离子或者缩水甘油酯离子的中间体,然后生成了3-氯丙醇酯(图6,图7)[28-33]。

图6 甘油二酯通过形成环氧酰鎓离子生成3-氯1,2-丙二醇酯的可能途径Fig.6 Proposed formation mechanism of 3-Monochloro-1,2-propanediol ester through acyloxonium ion generated by diglyceride
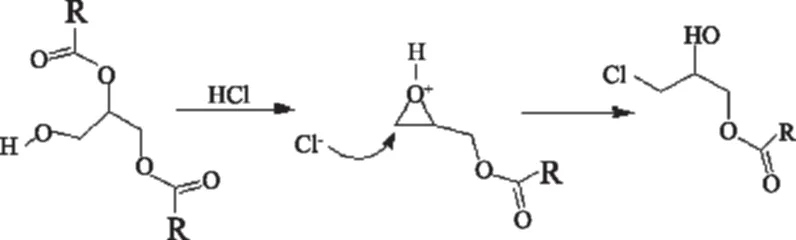
图7 1,3-甘油二酯通过形成缩水甘油酯生成3-氯-1-丙醇酯的可能途径Fig.7 Proposed formation mechanism of 3-Monochloro-1-propanediol ester through glycidyl ester generated by 1,3-diglyceride
无论是形成酰氧鎓离子还是缩水甘油酯离子中间体,都是采取的是SN1亲核取代的方式,该反应的进行程度很大程度上取决于酰氧鎓离子或缩水甘油酯离子的稳定性。从酰氧鎓离子和缩水甘油酯离子的结构来看,酰氧鎓离子的稳定性大于缩水甘油酯离子的稳定性。而且酰氧鎓离子是形成3-氯-1,2-丙二醇酯的中间体,缩水甘油酯离子则是形成3-氯-1-丙二醇单酯的中间体。
5 食用油中3-氯-1,2-丙二醇酯的去除
无论食用油中3-氯-1,2-丙二醇酯毒性大小,作为食用油中的非营养物质也应予以去除。总的来说去除3-氯-1,2-丙二醇酯共有三种方法。一是在产品加工前除掉原料中相关的反应物质;二是改良产品加工工艺流程;三是对精炼后产品中的3-氯-1,2-丙二醇酯进行去除[34-36]。
5.1 减少原油中3-氯-1,2-丙二醇酯的前体物质
3-氯-1,2-丙二醇酯的主要前体物质有甘油三酯、甘油二酯、甘油单酯以及含氯化合物,而3-氯-1,2-丙二醇酯的形成是在精炼过程中的高温环境下前体物质反应而生成的。鉴于含氯化合物与甘油酯在物理性质的差异性较大,因此除去未精炼油中的含氯化合物可以有效的减少加工后产品中的3-氯-1,2-丙二醇酯的含量。通过水或者乙醇洗涤未精炼的食用油可以部分去除未精炼油中的含氯化合物[37]。Matthäus等[34]发现,用水或75%的乙醇对精炼前的棕榈油进行洗涤,精炼后的棕榈油中3-氯-1,2-丙二醇酯的含量会相应降低20%和25%。
5.2 改良油脂精炼的工艺流程
3-氯-1,2-丙二醇酯主要是在精炼过程高温环境下生成的。因此改良油脂的精炼的工艺流程则可以减少3-氯-1,2-丙二醇酯的形成。在漂白过的食用油中加入0.5%~2.5%的乙醇或者甘油可以阻止部分的3-氯-1,2-丙二醇酯的产生。在除臭前加入1~5 mmol/kg的碳酸钠或者碳酸氢钠可以阻止3-氯-1,2-丙二醇酯以及缩水甘油酯的形成。在除臭环节中加入1%~10%的Kostrolith 5A型分子筛可以破坏3-氯-1,2-丙二醇酯的生成。在除臭环节蒸发前加入甘油二乙酸酯作为竞争分子和含氯化合物反应可以降低3-氯-1,2-丙二醇酯的生成[36]。因此适当的在精炼过程中增加一些环节可以减少3-氯-1,2-丙二醇酯的生成。
5.3 对于精炼后的油脂中的3-氯-1,2-丙二醇酯进行去除
对于精炼后的油脂可以采用吸附剂来吸附3-氯-1,2-丙二醇酯。Strijowski等人[38]用煅烧过的沸石以及合成的硅酸镁等吸附材料能将精炼后的棕榈油中40%的3-氯-1,2-丙二醇酯及其相关化合物去除,很大程度上降低了3-氯-1,2-丙二醇酯及其相关化合物的含量。也可以将3-氯-1,2-丙二醇酯转化成甘油等无害物质,从而间接的去除3-氯-1,2-丙二醇酯。Bornscheuer等人[39]则成功的用酶在水油两相中将3-氯-1,2-丙二醇酯先转化成3-氯-1,2-丙二醇,然后再用另一种酶在水相中将3-氯-1,2-丙二醇转化成无害的甘油。
6 展望
在很多食品中已经检测出了3-氯-1,2-丙二醇酯的存在。目前最需要去做的就是研究3-氯-1,2-丙二醇酯的形成机理,依据形成机理和形成条件及时的调整食用油精炼程序,尽可能降低乃至除去食用油中的3-氯-1,2-丙二醇酯,让广大人民群众吃到更加健康的更有营养价值的食用油及含油类产品[40]。
[1]Velíšek J,Davídek J,Kubelka V,et al. New chlorine-containing organic compounds in protein hydrolysates[J]. J Agric Food Chem,1980,28(6):1142-1144.
[2]Jedrkiewicz R,Glowacz A,Gromadzka J,et al. Determination of 3-MCPD and 2-MCPD esters in edible oils,fish oils and lipid fractions of margarines available on Polish market[J]. Food Control,2016,59:487-492.
[3]Weißhaar R. Fatty acid esters of 3-MCPD:Overview of occurrence and exposure estimates[J]. Eur J Lipid Sci Technol,2011,113(3):304-308.
[4]Dolezal M,Chaloupská M,Divinová V,et al. Occurrence of 3-chloropropane-1,2-diol and its esters in coffee[J]. Eur Food Res Technol,2005,221(3):221-225.
[5]Macmahon S,Begley T H,Diachenko G W. Occurrence of 3-MCPD and glycidyl esters in edible oils in the United States[J]. Food Additives & Contaminants:Part A,2013,30(12):2081-2092.
[6]Zelinková Z,Dolezal M,Velíšek J,et al. Occurrence of 3-chloropropane-1,2-diol fatty acid esters in infant and baby foods[J]. Eur Food Res Technol,2009,228(4):571-578.
[8]Onami S,Cho Y M,Toyoda T,et al. Orally administered glycidol and its fatty acid esters as well as 3-MCPD fatty acid esters are metabolized to 3-MCPD in the F344 rat[J]. Regulatory Toxicology and Pharmacology,2015,73:726-731.
[9]Abd Razak R A,Kuntom A,Siew W L,et al. Detection and monitoring of 3-monochloropropane-1,2-diol(3-MCPD)esters in cooking oils[J]. Food Control,2012,25(1):355-360.
[10]Li Chang,Li Linyan,Jia Hanbing,et al. Formation and reduction of 3-monochloropropane-1,2-diol esters in peanut oil during physical refining[J]. Food Chemistry,2016,199:605-611.
[11]Shimizu M,Weitkamp P,Vosmann K,et al. Temperature Dependency When Generating Glycidyl and 3-MCPD Esters from Diolein[J]. J Am Oil Chem Soc,2013,90(10):1449-1454.
[12]Zhang Zhongfei,Gao Boyan,Zhang Xiaowei,et al. Formation of 3-Monochloro-1,2-propanediol(3-MCPD)Di-and Monoesters from Tristearoylglycerol(TSG)and the Potential Catalytic Effect of Fe2+and Fe3+[J]. J Agric Food Chem,2015,63(6):1839-1848.
[13]Freudenstein A,Weking J,Matthäus B. Influence of precursors on the formation of 3-MCPD and glycidyl esters in a model oil under simulated deodorization conditions[J]. Eur J Lipid Sci Technol,2013,115(3):286-294.
[14]Mogol B A,Pye C,Anderson W,et al. Formation of Monochloropropane-1,2-diol and Its Esters in Biscuits during Baking[J]. J Agric Food Chem,2014,62(29):7297-7301.
[15]Ermacora A,Hrncirik K. Influence of oil composition on the formation of fatty acid esters of 2-chloropropane-1,3-diol(2-MCPD)and 3-chloropropane-1,2-diol(3-MCPD)under conditions simulating oil refining[J]. Food Chemistry,2014,161:383-389.
[16]Zhou Hongru,Jin Qingzhe,Wang Xingguo,et al. Effects of temperature and water content on the formation of 3-chloropropane-1,2-diol fatty acid esters in palm oil under conditions simulating deep fat frying[J]. Eur Food Res Technol,2014,238(3):495-501.
[17]Li Chang,Jia Hanbing,Shen Mingyue,et al. Antioxidants Inhibit Formation of 3-Monochloropropane-1,2-diolEsters in Model Reactions[J]. J Agric Food Chem,2015,63(44):9850-9854.
[18]Miyazaki K,Koyama K,Sasako H,et al. Indirect Method for Simultaneous Determinations of 3-Chloro-1,2-Propanediol Fatty Acid Esters and Glycidyl Fatty Acid Esters[J]. J Am Oil Chem Soc,2012,89(8):1403-1407.
[19]Dubois M,Tarres A,Goldmann T,et al. Comparison of indirect and direct quantification of esters of monochloropropanediol in vegetable oil[J]. 2012,1236:189-201.
[20]严小波,吴少明,里南. 油脂性食品中脂肪酸氯丙醇脂检测方法的研究进展[J]. 色谱,2013,31(2):95-101.
[21]王卫华,徐锐锋,刘军,等. 食品中氯丙醇测定方法研究进展[J]. 化学分析计量,2007,16(3):74-76.
[22]Liu Qing,Han Feng,Xie Ke. Simultaneous determination of total fatty acid esters of chloropropanols in edible oils by gas chromatography-mass spectrometry with solid-supported liquid-liquid extraction[J]. Journal of Chromatography A,2013,1314:208-215.
[23]Stadler R H. Monochloropropane-1,2-diol esters(MCPDEs)and glycidyl esters(GEs):an update[J]. Journal of Food Science,2015,6:12-18.
[24]Ma Fei,Li Peiwu,Matthäus B,et al. Optimization of ultrasonic-assisted extraction of 3-monochloropropane-1,2-diol(MCPD)and analysis of its esters from edible oils by gas chromatography-mass spectrometry[J]. J Sep Sci,2012,35(17):2241-2248.
[25]Li Chang,Jia Hanbing,Wang Yuting,et al. Determination of 3-Monochloropropane-1,2-Diol Esters in Edible Oil-Method Validation and Estimationof Measurement Uncertainty[J]. Food Anal Methods,2015,9(4):845-855.
[26]Ramli M R,Siew W L,Ibrahim N A,et al. Effects of Degumming and Bleaching on 3-MCPD Esters Formation During Physical Refining[J]. J Am Oil Chem Soc,2011,88(11):1839-1844.
[27]Destaillats F,Craft B D,Sandoz L,et al. Formation mechanisms of Monochloropropanediol(MCPD)fatty acid diesters in refined palm(Elaeis guineensis)oil and related fractions[J]. Contaminants:Part A,2012,29(1):29-37.
[28]Karin Rahn A K,Yaylayan V A. What do we know about the molecular mechanism of 3-MCPD ester formation?[J]. Eur J Lipid Sci Technol,2011,113(3):323-329.
[30]Zhang Hai,Jin Pengwei,Zhang Min,et al. Mitigation of 3-Monochloro-1,2-propanediol Ester Formation by Radical Scavengers[J]. J Agric Food Chem,2016,64(29):5887-5892.
[31]Aladedunye F. Toxic contaminants of thermo-oxidatively processed edible oils/fats[J]. Lipid Technology,2016,28(7):117-121.
[32]周红茹,金俊,杨娇. 油脂中3-氯丙二醇酯形成的化学反应机制[J]. 中国粮油学报,2012,27(10):118-122.
[33]Destaillats F,Craft B D,Dubois M,et al. Glycidyl esters in refined palm(Elaeis guineensis)oil and related fractions. Part I:Formation mechanism[J]. Food Chemistry,2012,131:1391-1398.
[34]Matthäus B. Organic or not organic-that is the question:How the knowledge about the origin of chlorinated compounds can help to reduce formation of 3-MCPD esters[J]. Eur J Lipid Sci Technol,2012,114(12):1333-1334.
[35]Matthäus B,Pudel F,Fehling P,et al. Strategies for the reduction of 3-MCPD esters and related compounds in vegetable oils[J]. Eur J Lipid Sci Technol,2011,113(3):380-386.
[36]Matthäus B,Pudel F. Mitigation of 3-MCPD and glycidyl esters within the production chain of vegetable oils especially palm oil[J]. Lipid Technology,2013,25(7):151-155.
[37]Craft B D,Nagy K. Mitigation of MCPD-ester and glycidyl-ester levels during the production of refined palm oil[J]. Lipid Technology,2012,24(7):155-157.
[38]Strijowski U,Heinz V,Franke K. Removal of 3-MCPD esters and related substances after refining by adsorbent material[J]. Eur J Lipid Sci Technol,2011,113(3):387-392.
[39]Bornscheuer U T,Hesseler M. Enzymatic removal of 3-monochloro-1,2-propanediol(3-MCP D)and its esters from oils[J]. Eur J Lipid Sci Technol,2010,112(5):552-556.
[40]Tan C P. Sustainable Development of the Palm Oil Industry via Process Improvement and Product Diversification[J]. J Dev Sus Agr,2015,10(2):107-114.
Review on the research of 3-Monochloro-1,2-propanediol ester in the oils
WANG Yong-rui1,2,ZHANG Jing-xing3,WEI Chang-qing1,*
(1.Food College,Shihezi University,Shihezi 832000,China;2.Food College,Shihezi University,Shihezi 832000,China;3.Food College,Shihezi University,Shihezi 832000,China)
In recent years,the topic 3-Monochloro-1,2-propanediol ester is common occurrence in the world,which is a kind of contaminant in the oils. As one of non-mutritive ingredient and one matter which has underlying hazard to human body,study on the formation mechanism and hazard of 3-Monochloro-1,2-propanediol ester is of vital significance to the safety of plant oil. This thesis mainly elaborates the source,detection method,formation mechanism and elimination method of 3-Monochloro-1,2-propanediol ester in edible oil.
edible oil;3-Monochloro-1,2-propanediol ester;detection method;formation mechanism;elimination method
2016-09-02
王永瑞(1991-),男,在读硕士研究生,研究方向:食品化学,E-mail:422972005@qq.com。
*通讯作者:魏长庆(1981-),男,博士,副教授,研究方向:粮食、油脂及植物蛋白工程,E-mail:Changqing_wei@126. com。
国家自然科学基金青年科学基金项目(31401617);石河子大学高层次人才项目(RCZX201524);2015五师科技计划专项(2060402);八师2016工业科技项目(2016HZ20);石河子大学SRP项目(SRP2015185)。
TS225.1
A
1002-0306(2017)06-0357-06
10.13386/j.issn1002-0306.2017.06.060

