黄连解毒汤对大鼠亚慢性毒性试验研究
刘芳,王立红, 董惠峰,赵晶晶,张俊霞,刘鼎阔1,,通信作者
黄连解毒汤对大鼠亚慢性毒性试验研究
刘芳2,3,王立红2,3, 董惠峰3,赵晶晶2,3,张俊霞3,刘鼎阔1,2,3,通信作者
(1. 中国农业大学动物医学学院,北京100094;2. 天津市饲用微生物制剂企业重点实验室,天津300383;3. 鼎正动物药业(天津)有限公司,天津300383)
研究黄连解毒汤连续灌服情况下对于SD大鼠的亚慢性毒性作用,揭示其临床安全性。SD 大鼠120只,雌雄各半,随机分为对照组和黄连解毒汤 20、10、5 mL/kg 剂量组,每组 30 只,连续给药6周,以SD大鼠的体重、血液学、血液生化学、组织病理学检查作为检查指标,全面评价连续灌服对大鼠的毒性作用。连续给药42 d后,与对照组相比,黄连解毒汤试验组大鼠的血常规及各项血液生化检测指标结果相近(>0.05)。组织病理学切片结果显示,黄连解毒汤20 mL/kg组大鼠肝脏和肾脏出现了轻微损伤,10 mL/kg和5 mL/kg 剂量组SD大鼠的的脾、肺、肝、肾、胃等组织亦均未发现异常的组织病理学变化。黄连解毒汤在10 mL/kg和5 mL/kg 剂量下连续灌服情况下对SD大鼠无不良影响。
黄连解毒汤;大鼠;亚慢性毒性
黄连解毒汤方出《外台秘要》引崔氏方,其方剂由黄连、黄芩、黄柏、桅子四味药组成,为清热解毒的代表方剂,具有多种药理活性,但是中药成分复杂,可由其所产生的安全问题不容忽视[1-2]。据报道,黄连解毒汤的君药黄连已引起了锥体外系反应,导致呼吸衰竭,肝功能损害,严重心律失常,甚至导致死亡[3-5]。然而,大多数研究仅涉及到黄连生物碱的细胞毒性和急性毒性、小檗碱的遗传毒性等,对黄连解毒汤在安全性全面的研究较少[6]。本研究主要通过临床观察、血液学和血液生化检测、病理检查等手段对黄连解毒汤连续应用情况下的亚慢性毒性作用进行研究,以期为临床应用提供参考。
1 材料与方法
1.1 试验药物
黄连解毒汤,由鼎正动物药业(天津)有限公司提供。
1.2 实验动物
4周清洁级SD大鼠120只,雌雄各半,体重在120~150 g之间,由中国人名解放军军事医学研究所实验动物中心提供,动物合格证号为:SCXK(军)2014-0001。
1.3 试验方法
试验动物随机分为4组,分别为黄连解毒汤20 mL/kg剂量组(20 mL/kg)、10 mL/kg剂量组(10 mL/kg)、5 mL/kg剂量组(5 mL/kg)和生理盐水对照组,每组动物30只,雌雄各半,分开饲喂。组内动物个体体重相差应不超过平均体重的10%,组间平均体重相差不超过5%。试验组大鼠每天均灌胃给药1次。连续给药42 d(即共6周)。
1.4 检测指标
1.4.1 临床表现
每天观察试验大鼠的健康状况、采食及饮水、体重等。分别于第1、2、3、4、5、6周称量体重,给药结束后计算平均摄食量和饲料利用率(动物每食入100 g饲料所增长的体重克数)。将给药剂量组与对照组进行比较和统计学处理。及时记录和分析大鼠的中毒症状及出现各症状的先后次序、时间。
1.4.2 血液学和血液生化检测
给药结束后,对大鼠心脏采血进行血液学和血液生化指标的检测。
血液学检测包括:血红蛋白(Hg)、红细胞计数(Ec)、白细胞计数(Lc)、嗜中性(NL)、嗜酸性(AL)、嗜碱性(BL)、淋巴(LM)、单核(ML)。
血液生化检测包括:丙氨酸氨基转换酶(ALT)、天门冬氨酸转换酶(AST)、尿素氮(BUN)、肌酐(Cr)、白蛋白(ALB)、总蛋白(TP)、总胆固醇(CHO)、甘油三酯(TG)。
1.5 病理检查
1.5.1 大体剖检
给药结束后,各组取10只大鼠(雌雄各半)进行剖检(结合采血进行)。做好记录,并将重要器官和组织固定保存。
1.5.2 脏器称重
剖检试验大鼠的同时,称取大鼠体重及各主要脏器(包括脾、肺、肝、肾、胃、肠、睾丸及卵巢)重量,做好记录。计算各脏器的相对重量(脏器重/体重),即脏器系数。
1.5.3 组织病理学检查
对20 mL/kg剂量组及对照组大鼠的主要脏器进行组织病理学检查,发现病变后再对较5 mL/kg剂量组大鼠的相应器官及组织进行检查。组织病理学检测项目包括:脾、肺、肝、肾、胃、肠。
1.6 数据处理
2 结果与分析
2.1 临床表现
各组大鼠灌胃给药期间各组均无死亡,20 mL/kg剂量组第2天出现稀便,10 mL/kg剂量组和5 mL/kg剂量组与对照组相比无明显变化,其他临床表现均属正常。各试验组给药结束,与对照组相比,雌性大鼠在3、4周,雄性大鼠在3、4、5周体重增重的差异具有统计学意义(<0.05),提示黄连解毒汤在20 mL/kg剂量可明显的抑制大鼠体重增长,10 mL/kg剂量、5 mL/kg剂量对大鼠体重增长无明显的影响(>0.05)(表1)。
表1 黄连解毒汤对大鼠体重增重的影响(s,n=10) g

表1 黄连解毒汤对大鼠体重增重的影响(s,n=10) g
检测指标20 mL/kg剂量组10 mL/kg剂量组5 mL/kg剂量组对照组 初重♂♀107. 03±4. 02101. 90±4. 47101. 43±2. 62109. 87±6. 16101. 13±7. 71110. 83±3. 57105. 80±4. 47111. 50±6. 67 1周♂♀140. 53±2. 22128. 20±4. 64142. 83±6. 04141. 47±6. 44188. 73±10. 98*139. 17±5. 64148. 67±6. 71145. 50±9. 60 2周♂♀177. 63±5. 04156. 27±12. 33173. 10±5. 33167. 93±3. 91188. 73±4. 98166. 23±4. 33198. 77±8. 78178. 73±10. 96 3周♂♀211. 53±4. 71176. 13±13. 64*218. 63±12. 79193. 80±2. 73233. 43±11. 31197. 90±2. 93245. 83±8. 82212. 30±13. 13 4周♂♀251. 67±7. 96*195. 37±6. 82*252. 20±11. 40218. 63±7. 89276. 13±10. 11221. 93±3. 16292. 80±9. 53230. 97±11. 58 5周♂♀282. 27±12. 38*218. 63±8. 56*291. 63±14. 64239. 63±3. 64319. 43±21. 96249. 90±2. 53338. 40±12. 13256. 60±8. 53 6周♂♀332. 53±17. 89*277. 47±20. 78329. 23±20. 98289. 73±5. 84357. 70±21. 60290. 97±9. 82371. 23±19. 16288. 63±7. 36
注:*为差异显著(0.01<<0.05)
与对照组相比,药物组各组的摄食量无明显的差异(>0.05),但是20 mL/kg剂量组饲料利用率的差异具有统计学意义(<0.05),10 mL/kg剂量、5 mL/kg剂量对大鼠饲料利用率无明显的影响(>0.05)(表2)。
2.2 脏器检测结果
与对照组相比,黄连解毒汤20 mL/kg剂量组、10 mL/kg剂量组、5 mL/kg剂量组脏器相对体质量均无显著变化(>0.05)(表3)。
表2 黄连解毒汤对大鼠进食量及食物利用率的影响(s,n=10)
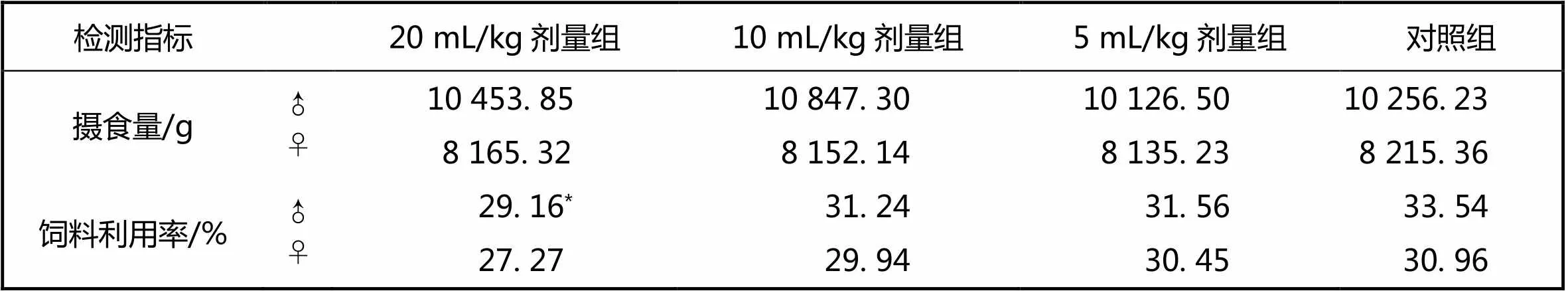
表2 黄连解毒汤对大鼠进食量及食物利用率的影响(s,n=10)
检测指标20 mL/kg剂量组10 mL/kg剂量组5 mL/kg剂量组对照组 摄食量/g♂♀10 453. 858 165. 3210 847. 308 152. 1410 126. 508 135. 2310 256. 238 215. 36 饲料利用率/%♂♀29. 16*27. 2731. 2429. 9431. 5630. 4533. 5430. 96
表3 黄连解毒汤对大鼠脏器相对体质量的影响(s,n=10) %
检测指标20 mL/kg剂量组10 mL/kg剂量组5 mL/kg剂量组对照组 心♂♀0. 37±0. 060. 37±0. 080. 35±0. 050. 32±0. 02 0. 42±0. 060. 33±0. 050. 41±0. 050. 40±0. 03 肝♂♀4. 00±0. 803. 90±0. 403. 60±0. 703. 60±0. 20 4. 30±0. 903. 70± 0.603. 50±0. 404. 30±0. 20 脾♂♀0. 34±0. 020. 30±0. 040. 20±0. 020. 18±0. 05 0. 18±0. 040. 21±0. 060. 15±0. 030. 17±0. 02 肺♂♀0. 56±0. 020. 48±0. 020. 49±0 .040. 45±0. 02 0. 58±0. 030. 47±0. 060. 49±0. 040. 50±0. 07 肾♂♀0. 83±0. 090. 82±0. 040. 75±0. 040. 79±0. 12 0.73±0. 030. 70±0. 090. 72±0. 050. 88±0. 11 睾丸♂10. 08±1. 159. 18±1. 0411. 09±1. 2310. 67±1. 41 卵巢♀0. 27±0. 090. 27±0. 020. 22±0. 070. 22±0. 05
表4 黄连解毒汤对大鼠血液学检测指标的影响(s,n=10)

表4 黄连解毒汤对大鼠血液学检测指标的影响(s,n=10)
组别白细胞数白细胞种类/%红细胞血红蛋白 109个·L-1嗜碱嗜酸中性淋巴单核102 g·L-1g·L-1 20 mL/kg剂量组♂♀11. 16±0. 980. 10±0. 021. 10±0. 1357. 70±3. 2463. 70±3. 543. 40±0. 566. 28±0. 44135. 00±4. 21 9. 21±1. 120. 20±0. 031. 24±0.1961. 40±4. 5665. 10±5. 143. 60±0. 485. 13±0. 52144. 00±1. 83 10 mL/kg剂量组♂♀9. 28±0. 890. 50±0. 061. 10±0. 2060. 70±3. 5258. 00±3. 144. 50±0. 246. 83±0. 43101. 00±10. 21 9. 99±0. 780. 20±0. 021. 40±0. 1358. 60±4. 2166. 30±3. 545. 20±0. 495. 01±0. 56127. 00±8. 76 5 mL/kg剂量组♂♀10. 57±1. 220. 10±0. 021. 12±0. 2158. 10±4. 2162. 80±4. 124. 30±0. 546. 91±0. 64129. 00±4. 28 9. 17±0. 840. 20±0. 021. 36±0. 2462. 10±3. 8460. 20±5. 024. 50±0. 757. 36±0. 59110. 00±5. 62 对照组♂12. 37±1. 020. 20±0. 031. 25±0. 3163. 20±3. 5168. 60±3. 154. 80±0. 626. 93±0. 71131. 00±10. 54 ♀11. 77±1. 420. 10 ±0. 031. 10±0. 1565. 10±4. 5366. 60±3. 244. 30±0. 695. 71±0. 24112. 00±4. 14
表5 黄连解毒汤对大鼠血液生化学检测指标(s,n=10)
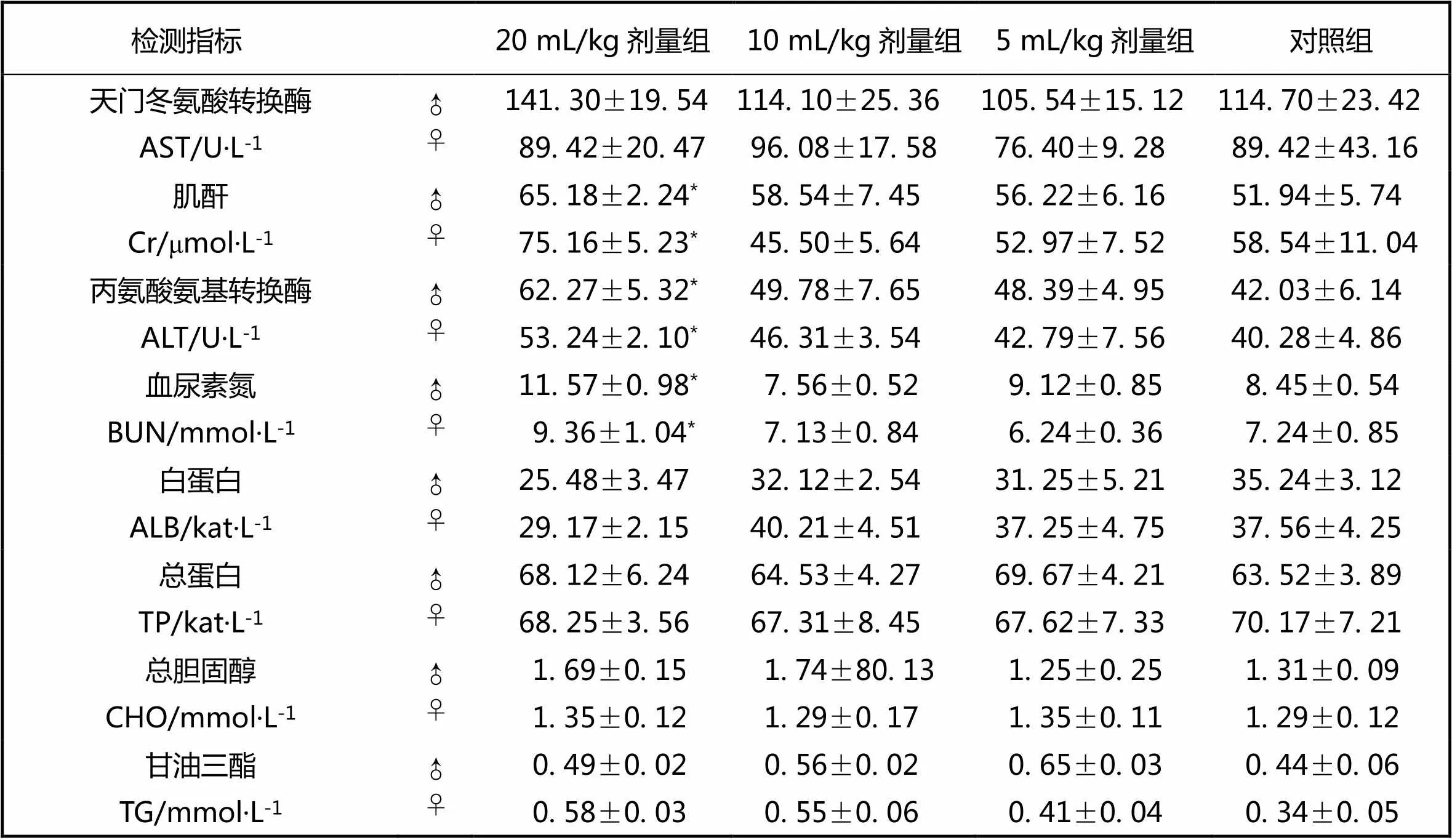
表5 黄连解毒汤对大鼠血液生化学检测指标(s,n=10)
检测指标20 mL/kg剂量组10 mL/kg剂量组5 mL/kg剂量组对照组 天门冬氨酸转换酶AST/U·L-1♂♀141. 30±19. 5489. 42±20. 47114. 10±25. 3696. 08±17. 58105. 54±15. 1276. 40±9. 28114. 70±23. 4289. 42±43. 16 肌酐Cr/μmol·L-1♂♀65. 18±2. 24*75. 16±5. 23*58. 54±7. 4545. 50±5. 6456. 22±6. 1652. 97±7. 5251. 94±5. 7458. 54±11. 04 丙氨酸氨基转换酶ALT/U·L-1♂♀62. 27±5. 32*53. 24±2. 10*49. 78±7. 6546. 31±3. 5448. 39±4. 9542. 79±7. 5642. 03±6. 1440. 28±4. 86 血尿素氮BUN/mmol·L-1♂♀11. 57±0. 98*9. 36±1. 04*7. 56±0. 527. 13±0. 849. 12±0. 856. 24±0. 368. 45±0. 547. 24±0. 85 白蛋白ALB/kat·L-1♂♀25. 48±3. 4729. 17±2. 1532. 12±2. 5440. 21±4. 5131. 25±5. 2137. 25±4. 7535. 24±3. 1237. 56±4. 25 总蛋白TP/kat·L-1♂♀68. 12±6. 2468. 25±3. 5664. 53±4. 2767. 31±8. 4569. 67±4. 2167. 62±7. 3363. 52±3. 8970. 17±7. 21 总胆固醇CHO/mmol·L-1♂♀1. 69±0. 151. 35±0. 121. 74±80. 131. 29±0. 171. 25±0. 251. 35±0. 111. 31±0. 091. 29±0. 12 甘油三酯TG/mmol·L-1♂♀0. 49±0. 020. 58±0. 030. 56±0. 020. 55±0. 060. 65±0. 030. 41±0. 040. 44±0. 060. 34±0. 05
2.3 血液学及血液生化参数
给药结束后,各组大鼠进行血液学和血液生化参数测定结果均分别见表4和表5。统计学分析显示,与对照组相比黄连解毒汤20 mL/kg剂量组BUN、Cr、ALT显著升高(<0.05),具有统计学意义,而10 mL/kg剂量组和5 mL/kg剂量组的血液学和血液生化参数之间差异不显著(>0.05)。
2.4 病理学变化
给药结束后,剖检大鼠,经肉眼观察均未发现任何异常和可疑病变。病理组织学检查结果显示:10 mL/kg剂量组、5 mL/kg剂量组、空白对照试验组的各组织器官切片结果均未发现异常的组织病理学损伤。20 mL/kg剂量组与对照组比肝脏、肾脏、小肠出现了一定的病理损伤,其中肝脏出现轻微的肝细胞变性和灶状坏死;肾小管被破坏,管腔扩张[7];小肠绒毛变短,淋巴滤泡浸润,肠壁变薄。将黄连解毒汤20 mL/kg剂量组和对照组大鼠的脾、肺、肝、肾、胃、肠等组织进行组织病理学切片对比(图1)。
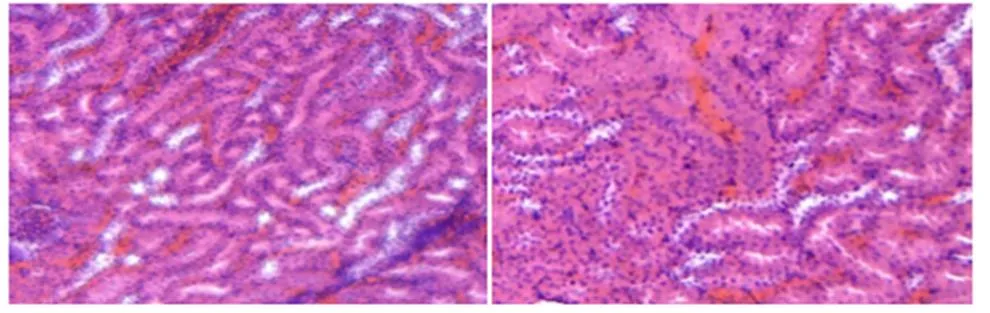
20 mL/kg剂量组脾×10 对照组脾×10
20 mL/kg剂量组肺×10 对照组肺×10
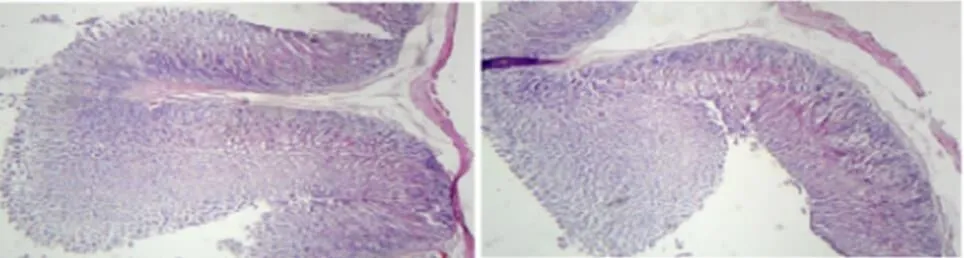
20 mL/kg剂量组胃×10 对照组胃×10
20 mL/kg剂量组肝×10 对照组肝×10

20 mL/kg剂量组肾×10 对照组肾×10
高剂量组肠×10 对照组肠×10
图1 大鼠20 mL/kg剂量组与空白组脏器组织切片HE染色图
3 讨论
给药后第2天,黄连解毒汤20 mL/kg剂量组大鼠粪便变稀,而10 mL/kg、5 mL/kg与对照组相比无显著变化,分析可能是黄连解毒汤中黄连、栀子有泻下的作用,过量使用后导致大鼠排便异常。这种泻下作用导致20 mL/kg剂量组大鼠体重增重减少,饲料利用率降低,小肠绒毛变短,肠壁变薄。除此之外,与对照组相比,其它试验组的体重增重、食物利用率等临床表现均属正常。连续给药42 d后,黄连解毒汤20 mL/kg剂量组血清中BUN、Cr、ALT含量升高,说明黄连解毒汤高剂量组对大鼠的肝肾功能有影响[8]。而黄连解毒汤试验其他组大鼠的血常规及各项血液生化检测指标结果相近,说明黄连解毒汤对大鼠正常生理功能不会产生影响。作为药物代谢的主要场所,黄连解毒汤20 mL/kg组大鼠肝脏和肾脏出现了轻微损伤,分析是长期高剂量服用黄连解毒汤导致药物在大鼠体内不能被快速的代谢排出,大量蓄积而产生毒副作用,进一步说明了肝脏和肾脏是黄连解毒汤所作用的主要靶器官。然而,黄连解毒汤10 mL/kg组和5 mL/kg组大鼠的脾、肺、肝、肾、胃等组织亦均未发现异常的组织病理学变化,说明黄连解毒汤在该剂量下长期服用不会出现中毒现象。
[1] 余园媛,王伯初,彭亮,等. 黄连的药理研究进展[J]. 重庆大学学报(自然科学版),2006,29(2):107-111.
[2] 李巧如,任健康,刘宗智,等. 18种中草药抗菌作用的筛选[J]. 陕西中医,2002,23(6):555-556.
[3] 温华珍,肖盛元,王义明,等. 黄芩化学成分及炮制学研究[J]. 天然产物研究与开发,2004,16(6):575-580.
[4] 李海丽. 黄芩的研究进展[J]. 化学工程与装备,2008(4):100-102.
[5] 廖静,鄂征. 中药黄柏的光敏抗癌作用研究[J]. 首都医科大学学报,1999,20(3):153-155.
[6] 孙健,马吉胜,金瑾,等. 黄连解毒汤各成分的HPLC-UV/MS定性与定量测定方法研[J]. 药学学报,2006,41(4):380-384.
[7] 孙保存. 病理学[M]. 北京:北京大学医学出版社,2009.
[8] 魏婷. 黄连解毒汤提取精制工艺及安全性评价[D]. 重庆:西南大学,2011.
责任编辑:张爱婷
Subchronic Toxicity of Coptidis Toxin Resolving Decoction in Rats
LIU Fang2,3, WANG Li-hong2,3, DONG Hui-feng3, ZHAO Jing-jing2,3, ZHANG Jun-xia3, LIU Ding-kuo1,2,3,Corresponding Author
(1. College of Veterinary Medicine at CAU , Beijing 100094, China; 2. Enterprise Key Laboratory of Feed Microbial Preparation, Tianjin 300383, China; 3. S&E animal pharmaceutical(Tianjin)Co, Ltd. , Tianjin 300383, China)
The subchronic toxicity of Coptidis Toxin Resolving Decoction in SD rats is researched by continuous perfusion in order to expose its clinical innocuity. 120 SD rats(males and females)were randomly devivided into control group and Coptidis Toxin Resolving Decoction in 3 different dosage groups(20, 10, and 5 mL/kg, 30 in each group). The SD rats were administered with Coptidis Toxin Resolving Decoction by continuous perfusion for 6 weeks. The body weight, hematology, blood biochemistry and histopathology examination were measured for the overall toxicity assessment to rats. After 42 days, contrasted with the control group, the test group rats blood routine examination index and blood index had an approximately result(>0.05). The result of histopathological slices showed that the liver and kidney of Coptidis Toxin Resolving Decoction 20 mL/kg group rats appeared slight damage, while the spleen, lung, liver, kidney and stomach of Coptidis Toxin Resolving Decoction 10 mL/kg group and 5 mL/kg group does not find abnormal histopathologic change. Conclusion With a dose of 10 mL/kg and 5 mL/kg Coptidis Toxin Resolving Decoction continuous perfusion, there is not harmful effect on SD rats.
Coptidis Toxin Resolving Decoction; rat; subchronic toxicity
1008-5394(2017)01-0023-05
S854.5
A
2016-04-25
天津市科技支撑计划项目“中草药在水产健康养殖中的应用与开发”(13ZCZDNC00700)
刘芳(1988-),女,山东潍坊人,助理畜牧师,硕士,主要从事中兽药新制剂开发。E-mail:liuf1201@163.com。
刘鼎阔(1981-),男,内蒙古赤峰人,畜牧师,硕士,主要从事中兽药新制剂开发。E-mail:liudingkuo1981@163.com。

