胆道镜清创治疗胰腺炎胰周脓肿经验总结
郝金成+梁雅静+曹广涛
(日照市中医医院普外科,山东日照 276800)
[摘 要] 目的:分析胆道镜清创治疗胰腺炎胰周脓肿的效果与安全性,总结治疗经验。方法:2012年2月~2016年2月59例胰腺炎胰周脓肿患者接受介入超声穿刺置管引流、窦道扩张、胆道镜清创治疗,记录其引流情况、清创情况、治疗效果、并发症发生情况及1年随访结果。结果:59例患者介入超声穿刺引流均成功实施,56例患者于数次清创后达到治愈标准,治愈率为94.92%。56例接受胆道镜清创治疗的患者中,共发生并发症4例。随访期间59例患者均未见病灶残余。结论:胆道镜清创治疗胰腺炎胰周脓肿效果确切、安全可靠。应注重彻底引流、避免脏器损伤,以达到挽救生命、控制损伤、保证疗效目的。
[关键词] 胆道镜;清创;胰腺炎;胰周脓肿
中图分类号:R657.5 文献标识码:A 文章编号:2095-5200(2017)04-027-03
DOI:10.11876/mimt201704011
Experience of choledochoscopy debridement in treatment of pancreatitis complicated with peripancreatic abscess HAO Jincheng,LIANG Yajing,CAO Guangtao. (Department of general surgery,Rizhao City Hospital of traditional Chinese Medicine Rizhao 276800 China)
[Abstract] Objective: This study aimed to analyse the effect and safety of choledochoscopy debridement in the treatment of pancreatitis complicated with peripancreatic abscess, and to summarize the experience of treatment. Methods: From February 2012 to February 2016, 59 patients with pancreatitis complicated with peripancreatic abscess received ultrasound-guided percutaneous drainage, sinus dilation, and choledochoscopy debridement, and their drainage, debridement, treatment effect, complications occurrence and 1 year follow-up results were recorded. Results: 59 patients were all successfully treated with ultrasound-guided percutaneous drainage. 56 patients were cured after several debridement. The cure rate was 94.92%. Of the 56 patients who underwent cholera debridement, 4 had complications. There were no lesion residues in 59 patients during follow-up. Conclusions: Choledochoscopy debridement is effective and safe in the treatment of pancreatitis complicated with peripancreatic abscess. Thorough drainage and avoiding organ damage should be paid attention, in order to save lives, control damage and ensure the efficacy.
[Key words] choledochoscope; debridement; pancreatitis; peripancreatic abscess
胰腺炎后期大量炎性组织液渗出至胰腺周围,引发的周围组织坏死、感染及脓肿形成具有病变广泛、持续时间长的特点,也是影响患者生存质量的主要原因[1]。对于胰腺炎胰周脓肿的治疗,一直是困扰临床的棘手问题,既往多采取外科手术或置管引流,但外科手术创伤较大且风险较高,而置管引流效果易受复杂胰周间隙影响,单纯外科手术及内科保守治疗均存在其局限性[2]。随着影像学技术与微创技术的发展,越来越多的学者倾向于借助超声引导建立引流并使用膽道镜清创、冲洗脓腔,以期在控制损伤的同时确保治疗的针对性[3]。我院于2012年2月~2016年2月,对59例患者实施胆道镜清创治疗,取得了满意的效果,现将治疗结果与经验总结如下。
1 资料与方法
1.1 对象
59例胰腺炎胰周脓肿患者均参照中华医学会消化病学分会胰腺疾病学组制定的胰腺炎胰周脓肿相关标准确诊[4],经保守治疗后无效中转介入超声联合胆道镜清创治疗,且随访时间≥1年。59例患者中,男32例,女27例,年龄20~81岁,平均(47.52±6.81)岁,病程3~22 d,平均(6.05±1.83)d;脓肿部位:胰头周围23例,小网膜囊36例,其中53例伴胰尾脾门区脓肿。
1.2 治疗方法
患者接受介入超声穿刺引流、窦道扩张、胆道镜清创治疗,治疗路径:1)介入超声穿刺引流:术前禁食12 h,于仰卧位行超声扫描,明确病变部位、病变范围、病灶外形及病灶深度,结合CT定位,选择1~3个穿刺点,穿刺点选取标准[5]:①接近靶目标,避免穿刺距离过长;②确认安全穿刺路径,避免伤及大血管或内脏器官;③穿刺层面超声显像清晰,未见盲区形成。常规消毒穿刺点周围皮肤,2%利多卡因局部麻醉,于超声引导下置入18G穿刺针,经针芯将0.035”引导丝置入预定部位,留置导丝,沿导丝走行置入8~12F引流管,外接引流管引流,引流物送病原菌培养及药敏检查,根据培养及检查结果调整抗生素使用方案。2)窦道扩张(穿刺通道直径>1.5 cm者无须实施窦道扩张):介入超声穿刺引流1周且可见窦道形成后,行窦道扩张治疗[6]。于超声引导下,沿引流管置入引导丝,拔除引流管,使用10~24F筋膜扩张器套件将窦道逐步扩张至24F,插入外鞘,取出扩张管,于外鞘置入20~24F引流管,拔除外鞘,引流管外接引流袋。3)胆道镜清创:窦道扩张1周后,拔除引流管,行病灶清创。于窦道置入胆道镜,仔细观察病灶内部状态,使用活检钳、取石网将坏死组织、脓苔取出,而后以生理盐水彻底灌洗脓腔,清创后重新连接引流管调整引流管位置,保证引流的充分性。根据患者病变情况选择清创频次,一般早期清创每周实施1~2次,若坏死组织、脓液明显减少,可将清创频次下调至每2周1次[7]。
治疗效果以治愈拔管判定,并记录治愈时间,治愈拔管标准[8]:1)胰周脓肿相关临床症状全部消失,在不使用抗生素及激素的前提下,体温、血象等指标恢复正常且持续≥1周;2)影像学检查未见胰周病变;3)引流管未见分泌物流出,持续≥5 d;4)镜检未见病灶内异物,内壁可见新鲜肉芽组织生长;1年随访过程中主要观察患者病灶残余及远期并发症发生情况。
2 结果
2.1 疗效及随访
59例患者介入超声穿刺引流均成功实施,穿刺点数量:单管引流5例,双管引流18例,三管引流36例;置管深度5~21 cm,平均(13.59±3.47)cm;清创次数2~10次,平均(5.52±0.87)次。
56例患者于数次清创后达到治愈标准,治愈率为94.92%,其余3例患者因胆道镜置入困难,中转开腹清创引流后治愈,无死亡患者。56例经胆道镜清创治愈者治愈时间35~113 d,平均(72.54±11.83)d,多数患者在清创1~3次后临床症状明显改善,出院后定期门诊治疗,17例患者因病情较重住院至痊愈。56例接受胆道镜清创治疗的患者中,共发生并发症4例,其中肠外瘘1例,创面渗血3例,均经对症处理后痊愈。
随访期间59例患者均未见病灶残余,其中3例患者存在进食后腹胀、食欲不振等远期并发症但正在轻微,经对症处理后症状消失。
2.2 典型病例
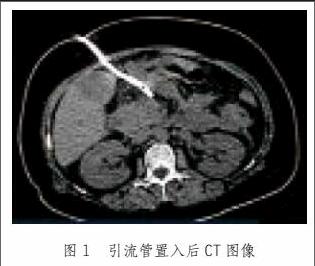
杨某,男,55岁,因“餐后急性腹痛3 h”入院,影像学检查示:重症急性胰腺炎合并胰周脓肿,脓肿位于小网膜囊且伴胰尾脾门区脓肿,常规超声引导病灶穿刺引流失败,改行介入超声穿刺置管引流,于胆囊与消化道间隙微通道进针,置入引流管1根(图1)。窦道扩张、胆道镜清创治疗均顺利实施,首次清创时病灶创面可见明显渗血,行局部电凝后成功止血。患者治愈时间为57 d,共计清创4次,随访1年未见病灶残余与远期并发症。
3 讨论
胰周脓肿是胰腺炎的严重并发症之一,多数患者存在高热、昏迷甚至胰性脑病等病变,需及时治疗。传统的胰周脓肿病灶外科处理方式为开腹病灶清除及脓肿引流,虽然可取得一定的效果,但开腹手术较大的创伤往往导致各类并发症的出现,甚至直接造成患者死亡[9-10]。因此,近年来临床愈发注重胰腺炎胰周脓肿治疗方案的优化。
单纯超声引导下置管引流往往无法取得满意的效果,其局限性在于引流管较细,易被坏死组织阻塞造成引流不畅,不仅难以达到充分引流,还可能因引流管阻塞引发新并发症出现[11]。故清创操作是胰周脓肿治疗过程中的重要环节,既往有学者将腹腔镜用于胰周坏死组织的清创,取得了一定成效,但腹腔镜清创术中易受角度影响,操作难度较高且清创能力有限[12]。加之胰周脓肿往往呈“山谷”样特点,即谷内存在大量坏死组织,且单次清创无法完全清除谷底脱落组织,故多数患者往往需反复接受多次清创[13-14],
这也给清创治疗的便捷性提出了更高的要求。
我中心在介入超声穿刺置管引流的基础上,将胆道镜清创用于胰腺炎胰周脓肿的治疗,结果表明,该法治愈率高达94.92%,且患者近远期并发症发生率较均低,安全性及治疗效果均值得肯定,其优势主要包括:1)1)操作简便:胆道镜清创全部操作均可在床旁进行,避免多次移动患者导致的不良事件风险[15];2)创伤较低:借助超声引导穿刺,能够最大限度保证穿刺位置的合理性与准确性,而胆道镜清创全程在微创、直视下进行,基本可以避免脏器或大血管损伤,与此同时,胆道镜下可直接电凝处理局部渗血,可有效控制持续出血;3)清创彻底:借助组织检查钳、取石网篮取出坏死组织后,通过胆道镜可导入大量生理盐水冲洗脓腔,彻底清除脓腔内残留坏死组织碎片与淤积脓液,且上述操作均具有可重复性,能够最大限度保障清创的彻底性[16];4)引流方便:在影像学引导下穿刺点可自由选择,通过多部位置管,保证各区域脓肿的充分引流,同时,引流管的管径一般能够满足脓腫引流需求,可取得较好的引流效果。
笔者结合多年临床经验及本研究诊治,总结经验如下:1)穿刺针的选择:若穿刺通道直径大于1.5 cm,可直接以粗套管针穿刺,此时不仅可满足一次置管到位要求,还可跳过窦道扩张环节,为胆道镜清创创造条件[17];2)保证引流的彻底性:超声引导下引流应采取低位引流,每次更换引流管时,管道腹内端均需达到脓腔深部及清创最远点,以扩大引流范围、避免深部坏死组织碎片残留;3)积极主动清创:胰周脓肿具有坏死组织多、病变范围广的特点,且脓腔为假性腔,故在注重彻底清创的同时,不应期望一次清创即清除全部坏死组织,盲目强行清创可能造成消化道瘘、大出血发生风险显著上升[18]。因此,条件允许时建议实施多次清创,每次清创操作中注重周围脏器组织与大血管的保护,尽可能降低清创操作对内环境的影响。
参 考 文 献
[1] Ignee A, Jenssen C, Cui X W, et al. Intracavitary contrast-enhanced ultrasound in abscess drainage–feasibility and clinical value[J]. Scand J Gastroenterol, 2016, 51(1):41-47.
[2] Fujii-Lau L L, Levy M J. Endoscopic ultrasound-guided pancreatic duct drainage[J]. J Hepatobiliary Pancreat Sci, 2015, 22(1):51-57.
[3] Kawakami H, Itoi T, Sakamoto N. Endoscopic ultrasound-guided transluminal drainage for peripancreatic fluid collections: where are we now[J]. Gut Liver, 2014, 8(8):341-355.
[4] 中华医学会消化病学分会胰腺疾病学组. 中国急性胰腺炎诊治指南(2013年,上海)[J]. 中华消化杂志, 2013, 33(4):656-660.
[5] Cheng C H, Wu C H, Bair M J. Endoscopic-ultrasound-guided cystogastrostomy for walled-off necrosis of the pancreas[J]. Adv Dig Med, 2016, 3(4):207-208.
[6] Tilara A, Gerdes H, Allen P, et al. Endoscopic ultrasound-guided transmural drainage of postoperative pancreatic collections[J]. J Am Coll Surg, 2014, 218(1):33-40.
[7] 阳凤, 彭燕. 重度急性胰腺炎并发胰腺脓肿的诊治进展[J]. 胃肠病学, 2016, 21(3):190-192.
[8] Lee B U, Song T J, Lee S S, et al. Newly designed, fully covered metal stents for endoscopic ultrasound (EUS)-guided transmural drainage of peripancreatic fluid collections: a prospective randomized study[J]. Endoscopy, 2014, 46(12):1078-1084.
[9] 邱懿德, 黄伟俊, 苏树英, 等. 介入超声置管引流联合胆道镜清创治疗胰周脓肿[J]. 肝胆胰外科杂志, 2014, 26(6):495-497.
[10] Denzer U W, Sioulas A D, Abdulkarim M, et al. Endoscopic ultrasound-guided drainage of abdominal fluid collections after pancreatic surgery: Efficacy and long-term follow-up[J]. Z Gastroenterol, 2016, 54(09):1047-1053.
[11] 陽凤, 徐劲, 罗旭娟, 等. 切开引流术和经皮穿刺置管引流术治疗重症急性胰腺炎并发胰腺脓肿的疗效分析[J]. 临床肝胆病杂志, 2016, 32(3):530-532.
[12] Fabbri C, Luigiano C, Lisotti A, et al. Endoscopic ultrasound-guided treatments: are we getting evidence based--a systematic review[J]. World J Gastroenterol, 2014, 20(26):8424-8448.
[13] 徐迅, 刘希胜, 俞同福, 等. CT引导结合Seldinger技术穿刺引流治疗胰腺周围深部脓肿[J]. 实用放射学杂志, 2016, 32(6):978-980.
[14] Mandai K, Uno K, Yasuda K. Endoscopic ultrasound-guided drainage of postoperative intra-abdominal abscesses[J]. World J Gastroenterol, 2015, 21(11):3402.
[15] Sharma V, Rana S S, Bhasin D K. Endoscopic ultrasound guided interventional procedures[J]. World J Gastroenterol Endosc, 2015, 7(6): 628.
[16] Chapman C G, Waxman I, Siddiqui U D. Endoscopic ultrasound (EUS)-guided pancreatic duct drainage: the basics of when and how to perform EUS-guided pancreatic duct interventions[J]. Clini Endosc, 2016, 49(2):161.
[17] Larson M M. Ultrasound Imaging of the Hepatobiliary System and Pancreas[J]. Vet Clin North Am Small Anim Pract, 2016, 46(3):453-480.
[18] Kobayashi S, Ikeura T, Takaoka M. Gastric wall abscess formation after endoscopic ultrasound-guided fine-needle aspiration of pancreatic cancer[J]. Dig Endosc, 2016, 28(2):220.
第一作者:郝金成,本科,主治医师,研究方向:普外科临床,Email:15206330725@139.com。

