美沙拉秦与曲美布汀联合对肠易激综合征患者结肠黏膜肥大细胞及其相关炎性介质的影响*
张 慧 苗 琪 吴跃龙 万 坚 王善娟 陆 芳 林永辉 任海峰 李晓波#
上海市嘉定区中心医院消化内科1(201800) 上海交通大学医学院附属仁济医院消化内科2 上海市嘉定区中心医院病理科3
美沙拉秦与曲美布汀联合对肠易激综合征患者结肠黏膜肥大细胞及其相关炎性介质的影响*
张 慧1苗 琪2吴跃龙3万 坚1王善娟1陆 芳1林永辉1任海峰1李晓波2#
上海市嘉定区中心医院消化内科1(201800) 上海交通大学医学院附属仁济医院消化内科2上海市嘉定区中心医院病理科3
背景:肠易激综合征(IBS)患者存在肥大细胞活化现象,对结肠黏膜肥大细胞及其相关炎性介质进行研究有助于疾病的评估和治疗。目的:探讨美沙拉秦联合曲美布汀对IBS患者结肠黏膜肥大细胞数量及其相关炎性介质的影响。方法:选取2014年10月—2016年6月上海市嘉定区中心医院40例腹泻型IBS(IBS-D)和40例便秘型IBS(IBS-C)患者,并以20名健康志愿者作为对照。将40例IBS-D和40例IBS-C患者均随机分为美沙拉秦+曲美布汀组和曲美布汀组,疗程均为4周。以改良甲苯胺蓝染色计数肥大细胞,免疫组化染色评估相关炎性介质的评分,评估患者的临床疗效。结果:与健康对照组相比,基线状态IBS-D患者和IBS-C患者肥大细胞数量均显著升高(P<0.05);给予美沙拉秦+曲美布汀治疗后,肥大细胞数量均显著降低(P<0.05)。基线状态时,IBS患者5-HT、IL-1、TNF-α、组胺和类胰蛋白酶免疫组化染色评分均显著高于健康对照组(P<0.000 1);给予美沙拉秦+曲美布汀治疗后,上述炎性介质的免疫组化染色评分均显著降低(P<0.05)。IBS-D患者中,美沙拉秦+曲美布汀组总有效率显著高于曲美布汀组(85.0%对45.0%,P=0.008),而IBS-C患者中两组总有效率无明显差异(55.0%对25.0%,P=0.053)。结论:美沙拉秦联合曲美布汀治疗可降低IBS患者结肠黏膜肥大细胞数量以及相关炎性介质的释放,对IBS-D患者的临床疗效更佳。
肠易激综合征; 美沙拉秦; 曲美布汀; 肥大细胞; 炎性介质
肠易激综合征(irritable bowel syndrome,IBS)是一种以反复发作的腹痛、腹泻、便秘和腹胀等为主要表现的肠道功能紊乱性疾病,普通人群的发病率为7%~21%[1]。IBS虽然不是器质性病变,但病程长且症状迁延导致就诊频繁,严重影响患者的日常工作、学习以及生活质量,给个人及其家庭造成了较大程度的身心和经济负担。美沙拉秦具有抗炎作用,能减少肥大细胞数量并减少其炎性介质的产生,从而缓解IBS患者腹痛等症状,改善粪便性状。目前国内尚未见美沙拉秦对IBS患者肥大细胞及其相关炎性介质5-羟色胺(5-hydroxytryptamine,5-HT)、白细胞介素-1(interleukin-1,IL-1)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、组胺和类胰蛋白酶影响的研究。曲美布汀为胃肠道运动节律调节剂,可对消化道的运动和平滑肌神经受体进行双向调节,用于改善IBS患者腹胀、腹痛、腹泻和便秘等临床症状。本研究通过给予IBS患者美沙拉秦联合曲美布汀治疗,旨在探讨美沙拉秦治疗IBS的疗效及其可能的机制,从而为IBS的治疗提供新思路和依据。
对象与方法
一、研究对象
纳入2014年10月—2016年6月上海市嘉定区中心医院消化科就诊的80例IBS患者,其中腹泻型IBS(IBS-D)和便秘型IBS(IBS-C)患者各40例,诊断符合罗马Ⅲ标准[2]。80例患者中,男36例,女44例,年龄21~68岁,平均42岁。排除标准:①妊娠或哺乳期患者;②过去12个月内结肠镜检查提示炎症性肠病或其他器质性肠病患者;③有腹部手术史的患者;④过去3个月内或试验期间服用抗菌药物、抗毒蕈碱药物、解痉药物、高剂量三环类抗抑郁药(>50 mg/d)、阿片类止泻药物或选择性5-羟色胺再摄取抑制剂者;⑤合并有严重的肝肾功能损伤者;⑥合并严重心肺疾病者;⑦依从性不佳者。同时选择同期健康体检者20名作为正常对照,其中男10名,女10名,年龄20~66岁,平均43岁。所有受试者均签署知情同意书。
二、研究方法
1.试验分组:将IBS-D和IBS-C患者参照随机数字表法随机分为美沙拉秦+曲美布汀组和曲美布汀组,每组各20例。曲美布汀组患者给予曲美布汀分散片(商品名:尼为孚,由浙江昂利康制药有限公司提供)100 mg tid,餐前30 min服用。在此基础上,美沙拉秦+曲美布汀组患者给予美沙拉秦(商品名:莎尔福,由康哲药业控股有限公司提供)500 mg tid,餐后服用。疗程均为4周。
2.病理检查:入选者口服甘露醇500 mL清洁肠道后行结肠镜检查。所有患者结肠镜下黏膜均未见异常,于距肛门20 cm处取黏膜2块,置于4%甲醛溶液中固定,脱水、石蜡固定、切片,行HE染色。美沙拉秦+曲美布汀组患者治疗4周后再次行结肠镜检查。
3.改良甲苯胺蓝染色[3]:取各组结肠组织,在高倍镜(×400)下计数肥大细胞,具体步骤参照试剂盒(购自上海虹桥乐翔医用试剂技术有限公司)说明书进行。
4.免疫组化染色:石蜡切片经脱蜡,封闭,抗原热修复,加入5-HT、IL-1、TNF-α、组胺和类胰蛋白酶一抗(均购自Sigma公司,工作浓度分别为1∶70、1∶60、1∶50、1∶75 和 1∶75)、二抗;显色、复染、封片。以PBS液代替一抗作为空白对照。
结果判断:以细胞质呈淡黄色者为阳性细胞。每张切片随机取5个视野,对染色强度和阳性细胞数进行计分。染色强度:无着色,0分;淡黄色,1分;棕黄色,2分;棕褐色,3分。阳性细胞数:阳性细胞数<5%,0分;6%~25%,1分;26%~50%,2分;51%~75%,3分;>75%,4分。染色总分为染色强度与阳性细胞数之积,0分,阴性(-);1~4分,弱阳性(+);5~8分,中度阳性(++);9~12分,强阳性(+++)。
5.临床疗效判断:治疗4周后对所有患者进行临床疗效评价。显效:腹痛、腹胀、腹泻和便秘消失,排便次数和性状均恢复正常;有效:腹痛、腹胀减轻,排便次数减少为2次/d,且不影响患者的日常工作和生活;无效:上述症状未明显减轻,反而进一步加重,严重影响患者的日常工作和生活。计算总有效率,总有效率(%)=(显效例数+有效例数)/总例数×100%。
三、统计学分析
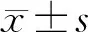
结 果
一、结肠黏膜肥大细胞
IBS-D患者基线状态肥大细胞数量显著高于健康对照组[(6.1±1.2)/HPF对(1.8±0.7)/HPF,P=0.022];给予美沙拉秦+曲美布汀治疗后,肥大细胞数量为(4.9±1.3)/HPF,较治疗前显著降低(P<0.000 1)。IBS-C患者基线状态肥大细胞数量显著高于健康对照组[(5.9±1.2)/HPF对(1.8±0.7)/HPF,P=0.027];给予美沙拉秦+曲美布汀治疗后,肥大细胞数量为(5.6±1.1)/HPF,较治疗前显著降低(P=0.031)(图1)。
二、免疫组化染色
基线状态时,IBS患者结肠黏膜肥大细胞相关炎性介质5-HT、IL-1、TNF-α、组胺和类胰蛋白酶的免 疫组化评分均显著高于健康对照组(P<0.000 1);给予美沙拉秦+曲美布汀治疗后,上述炎性介质的免疫组化评分均显著降低(P<0.001)(表1、图2~6)。
三、临床疗效评价
在IBS-D患者中,美沙拉秦+曲美布汀组的临床治疗总有效率显著高于曲美布汀组(85.0%对45.0%,P=0.008);在IBS-C患者中,美沙拉秦+曲美布汀组临床治疗的总有效率与曲美布汀组相比差异无统计学意义(55.0%对25.0%,P=0.053)(表2)。

A:基线IBS患者;B:治疗后IBS患者;C:健康对照组

A:基线IBS患者;B:治疗后IBS患者;C:健康对照组
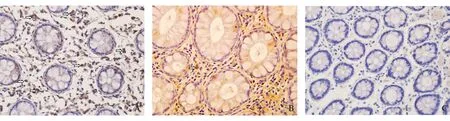
A:基线IBS患者;B:治疗后IBS患者;C:健康对照组

A:基线IBS患者;B:治疗后IBS患者;C:健康对照组

A:基线IBS患者;B:治疗后IBS患者;C:健康对照组

A:基线IBS患者;B:治疗后IBS患者;C:健康对照组

表1 各组患者肥大细胞相关炎性介质免疫组化染色评分
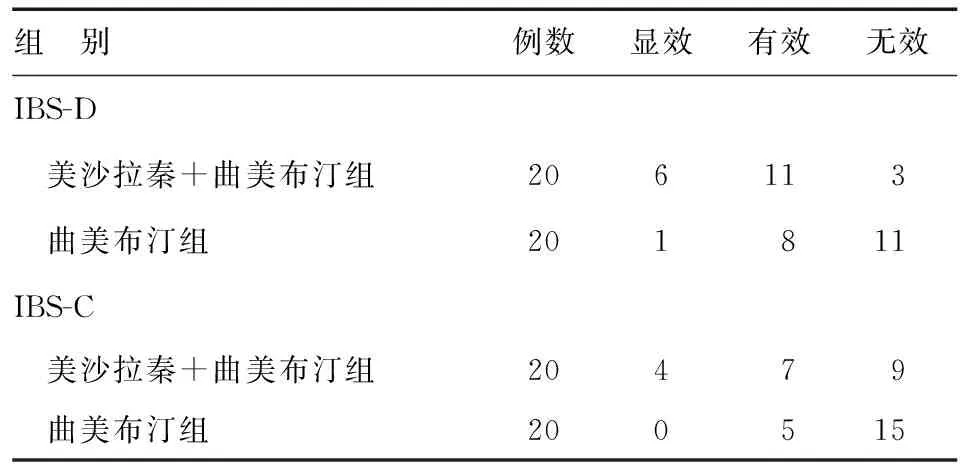
表2 各组IBS患者临床疗效评价(n)
讨 论
目前IBS的发病机制尚未完全明确,肠道细菌过度生长、不良饮食习惯以及心理因素等可能会导致IBS临床症状的发生。上述因素可能通过分子水平的细微变化,影响结肠微生态和局部免疫,减少黏液的分泌,从而削弱肠黏膜的保护作用[4]。肥大细胞可能在该过程中起有一定的作用,其能释放强有力的神经介质和免疫调节物质,如5-HT、IL-1、TNF-α和类胰蛋白酶,继而改变胃肠道功能[5]。IBS患者组织病理学检查常无阳性发现,偶尔可见结肠黏膜较小异常和水肿的最初表现。疾病的持续可能导致结肠黏膜上皮形态学发生改变,包括肥大细胞增多以及炎性细胞浸润。结肠黏膜中肥大细胞数量增加、活化明显可能是引起IBS的重要原因,其数量与IBS症状的严重程度相关[6]。本研究中,基线状态IBS-D和IBS-C患者的肥大细胞数量均明显高于健康对照组。
5-HT是一种与胃肠道蠕动关系密切的脑肠肽,在启动和维持肠道蠕动、调节肠壁分泌功能以及肠-脑感觉信号等环节中发挥重要作用[7-8]。目前认为肠道内5-HT的受体主要为5-HT3受体和5-HT4受体[9-10]。通过药物直接干预5-HT水平或使用5-HT受体激动剂/拮抗剂可能是治疗IBS的新方向。IL-1、TNF-α、组胺以及类胰蛋白酶均是活化肥大细胞释放的炎性介质,可诱发肠道黏膜炎症反应[11-12]。本研究行免疫组化染色发现,IBS患者5-HT、IL-1、TNF-α、组胺和类胰蛋白酶评分均明显高于健康对照组(P<0.000 1);给予美沙拉秦+曲美布汀治疗后,上述炎性介质的免疫组化评分均明显降低(P<0.05)。
控制结肠黏膜炎症是IBS的治疗方法之一。Klooker等[12]应用肥大细胞稳定剂酮替芬治疗皮肤点刺试验阳性的IBS患者,结果显示可降低患者的内脏敏感性,改善症状和生活质量。说明肥大细胞稳定剂对IBS患者有益。Leighton等[13]提出,长期抑制肥大细胞数量对IBS的疗效可能较使用肥大细胞或其产物的特异性抑制剂更佳。IBS患者结肠黏膜炎症或许能解释标准疗法效果不佳者长期反复复发的情况。美沙拉秦具有肠道抗炎作用,其主要成分5-氨基水杨酸(5-aminosalicylic acid,5-ASA)可针对抑制花生四烯酸代谢,通过抑制免疫炎症信号通路和直接抑制肥大细胞数量来减少黏膜的免疫活化,继而减少肥大细胞相关炎性介质(能增加肠道渗透性和敏感性)的释放,从而缓解患者腹痛、腹泻和便秘等症状[14]。Corinaldesi等[15]的随机双盲对照临床试验发现,与安慰剂组相比,IBS患者接受美沙拉秦治疗后肥大细胞数量明显降低(P=0.001 4),免疫细胞数量降低(P=0.008 2),总体临床表现明显改善(P=0.038)。一项针对感染后IBS(PI-IBS)患者的前瞻性研究[16]结果显示,美沙拉秦可通过调节黏膜免疫活性来减少后续PI-IBS的风险。Lam等[17]的一项为期12周的双盲、随机、安慰剂对照试验发现,与安慰剂相比,美沙拉秦对未经选择的IBS-D患者并未体现出任何临床获益或危害。而一项纳入意大利21个临床中心共185例IBS患者的随机、双盲、安慰剂对照研究[18]发现,虽然美沙拉秦在一级治疗终点(腹痛/不适的缓解达到满意程度)上并未优于安慰剂,但持续治疗应答的患者可从美沙拉秦治疗中获益。本研究中,给予美沙拉秦+曲美布汀联合治疗后,IBS-D患者结肠黏膜肥大细胞数量明显降低(P<0.000 1),且临床总有效率明显高于曲美布汀组(P=0.008);IBS-C患者肥大细胞数量亦明显降低(P=0.031),但临床总有效率与曲美布汀组无明显差异(P=0.053)。
本研究的不足之处在于仅接受曲美布汀治疗的患者治疗结束后未行结肠镜复查,未能比较曲美布汀治疗前后肥大细胞及其相关炎性介质的变化,故未能分析美沙拉秦对肥大细胞及其相关炎性介质的影响。
综上所述,美沙拉秦联合曲美布汀治疗能减少IBS患者结肠黏膜肥大细胞数量及其相关炎性介质的释放,对IBS-D患者的临床疗效更佳,可为IBS临床治疗方案的选择提供一定的依据。但该结论需行更大规模的临床试验提供循证学依据。
1 Chey WD,Kurlander J,Eswaran S.Irritable bowel syndrome:a clinical review[J].JAMA,2015,313 (9):949-958.
2 Longstreth GF,Thompson WG,Chey WD,et al.Functional bowel disorders[J].Gastroenterology,2006,130 (5):1480-1491.
3 张祥令,臧贵勇,黄悦,等.肥大细胞甲苯胺蓝-PAS改良染色法[J].局解手术学杂志,2011,20 (4):444-445.
4 Dorofeyev AE,Kiriyan EA,Vasilenko IV,et al.Clinical,endoscopical and morphological efficacy of mesalazine in patients with irritable bowel syndrome[J].Clin Exp Gastroenterol,2011,4:141-153.
5 Park JH,Rhee PL,Kim HS,et al.Mucosal mast cell counts correlate with visceral hypersensitivity in patients with diarrhea predominant irritable bowel syndrome[J].J Gastroenterol Hepatol,2006,21 (1 Pt 1):71-78.
6 Weston AP,Biddle WL,Bhatia PS,et al.Terminal ileal mucosal mast cells in irritable bowel syndrome[J].Dig Dis Sci,1993,38 (9):1590-1595.
7 Kanazawa M,Watanabe S,Tana C,et al.Effect of 5-HT4receptor agonist mosapride citrate on rectosigmoid sensorimotor function in patients with irritable bowel syndrome[J].Neurogastroenterol Motil,2011,23 (8):754-e332.
8 Spiller RC.Targeting the 5-HT(3) receptor in the treatment of irritable bowel syndrome[J].Curr Opin Pharmacol,2011,11 (1):68-74.
9 Kozlowski CM,Green A,Grundy D,et al.The 5-HT(3) receptor antagonist alosetron inhibits the colorectal distention induced depressor response and spinal c-fos expression in the anaesthetised rat[J].Gut,2000,46 (4):474-480.
10 Gershon MD,Tack J.The serotonin signaling system:from basic understanding to drug development for functional GI disorders[J].Gastroenterology,2007,132 (1):397-414.
11 Papadakis KA,Targan SR.Tumor necrosis factor:biology and therapeutic inhibitors[J].Gastroenterology,2000,119 (4):1148-1157.
12 Klooker TK,Braak B,Koopman KE,et al.The mast cell stabiliser ketotifen decreases visceral hypersensitivity and improves intestinal symptoms in patients with irritable bowel syndrome[J].Gut,2010,59 (9):1213-1221.
13 Leighton MP,Lam C,Mehta S,et al.Efficacy and mode of action of mesalazine in the treatment of diarrhoea-predominant irritable bowel syndrome (IBS-D):study protocol for a randomised controlled trial[J].Trials,2013,14:10.
14 Corsetti M,Whorwell P.Novel pharmacological therapies for irritable bowel syndrome[J].Expert Rev Gastroenterol Hepatol,2016,10 (7):807-815.
15 Corinaldesi R,Stanghellini V,Cremon C,et al.Effect of mesalazine on mucosal immune biomarkers in irritable bowel syndrome:a randomized controlled proof-of-concept study[J].Aliment Pharmacol Ther,2009,30 (3):245-252.
16 Andresen V,Löwe B,Broicher W,et al.Post-infectious irritable bowel syndrome (PI-IBS) after infection with Shiga-like toxin-producingEscherichiacoli(STEC) O104:H4:A cohort study with prospective follow-up[J].United European Gastroenterol J,2016,4 (1):121-131.
17 Lam C,Tan W,Leighton M,et al.A mechanistic multicentre,parallel group,randomised placebo-controlled trial of mesalazine for the treatment of IBS with diarrhoea (IBS-D) [J].Gut,2016,65 (1):91-99.
18 Barbara G,Cremon C,Annese V,et al.Randomised controlled trial of mesalazine in IBS[J].Gut,2016,65 (1):82-90.
(2016-10-18收稿;2016-11-17修回)
Effect of Mesalazine Combined with Trimebutine on Mast Cell and Related Inflammatory Mediators in Colonic Mucosa in Patients with Irritable Bowel Syndrome
ZHANGHui1,MIAOQi2,WUYuelong3,WANJian1,WANGShanjuan1,LUFang1,LINYonghui1,RENHaifeng1,LIXiaobo2.
1DepartmentofGastroenterology,ShanghaiJiadingDistrictCentralHospital,Shanghai(201800);2DivisionofGastroenterologyandHepatology,RenJiHospital,ShanghaiJiaoTongUniversitySchoolofMedicine,Shanghai;3DepartmentofPathology,ShanghaiJiadingDistrictCentralHospital,Shanghai
LI Xiaobo,Email:lxb_1969@163.com
Irritable Bowel Syndrome; Mesalazine; Trimebutine; Mast Cells; Inflammatory Mediators
10.3969/j.issn.1008-7125.2017.05.005
上海市嘉定区科委医学科研课题(2014-KW-09)
#本文通信作者,Email:lxb_1969@163.com
Background:Mast cell activation is a characteristic of irritable bowel syndrome (IBS).Study on mast cell and the related inflammatory mediators in colonic mucosa is helpful for the evaluation and treatment of IBS.Aims:To assess the effect of mesalazine combined with trimebutine on colonic mucosal mast cell and related inflammatory mediators in patients with IBS.Methods:Forty patients with diarrhea-predominant IBS (IBS-D) and 40 patients with constipation-predominant IBS (IBS-C) from Oct.2014 to June 2016 at Shanghai Jiading District Central Hospital were enrolled,20 healthy volunteers were served as controls.Forty patients with IBS-D and 40 patients with IBS-C were randomly divided into mesalazine+trimebutine group and trimebutine group,the treatment courses were all 4 weeks.Number of mast cell was counted by modified toluidine blue staining.Score of related inflammatory mediators were evaluated by immunohistochemistry.Clinical efficacy was assessed.Results:Compared with healthy controls,number of mast cell at baseline was significantly increased both in IBS-D and IBS-C patients (P<0.05).After treatment with mesalazine+trimebutine,number of mast cell was significantly decreased (P<0.05).At baseline,immunohistochemical staining score of 5-HT,IL-1,TNF-α,histamine,tryptase were significantly increased in IBS patients than in healthy controls (P<0.000 1).After treatment with mesalazine+trimebutine,above-mentioned inflammatory mediators were significantly decreased (P<0.05).In IBS-D patients,the total efficacy rate in mesalazine+trimebutine group was significantly increased than that in trimebutine group (85.0%vs.45.0%,P=0.008).In IBS-C patients,no significant difference in total efficacy rate was found between mesalazine+trimebutine group and trimebutine group (55.0%vs.25.0%,P=0.053).Conclusions:Mesalazine combined with trimebutine is an effective and safe approach to reduce mast cell infiltration and release of related inflammatory mediators,and is more efficient for patients with IBS-D.

