高亲和力的人源化CD20单克隆抗体的研究进展
张倩倩 郭尚敬,2*
(1山东省聊城大学药学院 252000; 2 山东省聊城大学农学院 252000)
据世界卫生组织统计,淋巴瘤发病率逐年增加,其中非霍奇金淋巴瘤(non Hodgkin′s lymphoma, NHL)是临床最常见的淋巴系统恶性肿瘤。NHL占中国整个肿瘤发生的4%,死亡率居第14位[1~4]。对于这类恶性肿瘤,传统的治疗方式主要是放化疗、骨髓移植或外周血造血干细胞移植等。然而,对于许多难治性、复发性及对化疗和干细胞移植耐受力较差的患者而言,研发低毒性、更有效的靶向性治疗方法显得尤为重要。本文简介抗CD20的单克隆抗体药物,并综述人源化CD20单克隆抗体亲和力和免疫原性的研究进展。
1 抗CD20的单克隆抗体药物
近年来,单克隆抗体及靶向治疗NHL的临床试验研究取得了重大进展,其中被广泛使用且富有成效的是抗CD20的单克隆抗体药物[5]。CD20分子是一种B淋巴细胞表面的特异性膜蛋白,以非糖基化形式存在。CD20分子有4个跨膜区,氨基端和羧基端都位于细胞质内侧,在第三跨膜区和第四跨膜区之间,有一个由43个氨基酸组成的环区(large loop),构成其主要的抗原表位[6,7]。该抗原表位仅存在于前B细胞、成熟B细胞和超过95%的恶性B细胞表面,而不表达于造血干细胞、浆细胞和其他组织中,且其与抗体结合后无显著内化和脱落,也不因与抗体结合而发生抗原调变,从而成为治疗B细胞非霍奇金淋巴瘤的理想靶点[8]。
目前有多个以CD20为靶点治疗非霍奇金淋巴瘤的单抗药物已被美国食品药品管理局批准上市(表1)。这些CD20单抗与B细胞淋巴瘤表面抗原结合后,主要通过补体依赖的细胞毒作用(complement dependent cytotoxicity,CDC)以及抗体依赖细胞介导的细胞毒作用 (antibody-dependent cell-mediated cytotoxicity,ADCC),直接诱导肿瘤细胞降解[9]。该药可特异性地与B淋巴细胞表面的CD20 抗原结合,激发机体免疫反应,为B细胞NHL的治疗提供了新的希望。
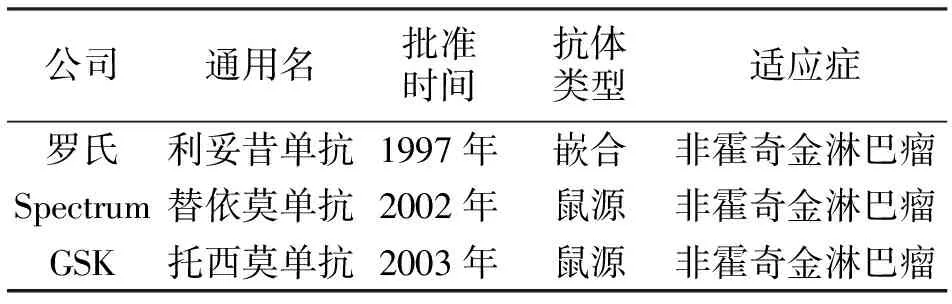
表1 FDA批准的治疗非霍奇金淋巴瘤的单抗药物
2 单克隆抗体药物的免疫原性
自1997年上市以来,利妥昔单抗(Rituximab)的销售成果—直较好,2007年旳销售额达到了22亿美元,2012年增长到67亿美元,毫无疑问地成为单克隆抗体药物市场的主导药物。但是,由于Rituximab是一种人鼠嵌合型的抗CD20抗体,抗体分子中仍然包含约30% 的鼠源序列,这类鼠源单克隆抗体进入人体后可能引起人抗鼠抗体免疫应答(HAMA),导致无法长期用药,严重制约Rituximab的使用。为此,需要降低该类药物的免疫原性,并提高其抗肿瘤活性,达到增加药效的目的。
从结构上看,Rituximab作为人鼠嵌合抗体,虽然含有人的Fc段,但抗体的重轻链可变区仍然是鼠源序列,分子中30%的氨基酸序列来源于鼠抗,仍被人体视为外源蛋白,具有免疫原性,诱发人体产生中和抗体,降低持续性用药的治疗效果。为进一步降低CD20抗体中鼠源序列的免疫原性,出现了以PDL公司的“complementarity-determining region,CDR”移植为主要手段的抗体人源化技术[10]。该技术将鼠抗的CDR区移接连入人抗体的框架区,从而减少鼠抗框架区导致的免疫原性。
尽管如此,这类抗体的人源化框架与鼠源性CDR区的氨基酸组合也可能被T细胞识别而引起免疫应答。T细胞对异源蛋白的识别主要由抗原呈递细胞表面的MHC II与蛋白多肽结合后,呈递给T细胞受体,进而活化淋巴细胞,产生免疫应答。因此,在设计选择人源框架时,应尽可能降低其框架多肽与MHC II分子的结合,从而使人源化抗体的免疫应答降低到最小。张海峰(专利US 20130089540A1)采用独特的抗体人源化技术,在鼠单抗2B8(Rituximab的原始鼠源单抗)的序列基础之上,设计选择了与MHC II结合位点少的人胚系(germline)抗体框架序列进行鼠源单抗2B8的人源化,大大减少了免疫原性,从而得到人源化的CD20抗体。通过该技术改造的人源化CD20抗体分子,表现出了较低的免疫原性。但因其未对该抗体的亲和力进行任何修改,其杀伤肿瘤细胞的活性仍较低,仍需增加药效提高其抗肿瘤活性,因此亲和力的提高是非常必要的。
3 单克隆抗体药物的亲和力
抗体亲和力是指抗原决定簇和抗体分子可变区互补构型的结合强度。亲和力越大表示抗体的结合反应越快,抗原抗体复合物越不易解离。亲和力的高低是由抗原分子的大小以及抗体分子的结合位点与抗原决定簇之间立体构型的合适度决定的。对于高度表达CD20的B细胞恶性淋巴瘤,Rituximab的临床疗效已得到肯定,但其临床反应率仅50%左右,完全缓解率只有10%[11]。随着治疗应用的推广,仍不断发现难以治愈的恶性淋巴瘤病例,且该类肿瘤一旦复发,其耐药再治疗的缓解率极低,为此需要不断提高单克隆抗体的亲和力,从而提高其抗肿瘤的活性。
迄今为止,提高抗体亲和力的方法主要是以原亲本单抗为改造模板,通过构建其突变体抗体库(如核糖体展示、酵母杂交、噬菌体展示文库等)进行筛选,最终获得更高亲和力的单克隆抗体。但以上这些技术都具有各自的局限性:如难以构建能覆盖所有位点、可以突变成任何氨基酸的抗体文库;构建抗体库及筛选过程费时、费力、费财等。近年来,应用计算机模拟突变方法提高抗体亲和力的技术,已成为该领域的热点。赵磊等在前期得到的Rituximab/CD20抗原肽共结晶的基础上,通过基于抗体进化规律的计算机辅助设计,将重链可变区57位天冬氨酸和102位酪氨酸分别突变成谷氨酸和赖氨酸,将轻链可变区93位天冬酰胺突变成精氨酸,使Rituximab的亲和力提高了15.47倍。尽管该三点组合突变体极大地提高了抗体的亲和力,但由于其整个可变区都是异源的,在进行临床试用时仍能够被人体的免疫系统识别而产生人抗鼠抗体(HAMA)反应,因此有必要对鼠单抗可变区作进一步的人源化改造。
4 展望
进行抗体的人源化有两个基本原则,即保持或提高抗体的亲和力和特异性,以及大大降低或基本消除抗体的免疫原性。但是目前为止,CD20抗体的人源化与亲和力的提高都是分别进行的,还没有发现将这两者同时进行的设计与改造,从而获得既有低免疫原性又有高亲和力的抗体药物。开发既有低免疫原性又有高亲和力的抗体药物,不仅具有重要的理论价值,而且具有巨大的应用前景。

