锂离子电池中苯衍生物氧化还原穿梭分子的一种稳定性模型:同时考虑成键/断键反应和还原反应
陈建华, 谢湘华, 朱云霞, 张 孟, 贺黎明, 王良琛
(华东理工大学物理系,上海 200237)
锂离子电池中苯衍生物氧化还原穿梭分子的一种稳定性模型:同时考虑成键/断键反应和还原反应
陈建华, 谢湘华, 朱云霞, 张 孟, 贺黎明, 王良琛
(华东理工大学物理系,上海 200237)
提出了锂离子电池中苯衍生物氧化还原穿梭分子的一种稳定性模型。此模型同时考虑了电池中氧化还原穿梭分子的成键/断键反应和还原反应,在100%穿梭分子保护充电次数的实验值(用对数表示)和组合反应指数(Eb(ER)+0.3Eb(Li))之间得到了很好的线性关系,其中Eb(ER)和Eb(Li)分别是氧化还原穿梭分子阳离子在模型反应中与乙基(ER)、Li原子团中单个Li原子的结合能。
锂离子电池; 苯衍生物; 氧化还原穿梭分子; 稳定性模型
锂离子电池是电动力车、混合动力车以及嵌入式混合动力车最具前景的电源之一。为了深入研究这一项技术,锂离子电池安全问题变得非常重要。锂电池的过充是非常普遍的,但却存在很大安全隐患。过充会使电池组分间发生各种化学和电化学反应[1-2],导致气体泄漏[1,3],电池温度快速升高[1-3],还会引发电池自加速反应从而导致热击穿甚至爆炸[4]。在电解液中加入氧化还原穿梭化合物(Redox shuttle additives)是一种有效防止锂电池过充的理想技术[5-17]。它利用了穿梭分子(梭子)的循环氧化还原反应:当锂电池过充时,阳极电压上升并达到梭子S的氧化电势Eox(一般高于阳极电压0.3~0.4V) 后,在阳极附近的电中性梭子S被氧化生成阳离子S+,S+之后迁移到阴极,被阴极电子还原成电中性梭子S,并扩散回到阳极。因此,过充时充电器强加的电流因阳离子S+在电池内部从阳极到阴极的迁移电流而消减,从而使锂离子电池的电压稳定在某一阈值电压之下,防止了电池的过充危害。
在锂离子电解液中加入梭子的技术难点是找到寿命长、稳定性好的梭子。文献[18]研究了58种芳香族有机梭子,其中2,5-双-叔丁基-1,4-二甲氧基苯(DTDMB)的寿命较长,100%过充循环保护次数(Ncycle)大于300次,有5种分子的Ncycle为12~33次,其余52种分子的Ncycle低于9次[18]。Chen和Amine小组[11,19-20]研究了DTDMB、1,4-二甲氧基苯(DMB)等几种苯衍生物梭子在过充时在电池内部可能发生聚合反应、分解反应等的副反应。本文将另辟蹊径,研究各种苯衍生物阳离子在成键/断键反应和氧化还原反应中的化学能和梭子稳定性之间的关系。
1 实验方法
本文中梭子实验数据都来自于戴尔豪斯(Dalhousie)大学Dahn实验室对于锂离子纽扣电池的测试结果[6-10,12-16]。测试条件:Li离子电池LiFePO4/Li4/3Ti5/3O4,电解液采用0.7mol/L的双草酸硼酸锂(LiBOB)溶液,溶剂为混合物(碳酸丙烯酯(PC)、碳酸二甲酯(DMC)、碳酸乙烯酯 (EC)、碳酸二乙酯(DEC)按照体积比1∶2∶1∶2混合),之后加入梭子使梭子浓度为0.1mol/L (若梭子最大浓度小于0.1mol/L,则添加到其最大溶解度)。LiFePO4来自于Phostech Lithium (Montreal,PQ,Canada),Li4/3Ti5/3O4来自于NEI Corp.(Piscataway,NJ,USA),LiBOB来自于德国的Chemetall。电极由w=10% Super S 炭黑 (MMM Carbon,Belgium)和w=10%聚偏二氟乙烯 (PVDF)2种活性材料制成。LiFePO4以及Li4/3Ti5/3O4电极涂布在铝箔上。阴极采用具有20%过载电容的材料,当锂电池充满时(LiFePO4),保证阴极相对Li/Li+电极有一个确定的稳定电势差。锂电池通常需要10h充满到100%的电量,实验中将电池充到200%的常规电量(100%的过充)或者达到一个特定的截止电压(一般来说对Li/Li+相对电势达4.9V)[8-9,15-16]。
本文中所有计算在Gaussian03软件中完成,该软件基于广泛使用的B3LYP杂化基组[21],Becke电子交换和Lee-Yang-Parr电子关联泛函[22]。
2 结果与讨论
梭子S在阳极氧化分解为阳离子S+,S+在电池内部迁移到阴极并被还原为梭子S,S再扩散回阳极,构成氧化还原循环。阳离子S+向阴极迁移的过程中,可能和电池内部其他物质发生各种复杂的化学或电化学反应,生成化合物从而失去锂电池过充保护剂的特性。梭子阳离子S+的活性越低,参与各种化学反应的能力越差,对应S化合物作为电池过充保护剂的稳定性越好。本文将避开可能发生的各种复杂反应,直接探讨S+化学活性和保护剂稳定性的关系,建立一个内在联系来预测未测试梭子的稳定性,并设计出更好的梭子结构。
为了定量评价S+的活性,在前期的工作中[23-24],设计了式(1)所示的S+与乙自由基C2H5—(ER)的模型反应,并用模型反应的负反应能Eb(ER)作为S+活性的评价指标,Eb(ER)的定义见式(2)。由于ER和S+成键位置不同,能量Eel(ER_S+)的取值也不同,式(2)中取最小能量。ER和 S+均为具有开放式电子结构的自由基,二者相加的能量必然大于结构更紧凑的ER_S+的能量,故Eb(ER)为正值。Eb(ER)大小仅表明各种S+的相对活性,即S+参与成键/断键反应的能力,Eb(ER)越大,阳离子S+的活性越大。
(1)
Eb(ER)=-{min[Eel(ER_S+)]-[Eel(ER)+Eel(S+)]}
(2)
表1列出了由式(2)计算得到的20种苯衍生物Eb(ER)值,实验测量得到的相对氧化电势(Eox)和100%过充保护最大次数(Ncycle)。Ncycle为苯衍生物作为锂电池过充保护剂的稳定性评价指标之一,Ncycle越大,对应保护剂的稳定性则越好。Eb(ER)在1.43~2.16eV变化,Ncycle超50的仅有5种,其余15种稳定性都较差,在2~49之间变化。Ncycle和Eb(ER)的关系如图1所示,Eb(ER)越大,Ncycle越小,即阳离子S+的活性越大,相应保护剂稳定性越差。
lnNcycle,fit=-5.453Eb(ER)+12.63
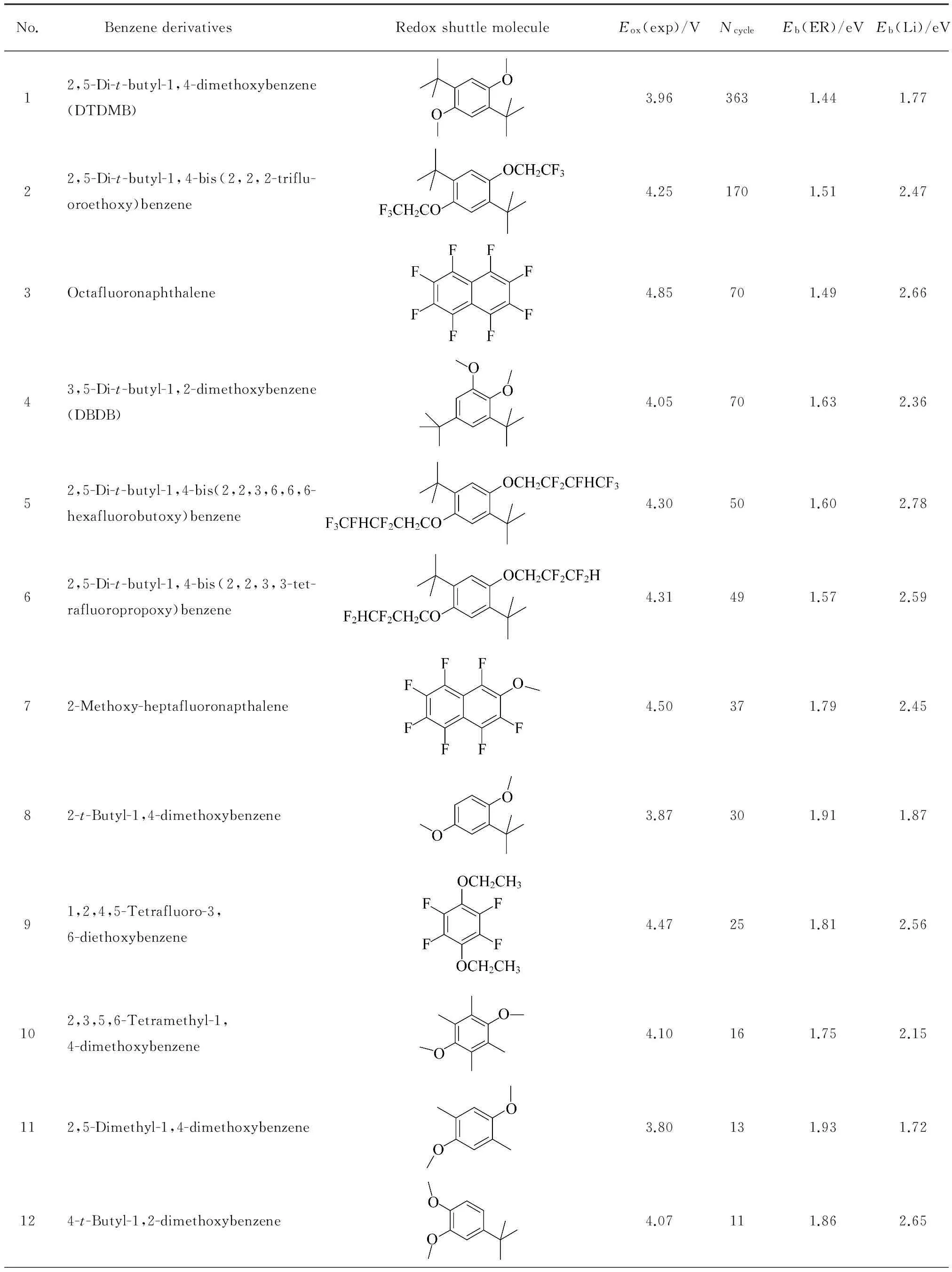
(3)表1 20种苯衍生物的活性参数Table 1 Activity parameters of twenty benzene derivatives
(续表1)

No.Benzenederivatives RedoxshuttlemoleculeEox(exp)/VNcycleEb(ER)/eVEb(Li)/eV13Hexamethylbenzene4.2072.162.56141,2,4,5-Tetrafluoro-3,6-dimethoxybenzene4.4941.832.60154-t-Butyl-1-methoxybenzene4.1542.112.35163,5-Di-t-butyl-1,2-bis(2,2,2-trifluoroethoxy)benzene4.5031.653.17171,3,5-t-Butyl-2-methoxybenzene4.4032.022.54182,3-Dimethoxytoluene4.0531.972.71192,5-di-t-Butyl-1,4-bis(difluoromethoxy)benzene4.9022.062.62202,5-di-t-Butyl-1,4-diethoxybenzene(DTDBE)3.80481.431.65
由图1中示出的数据计算得到的标准偏差为0.896,平均偏离系数Df为2.45,用Ncycle,fit/2.45和2.45Ncycle,fit分别对Eb(ER)作图,分别对应图1中2条虚线,则79%的数据点都落在这2条虚线之间。例如,假设得到某个分子Eb(ER)的计算值为1.60 eV,根据式(7)得到Ncycle,fit=50。那么,就可以预测这种分子作为锂电池梭子时,其循环次数有79%的概率落在20~123之间。将20#(DTBEB)的Eb(ER)值1.43 eV代入经验公式(7)可以得到预估循环次数为125,偏离因素为2.45,落在51~307的概率有79%。测试得到的循环次数为48,落在下边缘51附近。这个例子表明了Eb(ER)模型提供了DBDB梭子稳定性一个简单且有意义的解释,可以半定量地预测其循环次数,但还需要进一步进行修正。
在锂电池内部S+可能参与的各种副反应中,除了成键/断键反应外,还会存在一些氧化还原反应,对S+参与氧化还原的活性进行评价是非常必要的。由此,本文设计了式(4)的模型反应,选择小分子Li作为还原剂的代表,用该模型反应的负反应能Eb(Li)比较各种S+参与还原反应的相对活性,计算公式和结果分别见式(5)和表1。同理,Li和S键合的位置不同,计算得到的Eb(Li)也不同,取最小值。
(4)
图2中1#~19#样品Eb(Li)和Ncycle的关系曲线表明,Ncycle随Eb(Li)的增大而降低,lnNcycle,fit和Eb(Li)拟合结果用图中的实线表示,分散系数平均值为3.83,两条虚线分别为Ncycle,fit/3.83和3.83Ncycle,fit,Ncycle,fit落在两条虚线间的概率约为68%,图1表现得更加离散。
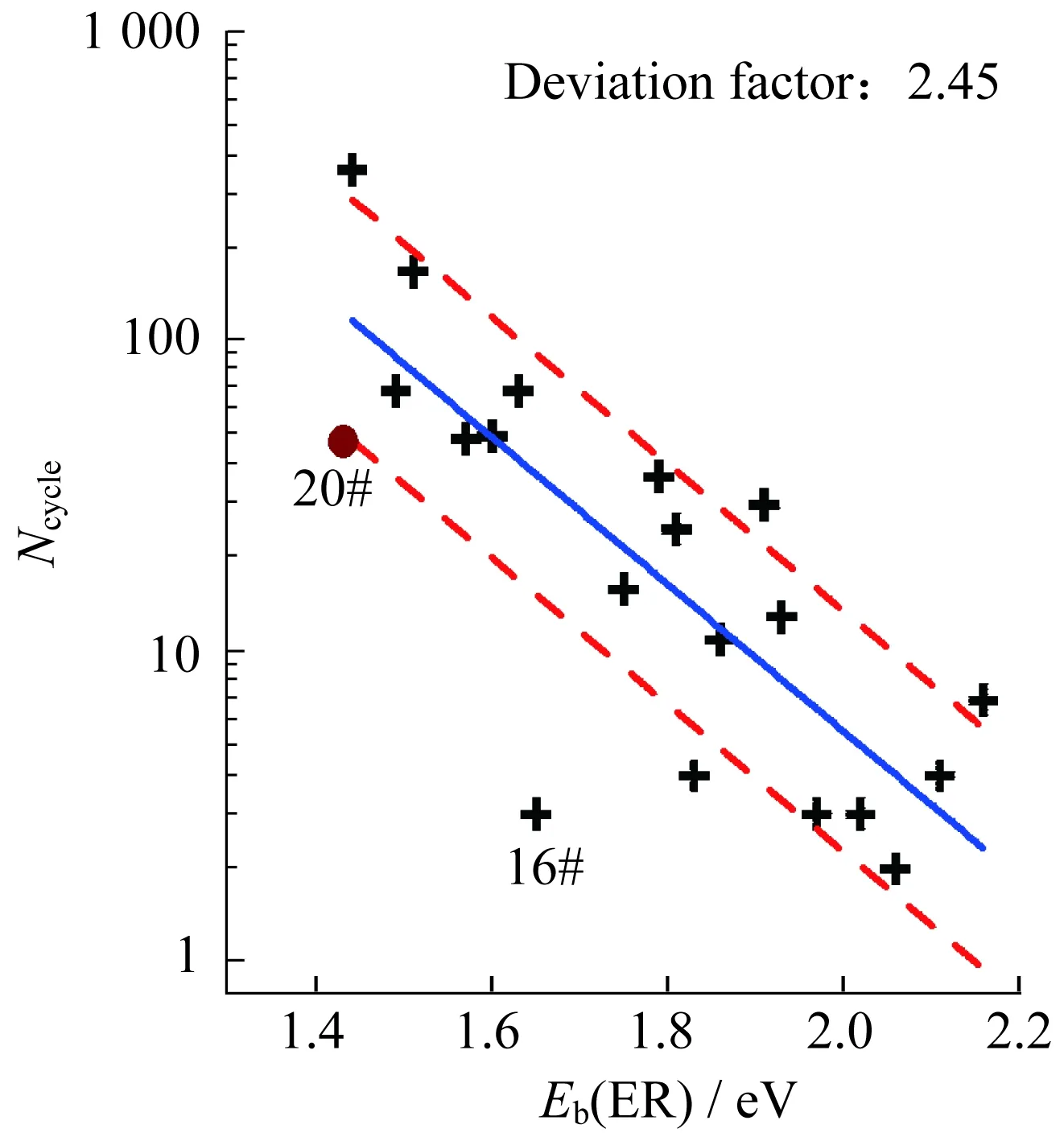
图1 各种苯衍生物梭子Ncycle和Eb (ER)的关系Fig.1 Relationship between Ncycle andEb (ER) of the benzene derivatives
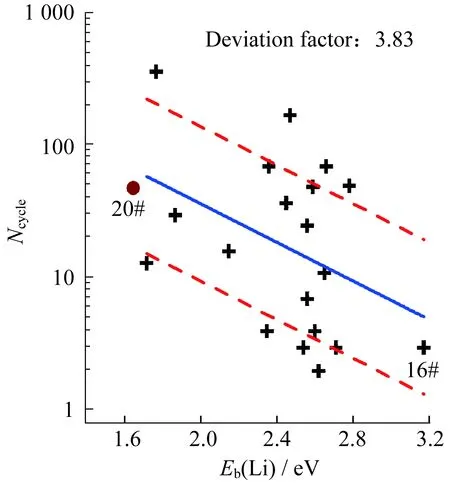
图2 各种苯衍生物梭子Ncycle和Eb (Li)的关系Fig.2 Relationship between Ncycle and Eb (Li) of the benzene derivatives
若同时考虑阳离子梭子参与成键/断键反应和氧化还原反应,则lnNcycle与Eb(ER)和Eb(Li)组合关系可拟合为:
(6)
其中a,b,c都是正值常数。
公式(6)的拟合结果取决于组合反应活性因子参数b。对表1中1#~19#数据进行综合计算,结果发现拟合偏离因子Df对参数b的取值并不敏感。当b取0.2,0.3和0.4的时候,这些经验性拟合的偏离因子分别为2.00,1.93和1.96;取b=0.3时,1#~19#梭子的数据分布如图3所示,其中17#,18#梭子数据基本重合,图3实线为lnNcycle与Eb(ER)+0.3Eb(Li)计算值的线性拟合结果,拟合标准差d为0.66,偏离系数平均值Df为1.93,经验拟合方程为
lnNcycle,fit=
(7)
图3中示出的偏差系数平均值为1.93,两条虚线分别为Ncycle,fit/1.93和1.93Ncycle,fit。68%的数据都在Ncycle,fit/1.93与1.93Ncycle,fit之间。也就是说,利用式(7)计算得到的Eb(ER)+0.3Eb(Li)来预测梭子的100%过充循环次数的话,实际上实验数据有68%的概率落在Ncycle,fit/1.93~1.93Ncycle,fit区间。一般来说,大的循环次数的相对实验误差要比小的循环次数的相对误差要小。图3显示了测量得到的Ncycle>10的1#~12#梭子更接近经验拟合的直线。对于这12种梭子来说,由式(7)拟合得到循环次数的平均偏差因数只有1.69。
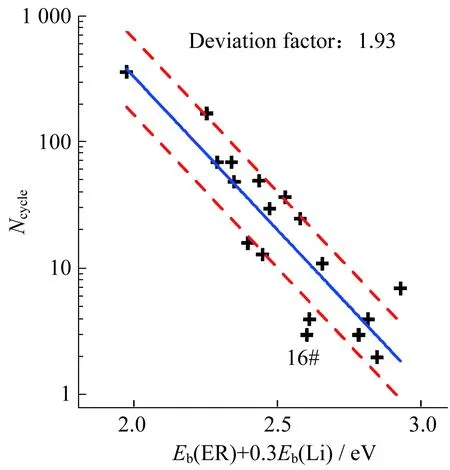
图3 19种梭子Ncycle和Eb(ER)+0.3Eb(Li)的关系Fig.3 Relationship between Ncycle and Eb (ER)+ 0.3Eb(Li) for 19 benzene derivatives
以图1中偏离最多的16#分子(3,5-二叔丁基-1,2-双(2,2,2-三氟乙氧基苯)为例,比较单一模型与组合模型的优劣。16#梭子Eb(ER)值相对较小,为1.65 eV。单纯考虑Eb(ER)拟合经验公式(3)计算得到的期望循环次数Ncycle,fit=38,实验结果Ncycle仅为3,其偏离因子Df=12.7,误差d=2.54,是拟合标准差(0.896)的2.8倍。将16#分子Eb(Li)值(3.17 eV)和Eb(ER)=1.65 eV代入公式(7)中,预测得到的循环次数为Ncycle,fit=11.5,相比测试得到的3次偏离不远,其偏离因子为3.8,误差为1.34,是拟合标准差(0.66)的2.0倍,组合模型比仅考虑Eb(ER)值的单一模型的误差要小很多。
组合模型比单一模型更准确地预测到某种苯衍生物梭子的稳定性,不仅考虑到了苯环上取代基的位置、个数和类型,同时还考虑到了取代支链上的情况。在表1所列1#~19#苯衍生物中,1#(DTDMB)最稳定,它的Eb(ER)值(1.44 eV)和Eb(Li)的值(1.77 eV) 都很小,表明它在断键/成键反应、还原反应过程中的活性都很差。4#梭子(DBDB)苯环上取代基种类,个数与DTDMB (1#)相同,但位置发生重排。相比DTDMB (1#),DBDB(4#)苯环上1-甲氧基上的氧原子缺少邻位烷基的保护,活性增大,Eb(ER)值上升到了1.63 eV,同时1,2-相邻两个氧原子中间区域形成氧化中心,发生氧化还原反应的活性增大,Eb(Li)值上升了0.59 V,达到2.36 eV。另一方面是支链氟化基的影响,2#和1#(DTDMB)的苯环取代基种类、个数和位置均相同,仅将1#中苯环1,4-对位上的两个甲氧基(--O--CH3)中的甲基替换成氟化乙氧基(--OCH2CF3),导致还原反应活性增强,Eb(Li)值上升到2.47 eV,比1#(1.77 eV)增大了0.7 V。16#的苯环基本结构同DBDB,而甲氧基上的甲基取代为--CH2CF3,基于上述2方面的原因,Eb(ER)(1.65 eV)和DBDB(2#)分子(1.63 eV)接近,而Eb(Li)预估值应达到3.06 eV(1.77+0.59+0.70),与计算得到的3.17 eV非常接近。
上述稳定性模型和经验拟合方程并不包含20#梭子(DTDEB),原因也许为:20#(DTDEB)和1#(DTDMB)苯环基本结构相同,仅仅1,4-对位上两个乙氧基取代了甲氧基。20#DTDEB的反应性指标Eb(ER)和Eb(Li)分别为1.43 eV和1.65 eV,该数据比1#DTDMB的1.44 eV和1.77 eV还要理想。因此,无论是从分子结构,还是反应性能计算值,20# DTDEB稳定性应该和1#DTDMB相当。然而,20#的100%过充循环次数的测量值仅为48,远远小于1#的363次,也远小于式(7)计算预期值495次。若将20#DTDEB包括到模型研究分子中,20种苯衍生物梭子lnNcycle与组合反应性指标Eb(ER)+0.3Eb(Li)的关系如图4所示,经验性拟合方程为:
(8)
拟合偏离因子为2.18。用此方程计算得到20# DTDEB的循环次数Ncycle,fit=255,是测量值(48次)的5.3倍。在图4中,其他19个数据点都分布在拟合直线的附近,只有DTDEB离开拟合直线非常远,并且具有2.4倍的标准差。这有可能是测量得到的DTDEB的循环次数为48次是不正确的,因为实验得到的梭子循环次数是基于人造的锂离子电池。猜测的证据就是,目前,Amine等[17]发现了一种新型的乙二醇类梭子2,5-二叔丁基-1,4-双(2-甲氧乙氧)苯(DBBB),该分子可以对锂电池提供高效的长时间过充保护(在C/2速率下,Ncylcle=180)。理论上讲,只要将20#DTDEB的两个乙氧基--OCH2CH3替换成两个甲氧乙氧基--OCH2CH2OCH3,就可以得到DBBB。从分子结构上看,这样的基团替换不会降低苯环分子的反应活性,也不会提高分子的稳定性。因此,实际的20#DTDEB的100%过充循环次数应该比报道的48次更高。
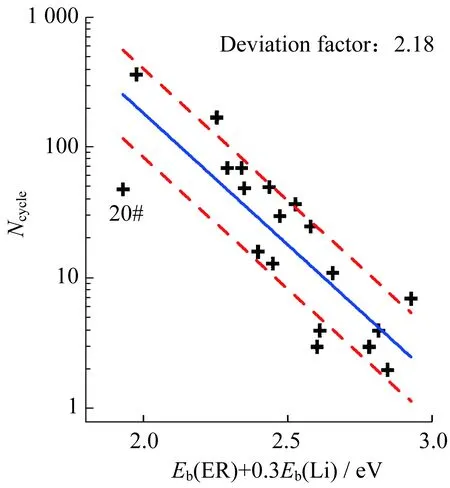
图4 20种梭子Ncycle和Eb(ER)+0.3Eb(Li)的关系图Fig.4 Relationship between Ncycle and Eb(ER)+ 0.3Eb(Li) for 20 benzene derivatives
3 结 论
本文介绍了一种新的锂电池苯衍生物梭子的稳定性模型。这个模型要比Eb(ER)模型更好,原因如下:
(1) 这个模型将梭子的循环次数和组合反应性指标Eb(ER)和Eb(Li)联系起来,分别对应断键/成键反应和还原反应。因此,这个模型考虑到了苯衍生物梭子在氧化之后成为具有开放电子结构的自由基的不稳定因素以及在高于5 eV的能量下形成阳离子的不稳定因素。
(2) 对于19种苯衍生物梭子,相比单一反应性指标Eb(ER),对数形式的100%过充保护循环次数的实验值与组合反应性指标(Eb(ER)+0.3Eb(Li))更具有关联性。后者拟合直线的偏离因子为1.93,前者的拟合直线的偏离因子为2.45。
(3) 对于只有3次100%过充循环次数的16#梭子3,5-二叔丁基-1,2-双(2,2,2-三氟乙氧基苯),它的Eb(ER)值为1.65 eV,是比较小的,而它的Eb(Li)值为3.17 eV,是这组分子中最大的。用Eb(ER)模型很难解释为什么16#梭子的测量循环次数会比模型预测的38次少很多,然而在这个新的模型中,考虑了还原反应的作用,预测得到的循环次数为11.5,与实验值相比差距小。
[1] LEISING R A ,PALAZZO M J ,TAKEUCHI E S ,etal.Abuse testing of lithium-ion batteries:Characterization of the overcharge reaction of LiCoO2/graphite cells [J] .Journal of Electrochemistry Society,2001,148(8):A838-A844.
[2] OHSAKI T,KISHI T ,KUBOKI T ,etal.Overcharge reaction of lithium-ion batteries [J].Journal of Power Sources,2005,146(1-2):97-100.
[3] LEISING R A,PALAZZO M J,TAKEUCHI E S,etal.Overcharge reaction of lithium-ion batteries [J] .Journal of Power Sources,2001,97-98:681-683.
[4] WANG H,CHEN M C.Modification of LiCoO2by surface coating with MgO/TiO2/SiO2for high-performance lithium-ion battery [J].Electrochemical and Solid-State Letters,2006,9:A82-A85.
[5] ABRAHAM K M.Electrochromism in nickel oxide thin films studied by OMA and raman spectroscopy[J].Journal of Electrochemistry Society,1988,137(7):A1856-A1857.
[6] CHEN J,BUHRMESTER C,DAHN J R.Chemical overcharge and overdischarge protection for lithium-ion batteries [J] . Electrochemical and Solid-State Letters,2005,8:A59-A62.
[7] DAHN J R,JIANG J,FLEISCHAUER M D,etal.High-rate overcharge protection of liFePO4-based Li-ion cells using the redox shuttle additive 2,5-ditertbutyl-1,4-dimethoxybenzene [J].Journal of Electrochemistry Society,2005,152 (6):A 1283-A1289.
[8] BUHRMESTER C,CHEN J,MOSHURCHAK L,etal.Studies of aromatic redox shuttle additives for liFePO4-based Li-ion cells [J].Journal of Electrochemistry Society,2005,152(12):A2390-A2399.
[9] BUHRMESTER C,MOSHURCHAK L,WANG R L,etal.Phenothiazine molecules:Possible redox shuttle additives for chemical overcharge and overdischarge protection for lithium-ion batteries [J].Journal of Electrochemistry Society,2006,153(2):A288-A294.
[10] BUHRMESTER C,MOSHURCHAK L,WANG R L,etal.The use of 2,2,6,6-tetramethylpiperinyl-oxides and derivatives for redox shuttle additives in Li-ion cells [J].Journal of Electrochemistry Society,2006,153(10):A1800-A1804.
[11] Chen Z,Wang Q,Amine K.Understanding the stability of aromatic redox shuttles for overcharge protection of lithium-ion cells [J]. Journal of Electrochemistry Society,2006,153(12):A2215-A2219.
[12] MOSHURCHAK L,BUHRMESTER C,WANG R L,etal.Comparative studies of three redox shuttle molecule classes for overcharge protection of LiFePO4-based Li-ion cells [J].Electrochimica Acta,2007,52(10):3779 -3784.
[13] MOSHURCHAK L M,BULINSKI M,LAMANNA W M,etal.Direct comparison of 2,5-di-tert-butyl-1,4-dimethoy-benzene and 4-tert-butyl-1,2-dimethoxybenzene as redox shuttles in LiFePO4-based Li-ion cells [J]. Electrochemistry Communications,2007,9(7):1497-1501.
[14] WANG R L,MOSHURCHAK L M,LAMANNA W M,etal.A combined computational/experimental study on tertbutyl- and methoxy-substituted benzene derivatives as redox shuttles for lithium-ion cells [J].Journal of Electrochemistry Society,2008,155(1):A66-A73.
[15] MOSHURCHAK L M,BUHRMESTER C,DAHN J R.Triphenylamines as a class of redox shuttle molecules for the overcharge protection of lithium-ion cells [J].Journal of Electrochemistry Society,2008,155(2):A129-A131 .
[16] MOSHURCHAK L M,LAMANNA W M,BULINSKI M,etal.High-potential redox shuttle for use in lithium-ion batteries [J].Journal of Electrochemistry Society,2009,156(4):A309-A312.
[17] ZHANG L,ZHANG Z,REDFERN P C,etal. Molecular engineering towards safer lithium-ion batteries:A highly stable and compatible redox shuttle for overcharge protection [J].Energy Environmental Science,2012,5(8):8204 -8207.
[18] VOLLMER J M,CURTISS L A,VISSERS D R,etal.Reduction mechanisms of ethylene,propylene,and vinylethylene carbonates:A quantum chemical study [J].Journal of Electrochemistry Society,2004,151(1):A178-A183.
[19] CHEN Z,AMINE K.Degradation pathway of 2,5-di-tert-butyl-1,4-dimethoxybenzene at high potential [J]. Electrochimica Acta,2007,53(2):453-458.
[20] CHEN Z,QIN Y,AMINE K.Redox shuttles for safer lithium-ion batteries [J].Electrochimica Acta,2009,54(24):5605-5613.
[21] BECKE A D.Density-functional thermochemistry:III.The role of exact exchange [J].The Journal of Chemical Physics,1993,98(7):5648-5652.
[22] LEE C,YANG W,PARR R G.Development of the colle-salvetti correlation-energy formula into a functional of the electron density [J].Physical Review,1998,B37(2):785-789.
[23] WANG R L,DAHN J R.Computational estimates of stability of redox shuttle additives for Li-ion cells [J].Journal of Electrochemistry Society,2006,153(10):A1922-A1928.
[24] CHEN J H,HE L M,WANG R L.Correlation between the stability of redox shuttles in Li ion cells and the reactivity defined by the binding energy of redox shuttle cations with ethyl radical [J].Journal of Electrochemistry Society,2012,159(10):A1636-A1645.
AStabilityModelforBenzeneDerivativeRedoxShuttlesinLithium-IonBatteries:IncludingbothBondForming/BreakingReactionsandReductionReactions
CHENJian-hua,XIEXiang-hua,ZHUYun-xia,ZHANGMeng,HELi-ming,WANGLiang-chen
(DepartmentofPhysics,EastChinaUniversityofScienceandTechnology,Shanghai200237,China)
A stability model is presented for the benzene derivative redox shuttles in lithium-ion batteries.This model takes both bond forming/breaking reactions and reduction reactions of redox shuttles in batteries into account and obtains a very good linear correlation between the experimental numbers of100% shuttle-protected overcharge cycles in logarithm scale and the combined reactivity indexes,Eb(ER)+0.3Eb(Li),where the values ofEb(ER) andEb(Li) are the binding energy of the redox shuttle cation in the model reactions with an ethyl radical (ER) and a Li atom in bulk,respectively.
lithium-ion battery; benzene derivative; redox shuttle; stability model
1006-3080(2017)04-0509-07
10.14135/j.cnki.1006-3080.2017.04.009
2016-12-26
陈建华(1961-),男,浙江杭州人,硕士,研究方向为化学物理。E-mail:chenjianhua@ecust.edu.cn
贺黎明,E-mail:lmhe@ecust.edu.cn
O561.4;O646.2
A

