新型糖尿病治疗药物西他列汀制备技术研究进展
章鹏鹏,孟凡婷,牛婷婷,王 普
(浙江工业大学药学院,浙江 杭州 310014)
新型糖尿病治疗药物西他列汀制备技术研究进展
章鹏鹏,孟凡婷,牛婷婷,王 普*
(浙江工业大学药学院,浙江 杭州 310014)
西他列汀是首个二肽基肽酶-4(DPP-4)抑制剂的II型糖尿病治疗药,该药物的制备技术主要经历了三代工艺路线的发展。本文主要综述了西他列汀的制备技术,以及生物催化法应用于西他列汀的合成工艺路线,并对今后西他列汀制备技术的发展方向进行了展望。
西他列汀;II型糖尿病;生物催化法
0 引言
近年来,糖尿病发病率逐年提高。糖尿病已成为继心血管类疾病、恶性肿瘤后又一严重威胁人类健康的非传染性疾病。而糖尿病的II型发病率占90%。II型糖尿病的发病机制主要是因为人机体对胰岛素的抗性和胰岛素β细胞的功能缺陷所引发的[1]。临床上用于II型糖尿病治疗药主要有胰岛素分泌促进剂 (磺酰脲类、氯茴苯酸类)、胰岛素增敏剂(双胍类、噻唑烷二酮类)、胰岛素及胰岛素受体激动剂和二肽基肽酶-4 (DPP-4)抑制剂。
西他列汀 (Sitagliptin,JanuviaR),化学名称为:(3R)-3-氨基-1-[3-(三氟甲基)-5,6,7,8-四氢-1,2,4-三唑并[4,3-a]吡嗪-7-基]-4-(2,4,5-三氟苯基)丁-1-酮,英文名称为(3R)-3-Amino-1-[3-(trifluoromethyl) -5,6,7,8-tetrahydro-1,2,4-triazolo[4,3-a]pyrazin-7-yl]-4-(2,4,5-trifluorophenyl)butan-1-one, 它是由 Merck Sharp&Dohme Ltd公司开发的首个二肽基肽酶-4(DPP-4)抑制剂,是II型糖尿病口服治疗药捷诺维(盐酸西他列汀片,JANUVIA)的活性成分,该药在2006年10月于美国上市。西他列汀是一种二肽基肽酶-4(DPP-4)抑制剂,通过酰胺部分与DPP-4活性部分结合(结合模式图见图1),抑制其活性延长降血糖素(Incretin)[2]的半衰期,使得血浆中GLP-1和GIP活性提高的同时只是轻度增加其含量,却不会引起因GLP-1含量过高而产生的副作用,具有较好的安全性和耐受性[3-5]。在联合用药方面,与二甲双胍[6]或吡格列酮[7]联合用药时均优于其各自单独用药。临床上对于西他列汀的应用相比于同类药物其用药优势突出,基于其良好的市场前景,西他列汀具有较好的研究价值。近年来,对于西他列汀用药的需求增加,西他列汀的制备技术受到广泛关注。本文主要综述了西他列汀的三代制备工艺路线的发展,并介绍了生物催化法应用于合成西他列汀的制备工艺。
1 西他列汀的三代制备工艺路线
西他列汀在工业化生产前在实验室研究阶段的合成路线,以及工业化生产的第一代和第二代的合成工艺路线合成过程每一步都经过化学合成而成。第三代工艺路线中将生物催化法应用于合成路线,使得西他列汀的产率和e.e.值都有明显的提高。

图1 西他列汀与DPP-IV活性部位结合Figure 1 Mechanism of Sitagliptin involving the active site of DPP-IV
1.1 西他列汀处于实验室研究阶段的制备工艺由Kim等[5]发表的处于实验室研究阶段的合成路线较为繁琐,所需的反应条件苛刻,需要低温及较长反应时间,反应路线中部分使用的试剂也较昂贵,因此该反应路线并没有用于实际的工业化的生产。
1.2 西他列汀第一代制备工艺的合成路线
用于西他列汀工业化生产的第一代合成路线是由Hansen等人[8]采用手性磷根钌催化剂催化合成的化学合成路线。其路线图如图2所示,该反应路线是由 4-(2,4,5-三氟苯基)-3-氧代丁酸甲酯(1)经手性金属催化剂(S)-联萘二苯膦-氯化钌[(S)-binap-RuCl2]催化不对称加氢后,于氢氧化钠的甲醇溶液中水解,得水解产物(2),(2)在N-乙基-N-二甲胺基丙胺碳二亚胺盐酸盐(EDC-HCl)作用下,与O-苄基羟胺经缩合后,在三苯基膦和偶氮二甲酸二异丙酯(DIAD)的作用下环合得到 β-内酰胺类化合物(3),(3)经氢氧化锂水溶液水解开环得(4),(4)与 3-(三氟甲基)-l,2,4-三唑并[4,3-a]吡嗪(5)缩合后、脱去保护基团,即得西他列汀。

图2 第一代合成路线Fig 2 1st Generation process
1.3 西他列汀第二代制备工艺的合成路线
西他列汀的第二代合成路线[9]是由美国默沙东公司开发的采用手性铑作催化剂构建手性中心的化学合成路线,该路线较之前降低了生产成本; 以 2,4,5-三氟苯乙酸 (7) 与 2,2-二甲基-1,3-二噁烷-4,6-二酮 (8)缩合后生成化合物(9),(9)与 3-(三氟甲基)-1,2,4-三唑并[4,3-a]吡嗪(5)缩合后得到(2Z)-4-氧代-4-[3-(三氟甲基)-5,6-二氢-[1,2,4] 三唑并 [4,3-a] 吡嗪-7-(8H)-基]-1-(2, 4,5-三氟苯基) 丁-2-酮(10),(10)与乙酸铵作用得烯胺,烯胺在二聚氯代(l,5-环辛二烯)铑[{Rh(cod)Cl}2]和(R)-(-)-[(S)-2-[二(4-三氟甲基苯基)膦]二茂铁基乙基-2-叔丁基膦(R,S-t-bujosiphos)的作用下发生不对称加氢反应,得到西他列汀。
1.4 第三代合成路线
西他列汀的第三代合成路线[10]是在第二代化学合成法的基础上,改进了工艺,利用了突变转氨酶构建手性中心的方法开发了绿色环保的新型生物催化合成路线。将西他列汀中间体(2Z)-4-氧代-4-[3-(三氟甲基)-5,6-二氢-[1,2,4]三唑并[4,3-a]吡嗪-7-(8H)-基]-1-(2,4,5-三氟苯基)丁-2-酮(10),通过突变转氨酶ATA117的转氨基作用,直接将(10)合成为西他列汀。将转氨酶法运用于第三代合成路线,其产率较第二代的合成路线提高了53%,e.e.值也提高至99.95%,同时废物的排放也减少了19%。

图3 第二代和第三代合成工艺路线Fig 3 2nd Generation process and 3rd generation process
2 生物催化法在西他列汀制备工艺中的应用
2.1 转氨酶法
转氨酶(aminotransferases,EC 2.6.1.X),属于转移酶类,是以辅因子磷酸吡哆醛(pyridoxal phosphate,PLP)为氨基转移媒介,通过可立体选择性催化氨基供体(氨基酸或简单胺类)的氨基转移到潜手性受体酮来获得目的产物。转氨酶主要用于手性胺、手性氨基酸、手性氨基醇的制备及重氢手性标记。
在三代的合成路线中,Savile等[10]利用生物催化法通过突变转氨酶构建手性中心,从而使得合成工艺得到大幅度的优化。其过程是采用计算机分子模拟技术研究底物与酶的分子识别机理,发现西他列汀前体酮对应的两个大口袋酶结合位点是实现立体识别并完成反应的关键。利用计算机辅助设计和蛋白质工程技术,在野生型ω-转氨酶的基础上对其进行定向改造,经由底物结构的理性化设计和同源酶模型ATA-117的迭代突变重组,先后对酶的两个大口袋位点进行组合突变定向改造,经11轮定向进化后筛选获得27位点突变的新酶氨基酸序列。重组酶易于表达,结构稳定性和热稳定性均良好,能以廉价的异丙胺为氨基供体,耐受高浓度的DMSO(底物助溶剂),催化效率高。当酶添加量为6 g/L,24 h可实现200 g/L底物完全转化,e.e.值>99.5%。但是该转氨酶生物催化剂开发改造过程难度大,突变筛选通量大,改造风险和投入成本高。
2.2 间接合成,羰基还原酶法合成关键手性中间体
Cardila Healthcare Limited公司设计了手性胺的间接合成路线(见图4),同样以西他列汀前体酮化合物OTPP为底物,利用重组羰基还原酶催化不对称还原合成中间体(S)-HTPP而获得手性中心,再分别与甲磺酰氯、叠氮化钠反应替换该手性中心的羟基后,与Pd/c和硼氢化钠反应即可获得西他列汀[11]。
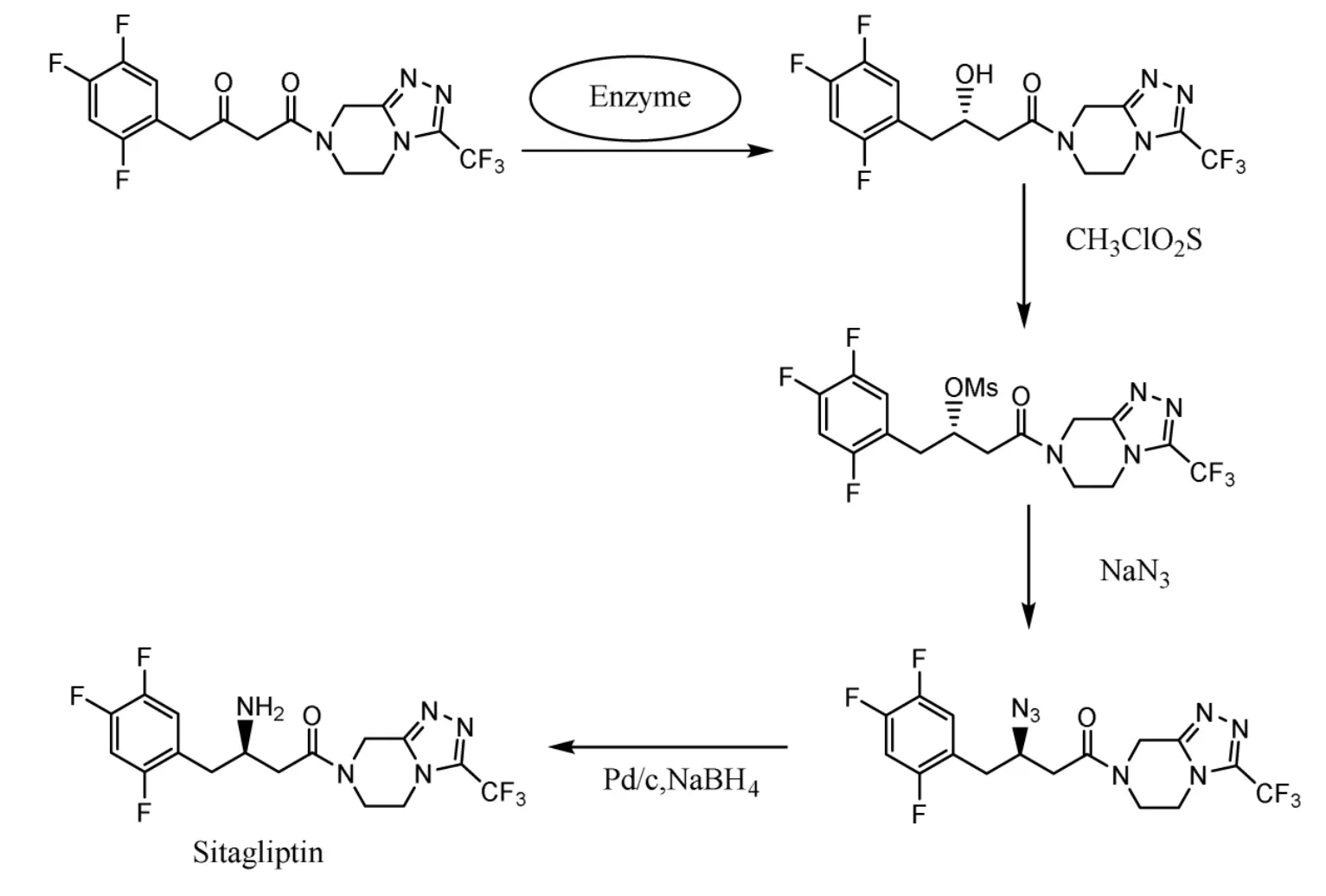
图4 手性胺的间接合成路线Fig 4 Indirect synthesis of chiral amines
以全细胞为催化剂不对称还原前体酮制备手性醇研究已经十分成熟,且将羰基还原酶法运用于该合成路线具备工艺的可行性,相关工艺也易于开发。故通过生物法不对称还原前体酮化合物OTPP制备该手性醇中间体(S)-HTPP(如图5)的研究便有着重要的意义。目前所报道的有Biocon Limited公司[12]利用真菌微生物短密青霉(Penicillium brevicompactum)MTCC 5962催化OTPP进行生物催化还原。

图5 全细胞催化OTPP制备手性醇中间体(S)-HTPPFig 5 Preparation of chiral alcohol intermediates(S) -HTPP by whole cell catalysis
针对相同的还原底物,笔者所在课题组[13]自行筛选得到了具有高立体选择性制备西他列汀关键手性中间体(S)-HTPP的菌种——小孢根霉须状变种 (Rhizopus microsporus var.rhizopodiformis)ZJPH1308。当底物浓度为 1~10 mmol/L时,反应产率达95%以上,提高底物浓度至15 mmol/L时,产率最高为85%;至20 mmol/L时,产率最高达到72%。而其e.e.值都保持>99%。另外,本课题组还从土壤中筛选得到一株恶臭假单胞菌(Pseudomonas putida)YHB3-10也可用于催化相同的反应,当底物浓度为10mmol/L时,反应24 h后产率为91.49%。当底物浓度提高至22.5mmol/L,并且在反应介质体系中加入5%(v/v)的邻苯二甲酸二丁酯,产率可达75.61%,较未添加的对照提高了 31.7%,e.e.值>99%[14]。
Xia等[15]利用筛选得到的假单胞菌(Pseudomonas Pseudoalcaligenes)静息细胞在DMSO溶剂中不对称还原OTPP合成(S)-HTPP,并且菌体细胞可实现重复批次利用。当底物浓度为25 mmol/L时,产率达90%以上,e.e.值>99%。
3 结论与展望
近年来,人们在物质生活水平快速提升的同时,II糖尿病的发病率也逐年提高,对人类的健康问题的威胁也在逐渐增大。西他列汀是目前II糖尿病的首选治疗药,有着较好的市场前景,其开发上市和制备技术的发展受到广泛的关注。目前对于西他列汀的制备技术虽然已较为成熟但仍存在不足,所以对于西他列汀的制备技术的开发仍值得研究。生物催化法在化合物合成上因其能避免一些化学法所必须的苛刻条件等优势,因此得到了广泛的应用。如何更好地将生物法运用于西他列汀制备的工艺路线中是未来研究的方向。
[1] 孙志,马丽,邱玉芹,等.2型糖尿病发病机制及胰岛β细胞功能障碍的研究进展[J].医学综述,2008,14(9):1371-1373.
[2] Idris I,Donnelly R.Dipeptidyl peptidase-IV inhibitors:a major new class of oral antidiabetic drug[J].Diabetes,Obesity and Metabolism, 2007, 9(2):153-165.
[3] Mu J, Woods J, Zhou Y P, et al.Chronic inhibition of dipeptidyl peptidase-4 with a sitagliptin analog preserves pancreaticβ-cellmass and function in a rodentmodel of type 2 diabetes[J].Muppidi Daniel JMD in Northborough,2006,5:1695-1704.
[4]Barnett A.DPP-4 inhibitors and their potential role in the management of type 2 diabetes[J].International Journal of Clinical Practice, 2006, 60(11):1454-1470.
[5]Kim D,Wang L P,BeconiM,et al.(2R)-4-Oxo-4-[3-(trifluoromethyl) -5,6-dihydro[1,2,4]triazolo[4,3-a]pyrazin-7 (8H)-yl]-1-(2,4,5-trifluorophenyl)butan-2-amine:a potent,orally active dipeptidyl peptidase IV inhibitor for the treatment of type 2 diabetes[J].Journal of Medicinal Chemistry, 2005, 48:141-151.
[6] Charbonnel B,Karasik A,Liu J,et al.Efficacy and safety of the dipeptidyl peptidase-4 inhibitor sitagliptin added to ongoing metformin therapy in patients with type 2 diabetes inadequately controlled with metformin alone[J].Diabetes Care, 2006, 29(12):2638-2643.
[7]Rosenstock J, Brazg R, Andryuk P J, et al.Efficacy and safety of the dipeptidyl peptidase-4 inhibitor sitagliptin added to ongoing pioglitazone therapy in patients with type 2 diabetes:a 24-week, multicenter, randomized, doubleblind, placebo-controlled, parallel-group study[J].Clinical Therapeutics, 2006, 28(10):1556-1568.
[8] Hansen K B, Balsells J, Dreher S, et al.First generation process for the preparation of the DPP-IV inhibitor Sitagliptin[J].Organic ProcessResearch&Development,2005, 9(5):634-639.
[9]Dreher SD,Ikemoto N,Gresham V,etal.Highly selective synthesis of 2-substituted-5-hydroxy-6-oxo-1,6-dihydropyrimidine-4-carboxylic acid derivatives using a novel protected dihydroxyfumarate[J].Tetrahedron Letters, 2004,45(31):6023-6025.
[10]Savile C K,Janey JM,Mundorff E C,et al.Biocatalytic asymmetric synthesis of chiral amines from ketones applied to sitagliptin manufacture[J].Science, 2010, 329(5989):305-309.
[11]Mendirata S K,Pandey B,Joshi R,et al.Process for preparing an intermediate of sitagliptin via enzymatic conversion:WO,2012/046254A2[P].2012-04-12.
[12]Singh S, Saravanan J, Despande S, et al.Fungal stereoselective reduction of keto intermediates of pharmaceutically active compounds to their corresponding hydroxy compounds:WO,2015/071861A2[P].2015-05-21.
[13]Sun J, Huang J, Ding X Z, et al.Efficient enantioselective biocatalytic production of a chiral intermediate of sitagliptin by a newly filamentous fungus isolate[J].Applied Biochemistry and Biotechnology, 2016, 18(4):695-706.
[14]孙佳.生物催化不对称合成西他列汀关键手性中间体[D].杭州:浙江工业大学,2016.
[15]Wei Y C,Xia SW,He C L,et al.Highly enantioselective production of a chiral intermediate of sitagliptin by a novel isolate of Pseudomonas pseudoalcaligenes[J].Biotechnology Letters, 2016, 38(5):841-846.
Abstract:Sitagliptin is the firstdipeptidylpeptidase-4 (DPP-4) inhibitor type IIdiabetesdrug.The developmentof this drug after themarkethas gone through three generations of the development process line.In this paper,the preparation technology of sitagliptin and the biocatalytic method applied in the synthesis of sitagliptin weremainly introduced.The future development of sitagliptin preparation technology was also discussed.
Keywords:Sitagliptin;type 2 diabetes;biocatalysis
Research Progress in Preparation Technique of Type 2 Diabetes Drug Sitagliptin
ZHANG Peng-peng,MENG Fan-ting,NIU Ting-ting,WANG Pu*
(College of Pharmaceutical Science,Zhejiang University of Technology,Hangzhou,Zhejiang 310014,China)
1006-4184(2017)9-0015-05
2017-02-22
浙江省自然科学基金项目(LY16B060010);国家自然科学基金项目(21676250)资助。
章鹏鹏(1993-),男,硕士研究生,研究方向:生物催化与手性合成。
*通讯作者:王普,女,教授,博士生导师。E-mail:wangpu@zjut.edu.cn

