水泥中三氧化硫含量的电导法测定及影响因素分析
郭维维
(山西省水利水电科学研究院 山西太原 030002)
水泥生产过程中三氧化硫含量要控制在适宜的范围内,否则水泥会产生速凝现象,也会影响到后期的强度及其他性能。标准规定:三氧化硫的含量在硅酸盐水泥、粉煤灰水泥及火山灰水泥中应在3.5%内,其含量在矿渣水泥中应小于4.0%[1]。尽管测定水泥中SO3的含量可以采用重量法、高速分析法[2]和电导滴定法[3]等多种方法,但重量法由于操作复杂难以满足实际需要;高速分析法需要特殊的添加剂;电导滴定法还未进行过这方面的相关研究,因而本文采用电导滴定法对水泥中SO3的含量进行试验测定,同时对影响结果的因素进行分析。
1 仪器、试剂
本试验仪器主要有数字电导率仪(DDS-IIA型)、电导电极(DJS-1型)、电磁加热搅拌器(78-1型)。采用的试剂为0.100 mol/L BaCl2标准滴定溶液和0.010 mol/L Na3PO4标准溶液。
2 试验
2.1 试验方法
称取磨细水泥样品0.500 0 g经(105±5)℃烘干后置于200 mL的烧杯中,并加入100 mL热蒸馏水后于电磁加热搅拌器上搅拌大约7 min后,将1~2滴1%的酚酞指示剂滴入烧杯,用稀盐酸(1∶10)调溶液至无色,将BaCl2标准溶液滴入其中,由于BaSO4沉淀的生成导致溶液电导率变化,根据此确定滴定终点。
2.2 试验基本原理
水泥中大都是可溶性的的硫酸盐,因此,当在水泥样品中加入热水后,硫酸根离子与BaCl2标准溶液发生以下反应:SO4-2+Ba2++2Cl-=BaSO4↓+2Cl-产生BaSO4沉淀,沉淀的不断生成,使得SO4-2离子不断减小,而溶液中Cl-不断增加,接近滴定点时,Cl-浓度增加较快,溶液的电导率增加;滴定点过后,BaSO4沉淀基本不再生成,BaCl2溶液的继续加入,使得溶液中离子浓度持续增加,电导率上升幅度较大,如图1电导滴定曲线图所示,在该曲线上有一个拐点比较明显,该点所对应的横坐标即为滴定终点,采用二次微商法或切线法可确定此拐点[3],根据滴定终点BaCl2标准溶液消耗的体积V,按公式(1)即可求出水泥中SO3的质量百分数:

式中:Wso3为水泥中SO3的质量百分数(%);C为标准溶液中BaCl2的摩尔浓度,mol/L;V为BaCl2标准溶液的滴定体积,ml;SO3的摩尔质量,g为80;m为水泥样品的质量,g。
3 试验测定结果
3.1 电导法测定水泥样品溶液的电导率随BaCl2标准溶液体积变化的规律
表1为试验时BaCl2标准溶液滴定体积对溶液电导率的影响规律,其相应的变化曲线如图1所示,通过切线法可知滴定终点BaCl2标准溶液消耗的体积V≈0.89 mL。
将水泥质量m=0.500 4 g,V≈0.89 mL代入计算公式(1),通过计算可知此样品中SO3含量为:
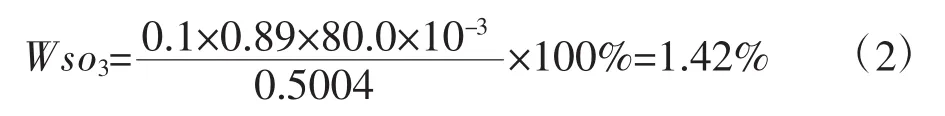

表1 电导滴定中溶液的电导率变化

图1 溶液电导率随BaCl2体积变化规律
3.2 电导法测定结果与重量法结果的对比
表2及表3分别为水泥中SO3含量用电导法和重量法两种不同方法测得的6次结果,通过对比可以看出,两种方法的试验结果基本一致,而且对比测定过程,电导法每个样品大约需要40 min,操作简单而快速。

表2 水泥中SO3的质量百分数(电导法)

表3 水泥中SO3的含量(重量法)
4 影响电导法测定结果的因素分析
4.1 溶液pH值对结果的影响
在用电导法对结果测定的过程中发现结果受溶液的pH值影响较大,溶液的pH值太大,会导致Ba2+的水解加快,对SO3含量的测定有影响;反之,如果pH值太小,电导率变化曲线上拐点不明显,难以确定滴定终点。为了研究该影响过程,调水泥样品溶液至不同pH值测定其SO3的含量,并与重量法的测定结果(1.42%)进行比较,如表4所示。由表可知,溶液的pH值在5~9范围内时,用电导法测定水泥中SO3含量结果较好。
4.2 水泥样品溶解的温度及搅拌时间对测定结果的影响
表5为电导法测定时在不同溶解温度及搅拌时间情况下的测定结果,括号内的数据为与重量法测定结果对比的绝对误差(标准值为1.42%),由表5可以看出:溶液温度的升高及搅拌时间的延长都会使得电导法测定结果越来越准确,溶解样品溶液的温度大于70℃,搅拌时间长于7 min测定结果比较准确,测定的相对误差在±3%以内。
5 结论
1)水泥中SO3含量的测定用电导滴定法准确性较高同时该法操作简单、快速、受干扰因素少,每个样品完成测定大约需40 min。
2)溶液的pH值和溶解样品的温度及时间对电导法测定水泥中SO3含量的结果影响较大,pH值在5~9左右,测定的结果比较准确。

表4 不同溶液pH值下电导滴定法测水泥样品中SO3的质量百分数

表5 溶解水泥样品溶液的温度与搅拌时间对SO3质量百分数的影响
[1]中国建筑材料科学研究总院中国建筑材料检验认证中心.GB/T176-2008水泥化学分析方法[S].北京:中国标准出版社,2008.
[2]杨文安,余乃越,玻璃和水泥中三氧化硫的高速分析.[M]//理化检验-化学分册,2001:64-65.
[3]顾鸿语,王遵尧.石膏和水泥中三氧化硫含量的电导滴定[J].分析化学,1997(10):1236.

