饮用水中亚硝酸盐高通量检测微孔板法的研究
刘凤银,张媚健,李 轩,谢丽君,袁学文,黄燕璇,梁 岳,穆洪涛,*
(1.广东第二师范学院生物与食品工程学院,广东广州 510310;2.中国医学科学院药物研究所,北京 100050;3.广东第二师范学院化学系,广东广州 510310)
亚硝酸盐具有氧化性,常作为护色剂、防腐剂被广泛应用于食品行业中[13]。但研究发现,亚硝酸盐可使血液中低铁血红蛋白氧化成高铁血红蛋白,失去运氧的功能,短期大量摄入可导致组织缺氧甚至死亡[45]。此外,亚硝酸盐可与体内的胺类物质反应生成“亚硝胺”,后者具有致癌作用,长期过量摄入易诱发食道癌、胃癌和肠癌等[6]。亚硝酸盐作为生态系统中氮循环的一个自然组成部分,广泛存在于天然水体中。但工业废水、水产养殖业、运输管道等污染,会导致水体中亚硝酸盐含量大幅度升高[78]。世界卫生组织规定每日允许亚硝酸盐摄入量不得超过0.2 mg/kg·bw[9];我国卫生部2017年出台的《食品安全国家标准食品中污染物限量》,规定矿泉水中亚硝酸盐含量不能超过0.1 mg/L[10]。
我国对食品安全高度重视,随着抽检覆盖率提高,快速检测作为实验室检测的有益补充,可实现大量样品的现场筛查,增加样品检测数量,扩大食品安全控制范围,大大提高监管效率[1112]。目前已报道的亚硝酸盐快速检测方法主要有试纸法[1315]和速测管法[16],它们都具有快速、简便等优点,但灵敏度低,只能定性或半定量检测,且无法进行高通量检测,限制了应用。郑晓宏等报道了一种微孔板法,实现了对亚硝酸盐的定量、高通量检测,但该方法采用氨基苯磺酸盐酸萘乙二胺双显色剂,但步骤多、操作繁杂、耗时长、干扰因素多等[17]。李永芳等[18]研究发现,间苯二胺可独立作为重氮化偶联试剂,用于亚硝酸盐的检测,其原理是利用间苯二胺的两个伯氨基,其中一氨基先与亚硝酸盐发生重氮化反应生成重氮盐,再利用分子的另一氨基,发生分子内偶联反应,生成橙红色环偶氮亚氨基苯,该研究采用单一试剂作为重氮化偶联试剂,具有灵敏、快速、稳定、操作简便等优点,但无法实现高通量检测。
本研究拟以微孔板为载体,采用间苯二胺作为显色剂,通过确定最佳测定波长、优化工作条件,以期建立一种高通量检测方法,用于饮用水等食品中亚硝酸盐残留的快速检测。
1 材料与方法
1.1 材料与仪器
亚硝酸钠 优级纯;间苯二胺、盐酸、亚硫酸钠、亚铁氰化钾、碘化钾、氯化钙、氯化钴、氯化铝、硫酸镍、氯化铵、氯化镁、溴化钠、乙酸锌、硝酸钠、硼酸钠、硫酸铜、氯化铬 均为分析纯;实验用水 屈臣氏蒸馏水。
SPMax 2300A2光吸收型全波长酶标仪 上海闪谱生物科技有限公司;JA2603B(M)分析天平(0.1 mg) 上海精科科学仪器有限公司;微量移液器 德国艾本德股份公司;DHG9140AD鼓风干燥箱 上海东麓仪器设备有限公司;96孔微孔板 厦门怡佳美实验器材有限公司。
1.2 实验方法
1.2.1 最佳测定波长确定 将间苯二胺用0.5 mol/L盐酸溶解稀释,配制间苯二胺显色剂(20 g/L)。以96孔微孔板为载体,使用移液器将5 mg/L亚硝酸钠标准溶液、间苯二胺显色剂加入微孔板中混合,两者的体积比为1∶9,分别为25、225 μL。反应10 min后,对反应后的体系在400~800 nm处进行全波长扫描。选择吸光值最大的波长作为最佳测定波长。
1.2.2 单因素实验 与5 mg/L亚硝酸钠标准溶液进行显色反应,采用酶标仪,测定各孔吸光值A451 nm。固定间苯二胺显色剂浓度为20 g/L,反应时间为10 min,考察盐酸浓度(0.1、0.2、0.3、0.4、0.5 mol/L)对显色效果的影响;固定盐酸浓度为0.4 mol/L,反应时间为10 min,考察显色剂浓度(10、20、30、40、50、60 g/L)对显色效果的影响;固定盐酸浓度为0.4 mol/L,间苯二胺显色剂浓度为30 g/L,考察反应时间(2、5、10、15、20、30 min)对显色效果的影响。
1.2.3 正交实验 以盐酸浓度、显色剂浓度、反应时间为考察因素,吸光值A451 nm为指标,根据单因素实验的结果,进行3因素3水平正交实验。正交实验因素水平设置见表1。
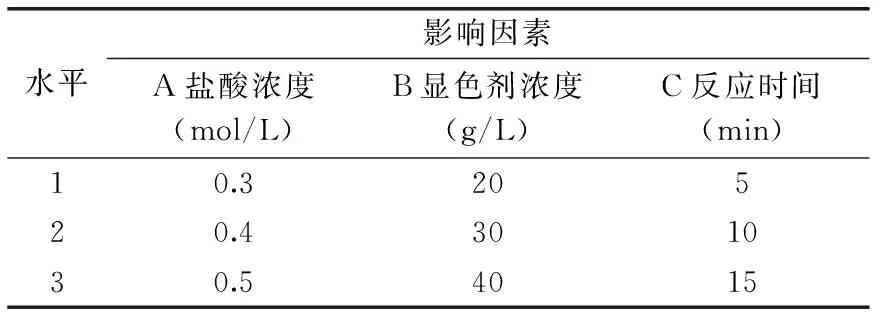
表1 正交实验因素水平Table 1 Factors and levels of orthogonal experiment
1.2.4 标准曲线的建立 配制0、0.05、0.1、0.2、0.4、0.8、1.6、3.2、5 mg/L亚硝酸钠标准溶液,在最佳显色条件下进行显色反应。以亚硝酸钠浓度为横坐标、吸光值为纵坐标,绘制标准曲线。
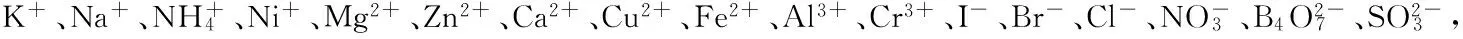
1.2.6 检出限 吸取20份空白水样,进行测定。计算空白值的平均值B0及其标准差SDB0。按照下式计算检出限(LOD)。
LOD=B0+3SDB0
式(1)
1.2.7 空白添加回收实验 取18等份空白水样分为3组进行6等份样品平行实验,分别以0.05、0.10、0.15 mg/L三个不同亚硝酸钠浓度水平进行测定。按照以下公式计算空白加标回收率及变异系数。
式(2)

式(3)
1.3 数据处理
实验做3个平行实验,实验数据采用平均值±标准差的形式表示。采用Excel计算数据平均值及标准差;采用SPSS 19.0进行正交实验设计及数据方差分析;采用Origin 8.5对数据进行拟合分析。
2 结果与分析
2.1 最佳测定波长确定
由图1可知,反应后体系在451 nm处具有最大吸收峰。因此,选择451 nm作为最佳测定波长。
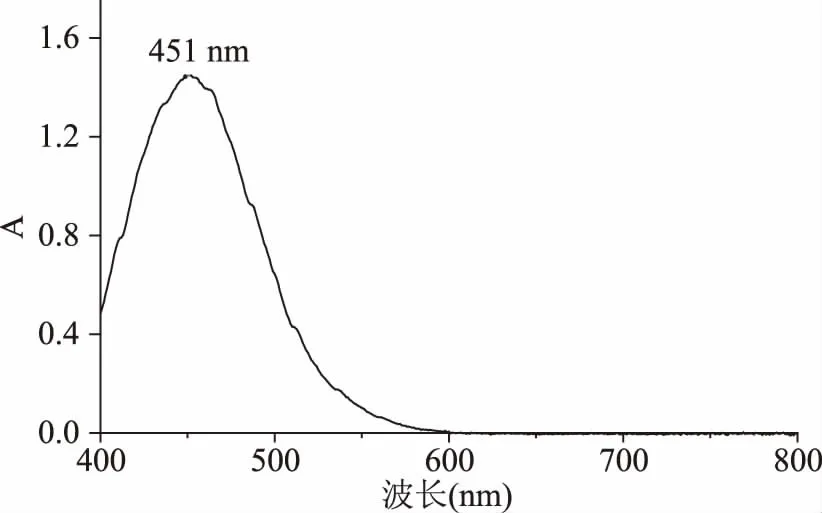
图1 反应产物吸收光谱曲线Fig.1 Absorption spectrum curve of reaction product
2.2 工作条件优化
2.2.1 单因素实验
2.2.1.1 盐酸浓度对显色效果的影响 亚硝酸盐与间苯二胺重氮化显色反应需在强酸条件下进行,盐酸浓度会影响显色反应的效果。吸取5 mg/L亚硝酸钠标准溶液在不同盐酸浓度下进行显色反应,采用酶标仪于451 nm处测定吸光值,结果见图2。随着盐酸浓度的升高,吸光值先增大后减小,0.4 mol/L时,反应最为充分,吸光值最大。
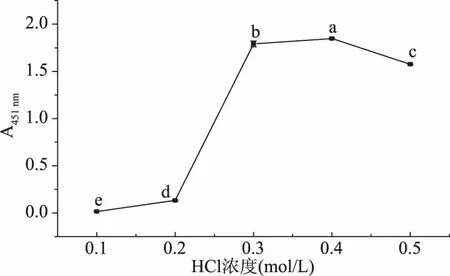
图2 盐酸浓度对显色效果的影响Fig.2 Effect of concentration of hydrochloric acid on chromogenic reaction注:不同字母表示差异显著(p<0.05),图3、图4同。
2.2.1.2 显色剂浓度对显色效果的影响 吸取5 mg/L亚硝酸盐标准溶液与不同浓度的间苯二胺显色剂进行显色反应,结果见图3。在间苯二胺浓度为30 g/L时,具有稳定最大吸光值,浓度低或者高于30 g/L时,吸光值逐渐减小。可能原因是,显色剂浓度过低,显色不充分,吸光值偏低;显色剂浓度过高,过量的显色剂被空气氧化为褐色,对实验测定产生了干扰,吸光值降低[19]。
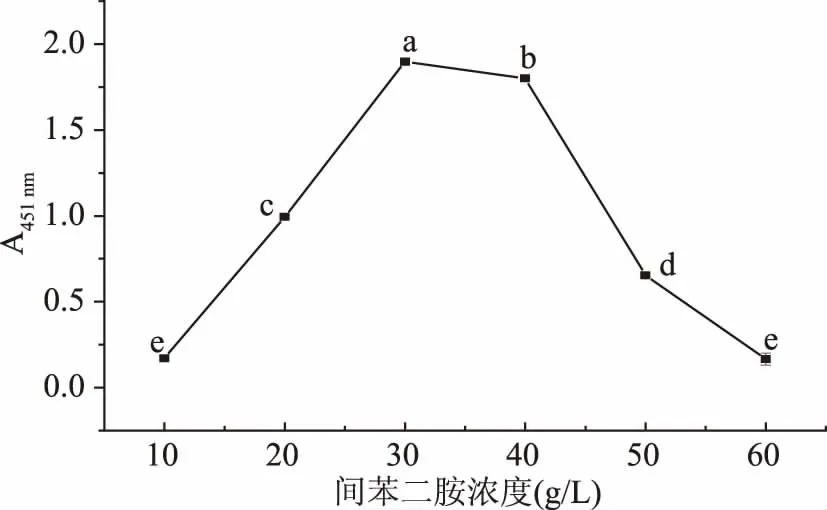
图3 显色剂浓度对显色效果的影响Fig.3 Effect of concentration of chromogenic agent on chromogenic reaction
2.2.1.3 反应时间对显色效果的影响 由图4可知,反应时间过短,显色不充分;反应时间过长,延长了检测时间,不利于快速检测需要。当显色反应10 min后,反应完全,吸光值达到最大值,且在实验时间内保持稳定。
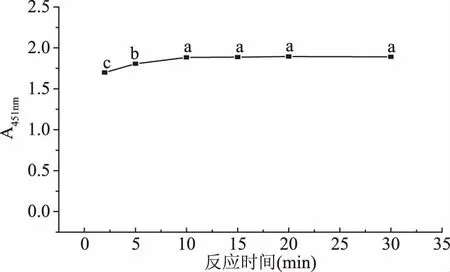
图4 反应时间对显色效果的影响Fig.4 Effect of time on chromogenic reaction
2.2.2 正交实验 根据单因素实验结果,以盐酸浓度、显色剂浓度、反应时间为考察因素。进行L9(33)正交实验。正交实验直观分析表见表2,方差分析表见表3。由极差分析结果可知,对显色效果影响的主次顺序为:B>A>C,即显色剂浓度>盐酸浓度>反应时间。由方差分析表可知,显色剂浓度对方法灵敏度影响显著,盐酸浓度、反应时间对灵敏度影响不显著。由k值大小可知,优化工作条件组合为A2B2C2,此结果与单因素实验筛选出的最佳条件组合一致。此组合在表2中未出现,正交实验均值最高组合为A2B2C3,比较两组合差异在于反应时间。由于反应时间对灵敏度影响不显著,为节约检测时间,确定最佳工作条件组合为A2B2C2,即盐酸浓度为0.4 mol/L,间苯二胺显色剂浓度为30 g/L,反应时间为10 min。进一步重复实验表明,该工作条件下,反应稳定性良好,A451 nm为2.5462。
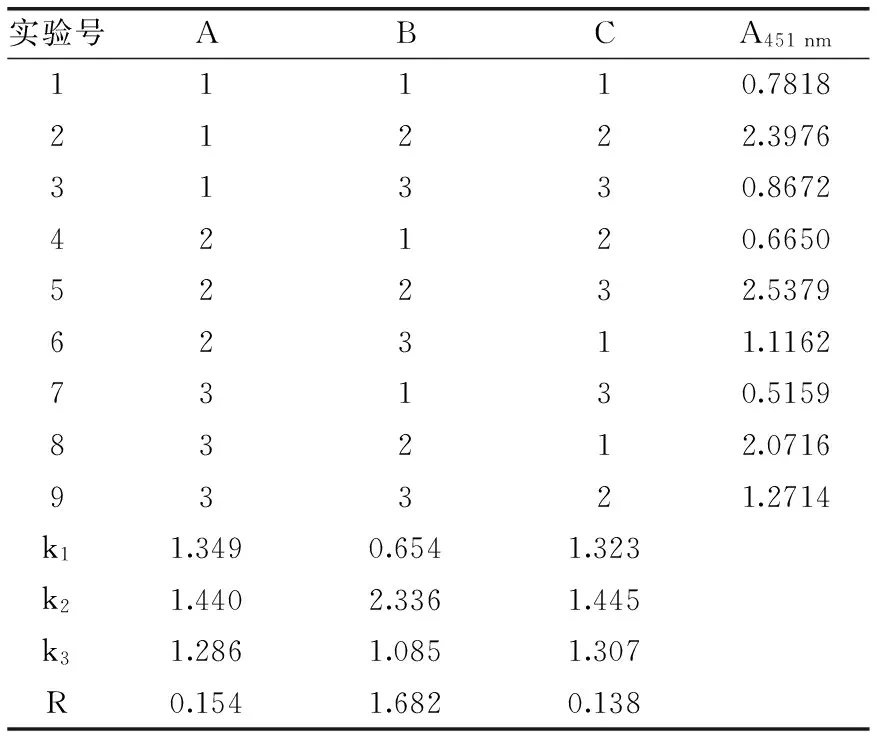
表2 正交实验结果Table 2 Results of orthogonal experiment
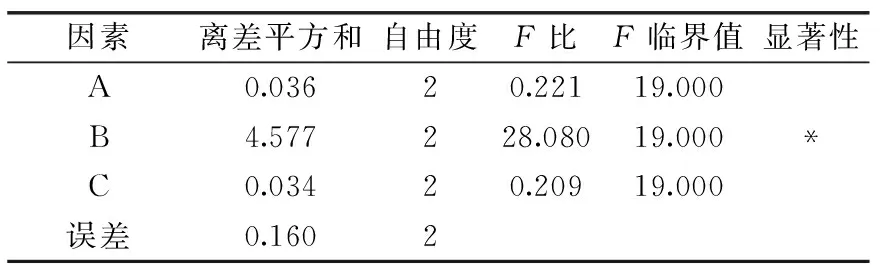
表3 正交实验方差分析Table 3 The variance analysis of orthogonal experiment
2.3 标准曲线绘制
在最佳工作条件下,吸取一系列浓度梯度的亚硝酸钠标准溶液进行显色反应,在451 nm处测定吸光值,绘制标准曲线,见图5。线性范围为0~5 mg/L。
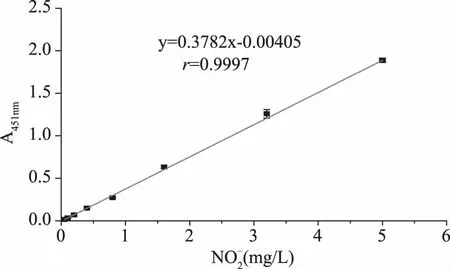
图5 亚硝酸钠测定标准曲线Fig.5 Standard curvefor nitrite determination
2.4 共存离子干扰实验

2.5 检出限
国际纯粹与应用化学联合会(IUPAC)规定,检出限是一个分析方法能够可靠地检测出被分析物的最低浓度[20]。吸取20份空白水样,进行测定。计算得检出限为0.017 mg/L。
2.6 空白添加回收实验
添加回收率常用来评价一个分析方法的准确度[21]。分别以0.5、1.0、1.5倍允许限量,即0.05、0.10、0.15 mg/L三个浓度水平进行添加,添加量在方法的线性范围内。澄清水样可直接取样检测。测定结果见表4。可以看出,空白加标回收率在95.24%~103.98%之间,变异系数<5%。说明,本研究所建立的亚硝酸钠微孔板法具有良好的准确度和精密度。
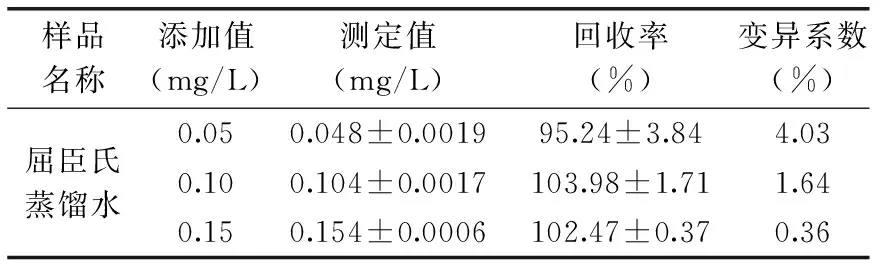
表4 空白加标回收率测定Table 4 Recoveries of nitrite from spiked samples
3 结论
本研究基于亚硝酸盐可与间苯二胺在强酸性条件下发生重氮化偶联反应,生成橙红色偶联产物环偶氮亚氨基苯的原理,建立了一种微孔板法,可用于饮用水等食品中亚硝酸盐残留量的高通量定量测定。该微孔板法以间苯二胺为显色剂,最佳测定波长为451 nm;最佳工作条件为盐酸浓度为0.4 mol/L、间苯二胺浓度为30 g/L、反应时间为10 min;检出限为0.017 mg/L,线性范围为0~5 mg/L。该微孔板法具有快速、灵敏,可实现高通量检测等优点,可用于饮用水等食品中亚硝酸盐残留量的现场快速高通量检测,可进一步开发为商品化试剂盒,具有良好的社会效益和经济效益。
[1]史智佳,臧明伍,王宇,等. 肉制品中减少亚硝酸盐添加量的方法及存在的问题[J].食品工业科技,2011(8):418422.
[2]Woolford M K. Microbiological screening of food preservatives,cold sterilants and specific antimicrobial agents as potential silage additives[J]. Journal of the Science of Food and Agriculture,1975,26(2):229237.
[3]Kilic A,Oztan A. Preservative characteristics of ascorbic acid on color,texture and fatty acid of coldsmoked fish[J]. International Journal of Food Engineering,2016,12(1):4961.
[4]Fan A M,Steinberg V E. Health implications of nitrate and nitrite in drinking water:An update on methemoglobinemia occurrence and reproductive and developmental toxicity[J]. Regulatory Toxicology and Pharmacology,1996,23(1):3543.
[5]Samuni A,Maimon E,Goldstein S. Nitroxides catalytically inhibit nitrite oxidation and heme inactivation induced by H2O2,nitrite and metmyoglobin or methemoglobin[J]. Free Radical Biology and Medicine,2016,101:491499.
[6]Habermeyer M,Roth A,Guth S,et al. Nitrate and nitrite in the diet:How to assess their benefit and risk for human health[J]. Molecular Nutrition and Food Research,2015,59(1):106128.
[7]Jones R R,Weyer P J,DellaValle C T,et al. Nitrate from drinking water and diet and bladder cancer among postmenopausal women in Iowa[J]. Environmental Health Perspectives,2016,124(11):1751.
[8]Wang L,Wang X,Yang F,et al. Nitrogen removal performance and ammoniaand nitriteoxidizing bacterial community analysis of a novel industrial wastebased biofilter[J]. Chemical Engineering Journal,2016,299:156166.
[9]郑鹏然. 粮农组织和世界卫生组织(FAO/WHO)关于食品添加剂每日允许摄入量(ADI)的建议[J]. 国外医学参考资料:卫生学分册,1977(1):5759.
[10]国家食品药品监督管理总局.GB 27622017.食品安全国家标准食品中污染物限量[S]. 北京:中国标准出版社,2017.
[11]马向南,杜美红. 食品安全领域快速检测仪器的发展现状与展望[J]. 食品安全质量检测学报,2015(5):18281833.
[12]Zhao X,Lin C W,Wang J,et al. Advances in rapid detection methods for foodborne pathogens[J]. Journal of Microbiology and Biotechnology,2014,24(3):297312.
[13]Jayawardane B M,Wei S,McKelvie I D,et al. Microfluidic paperbased analytical device for the determination of nitrite and nitrate[J].Analytical Chemistry,2014,86(15):72747279.
[14]顾翔宇. 两种剂型亚硝酸盐快速检测试剂的研制[D].呼和浩特:内蒙古农业大学,2016.
[15]汪菊,付大友,徐晨曦. 食品中亚硝酸盐快速检测方法的研究[J]. 食品工业科技,2015,36(9):278281.
[16]郭军,王芳,孟兰环,等.一种半固体型亚硝酸盐快速检测管及其制备方法:中国,CN 103529031 A[P]. 2014122.
[17]郑晓宏,林映芳,巫伟鑫,等.微孔板式亚硝酸盐试剂盒的研制[J].江西化工,2011(1):5255.
[18]李永芳,侯晓燕. 盐酸间苯二胺紫外分光光度法测定亚硝酸盐的探讨与应用[J].中国卫生检验杂志,2001,11(1):1718.
[19]李永芳,侯晓燕. 盐酸间苯二胺紫外分光光度法测定亚硝酸盐的探讨与应用[J].中国卫生检验杂志,2001,11(1):1718.
[20]Mcnaught A D,Wilkinson A. IUPAC compendium of chemical terminology[J].Encyclopedic Dictionary of Polymers,2006.
[21]Irving N M,Leonard H M N H,MA. Nomenclature for liquidliquid distribution(solvent extraction)(IUPAC Recommendations 1993)[J].Pure & Applied Chemistry,1993,65(11):23732396.

