鲁西南地区小麦茎基腐病病原菌鉴定及其致病力分析
吴 斌,郭 霞,张 眉,姜珊珊,辛志梅,王升吉,辛相启
(山东省农业科学院植物保护研究所/山东省植物病毒学重点实验室,山东济南 250100)
小麦茎基腐病(wheat crown rot,WCR)是小麦生产中的主要真菌病害,小麦从苗期到成株期均可感此病,起初病菌可从幼芽鞘侵入,使幼根和芽鞘变褐、腐烂,即使出苗也生长细弱,茎基部变褐,中后期病部逐渐蔓延至小麦第一、二节茎,导致病部变褐、腐烂,发病较轻的病株穗粒干瘪,严重时穗部结成“白穗”,结实率大大降低,严重影响小麦的产量和品质[1-2]。
国内外研究表明,小麦茎基腐病的病原菌组成比较复杂,且因各地生态环境不同,优势致病菌也不同。美国和澳大利亚相关研究者发现,引起小麦茎基腐病害的病原菌主要是假禾谷镰孢菌(Fusariumpseudograminearum)[3],在中国引起小麦茎基腐病的病原菌包括镰孢菌(Fusariumspp.)、根腐离蠕孢菌(Bipolarissorokiniana)、交链孢菌(Alternariaspp.)、雪霉叶枯菌(Microdochiumnivale)和黑附球菌(Epicoccumnigrum)等,但主要且致病力最强的致病菌是镰孢菌,交链孢菌次之[4-5]。
近年来,由于实施秸秆还田,土壤中的菌源不断积累,且现有栽培品种抗性较差、农事操作粗放,加之气候因素影响,小麦茎基腐病在我国河南、河北、山东、安徽等省份普遍发生,而且呈现不断加重和蔓延趋势[6-8]。2016年鲁西北、鲁南地区普遍发生小麦茎基腐病害,重病田植株发病率达10%~30%,但是对这些地区该病害的病原菌组成和致病力等一直缺乏系统研究。本研究对山东省7个地方表现有茎基腐病症状的小麦植株进行采样及病原菌分离,利用分子生物学方法对获得的菌株进行鉴定及同源性分析,在温室开展苗期致病力测定,以期为该病的防治和抗病育种工作奠定基础。
1 材料与方法
1.1 供试材料
供试样品:2016年5月采集自山东省小麦茎基腐病发病严重的7个地点共105个病株(表1)。试验所用小麦品种均为济南15。
1.2 病原菌的分离
参照方中达[9]的方法,选取小麦受侵染根茎部的病健交界处,采用70%(v/v)的酒精进行组织表面消毒,无菌水冲洗5次,在无菌滤纸上晾干后置于PDA培养基平板上,于28 ℃黑暗培养,2 d后选取具真菌特征的菌落边缘菌丝转接至新的PDA平板上以获得纯培养,每个地点挑取菌落生长性状不同的菌株纯化培养,备用。
1.3 基因组DNA的提取
纯化后的菌株培养3~5 d,收集菌丝至2 mL的Eppendorf离心管中,用液氮迅速冷冻并快速研磨成粉末,采用真菌基因组DNA提取试剂盒(HP Fungal DNA Kit,Omega公司,美国)提取所有分离菌株的基因组DNA。
1.4 菌株的鉴定与序列分析
采用真菌rDNA-ITS通用引物 ITS1(5′-TCCGTAGGTGAACCTGCGG-3′)和ITS4(5′-TCCTCCGCTTATTGATATGC-3′)扩增所有分离菌株基因组的ITS区。PCR反应程序:94 ℃预变性2 min;94 ℃变性1 min,56 ℃退火1 min,72 ℃延伸1 min,35个循环;72 ℃延伸10 min。扩增产物用1%(w/v)琼脂糖凝胶电泳检测,并采用SanPrep柱式DNA胶回收试剂盒[生工生物工程(上海)股份有限公司]对目的条带进行回收,回收产物送铂尚生物技术(上海)有限公司进行测序,获得序列在NCBI中进行Blast检索比对。
对于ITS鉴定结果为镰孢菌的菌株进行EF-1α基因和β-tublin基因扩增,引物为 EF1T(5′-ATGGGTAAGARGACAAGAC-3′)和EF2T(5′-GGARGTACCAGTSATCATGTT-3′)、T1(5′-AACATGCGTGAGATTCTAAGT-3′)和T2(5′-TCTGGATGTTGTTGGGAATCC-3′)。PCR 反应程序为:95 ℃ 4 min;94 ℃ 1 min,58 ℃ 50 s,72 ℃ 1 min,35个循环;72 ℃ 10 min[10]。PCR产物经电泳检测后切胶、回收,回收产物送铂尚生物技术(上海)有限公司测序。
采用软件DNAStar(ver. 6.1)对所有被测镰孢菌的序列进行格式转换和初步整理,从GenBank数据库中下载镰孢菌典型分离物的 EF-1α基因序列,利用软件MEGA(ver. 4.1)的邻接法(neighbor-joining,NJ)构建系统发育树,各分支置信度(Bootstrap)进行500次重复分析。
1.5 病原菌的致病力测定
对分离得到的镰孢菌菌株在温室条件下进行小麦苗期致病力的测定。挑取饱满的济南15小麦种子,播种于装有无菌土(121 ℃高温灭菌1 h)的塑料钵(直径为9 cm)中,每盆播20~25粒,上面覆盖灭菌的蛭石,置于25 ℃的温室。当小麦长至2叶期时,选取大小基本一致的小麦种子,于无菌水中浸泡过夜(约16 h)后,置于150 mL三角瓶中,每瓶约15 g种子,121 ℃灭菌1 h,待完全冷却后接入在PDA培养基上生长7 d的镰孢菌菌株,28 ℃静置培养7~10 d,每隔2 d摇晃三角瓶使每粒种子带菌量尽量一致。当小麦生长至三叶一心时,在每株小麦的根部土壤中放置一粒带菌小麦种子,每个菌株设置3个重复,每个重复20株小麦,28 ℃保湿培养。接种病原菌3周后,参考李 伟等[5]调查纹枯病的9级分级标准并适当修改,调查病害发生情况。分级标准:0级,无症状;1级,外层叶鞘有明显的褐色或黑褐色斑,但病斑小于1/2直径,第1片叶明显褪绿黄化;3级,外层叶鞘有明显的褐色或黑褐色斑,病斑大于1/2直径,但内层叶鞘无症状,第2片叶叶尖褪绿黄化;5级,内层叶鞘有褐色或黑褐色斑,但病斑小于1/2直径,第1片叶枯死,第2片叶整叶黄化;7级,内层叶鞘有褐色或黑褐色斑,病斑大于1/2直径,第2片叶枯死,第3片叶有明显褐枯,但植株不死苗;9级,植株枯死。
利用下列公式计算病情指数,病情指数=Σ(各病级株数×各病级代表值)/(总株数×最高级代表值)×100。根据病原菌侵染小麦植株表现出的相关症状,每个菌株的3个重复各选取3株具有小麦茎基腐病典型症状的病株,每株发病叶鞘各剪取3份材料,分别进行病原菌的重新分离,每株菌的重新分离率=分离到与原接种菌相同菌落的材料数/总分离材料数×100%。重分离菌的鉴定同1.4。
1.6 数据处理
使用DPS(ver. 7.5)对病情指数进行统计分析。
2 结果与分析
2.1 病原菌分离与鉴定
对所有小麦病样选取症状明显的根茎部组织进行常规真菌分离,共获得真菌菌株45株(表1)。采用真菌rDNA-ITS通用引物 ITS1/ ITS4扩增分离菌株基因组的ITS区,获得片段约为600 bp目的条带。ITS序列分析表明,22株为镰孢菌(图1),其余菌株属于链格孢菌。聊城市高唐县固河镇共分离到3株镰孢菌,编号为GW1-3;高唐县赵庄乡(GD)共分离得到4株镰孢菌,编号为GD1-4;茌平县温陈乡(CW)分离到的3株镰孢菌,编号为CW1-3;茌平县韩屯镇样品(CH)得到的3株镰孢菌,编号为CH1-3;德州市齐河县焦庙镇样品共分离到4株镰孢菌,编号为QH1-4;禹城市房寺镇样品(YC)分离到的3株镰孢菌,编号为YC1-3;临沂市莒南县板泉镇样品共分离到2株镰孢菌,编号为JC1-2。
对22株镰孢菌进一步扩增EF-1α及β-tublin基因,BLAST(https://blast.ncbi.nlm.nih.gov/Blast.cgi)基因比对分析表明,聊城市4个采样点共获得9株假禾谷镰孢菌(F.pseudograminearum)和4株禾谷镰孢菌(F.graminearum);德州市2个采样点的7个菌株,除禹城市的1株为禾谷镰孢菌外,其余6株均为假禾谷镰孢菌;临沂市1个采样点获得2株亚洲镰孢菌。22株镰孢菌中,假禾谷镰孢菌(F.pseudograminearum)的分离频率最高,为68.18%;其次为禾谷镰孢菌(F.graminearum),分离频率为22.73%,亚洲镰孢菌(F.asiaticum)的分离频率为9.09%。
2.2 菌株的系统发育学分析
对获得的22株镰孢菌的 EF-1α基因进行扩增,与GenBank(https://www.ncbi.nlm.nih.gov/genbank/)中的序列进行BLAST比对,发现测试菌株与NCBI数据库中相近种菌株的 EF-1α基因序列同源性达到98%~100%,GenBank数据库中的42个 EF-1α基因序列信息见表2,采用软件MEGA (ver. 4)的邻接法(neighbor- joining,NJ)构建系统进化树如图2。由图2可以看出,分离菌株GD1、GD2、GD3、GD4和YC3共5个菌株与禾谷镰孢菌(F.graminearum)菌株聚类在一个组,自展支持率为59;分离菌株JC1和JC2与亚洲镰孢菌(F.asiaticum)菌株聚类在一个组,自展支持率为57;这两个组聚类在一个大组,且自展支持率为100;而其余的分离菌株GW1、GW2、GW3、CW1、CW2、CW3、CH1、CH2、CH3、QH1、QH2、QH3、QH4、YC1和YC2共15个菌株与假禾谷镰孢菌(F.pseudograminearum)的所有菌株聚类在另外一个大组,聚类结果和测序分析结果一致。从菌株的地区分布来看,采自聊城市高唐县赵庄乡的4个菌株(GD1、GD2、GD3和GD4)亲缘关系较近,禹城市房寺镇房寺村的1个菌株YC3与这4个菌株聚类在同一个分支,并且菌株YC3和GD1的亲缘关系非常近;分离自临沂市莒南县的2株JC1和JC2聚类在一同个分支;假禾谷镰孢菌的地区分布规律不明显。
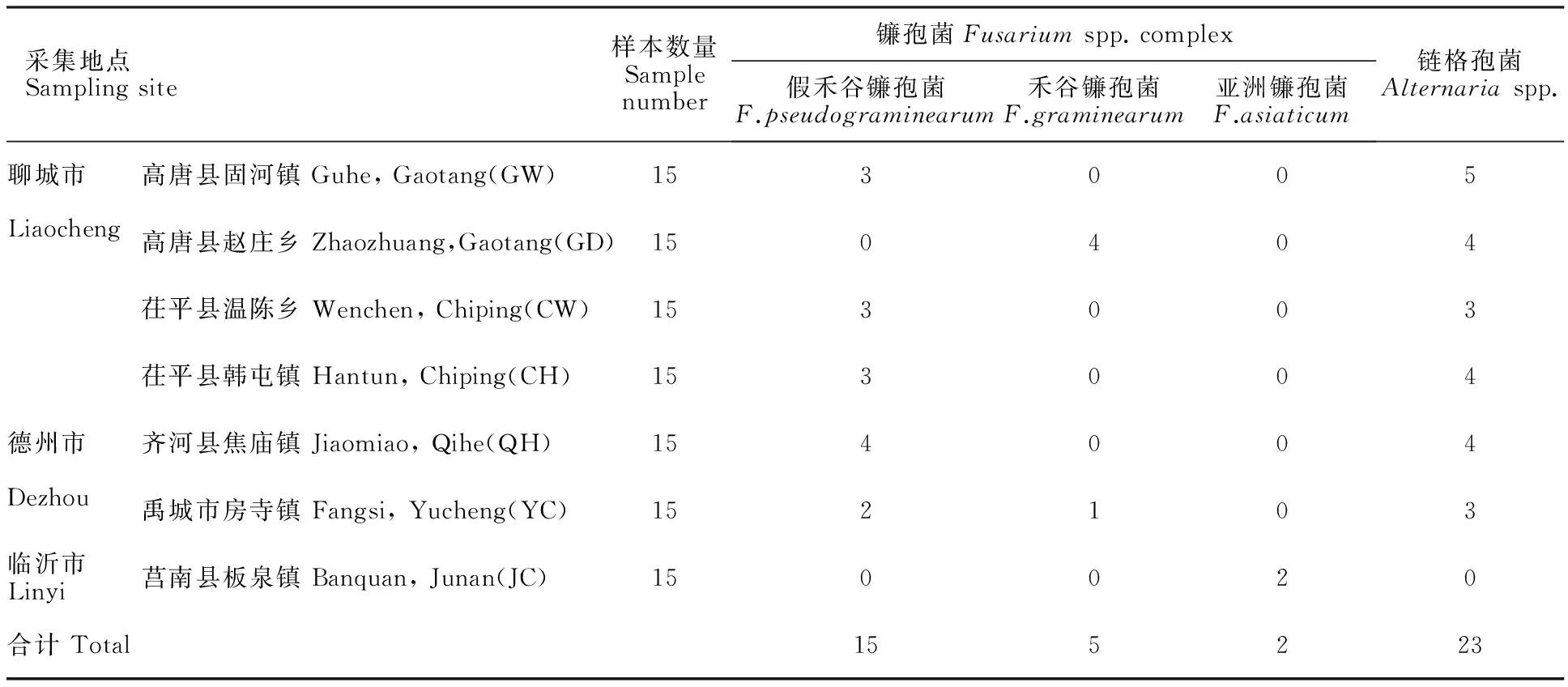
表1 采样点及所分离病原菌的种类及数量Table 1 Information of sample collection and type and number of pathogens that were isolated

M:DL2000 Maker; 1-3:GW1-3; 4-7:GD1-4; 8-10:CW1-3; 11-13:CH1-3; 14-17:QH1-4; 18-20:YC1-3; 21-22:JC1-2.
图122株镰孢菌的ITS区扩增结果
Fig.1PCRamplificationwithITS1/ITS4primersforITSregionof22Fusariumspp.
2.3 病原菌的致病力
在温室条件下,通过病麦粒接种法对22株镰孢菌进行盆栽苗的致病力测定。结果表明,小麦苗接种病原菌7 d后开始出现症状,起初第一片叶变黄萎蔫,由叶鞘处开始出现黑褐色病斑。随着侵染时间的延长,小麦茎基部病斑自下而上、由外到内扩展,接种3周后,发病严重的小麦植株枯萎,甚至死亡。
22株镰孢菌对供试小麦均有致病性(表3),且假禾谷镰刀菌的致病力明显强于禾谷镰刀菌及亚洲镰孢菌,后2种病原菌的致病力差异不显著。从病原菌分离的地区来看,德州市的假禾谷镰孢菌株的平均病情指数均达到79以上,齐河县有2株菌株QH2和QH4的平均病情指数大于90,分别为97.64和90.85,此外,平均病情指数大于90的菌株还有分离自德州市高唐县的菌株GW2。
3种镰孢菌均可引起小麦发病,但是症状略有不同(图2、图3)。接种假禾谷镰孢菌(F.pseudograminearum)的小麦植株茎基部症状明显,发病严重,湿度大时基部叶鞘上产生红色分生孢子粉层;禾谷镰孢菌(F.graminearum)根部的病麦粒外层被浅黄色菌丝球包裹,茎基腐症状不太明显,发病程度轻;接种亚洲镰孢菌(F.asiaticum)的小麦植株茎基部症状明显,发病不严重,湿度大时基部叶鞘上产生红色分生孢子粉层。就接种病株分离得率而言,假禾谷镰孢菌、禾谷镰孢菌及亚洲镰孢菌分别为55.56%、45.46%和100%,所有重新分离得到的菌株经测序鉴定均与接种病原菌种类相同。

表2 GenBank数据库中的42个EF-1α基因信息Table 2 Data of forty two EF-1α gene in GenBank database
-:未查到寄主名称。
-:No host finded.
3 讨 论
小麦茎基腐病是由多种病原菌引起的一种重要的土传病害,其田间发生情况较为复杂,病原分布及组成因地区差异、气候变化而不同[8,11],并且同一地块茎基腐病和赤霉病复合侵染常同时发生,对病原菌研究及病害防治造成一定的困难。而且这两种病害在病原菌的生物学特性、致病力及病害的流行上也存在联系,从小麦茎基部可以分离到赤霉病的主要致病菌禾谷镰孢菌(F.graminearum),而引起澳大利亚小麦茎基褐腐的病原菌假禾谷镰孢菌(F.pseudograminearum)也曾导致赤霉病的流行[1,12-13]。

图2 基于EF1-α基因构建的系统发育树
国内外研究发现,不同国家或地区小麦茎基腐病的病原菌组成不同。澳大利亚地区引起小麦茎基腐病的主要病原菌为假禾谷镰孢菌(F.pseudograminearum),美国的小麦茎基腐病病原菌包括假禾谷镰孢菌(F.pseudograminearum)、黄色镰孢菌(F.culmorum)和燕麦镰孢菌(F.avenaceum)等,欧洲小麦茎基腐病的主要致病菌为黄色镰孢菌[1,3]。2009-2010年,李 伟等[5]对引起江苏、安徽、河南、湖北、河北和四川6个省份小麦茎基腐病的病原菌进行了鉴定分析,发现其病原菌主要为小麦根腐离蠕孢(Bipolarissorokiniana)和镰孢菌(Fusariumspp.)。张向向等[2]对5个冬小麦主产省份的茎基腐病病原菌组成的研究发现,分离得到的镰孢菌中亚洲镰孢菌菌株所占比例最大,达76.30%,其余依次为禾谷镰孢菌(F.graminearum)、锐顶镰孢菌(F.acuminatum)、假禾谷镰孢菌(F.pseudograminearum)和燕麦镰孢菌(F.avenaceum)。近年来的研究报道均表明侵染我国小麦的茎基腐镰孢属病原菌种类主要为禾谷镰孢菌(F.graminearum)和亚洲镰孢菌(F.asiaticum),并且禾谷镰孢菌菌株多数分布在年平均气温低于15 ℃的寒冷地区,比如黄淮麦区和北方麦区,而亚洲镰孢菌常分布在年平均气温高于15 ℃的温暖地区,如长江流域的江苏等省[14],表明我国茎基腐病病原镰孢菌组成与北美洲以及澳大利亚有所差别。
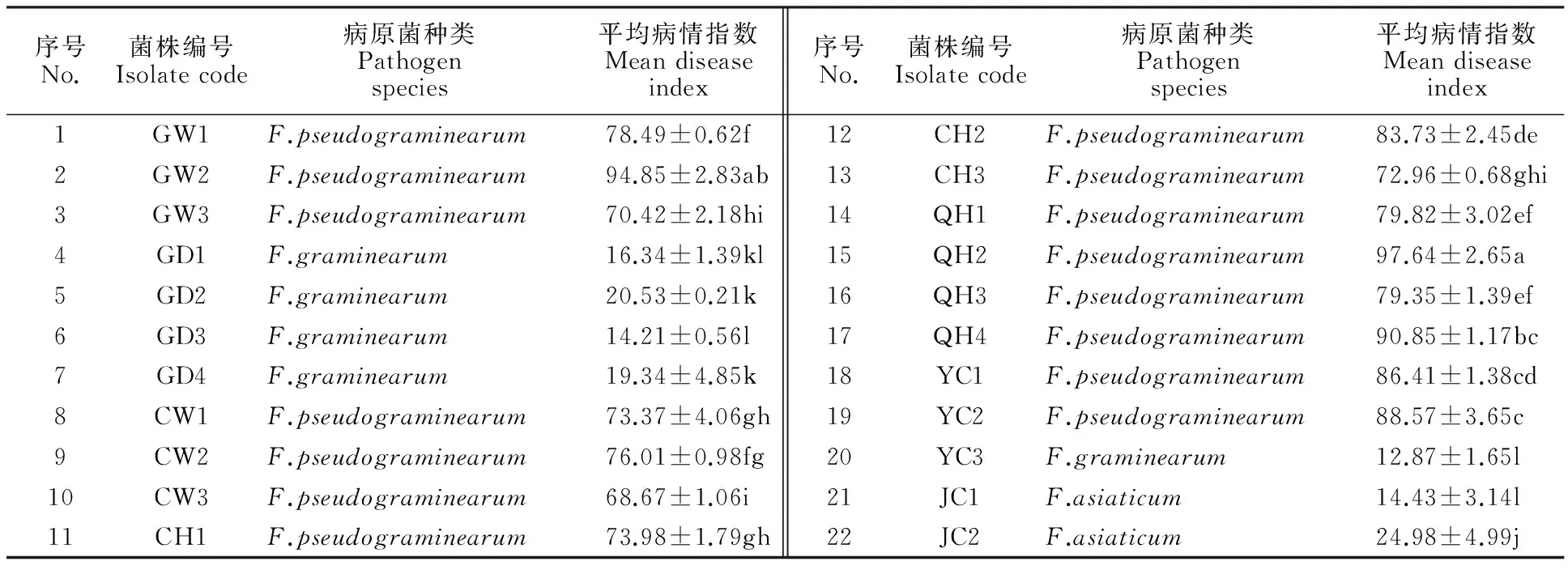
表3 22株镰孢菌致病力Table 3 Pathogenicity of 22 Fusarium spp.
表中数据为平均值±标准误;平均病情指数后的不同小写字母表示差异显著(P<0.05)。
Data were mean value± SE(standard error); Different letters following data of mean disease index were significant difference among isolates at 0.05 level.

a:田间发病症状;B:病菌回接症状;C:对照。
a:Symptom of natural infection; B:Symptom of diseased wheat after inoculation; C:Control.
图3小麦接种F.pseudograminearum后发病症状
Fig.3SymptomsofwheatthatwereinoculatedF.pseudograminearum

a:对照;B:发病程度轻;C:发病程度重。
A:Control; B:The lower disease degree; C:The higher disease degree.
图4小麦济南15茎基腐致病力测定
Fig.4PathogenicityofthecrownrottowheatJinan15cultivars
本研究通过对山东省小麦茎基腐病严重发生地区2016年小麦茎基腐病害样品的采集、分离,对获得的镰孢菌菌株进行了分类鉴定,结果发现引起这些地区小麦茎基腐病的病原菌有3种,分别为假禾谷镰孢菌(F.pseudograminearum)、禾谷镰孢菌(F.graminearum)和亚洲镰孢菌(F.asiaticum),其中分离数量最多的是假禾谷镰孢菌,致病力也最强,平均病情指数均达到79以上,甚至大于90。2012年Li等[15]首次在我国报道了由假禾谷镰孢菌(F.pseudograminearum)引起的小麦茎基腐病,分离频率仅为5.97%,张向向等[2]于2012年仅在江苏的小麦茎基腐病病株上分离到假禾谷镰孢菌1株。与此形成鲜明对比的是,本研究中假禾谷镰孢菌的分离比例较高,由此表明,山东小麦茎基腐病病原菌优势菌群的组成及其致病力程度可能已经发生了变化,需要引起重视。另外,本研究还分离得到了23株链格孢菌(Alternariaspp.),经过测序鉴定发现其菌株种类单一,大多数为细极链格孢菌(Alternariatenuissima),还有少量的链格孢菌(A.alternata),前人报道中有提及链格孢菌属(Alternariaspp.)为小麦茎基腐的病原菌,但致病力较镰孢菌(Fusariumspp.)弱[5],且该类病原菌主要引起小麦根腐病,故未对其进行深入研究。
到目前为止,尚未有标准的小麦茎基腐发病程度评估方法,研究者常根据茎基部褐色病斑大小、叶鞘发病级别、茎基腐病情指数等判别病情程度,而且国内对小麦茎腐病抗源的筛选报道较少,还未发现对该病害表现免疫或者高抗的品种,特别是缺乏适宜山东各麦区的抗病种质。因此,建议加强小麦抗茎腐病种质资源的筛选,并且建立统一、合理的茎基腐抗性鉴定体系,制定适宜的病害评价体系,以便于不同研究者对鉴定结果的相互比较,提高防治病害的有效性。
参考文献:
[1] CHAKRABORTY S,LIU C J,MITTER V,etal.Pathogen population structure and epidemiology are keys to wheat crown rot and Fusarium head blight management [J].AustralasianPlantPathology,2006,35:644.
[2] 张向向,孙海燕,李 伟,等.我国冬小麦主产省小麦茎基腐镰孢菌的组成及其致病力[J].麦类作物学报,2014,34(2):272.
ZHANG X X,SUN H Y,LI W,etal.Composition and pathogenicity of Fusarium crown rot pathogens of wheat in major winter wheat production areas of China [J].JournalofTriticeaeCrops,2014,34(2):272.
[3] SMILEY R W,PATTERSON L M.Pathogen fungi associated with Fusarium foot rot of winter wheat in the semiarid Pacific Northwest [J].TheAmericanPhytopathologicalSociety,1996,80:945.
[4] 陈厚德,王彰明,袁树忠,等.小麦茎基褐腐病的发生特点及其对产量的影响[J].扬州大学学报(自然科学版),2001,4(4):43.
CHEN H D,WANG Z M,YUAN S Z,etal.Study on occurrence characteristics and yield loss of the disease caused by wheat brown foot rot in Jiangsu Province [J].JournalofYangzhouUniversity,2001,4(4):43.
[5] 李 伟,陈 莹,张晓祥,等.小麦茎基褐腐病病原菌组成及其致病力研究[J].麦类作物学报,2011,31(1):171,174.
LI W,CHEN Y,ZHANG X X,etal.Pathogenic fungi of wheat brown foot rot and their pathogenicity in China [J].JournalofTriticeaeCrops,2011,31(1):171,174.
[6] 李冬梅,曹克强,王爱英,等.河北省小麦根病发生现状及致病病原种类调查[J].河北农业大学学报,2011,24(3):41,42.
LI D M,CAO K Q,WANG A Y,etal.Investigation on the occurrence and pathogen species of wheat root diseases in Hebei province [J].JournalofAgriculturalUniversityofHebei,2011,24(3):41,42.
[7] 李鹏昌.山东小麦根茎部主要真菌病害病原的分离鉴定和分子检测[D].济南:山东农业大学,2014:7.
LI P C.Identification and molecular detection of pathogen of soilborne fungi disease in wheat of Shandong region [D].Jinan:Shandong Agricultural University,2014:7.
[8] 周海峰,杨 云,牛亚娟,等.小麦茎基腐病的发生动态与防治技术[J].河南农业科学,2014,43(5):114.
ZHOU H F,YANG Y,NIU Y J,etal.Occurrence and control methods of crown rot of wheat [J].JournalofHenanAgriculturalSciences,2014,43(5):114.
[9] 方中达.植病研究方法[M].北京:中国农业出版社,2007:124.
FANG Z D.Research methods of plant disease [M].Beijing:China Agriculture Press,2007:124.
[10] ZHAO Z H,LU G Z.Fusariumsinensis sp.Nov. a new species from wheat in China [J].Mycologia,2008,100(5):747.
[11] 张向向.我国冬小麦主产省小麦茎基腐镰孢菌组成、地理分布及致病基因研究[D].南京:南京农业大学,2014:27,28.
ZHANG X X.Fusariumspp.causing wheat crown rot in major winter wheat growing regions of China and the function of deoxynivalenol on the infection [D].Nanjing:Nanjing Agricultural University,2014:27,28.
[12] BURGESS L W,KLEIN T A,BRYDEN W L,etal.Head blight of wheat caused byFusariumgraminearumgroup 1 in New South Wales in 1983 [J].AustralasianPlantPathology,1987,16:73.
[13] SWAN L J,BACKHOUSE D,BURGESS L W.Surface soil moisture and stubble management practice effects on the progress of infection of wheat byFusariumpseudograminearum[J].AustralianJournalofExperimentalAgriculture,2000,40:697.
[14] SUGA H,KARUGIA G W,WARD T,etal.Molecular characterization of theFusariumgraminearumspecies complex in Japan [J].Phytopathology,2008,98(2):165.
[15] LI H L,YUAN H X,FU B,etal.First report ofFusariumpseudograminearumcausing crown rot of wheat in Henan,China [J].PlantDisease,2012,96(7):1065.

