UPLC-HR-MS/MS法对吡唑醚菌酯原药中主要杂质的定性分析
管阳凡,樊 凯,张金凯,高士杰,郑锦彪
(上海晓明检测技术服务有限公司,上海 200335)
吡唑醚菌酯是巴斯夫公司于1993年发现的一种新型甲氧基丙烯酸酯类杀菌剂,其化学结构式示于图1。它不仅广谱、高效,而且对作物具有保健增产的作用,是美国环保署就此功能登记的第一个产品[1]。自2002年吡唑醚菌酯上市至今,在杀菌剂中它的销售额稳居前5名[2]。国内对吡唑醚菌酯原药和复配制剂的研发[3-6]、登记需求也持续高涨,关于吡唑醚菌酯原药中常见杂质的定性分析已成为关注的热点。
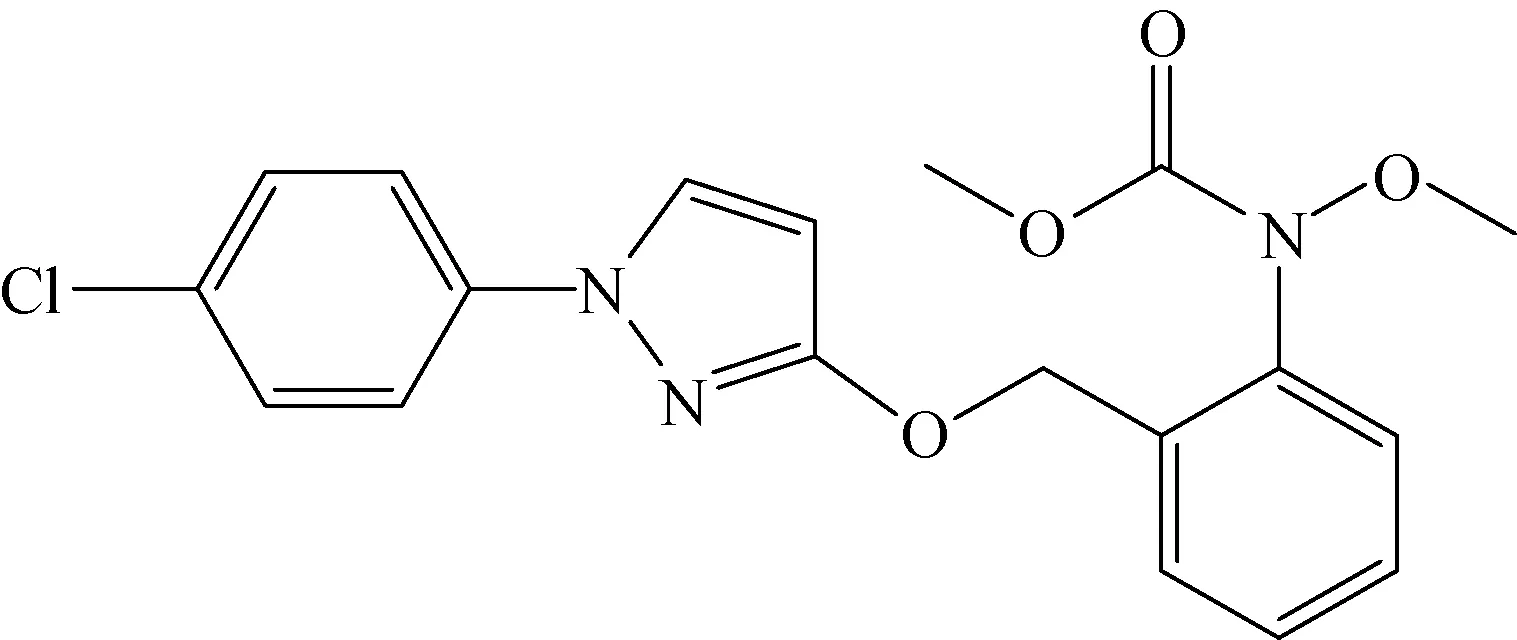
图1 吡唑醚菌酯的化学结构式Fig.1 Chemical structure of pyraclostrobin
近几年,HPLC-MS联用技术广泛应用于原料药的杂质分析中,包括对已知杂质的定量分析和未知杂质的结构解析[7-9]。但对于鉴定结构复杂的化合物,或区分一些同分异构体,LC/MS谱所提供的信息尚不充分,还需要借助MS/MS[10-12]、NMR、IR、X射线衍射等技术,或采用相似化合物谱图对照[13]的方法进一步分析。高能诱导裂解(higher energy collision induced dissociation, HCD)是一项新型的裂解技术,结合高分辨质谱数据,可用于化合物结构、质谱裂解机理的推测。解析杂质谱图信息后,通常用杂质对照品进行色谱对照,以便验证所得结论的准确性。
本实验拟利用UPLC-MS法分析实验室合成的吡唑醚菌酯原药,运用高能诱导裂解质谱(HCD MS/MS)法对原药中存在的主要杂质进行解析,并通过与对照品比对验证结论的准确性。希望为吡唑醚菌酯中杂质的定性分析提供方法参考,并为其他甲氧基丙烯酸酯类杀菌剂中杂质的解析提供方法借鉴。
1 实验部分
1.1 主要仪器与装置
Acquity UPLC H-Class超高压液相色谱仪:美国Waters公司产品;Dionex Ultra 3000型超高压液相色谱仪,Q-ExactiveTM组合型四极杆-高分辨轨道阱质谱仪,Xcalibur工作软件:美国Thermo-fisher公司产品;十万分之一天平:德国赛多利斯公司产品。
1.2 主要材料与试剂
乙腈:HPLC级,Tedia公司产品;吡唑醚菌酯原药:含量≥97%,由实验室参照文献[4]的方法合成;实验用水:Milli-Q超纯水。
1.3 实验条件
1.3.1色谱条件 色谱柱:Waters Acquity BEH C18柱(100 mm×2.1 mm×1.7 μm);流动相:A为乙腈,B为超纯水;梯度洗脱程序:0~2 min(40%A),2~12 min(40%~60%A),12~18 min(60%A),18~25 min(60%~90%A),25~30 min(90%A),30~30.01 min(90%~40%A),30.01~36 min(40%A);流速0.2 mL/min;柱温30 ℃;进样量2 μL;全波长扫描模式。
1.3.2质谱条件 ESI源正离子模式;质量扫描范围m/z100~1 000;一级质谱采用全扫描模式,二级质谱采用平行反应监测(parallel reaction monitoring, PRM)模式;喷雾电压:3.5 kV;离子传输管温度:320 ℃;金属喷针温度:300 ℃;鞘气压强:241 kPa;辅助气压强:69 kPa;碰撞能量:20~50 eV。
2 结果与讨论
2.1 液相色谱分析结果
实验采用Acquity UPLC H-Class超高效液相色谱仪进行分析,Dionex Ultra 3000型超高压液相色谱仪进行杂质对照品比对实验,液相色谱条件根据国际农药分析协作委员会发布的吡唑醚菌酯CIPAC方法调整得到。吡唑醚菌酯原药中主要杂质的UPLC谱图示于图2,采用面积归一法确定各组分的相对百分含量。由于吡唑醚菌酯在190~290 nm波长范围内均有紫外吸收,本实验考察了211、254、278 nm 3个波长下杂质的分布,将3个含量大于0.1%的杂质(A、B、C)作为分析对象,其结果列于表1。
2.2 质谱分析结果
2.2.1吡唑醚菌酯的质谱分析 在正离子模式下,吡唑醚菌酯原药主要成分的质谱图示于图3。从同位素峰强度来看,强度最高的m/z388.105 2、410.087 1两个离子均含有1个氯原子,推测其分别为[M+H]+和[M+Na]+离子,与吡唑醚菌酯正离子的理论分子质量(388.105 9 u)相吻合,一级质谱的误差为0.7个原子单位。选择m/z388.105 2为母离子进行HCD MS/MS测定,观察到4个主要的碎片离子峰m/z296.058 4、194.081 3、164.070 8、163.062 8,推测其质谱裂解途径示于图4。
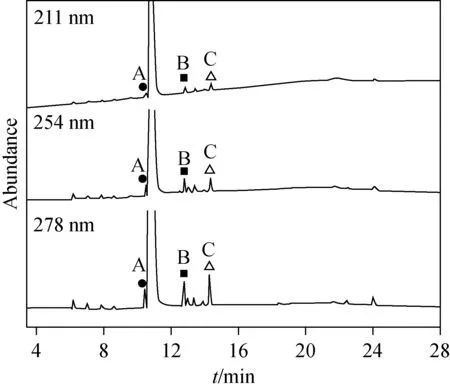
图2 吡唑醚菌酯原药中主要杂质的UPLC谱图Fig.2 UPLC spectra of the main impurities in pyraclostrobin
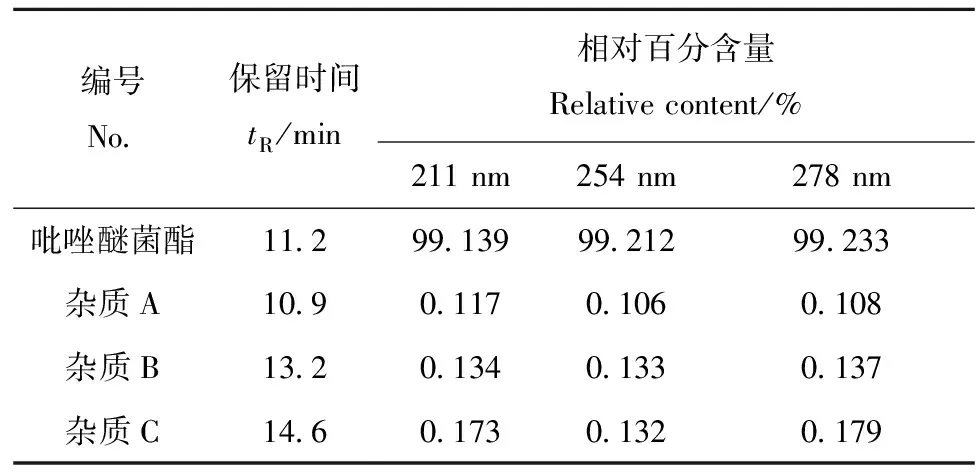
编号No 保留时间tR/min相对百分含量Relativecontent/%211nm254nm278nm吡唑醚菌酯11 299 13999 21299 233杂质A10 90 1170 1060 108杂质B13 20 1340 1330 137杂质C14 60 1730 1320 179
根据吡唑醚菌酯的相对分子质量推断各碎片离子的可能结构。由于m/z163.062 8是吡唑醚菌酯有效成分二级质谱中的碎片峰,因此它所含元素种类只可能有C、H、O、N,从数学角度将这4种元素拟合的化学式按照误差由小到大排列为:C9H9NO2、C7H7ON4、C6H11O5、C5H5N7、C4H9O4N3等。高分辨质谱中,经过质量轴校准后的误差一般不会超过0.004个原子单位,因此只有前5个拟合结果可能性最大。由于吡唑醚菌酯正离子的化学式为C19H19ClN3O4+,其碎片化学式中C、H、O、N各元素的个数不可能超过母离子,所以第2、3、4个化学式不符合实际情况,而第5个化学式的不饱和度与吡唑醚菌酯本身含多个芳香环的结构特点不符。因此,可以确定m/z163.062 8对应的化学式是C9H9NO2+。同理,可依次推断另外3个碎片离子m/z296.058 4、194.081 3、164.070 8对应的化学式分别为C16H11ClN3O+、C10H12NO3+、C9H10NO2+。
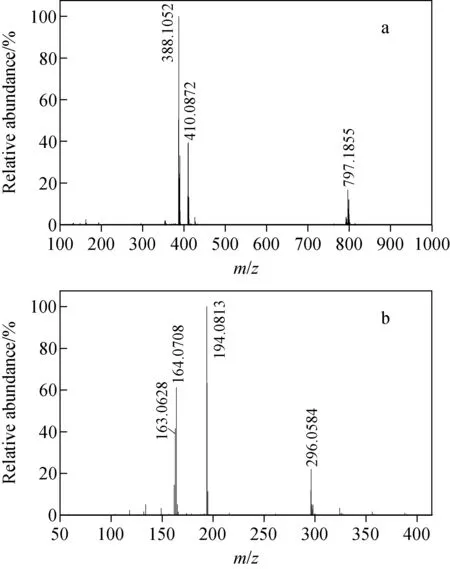
图3 吡唑醚菌酯原药主要成分的一级(a)与二级(b)质谱图Fig.3 MS (a) and MS/MS (b) spectra of pyraclostrobin
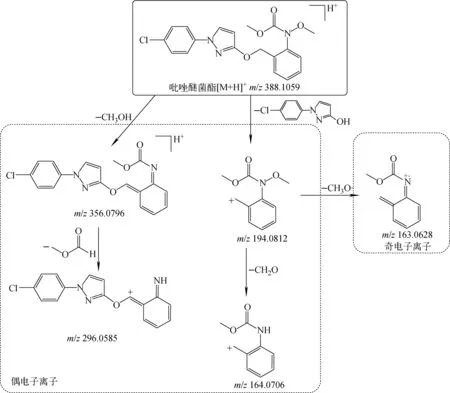
注:图中各碎片离子的分子质量为理论值图4 吡唑醚菌酯原药主要成分可能的裂解途径Fig.4 Proposed fragmentation pathway of pyraclostrobin
ESI电离源一般是电荷诱导发生的,通常失去中性分子发生电子对的转移,能够观察到偶电子离子。但对于某些化合物,偶电子离子也会丢失1个中性自由基生成奇电子离子[14]。丁友超等[15]在研究4种染料的ESI MS/MS中发现,产生的特征奇电子离子与偶氮、三苯甲烷、蒽醌和硝基苯这4种发色团的诱导裂解有关。这种现象在ESI质谱中已有较多的报道,但目前尚缺乏成体系的理论支持。本实验中的4个碎片离子均含有奇数个氮原子,一般来说它们的相对分子质量应为偶数,而m/z163.062 8离子的相对分子质量却为奇数,因此推断其为奇电子离子,是由某个偶电子离子失去1个自由基得到的。m/z194.081 3与m/z163.062 8相差31.018 5 u,是1个甲氧基自由基的相对分子质量。因此,推测m/z163.062 8是由m/z194.081 3在高能碰撞诱导下裂解失去1个甲氧基自由基后发生电子重排得到的。
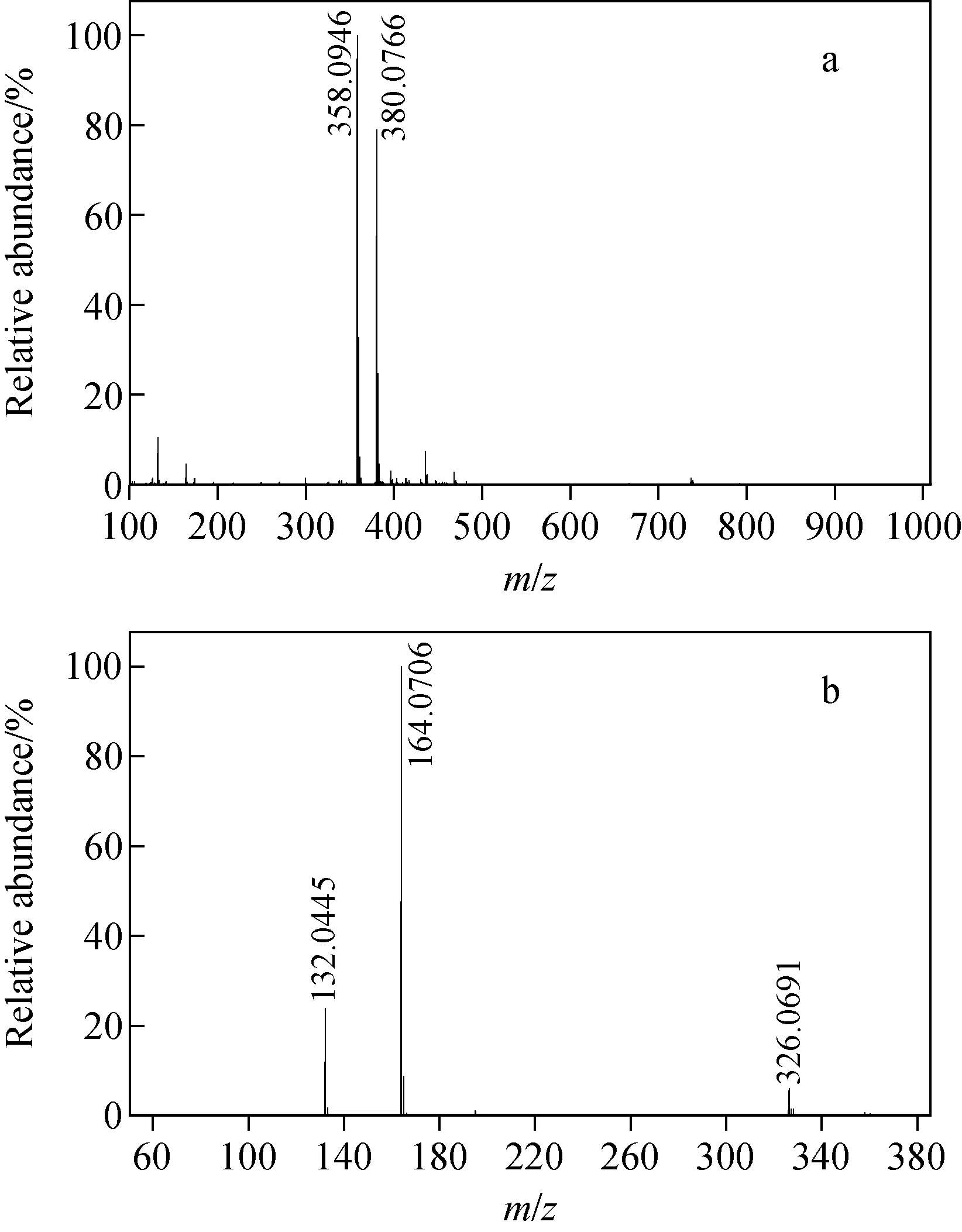
图5 杂质A的一级(a)与二级(b)质谱图Fig.5 MS (a) and MS/MS (b) spectra of impurity A
2.2.2杂质A的质谱分析 杂质A在正离子模式下的一级质谱图示于图5a,图中可以观察到m/z358.094 6、380.076 6离子信号,分别为[M+H]+和[M+Na]+离子,其中,m/z358.094 6比吡唑醚菌酯正离子少了30.010 0 u,恰好是1个甲醛(30.010 6 u)的分子质量。选择m/z358.094 6为母离子进行二级质谱(碰撞能量20 eV)测定,观察到3个主要的碎片离子峰m/z326.069 1、164.070 6、132.044 5,示于图5b。杂质A与吡唑醚菌酯有着共同的碎片离子m/z164.070 6,但没有m/z194.081 3碎片,说明杂质A与主成分的氨基甲酸酯部分可能相同,但又缺失了氨基上的甲氧基。因此,推测杂质A可能的裂解途径示于图6。杂质A的裂解途径有2种可能:一种是先失去1分子甲醇后得到m/z326.069 1的中间过渡态,经过电子重排后得到更稳定的共轭结构;另一种是直接失去1分子对氯吡唑醇,得到与吡唑醚菌酯相同的碎片离子m/z164.070 6。
2.2.3杂质B的质谱分析 杂质B在正离子模式下的质谱图示于图7,图7a中m/z436.082 0、458.063 8离子信号分别为[M+H]+和[M+Na]+离子。选择m/z436.082 0为母离子进行MS/MS测定(碰撞能量20 eV),产生4个主要的碎片离子峰m/z296.058 5、 242.057 9、212.047 3、163.062 9,同时还有m/z356.077 2、63.000 3等强度相对较弱的特征碎片峰,示于图7b。通过杂质B分子离子峰的同位素比,发现其含有2个氯原子,比吡唑醚菌酯分子质量多47.977 1 u,即1个氯甲烷的分子质量;二级质谱图中观察到的m/z63.000 1碎片峰与氯乙烷ClCH2CH2+碎片的精确理论分子质量相吻合。这是因为在合成吡唑醚菌酯反应过程中使用了二氯乙烷为反应溶剂。基于以上信息,推测杂质B的结构可能是氯乙基取代了吡唑醚菌酯的1个甲基。通过二级质谱图中的m/z356.077 2、296.058 5碎片峰,推测杂质B与吡唑醚菌酯分子的氨基甲酸酯部分可能相同,其可能的裂解途径示于图8。其中,碎片离子m/z163.062 8是由m/z242.057 9失去1个氯乙氧基自由基后重排得到的奇电子离子,该杂质可能是羟胺中间体与二氯乙烷溶剂在碱性环境下发生取代反应脱去1分子氯化氢的产物。
2.2.4杂质C的质谱分析 杂质C在正离子模式下的质谱图示于图9,图9a中m/z466.015 9、487.997 8离子信号分别为[M+H]+和[M+Na]+离子。选择m/z466.015 9为母离子进行MS/MS测定(碰撞能量20 eV),产生了4个主要的碎片离子m/z355.071 7、194.081 3、164.070 6、163.062 8,示于图9b。从图9a可以看出,杂质C分子结构中含有多个卤原子,比吡唑醚菌酯的分子质量多77.911 2 u,即1个Br的原子质量。因此,推测杂质C的结构可能为吡唑醚菌酯的1个H原子被Br原子取代。
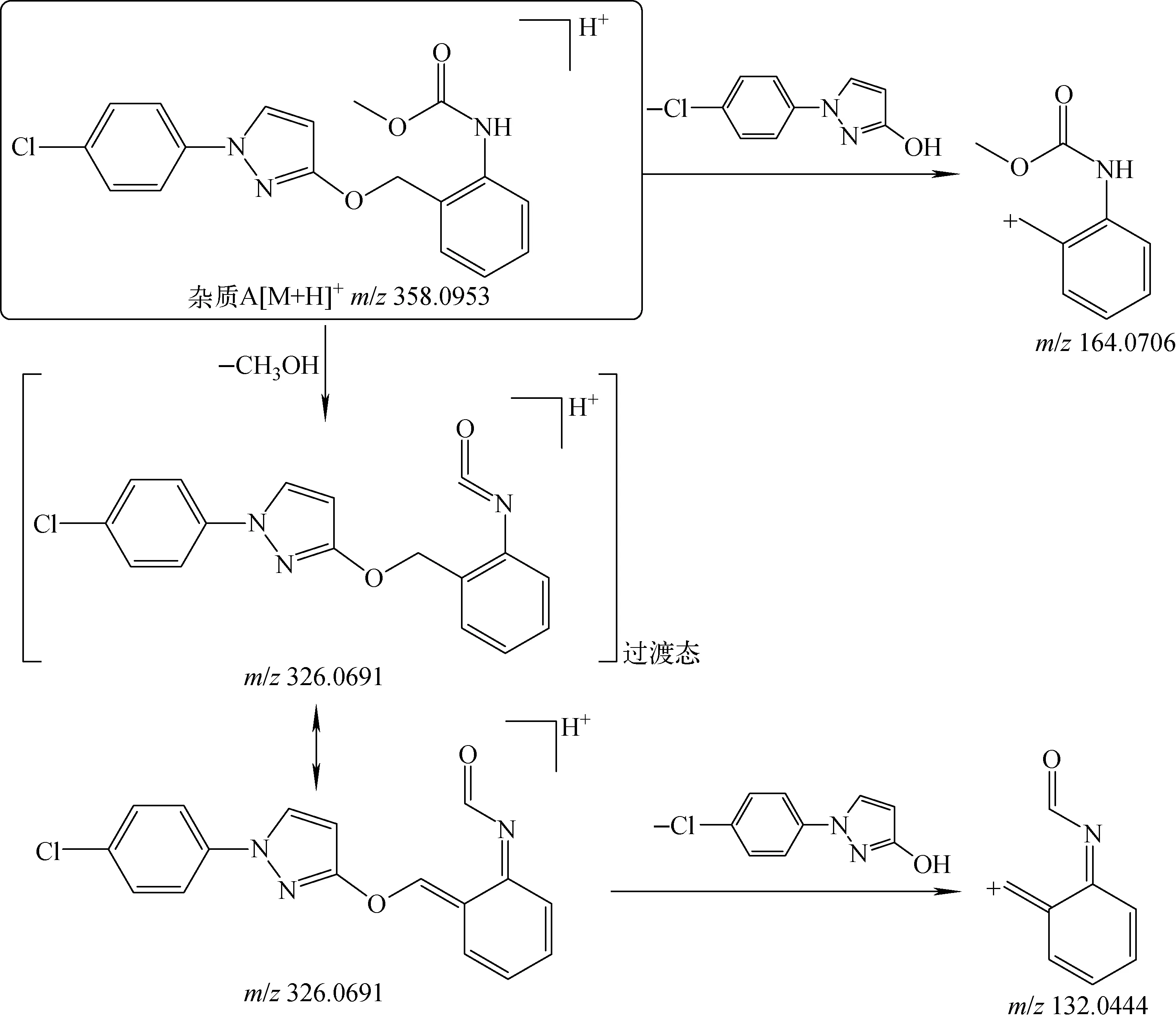
图6 杂质A可能的裂解途径Fig.6 Proposed fragmentation pathway of impurity A

图7 杂质B的一级(a)与二级(b)质谱图Fig.7 MS (a) and MS/MS (b) spectra of impurity B
从合成路线分析Br原子的位置,有2种可能性,示于图10。一种可能性是苄基溴化的步骤中发生了二溴化副反应,苄基上有2个H原子被Br原子取代,继续反应,其中1个Br原子被1-(4-氯苯基)-1H-3-吡唑醇取代,而另1个Br原子则保留在苄基上,这种解释更符合合成理论的预期;另一种可能性是Br原子取代了吡唑环上的4号位H,其来源是苄溴化反应中过量的Br被带入到了下一步反应,直接与吡唑醚菌酯发生了溴化反应。
进一步分析杂质C的二级质谱图,发现其含有与吡唑醚菌酯相同的主要碎片离子m/z194.081 3、164.070 6,说明杂质C与吡唑醚菌酯分子的甲氧基氨基甲酸酯部分可能是相同的,m/z194.081 3碎片是杂质C失去1分子溴代1-(4-氯苯基)-1H-3-吡唑醇得到的,由此推测Br原子可能位于吡唑醇片段上。综合质谱和合成路线分析的结果,杂质C的结构可能是吡唑醚菌酯吡唑环被溴化的产物(图10中可能性2),由此进一步推测杂质C可能的裂解途径,示于图11。其中,m/z355.070 6是一个奇电子离子。

图8 杂质B可能的裂解途径Fig.8 Proposed fragmentation pathway of impurity B
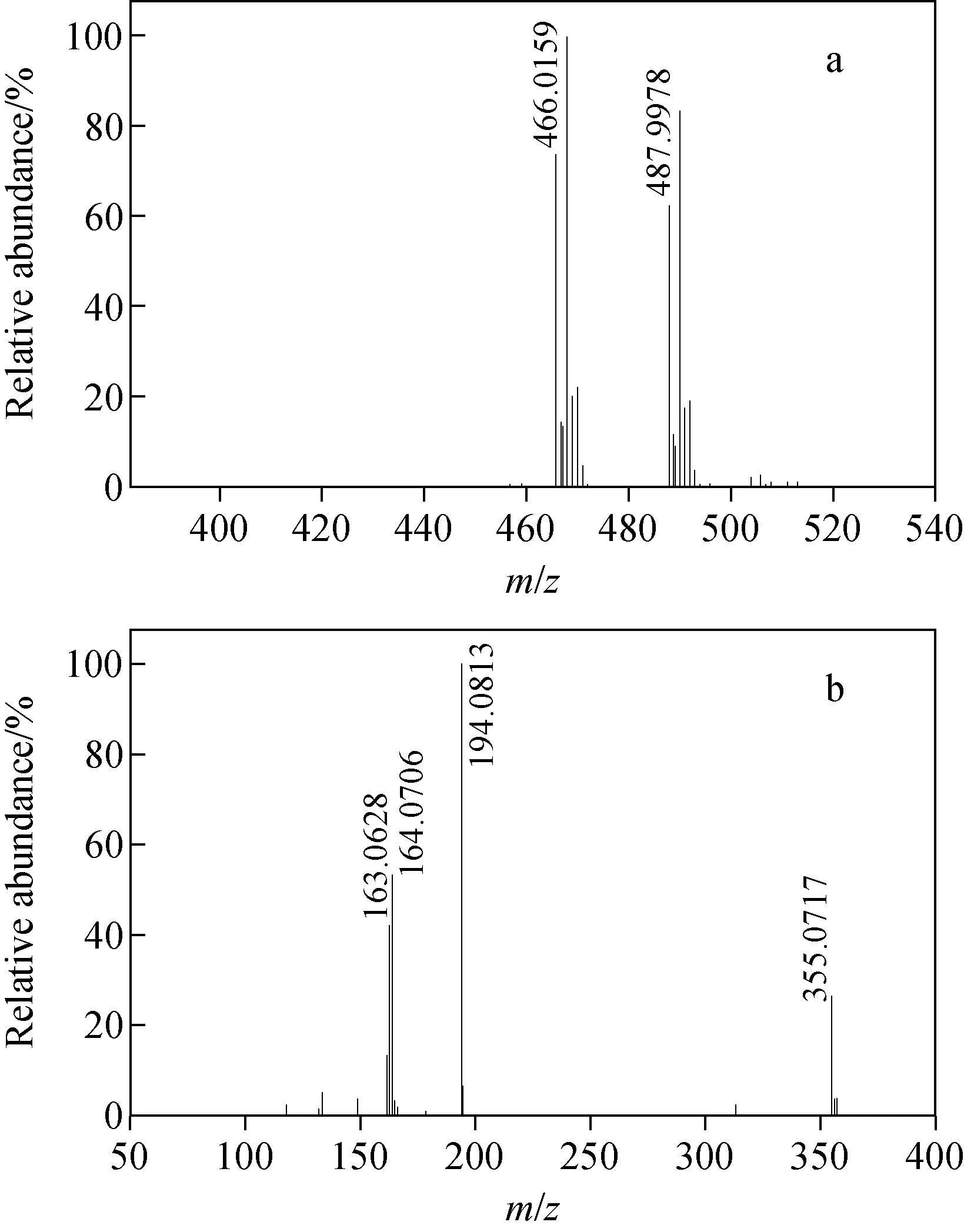
图9 杂质C的一级(a)与二级(b)质谱图Fig.9 MS (a) and MS/MS (b) spectra of impurity C
2.3 杂质对照品的比对与确认
根据以上由质谱和合成路线推测的杂质结构,经过实验室合成得到杂质对照品,将对照品的保留时间、质谱信息与原药中的杂质对比,结果列于表2。结果表明,合成的杂质对照品与原药中杂质的保留时间、质谱图一致,说明质谱分析结果准确可靠。
3 结论
本工作应用UPLC-MS和HCD MS/MS技术分析了实验室合成的吡唑醚菌酯原药中3个主要杂质。结果表明,在吡唑醚菌酯以及杂质B、C的HCD质谱中,同时存在着偶电子离子和奇电子离子。结合原药合成路线推测出3个杂质可能的结构:杂质A产生于硝基羟胺化还原步骤中;杂质B由羟胺中间体与二氯乙烷溶剂反应产生;杂质C是苄溴化反应步骤中过量的溴导致的。由此可见,在吡唑醚菌酯原药的工艺改进活动中,控制羟胺化、溴化两个步骤中的副反应,有助于提升原药的质量。
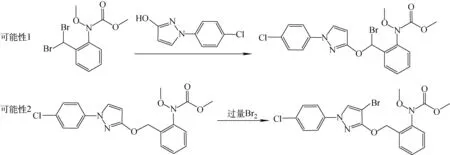
图10 杂质C生成的2种途径Fig.10 Two possible formation pathways of impurity C

图11 杂质C可能的裂解途径Fig.11 Proposed fragmentation pathway of impurity C
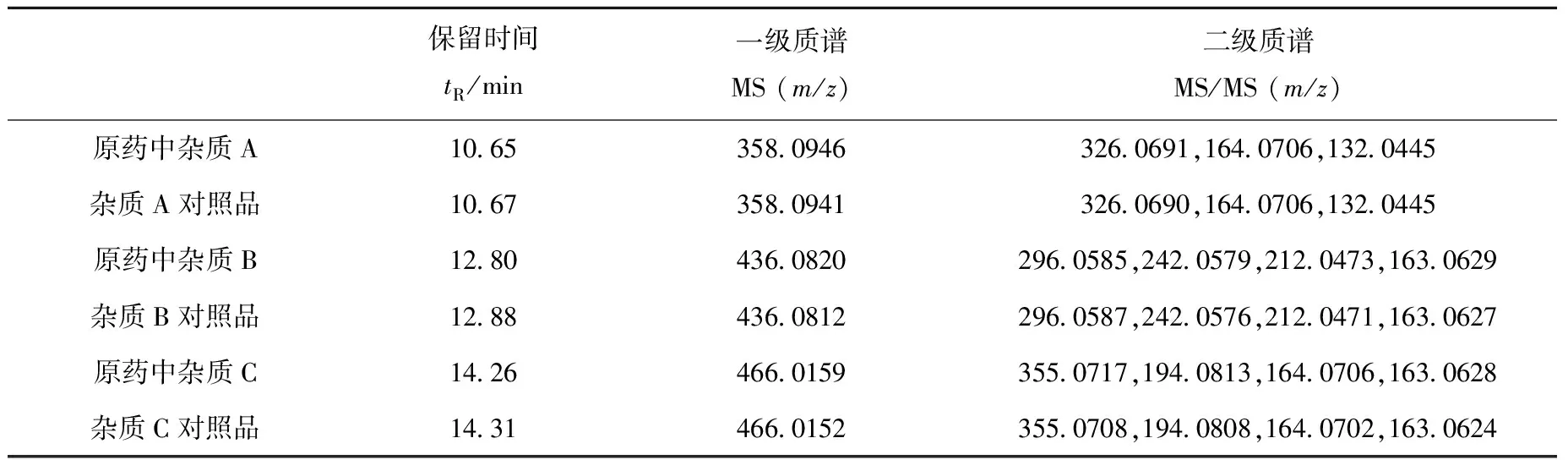
保留时间tR/min一级质谱MS(m/z)二级质谱MS/MS(m/z)原药中杂质A10 65358 0946326 0691,164 0706,132 0445杂质A对照品10 67358 0941326 0690,164 0706,132 0445原药中杂质B12 80436 0820296 0585,242 0579,212 0473,163 0629杂质B对照品12 88436 0812296 0587,242 0576,212 0471,163 0627原药中杂质C14 26466 0159355 0717,194 0813,164 0706,163 0628杂质C对照品14 31466 0152355 0708,194 0808,164 0702,163 0624
参考文献:
[1] 陈雨,张爱芳,夏本勇,等. 吡唑醚菌酯对大豆炭疽病防效及保健增产作用[J]. 农药,2011,50(9):697-699.
CHEN Yu, ZHANG Aifang, XIA Benyong, et al. Efficacy of pyraclostrobin in controlling soybean anthracnose and theireffects on the health protection and yield increase[J]. Agrochemicals, 2011, 50(9): 697-699(in Chinese).
[2] 张梅凤,吕秀亭. 2011年-2015年专利到期的农药品种之吡唑醚菌酯[J]. 今日农药, 2012, (8): 36-38.
ZHANG Meifeng, LV Xiuting. Patent expired pesticide during 2011-2015: pyraclostrobin[J]. Current Pesticide, 2012, (8): 36-38(in Chinese).
[3] 陶贤鉴,罗亮明,黄超群,等. 吡唑醚菌酯的合成研究[J]. 农药研究与应用,2009,13(1):16-21.
TAO Xianjian, LUO Liangming, HUANG Chaoqun, et al. Synthesis of pyraclostrobin[J]. Agrochemicals Research & Application, 2009, 13(1): 16-21(in Chinese).
[4] 李清,李巍,刘东志,等. 吡唑醚菌酯的合成研究[J]. 化学工业与工程,2016,33(1):45-50.
LI Qing, LI Wei, LIU Dongzhi, et al. Synthesis of pyraclostrobin[J]. Chemical Industry and Engineering, 2016, 33(1): 45-50(in Chinese).
[5] 马海军,曹庆亮,马亚芳,等. 吡唑醚菌酯的合成和初步生物活性[J]. 农药,2013,52(6):408-410.
MA Haijun, CAO Qingliang, MA Yafang, et al. Synthesis and biological activities of pyraclostrobin[J]. Agrochemicals, 2013, 52(6): 408-410(in Chinese).
[6] 杨丽娟,柏亚罗. 甲氧基丙烯酸酯类杀菌剂-吡唑醚菌酯[J]. 现代农药,2012,11(4):46-50.
YANG Lijuan, BAI Yaluo. Strobilurin fungicide-pyraclostrobin[J]. Modern Agrochemicals, 2012, 11(4): 46-50(in Chinese).
[7] 陈海燕,陶文波,丁克鸿. 液质联用分析嘧菌酯合成中的副反应[J]. 农药,2016,(10):725-728.
CHEN Haiyan, TAO Wenbo, DING Kehong. Analysis of side reactions in the synthesis of azoxystrobin by LC/MS[J]. Agrochemicals, 2016, (10): 725-728(in Chinese).
[8] 王金秋,马建民,夏曦,等. 超高效液相色谱-串联质谱法同时测定猪肌肉中13种喹诺酮药物残留[J]. 质谱学报,2014,35(2):185-192.
WANG Jinqiu, MA Jianmin, XIA Xi, et al. Determination of 13 quinolone antibiotic residues in swine muscle by UPLC MS/MS[J]. Journal of Chinese Mass Spectrometry Society, 2014, 35(2): 185-192(in Chinese).
[9] 周建良,周哲,陈碧莲,等. UHPLC/LTQ Orbitrap MS法解析一种未知西地那非衍生物[J]. 质谱学报,2016,37(5):422-430.
ZHOU Jianliang, ZHOU Zhe, CHEN Bilian, et al. Identification of an unknown derivative of sildenafil by UHPLC/LTQ Orbitrap MS[J]. Journal of Chinese Mass Spectrometry Society, 2016, 37(5): 422-430(in Chinese).
[10] 王子健,刘颖,刘思燚,等. UPLC-HRMSn结合高能诱导裂解快速鉴定麦冬中高异黄酮类成分[J]. 质谱学报,2016,37(6):481-491.
WANG Zijian, LIU Ying, LIU Siyi, et al. Rapid identification of homoisoflavonoids in ophiopogon japonicas based on UPLC-HRMSncombined HCD method[J]. Journal of Chinese Mass Spectrometry Society, 2016, 37(6): 481-491(in Chinese).
[11] 王敏,张海燕,杨金良,等. 磺胺类药物电喷雾质谱高能裂解规律[J]. 温州医学院学报,2013,43(10):642-646.
WANG Min, ZHANG Haiyan, YANG Jinliang, et al. Research on fragmentation pathways of sulfonamide by ESI high energy collision induced dissociationtechnique[J]. Journal of Wenzhou Medical College, 2013, 43(10): 642-646(in Chinese).
[12] GODFREY A R, WILLIAMS C M, DUDLEY E, et al. Investigation of uremic analytes in hemodialysate and their structural elucidation from accurate mass maps generated by a multi-dimensional liquid chromatography mass spectrometry approach[J]. Rapid Communications in Mass Spectrometry, 2009, 23(19): 3 194-3 204.
[13] HOSSEINI S E, SAEIDIAN H, AMOZADEH A, et al. Fragmentation pathways and structural characterization of organophosphorus compounds related to the chemical weapons convention by electron ionization and electrospray ionization tandem mass spectrometry[J]. Rapid Communications in Mass Spectrometry, 2016, 30(24): 2 585-2 593.
[14] KARNI M, MANDELBAUM A. The even electron rule[J]. Organic Mass Spectrometry, 1980, 15(2): 53-64.
[15] 丁友超,杨安南,蔡建和,等. 官能团对染料在电喷雾串联质谱中的离子化和裂解行为的影响[J]. 质谱学报,2009,30(6):340-345.
DING Youchao, YANG Annan, CAI Jianhe, et al. Effects of functional groups on ionization andfragmentation of dyestuffs by ESI-MS/MS[J]. Journal of Chinese Mass Spectrometry Society, 2009, 30(6): 340-345(in Chinese).

