富硒蛹虫草中有机硒的分析
陈尚龙,刘辉,张建萍,*,戴意强,魏云
(1.徐州工程学院食品(生物)工程学院,江苏徐州221018;2.徐州工程学院江苏省食品资源开发与质量安全重点建设实验室,江苏徐州221018)
Se是1种对人体健康有着重大意义的必需微量营养元素,它可以与人体内一些酶结合形成具有很强抗氧化能力的物质,从而增强人体的免疫力[1]。Se需要通过食物从外界摄入,平时食用的食物中Se含量极低,很难满足人体正常需要,导致缺Se现象较为普遍,严重威胁人体健康[2-3]。如何科学地补Se已成为研究热点。近年来,随着对富硒产品功能研究的深入,已经认识到高品质富硒产品不仅取决于硒的含量,还与硒的形态有着密切关联[4-8]。在人体内不同形态的Se有着不同的化学行为和生物活性[9-10]。相关研究报告表明,无机硒不易被人体吸收,生物活性低,具有一定毒性,摄入不当会引起慢性中毒;而经过生物转换的有机硒,易被人体吸收,毒性低,具有的生物学功能是由硒蛋白来调控和实现的[11-14],因此与无机硒相比,有机硒更为重要。
本试验以实验室研制的富硒蛹虫草为研究对象。首先,参照DBS42/002-2014《湖北省食品安全地方标准富有机硒食品硒含量要求》制备出富硒蛹虫草总硒测定试样;其次,参照GB 1903.21-2016《食品安全国家标准食品营养强化剂富硒酵母》制备出富硒蛹虫草无机硒测定试样;然后,再使用高分辨-连续光源石墨炉原子吸收光谱法(high resolution-continuum source graphite furnace atomic absorption spectrophotometry,HR-CSGFAAS)[15-23]进行测定;最后,根据“有机硒含量(mg/g)=总硒含量(mg/g)-无机硒含量(mg/g)”计算出富硒蛹虫草中有机硒含量,为快速、准确检测食品中微量元素含量及其形态提供科学依据。
1 材料与方法
1.1 材料与试剂
富硒蛹虫草:江苏省食品资源开发与质量安全重点建设实验室研发的样品。
浓硝酸、高氯酸、φ(乙醇)=95%、Mg(NO3)2、Pd(NO3)2(均为优级纯):国药集团化学试剂有限公司;Se标准溶液(1 g/L):国家化学试剂质检中心;18.2MΩ·cm超纯水;氩气(纯度大于99.99%);玻璃器皿均用φ(HNO3)=5%溶液浸泡24 h以上。
1.2 仪器与设备
ContrAA 700高分辨连续光源原子吸收光谱仪(配有MPE60自动进样器):德国Analytik Jena公司;L550离心机:湖南湘仪离心机仪器有限公司;CascadaTM实验室超纯水系统:美国Pall公司;FA-2004B电子天平:上海越平科学仪器有限公司;220V-AC电子电炉(0~2 000W):上海树立仪器仪表有限公司;移液器:德国Eppendorf公司。
1.3 方法
1.3.1 仪器工作参数
HR-CSGFAAS测定Se工作参数:分析谱线为196.026 7 nm,载气为高纯氩气,基体改进剂为Pd(NO3)2(1 g/L)和 Mg(NO3)2(0.5 g/L)混合溶液,基体改进剂添加体积为5μL,进样体积为20μL,灰化温度为1 100℃,原子化温度为2 200℃,原子化升温速度为1 500℃/s。
1.3.2 基体改进剂溶液的配制
用 φ(HNO3)=0.5%溶液溶解 0.1 g Pd(NO3)2和0.05 g Mg(NO3)2后转移至 100mL 容量瓶中,再用此溶液定容至刻度,配制成1 g/L Pd(NO3)2和0.5 g/L Mg(NO3)2混合溶液。
1.3.3 标准工作曲线的配制
用移液枪准确移取60μLSe标准溶液(1 g/L)置于100mL容量瓶中,再用φ(HNO3)=0.5%溶液定容至刻度,配制成质量浓度为0.6mg/L的Se标准使用液,再通过MPE自动进样器实现标准曲线质量浓度梯度为 0.03、0.09、0.15、0.30、0.45、0.60mg/L。
1.3.4 样品前处理
总硒测定试样制备(参照DBS42/002-2014):准确称取0.5 g~2.0 g(精确至0.1mg)富硒蛹虫草粉末试样,置于150mL高筒烧杯内,加10.0mL混合酸(硝酸与高氯酸按体积比4∶1混合)及几粒玻璃珠,盖上表面皿冷消化过夜。次日于电热板上加热,并及时补加混合酸。当溶液变为清亮无色并伴有白烟时,再继续加热至剩余体积2mL左右,切不可蒸干。冷却,再加5mL盐酸(6mol/L),继续加热至溶液变为清亮无色并伴有白烟出现,以完全将六价硒还原成四价硒。冷却,转移定容至50mL容量瓶中,同时做空白试验。
无机硒测定试样制备参照GB 1903.21-2016:准确称取1 g左右(精确至0.1mg)富硒蛹虫草粉末试样,置于50mL小烧杯中,加入25mLφ(乙醇)=95%,在磁力搅拌器中搅拌30min,使试样充分溶解,转移至100mL容量瓶中,用φ(乙醇)=95%定容至刻度,振荡、摇匀,静置于冰箱1 h。将定容后的溶液置于4 000 r/min条件下离心30min。同时做空白试验。
2 结果与分析
2.1 基体改进剂添加体积的优化
试验以 Pd(NO3)2(1 g/L)和 Mg(NO3)2(0.5 g/L)混合溶液为基体改进剂,基体改进剂的添加体积是影响Se吸光度的因素之一,为了最大限度地消除基体干扰,提高Se的吸光度。试验在固定其他参数条件下,只改变基体改进剂的添加体积,测定Se的吸光度,结果如图1所示。
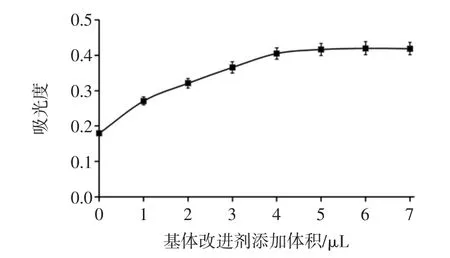
图1 基体改进剂的体积对吸光度的影响Fig.1 Effectofm atrixm odifier volum eon absorbancy
由图 1 可知,以 Pd(NO3)2(1 g/L)和 Mg(NO3)2(0.5 g/L)混合溶液为基体改进剂能显著地提高Se的吸光度,这是由于不添加基体改进剂时,过高的灰化温度会导致Se挥发损失,使Se的吸光度降低。当添加体积<5μL时,Se的吸光度随着基体改进剂添加体积的增大而增大;当体积≥5μL时,增加趋势趋于平缓。因此,试验选择基体改进剂最佳添加体积为5μL。
2.2 灰化温度的优化
灰化温度是影响Se吸光度的因素之一,过低的灰化温度无法使基体完全灰化,导致背景吸光度升高;过高的灰化温度会导致Se挥发损失,使Se的吸光度降低,重复性变差。试验在固定其他参数条件下,只改变灰化温度,测定Se的吸光度,结果如图2所示。
由图2可知,当灰化温度<1 100℃时,Se的吸光度随着灰化温度的增大而增大;当灰化温度≥1 100℃时,Se的吸光度开始下降。因此,试验选择最佳的灰化温度为1 100℃。
2.3 原子化温度的优化
原子化温度也是影响Se吸光度的因素之一,过低的原子化温度无法使Se彻底原子化,导致其吸光度降低,吸附峰峰形变差;过高的原子化温度会减少石墨管的使用次数。试验在固定其他参数条件下,只改变原子化温度,测定Se的吸光度,结果如图3所示。不同原子化温度条件下,Se的吸收峰峰形如图4所示。

图2 灰化温度对吸光度的影响Fig.2 Effectof ashing temperatureon absorbancy
由图3可知,当原子化温度<2 200℃时,Se的吸光度随着原子化温度的增大而增大;当原子化温度≥2 200℃时,Se的吸光度趋于稳定。由图4可知,当原子化温度为2 000℃和2 100℃时,Se的吸收峰峰形较差,拖尾现象明显;当原子化温度为2 200℃和2 300℃时,Se的吸收峰峰形较好,无明显拖尾现象。因此,试验选择最佳的原子化温度为2 200℃。

图3 原子化温度对吸光度的影响Fig.3 Effectof atom izing temperatureon absorbancy
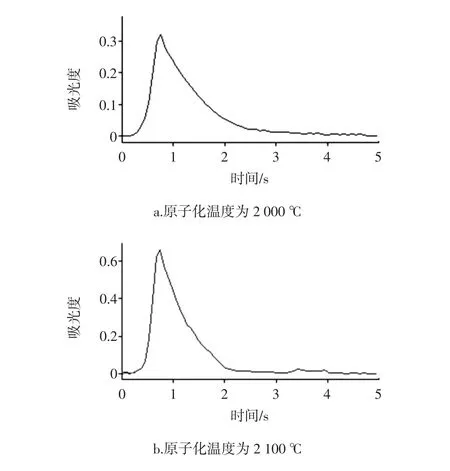
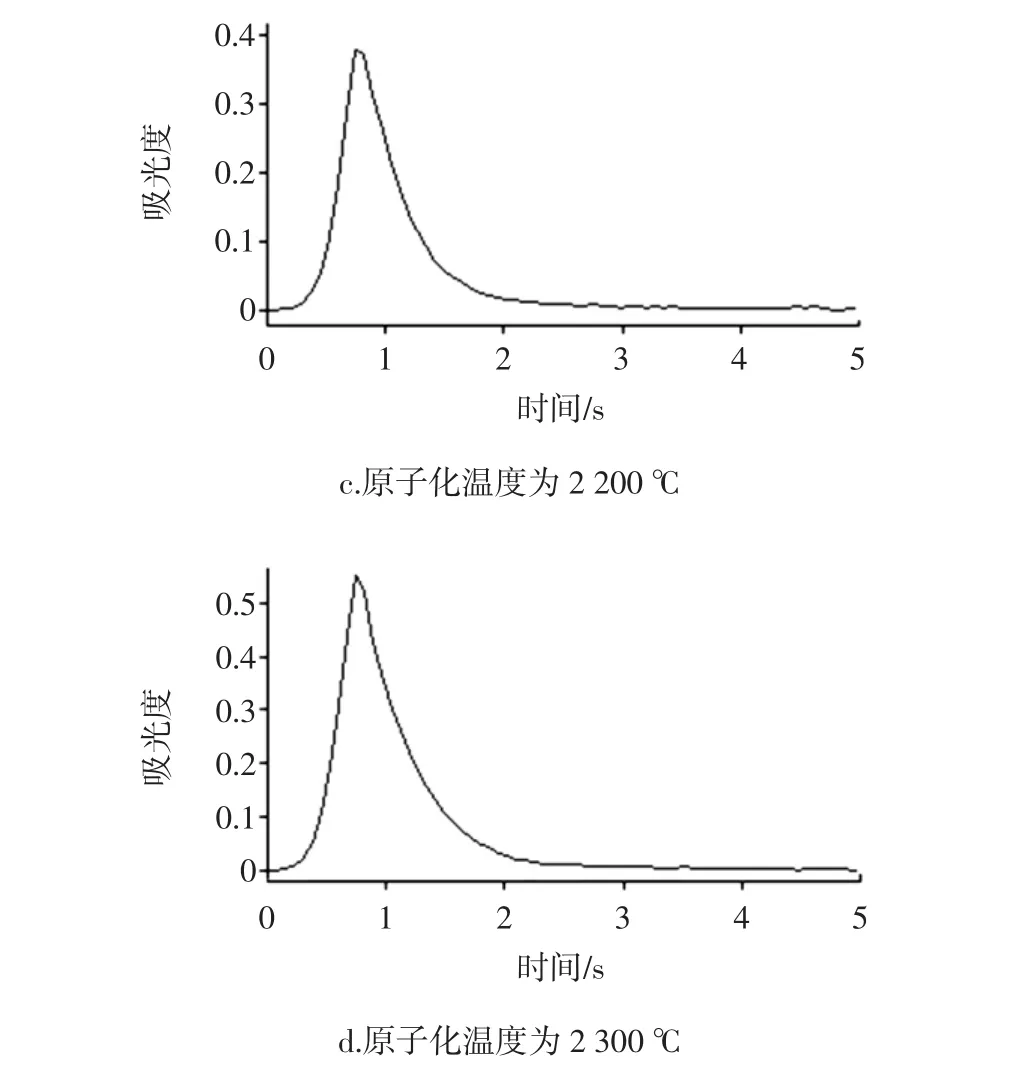
图4 原子化温度对Se吸收峰的影响Fig.4 Effectof atom izing tem peratureon selenium absorption peak
2.4 标准工作曲线
通过ASpect CS软件设置Se的检测方法,将0.60mg/LSe 标准使用液、Pd(NO3)2(1 g/L)和 Mg(NO3)2(0.5 g/L)混合溶液、稀释适当倍数的空白溶液和待测样品溶液放入MPE自动进样器的对应位置,建立相应的测定序列,使用HR-CSGFAAS进行顺序测定。以Se的质量浓度为横坐标、Se的吸光度为纵坐标,经AS-pectCS软件绘制非线性标准工作曲线如图5所示。
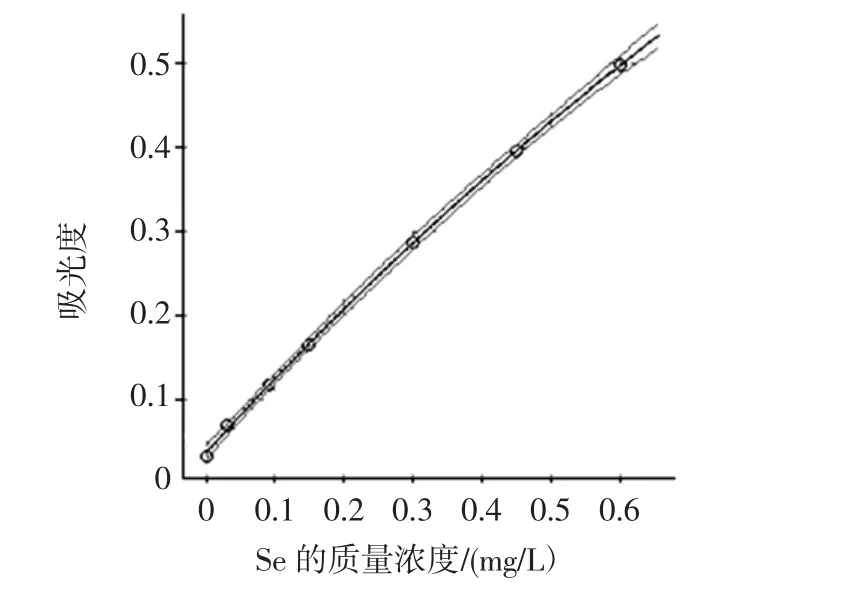
图5 标准工作曲线Fig.5 Standard working curves
所得方程为A=(0.037 312 5+0.917 625 5c)/(1+0.304 683 9c),相关系数为 0.999 2,表明在 0~0.6mg/L范围内,Se的质量浓度与吸光度呈现良好的关系。
2.5 富硒蛹虫草中有机硒的测定
在最佳试验条件下测定总硒和无机硒的含量,根据“有机硒含量(mg/g)=总硒含量(mg/g)-无机硒含量(mg/g)”计算出富硒蛹虫草中有机硒的含量,结果见表1。
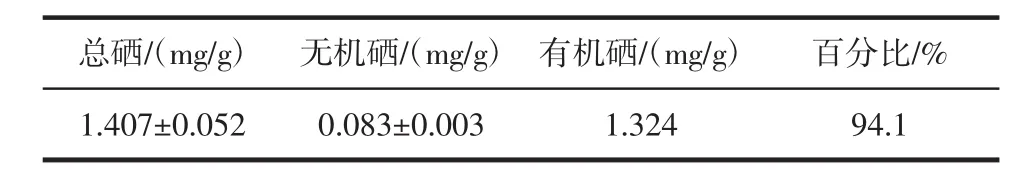
表1 富硒蛹虫草中有机硒的含量(n=3)Tab le1 The contentsof organic Se in selenium-enriched Cordycepsm ilitaris(n=3)
由表1可知,富硒蛹虫草总硒含量为1.407mg/g,无机硒含量为0.083mg/g,计算出有机硒含量为1.324mg/g,所占百分比为94.1%,这说明富硒蛹虫草含有丰富的有机硒,是补硒良品。
2.6 加标回收率试验
将一定体积Se标准溶液和富硒蛹虫草一起加入到烧杯或锥形瓶中,按1.3.4节进行操作,在最佳试验条件下进行测定,计算Se的加标回收率[24-25],结果见表2。
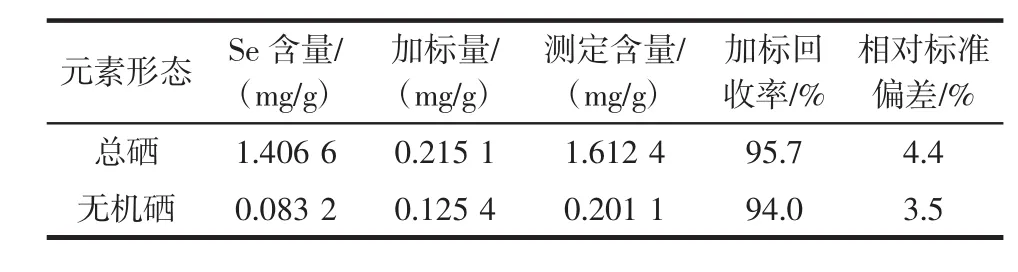
表2 加标回收率(n=3)Table2 Recoveriesof Se in selenium-enriched Cordycepsm ilitaris(n=3)
由表2可知,总硒和无机硒的加标回收率分别为95.7%和94.0%,相对标准偏差<4.5%,表明参照DBS42/002-2014和GB 1903.21-2016测定富硒蛹虫草总硒和无机硒,结果准确可靠,添加的Se标准溶液(无机硒)几乎全部在待测无机硒试样中。
3 结论
试验以 Pd(NO3)2(1 g/L)和 Mg(NO3)2(0.5 g/L)混合溶液为基体改进剂,通过试验优化出基体改进剂最佳添加体积为5μL,最佳灰化温度为1 100℃,最佳原子化温度为2 200℃。测定结果表明,富硒蛹虫草总硒含量为1.407mg/g,无机硒含量为0.083mg/g,计算出有机硒含量为1.324mg/g,所占百分比为94.1%,这说明富硒蛹虫草含有丰富的有机硒,是补硒良品。总硒和无机硒的加标回收率分别为95.7%和94.0%,相对标准偏差<4.5%,表明参照DBS42/002-2014和GB 1903.21-2016测定富硒蛹虫草总硒和无机硒,结果准确可靠,添加的Se标准溶液(无机硒)几乎全部在待测无机硒试样中。
参考文献:
[1]王明洋,方勇,裴斐,等.硒对杏鲍菇营养品质和抗氧化酶活性的影响[J].食品科学,2016,37(11):208-213
[2]Zhang Z,Zhao P,Guo J,et al.The extraction of different solubility protein in selenium enriched peanuts and the analysis of their antioxidantactivity[J].Science&Technology of Food Industry,2012,33(4):323-326
[3]BodnarM,Konieczka P.Evaluation of candidate referencematerial obtained from selenium-enriched sprouts for the purpose of selenium speciation analysis[J].LWT-Food Scienceand Technology,2016,70:286-295
[4]李红卫,王开萍,吴娱,等.柱前衍生-反相高效液相色谱法研究富硒米曲霉中有机硒形态[J].食品科学,2015,36(22):137-141
[5]Mao G H,Ren Y,Li Q,et al.Anti-tumor and immunomodulatory activity ofselenium (Se)-polysaccharide from Se-enriched Grifola frondosa[J].International Journal of Biological Macromolecules,2016,82(10):607-613
[6]Wang Y D,Wang X,Wong Y S.Generation of selenium-enriched ricewith enhanced grain yield,selenium contentand bioavailability through fertilisation with selenite[J].Food Chemistry,2013,141(3):2385-2393
[7]Bo Y,WangD,WeiG,etal.Selenium-enriched Candidautilis:Efficient preparation with l-methionine and antioxidant capacity in rats[J].Journal of Trace Elements in Medicine&Biology,2012,27(1):7-11
[8]Gionfriddo E,Naccarato A,Sindona G,etal.A reliable solid phase microextraction-gas chromatography-triple quadrupolemass spectrometry method for the assay of selenomethionine and selenomethylselenocysteine in aqueous extracts:Difference between selenized and not-enriched selenium potatoes[J].Analytica Chimica Acta,2012,747(20):58-66
[9]Mahn A,Zamorano M,Barrientos H,etal.Optimization of a process toobtain selenium-enriched freeze-dried broccoliwith high antioxidantproperties[J].LWT-Food Science and Technology,2012,47(2):267-273
[10]LIU LIHANG,FAN WANLUN.Incomplete digestion FAAS-faes determination ofcalcium,magnesium and potassium in human footexuviae[J].Physical Testing and Chemical Analysis PartB:Chemical Analysis,2005,37(2):348-352
[11]Dong JZ,Ding J,Yu PZ,etal.Composition and distribution of the main active components in selenium-enriched fruit bodies of Cordycepsmilitaris,link[J].Food Chemistry,2013,137(1/4):164-167
[12]Zhang B,Zhou K,Zhang J,etal.Accumulation and speciesdistribution ofselenium in Se-enriched bacterial cellsof the Bifidobacterium animalis01[J].Food Chemistry,2009,115(2):727-734
[13]王欣,幸苑娜,陈泽勇,等.高效液相色谱-电感耦合等离子体质谱法检测富硒食品中6种硒形态[J].分析化学,2013,41(11):1669-1674
[14]杨洋,吴小勇,张湛,等.富硒灵芝发酵培养工艺及产物抗氧化能力研究[J].现代食品科技,2010,26(12):1349-1353
[15]Peronico V CD,Raposo JL.Ultrasound-assisted extraction for the determination ofCu,Mn,Ca,and Mg in alternative oilseed cropsusing flame atomic absorption spectrometry[J].Food Chemistry,2016,196:1287-1292
[16]Ozbek N,Baysal A.A new approach for the determination ofsulphur in food samples by high-resolution continuum source flame atomic absorption spectrometer[J].Food Chemistry,2015,168(168):460-463
[17]Paz-Rodríguez B,Aboal-Somoza M,Bermejo-Barrera P.Application of High Resolution-Continuum Source Flame Atomic Absorption Spectrometry(HR-CSFAAS):Determination of traceelements in teaand tisanes[J].Food Chemistry,2015,170:492-500
[18]JSantos,M TOliva-Teles,CDelerue-Matos,etal.Multi-elemental analysis of ready-to-eat“baby leaf”vegetables usingmicrowave digestion and high-resolution continuum source atomic absorption spectrometry[J].Food Chemistry,2014,151(151):311-316
[19]Baysal A,Akman S.A practicalmethod for the determination ofsulphur in coal samples by high-resolution continuum source flame atomic absorption spectrometry[J].Talanta,2011,85(5):2662-2665
[20]Ozbek N,Akman S.Method development for the determination of fluorine in toothpaste viamolecular absorption of aluminum mono fluoride using a high-resolution continuum source nitrous oxide/acetylene flame atomic absorption spectrophotometer[J].Talanta,2012,94(6):246-250
[21]Brandao GC,Jesus RM D,Silva EG PD,etal.Use of slurry sampling for the direct determination of zinc in yogurt by high resolution-continuum source flameatomic absorption spectrometry[J].Talanta,2010,81(4/5):1357-1359
[22]秦杰,陈尚龙,张建萍,等.微波消解-原子吸收法测定鸡精中金属元素[J].食品研究与开发,2014(22):63-67
[23]张建萍,陈尚龙,刘恩岐,等.微波消解-HR-CSAAS法测定几种调味品中的微量元素[J].现代食品科技,2013,29(6):1424-1427
[24]陈安徽,陈尚龙,巫永华,等.黄精酵素口服液中钙、铁和锌的形态分析[J].现代食品科技,2016,32(1):1425-1427
[25]陈琛,苏珂,陈贵堂,等.灰树花中铁的存在形态分析[J].食品科学,2013,34(22):189-192

