脑转移瘤放射治疗的剂量学研究
孔琪 陈香存 童铸廷 李云 王凡
安徽医科大学第一附属医院放疗科(合肥 230032)
颅脑是多种恶性肿瘤的常见转移部位,有20%~40%的原发肿瘤患者会发生脑转移,原发灶以肺癌最多见[1-2]。脑转移瘤的治疗既往以全脑放射治疗(whole⁃brain radiotherapy,WBRT)为主,但其颅内病灶控制率约60%,中位生存期仅3~6个月[3-4]。调强放疗(intensity⁃modulated radiothera⁃py,IMRT)技术的出现解决了WBRT肿瘤靶区照射剂量低,副反应大这一缺点,其可实现肿瘤靶区和邻近重要组织分别接受不同剂量照射,有效提高肿瘤的控制率和最大限度减少重要组织的损伤。IMRT包括序贯加量调强放疗(sequential intensity⁃modulated radiotherapy,sIMRT)和同步加量调强放疗(simultaneously integrated boost intensity⁃modulat⁃ed radiotherapy,SIB⁃IMRT)等,在肿瘤的治疗上两者均具有较好的靶区适形性、均匀性,能较好地保护周围正常组织[5-6]。研究[7]表明,在头颈部肿瘤的治疗上,SIB⁃IMRT与sIMRT技术相比,能更好地覆盖靶区,保护周围危及器官。对于脑转移瘤的治疗,IMRT技术也表现出明显的剂量学优势[8]。但两种调强技术在脑转移瘤治疗上的剂量学比较很少引起关注,本研究通过比较两者在优化脑转移瘤靶区的适形性和均匀性、降低危及器官的剂量等差异,为临床治疗脑转移瘤提供参考。
1 资料与方法
1.1 一般资料 选取2016年4月至2017年5月就诊于安徽医科大学第一附属医院放疗科的脑转移瘤患者20例,其中男14例,女6例;原发病灶分别为肺癌13例、乳腺癌5例、胃癌1例、直肠癌1例;年龄40~76岁,中位年龄为62岁。所有患者均符合以下条件:原发灶经病理学确诊,脑转移瘤均经头颅磁共振(MRI)证实;脑部转移灶未经手术治疗;放疗前完善血常规、生化、胸片及心电图等常规检查;无明显的精神行为障碍;KPS评分60分以上;所有患者均签署放疗知情同意书。
1.2 方法
1.2.1 模拟定位、靶区勾画及计划设计 采用瓦里安ACUITY模拟定位机定位,患者平躺,头部采用热塑模型固定,以肿瘤大致中心为定位点,将定位标志点标志于热塑模型上。采用美国西门子Artiste直线加速器进行定位扫描,扫描范围为整个颅脑,层厚3 mm,将扫描图像传至TPS治疗计划系统。由同一位临床医生进行靶区勾画,以患者头颅MRI显示的肿瘤病灶作为肿瘤靶区(gross tumor volume,GTV),全脑作为临床靶区(clinical target volume,CTV),然后均匀性外扩作为计划靶区(planning target volume,PTV),即将GTV、CTV分别外扩3 mm分别作为P⁃GTV、P⁃CTV;勾画两侧晶体、脑干等危及器官。对入组的每例患者分别设计sIMRT及SIB⁃IMRT计划,两者均采用五野分布照射方式,6⁃MV X射线进行计划制定。
1.2.2 靶区剂量设计 在sIMRT计划中,给予全脑计划靶区(P⁃CTV)40 Gy/20 f,后对转移瘤计划靶区(P⁃GTV)加量20 Gy/10 f,1次/d,5次/周;SIB⁃IMRT计划分别给予P⁃CTV 40 Gy/24 f,P⁃GTV 60 Gy/24 f,1次/d,5次/周。靶区剂量设计要求如下:(1)处方剂量要求为95%的PTV所接受的最低剂量;(2)接受≥110%处方剂量的PTV体积≤20%;(3)<3%的PTV体积接受<93%处方剂量;(4)除外PTV以外的其他地方不允许出现>110%处方剂量的吸收剂量。
1.2.3 危及器官剂量限制 危及器官为两侧晶体、脑干。晶体最大照射剂量<9 Gy;脑干最大受照剂量<54 Gy。
1.2.4 剂量学评价 通过剂量体积直方图(dose⁃volume histogram,DVH)对两种计划的剂量学分布进行比较,评价指标包括P⁃CTV、P⁃GTV靶区剂量的最大值、平均值和最小值及靶区的适形性指数(conformation index,CI)、均匀性指数(homogeneity index,HI)。CI取值范围为0 ~ 1,数值越接近于1表明靶区适形性越好;HI值越接近于1,靶区剂量越均匀。并记录两种计划中脑干、双侧晶体的最大剂量、平均剂量。
1.3 统计学方法 采用SPSS 21.0统计软件进独立样本t检验,P<0.05视为差异有统计学意义。
2 结果
2.1 sIMRT与SIB⁃IMRT计划中靶区剂量参数比较 见表1。SIB⁃IMRT计划与sIMRT计划相比,前者的P⁃GTV和P⁃CTV靶区剂量最大值、P⁃GTV靶区剂量平均值均高于后者,两者差异有统计学意义(P< 0.01);前者的P⁃GTV靶区剂量最小值、P⁃CTV靶区剂量平均值和最小值均稍低于后者,两者差异无统计学意义(P>0.05)。
表1 两种调强技术的靶区剂量参数比较Tab.1 Comparison of target areas parameters of two kinds of intensity modulation technique ±s,Gy
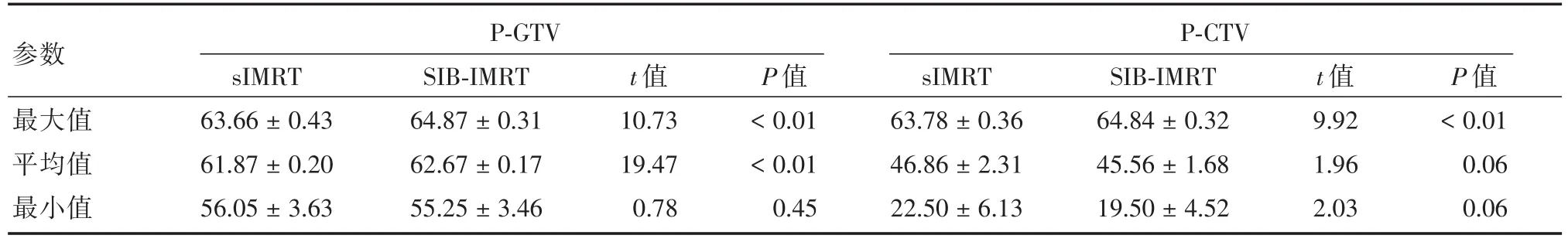
表1 两种调强技术的靶区剂量参数比较Tab.1 Comparison of target areas parameters of two kinds of intensity modulation technique ±s,Gy
参数最大值平均值最小值P⁃GTV P⁃CTV sIMRT 63.66±0.43 61.87±0.20 56.05±3.63 SIB⁃IMRT 64.87±0.31 62.67±0.17 55.25±3.46 t值10.73 19.47 0.78 P值<0.01<0.01 0.45 sIMRT 63.78±0.36 46.86±2.31 22.50±6.13 SIB⁃IMRT 64.84±0.32 45.56±1.68 19.50±4.52 t值9.92 1.96 2.03 P值<0.01 0.06 0.06
表2 两种放疗计划中靶区的CI值的比较Tab.2 Comparison of conformation index of target areas in two radiotherapy schemes ±s
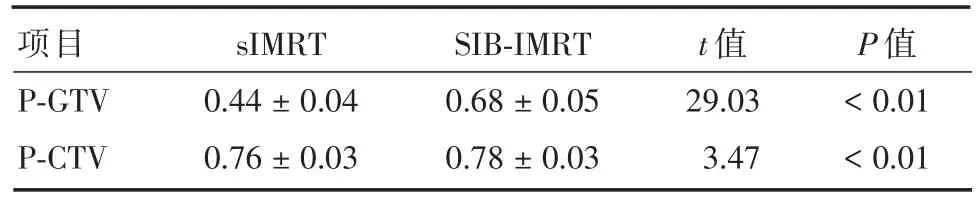
表2 两种放疗计划中靶区的CI值的比较Tab.2 Comparison of conformation index of target areas in two radiotherapy schemes ±s
项目P⁃GTV P⁃CTV sIMRT 0.44±0.04 0.76±0.03 SIB⁃IMRT 0.68±0.05 0.78±0.03 t值29.03 3.47 P值<0.01<0.01
2.2 两种放疗计划的靶区适形性指数与均匀性指数分析 在P⁃GTV、P⁃CTV的靶区适形性(CI)方面上,SIB⁃IMRT计划较sIMRT计划表现出明显的优势,两者之间差异有显著性(P<0.01),见表2。
SIB⁃IMRT计划在P⁃GTV的靶区均匀性(HI)方面较sIMRT计划表现出明显的优势,两者差异具有统计学意义(P<0.01);两者在P⁃CTV靶区的均匀性上无明显差异(P=0.05)。见表3。
2.3 两种调强放疗计划中危及器官的剂量分布比较 与sIMRT计划相比,SIB⁃IMRT计划中两侧晶体及脑干受照射的最大剂量及平均剂量均较前者减小,在脑干受照射剂量的平均值上,两者无明显差异(P=0.15);但在两侧晶体受照剂量的最大值、平均值、脑干受照剂量的最大值上,SIB⁃IMRT计划优势明显,两者差异具有统计学意义(P<0.01)。见表4。
表3 两种放疗计划中靶区的HI值的比较Tab.3 Comparison of homogeneity index of target areas in two radiotherapy schemes ±s

表3 两种放疗计划中靶区的HI值的比较Tab.3 Comparison of homogeneity index of target areas in two radiotherapy schemes ±s
项目P⁃GTV P⁃CTV sIMRT 1.06±0.01 1.46±0.04 SIB⁃IMRT 1.03±0.01 1.42±0.13 t值8.64 2.07 P值<0.01 0.05
表4 两种放疗计划中各危及器官受照射剂量值比较Tab.4 Comparison of radiation dose values of each organ in two radiotherapy schemes±s,Gy

表4 两种放疗计划中各危及器官受照射剂量值比较Tab.4 Comparison of radiation dose values of each organ in two radiotherapy schemes±s,Gy
最大值平均值器官脑干左晶体右晶体sIMRT 46.27±3.57 5.09±0.76 4.98±0.55 SIB⁃IMRT 45.09±2.27 4.28±0.54 4.24±0.52 t值3.25 4.49 5.98 P值<0.01<0.01<0.01 sIMRT 42.69±2.18 4.62±0.77 4.47±0.70 SIB⁃IMRT 41.98±0.96 3.88±0.52 3.87±0.66 t值1.50 3.46 3.89 P值0.15<0.01<0.01
3 讨论
放射治疗是脑转移瘤重要的治疗手段之一,如何在提高靶区剂量、提高局部控制率的同时降低周围正常组织的受照剂量、降低放疗副反应,是笔者面临的重要问题。WBRT作为一种二维普通放疗广泛应用于脑转移瘤的治疗,其主要的限制因素是过高的剂量对周围危及器官损伤明显,不良反应较重,因此其难以实现对肿瘤靶区的高剂量照射,对于脑部转移瘤病灶较大的患者不能达到肿瘤致死剂量,颅内病灶的局部控制率较低,预后较差。且研究[9-11]表明,WBRT引起的认知功能障碍较为广泛,主要表现在学习、记忆方面的变化,这可能与全脑放疗未能保护海马组织有关。随着放疗技术的发展,IMRT技术在肿瘤放射治疗上的优势逐渐得到认可,其良好的治疗疗效也引起人们的关注[12]。大量文献[13-14]指出,与WBRT、三维适形放疗相比,IMRT具有更好的靶区覆盖率及剂量分布,在危及器官的保护方面亦优于前两者。SIB⁃IMRT作为IMRT技术的一种,其采用同步加量的方式,在相同治疗次数下满足不同靶区的剂量要求,同时实现大野照射和小野追加照射,缩短了总的放疗时间,减少了周围正常组织的照射剂量及受照体积,在提高肿瘤照射剂量的同时降低了患者的不良反应。FERRO等[15]采用SIB⁃IMRT技术治疗1例多发脑转移瘤患者,给予全脑40 Gy/20 f,转移瘤50 Gy/20 f,结果显示95%的肿瘤靶区体积均达到处方剂量,靶区剂量均匀性较好,各危及器官受照剂量均在限定范围内;3个月后复查脑部MRI,大部分脑部病灶已完全缓解,40个月后所有病灶缓解且患者未出现明显的认知功能损害等不良反应。其他研究也提出在脑转移瘤的治疗上,SIB⁃IMRT技术安全可行,疗效明显[16]。
sIMRT与SIB⁃IMRT技术均属于调强放疗技术,但两者实现调强的方式不同,导致了两者在剂量学分布及治疗时间的差异。FENG等[17]对10例晚期宫颈癌患者分别制定SIB⁃IMRT与sIMRT计划进行剂量学比较,结果表明SIB⁃IMRT较sIMRT技术具有更好的靶区均匀性、适形性,且能减少靶区照射热点、对周围危及器官的保护作用也更显著。国内相关研究也指出对于盆腔淋巴结阳性的宫颈癌患者,SIB⁃IMRT较sIMRT技术能减少小肠、直肠等危及器官的照射剂量,且具有更好的靶区适形性[18]。该研究中,比较了两种放疗技术应用于脑转移瘤治疗上的剂量学优劣,结果表明,在全脑靶区(P⁃CTV)的靶区HI方面,两者无统计学差异(P> 0.05),但在肿瘤靶区(P⁃GTV)的靶区CI、HI以及全脑靶区的CI上,SIB⁃IMRT较sIMRT技术均表现出明显的优势(P<0.05);且能降低双侧晶体、脑干的受照射剂量,尤其在双侧晶体的保护上差异较显著(P<0.05);在P⁃GTV的最高剂量及平均剂量、P⁃CTV的最高剂量上,SIB⁃IMRT较sIMRT计划亦表现出明显的优势(P<0.05)。在头颈部肿瘤的治疗上两种放疗技术也表现出了相似的结果,MIYAZAKI等[19]对20例头颈部肿瘤患者放疗方式的比较中发现SIB⁃IMRT较sIMRT技术具有更好的靶区适形性、均匀性,且能降低危及器官的照射剂量。本实验的研究结果与以上研究一致,SIB⁃IMRT较sIMRT技术具有更好的靶区覆盖率,能更好地保护周围正常器官。近期研究也表明,在局部晚期宫颈癌患者中,SIB⁃IMRT较sIMRT技术能降低放疗的不良反应[20]。
在该研究中,两种放疗方式在靶区及危及器官的最大照射剂量上均表现出明显的差异,这意味着SIB⁃IMRT技术能改善对照射热点区域的控制,并将高剂量射线在危及器官中重新分配,但sIMRT技术却很难控制热点重叠问题。尽管在该研究中,SIB⁃IMRT较sIMRT技术在脑转移瘤的治疗上表现出明显的剂量学优势,但该研究样本量较少,物理师制定计划的主观性都会影响研究结果,在治疗过程中患者的摆位误差,不同技师进行治疗也会影响患者的治疗疗效。且在实际放疗过程中,两种放疗方式对患者可能产生的急性不良反应及最终疗效也需要进一步的研究。
综上所述,在脑转移瘤的治疗上,SIB⁃IMRT较sIMRT技术明显提高了肿瘤靶区的适形性、均匀性;在提高肿瘤靶区剂量的同时又能降低周围正常组织的受照射剂量,减少患者的不良反应。在病灶接受相同的物理剂量条件下,SIB⁃IMRT技术能明显缩短患者总的治疗时间,更适用于老龄、体弱、不能耐受长时间放疗的患者,在临床治疗脑转移瘤上可优先考虑。
参考文献
[1]ANDREVSKA A,KNIGHT K A.The feasibility and benefits of using volumetric arc therapy in patients with brain metastases:a systematic review[J].J Med Radiat Sci,2014,61(4):267⁃276.
[2]宁丽华,赵桂芝,张磊,等.全脑放疗伴随1~4个脑转移瘤同期加量不同调强技术的剂量学研究[J].中国医学物理学杂志,2016(2):128⁃133.
[3]ZHOU L,LIU J,XUE J,et al.Whole brain radiotherapy plus si⁃multaneous in⁃field boost with image guided intensity⁃modulated radiotherapy for brain metastases of non⁃small cell lung cancer[J].Radiat Oncol,2014,9:117.
[4]BERNHARDT D,ADEBERG S,BOZORGMEHR F,et al.Out⁃come and prognostic factors in patients with brain metastases from small⁃cell lung cancer treated with whole brain radiothera⁃py[J].J Neurooncol,2017,134(1):205⁃212.
[5]ZHOU G,SUN Y,QIAN J,et al.The dosimetric comparison of the radiotherapeutic plans between composite and synchronous planning approaches in sequential IMRT for nasopharyngeal car⁃cinoma[J].Int J Clin Exp Med,2015,8(9):15975⁃15982.
[6]MATSUO Y,SHIBUYA K,OKUBOK,et al.Long⁃term out⁃comes of intensity⁃modulated radiotherapy following extra⁃pleu⁃ral pneumonectomy for malignant pleural mesothelioma[J].Ac⁃ta Oncol,2017,56(7):957⁃962.
[7]NARAYANASAMY G,JANG S,PYAKURYAL A,et al.SU⁃E⁃T⁃301:evaluation of simultaneously integrated boost(SIB)and sequential IMRT boost(SqIB)treatments of head and neck can⁃cer using empirical radiobiological modeling[J].Med Phys,2013,40(6Part15):273.
[8]BORGHETTI P,PEDRETTI S,SPIAZZI L,et al.Whole brain radiotherapy with adjuvant or concomitant boost in brain metas⁃tasis:dosimetric comparison between helical and volumetric IMRT technique[J].Radiat Oncol,2016,11:59.
[9]姜群群,唐荣华.放射治疗所致神经系统损伤[J].神经损伤与功能重建,2014(6):522⁃525.
[10] ZHAO R,KONG W,SHANG J,et al.Hippocampal⁃sparing whole⁃brain radiotherapy for lung cancer[J].Clin Lung Can⁃cer,2017,18(2):127⁃131.
[11] WANG S,ZHENG D,ZHANG C,et al.Automatic planning on hippocampal avoidance whole ⁃brain radiotherapy[J].Med Dosim,2017,42(1):63⁃68.
[12] 李坊铭,林剑毅,程霞.局部中晚期喉癌术后调强放疗近期疗效[J].实用医学杂志,2017,33(9):1475⁃1478.
[13] 刘振,张军宁.单发脑转移性癌IMRT与3D⁃CRT剂量学对比分析[J].实用癌症杂志,2016(8):1345⁃1348.
[14] XU D,LI G,LI H.Comparison of IMRT versus 3D⁃CRT in the treatment of esophagus cancer:a systematicreviewandmeta⁃anal⁃ysis[J].Medicine,2017,96(31):e7685.
[15] FERRO M,CILLA S,MACCHIA G,et al.On the cutting edge of intensity modulated radiotherapy and simultaneous integrated boost(IMRT⁃SIB):The case of a patient with 8 brain metasta⁃ses[J].Rep Pract Oncol Radiother,2015,20(4):316⁃319.
[16] FRRRO M,CHIESA S,MACCHIA G,et al.Intensity modulat⁃ed radiation therapy with simultaneous integrated boost in pa⁃tients with brain oligometastases:a phase 1 study(ISIDE⁃BM⁃1)[J].Int J Radiat Oncol Biol Phys,2017,97(1):82⁃90.
[17] FENG C H,HASAN Y,KOPEC M.Simultaneously integrated boost(SIB)spares OAR and reduces treatment time in locally advanced cervical cancer[J].J Appl Clin Med Phys,2016,17(5):1⁃12.
[18] 陈冉,权循凤,陈香存.淋巴结阳性宫颈癌患者同步整合和序贯加量调强放疗的剂量学比较[J].安徽医学,2017,38(6):713⁃716.
[19] MIYAZAKI M,NISHIYAMA K,UEDA Y,et al.Preliminary analysis of the sequential simultaneous integrated boost tech⁃nique for intensity⁃modulated radiotherapy for head and neck cancers[J].J Radiat Res,2016,57(4):406⁃411.
[20] CIHORIC N,TAPIA C,KRUGERr K,et al.IMRT with18FDG⁃PETCT based simultaneous integrated boost for treatment of nodal positive cervical cancer[J].Radiat Oncol,2014,9:83.

