以甾醇为底物微生物法合成甾体类化合物的研究进展
金俊,卢梦瑶,厉秋岳,吴正章,张鹏,冯文欢,常明,金青哲,*
(1.江南大学食品学院,江苏省食品安全与质量控制协同创新中心,国家功能食品工程技术研究中心,江苏无锡214122;2.浙江省粮食科学研究所有限责任公司,浙江杭州310012;3.江苏科鼐生物制品有限公司,江苏泰兴225400)
甾体化合物是一类重要的生命物质,被Witzmann博士誉为“生命的钥匙”[1]。所有甾体化合物均由环戊烷多氢菲核(如图1所示)为母核衍生而来,其中A、B、C为六元环,D为五元环,在C3、C11、C17位上可接羟基或酮基,在C10、C13位上可接角甲基,在C17位上可接烃基,在A或B环上可有部分双键,这些官能团通过不同的组合进而衍生出各类甾体化合物[2]。甾体类化合物按用途主要分为甾体类药物和甾体类功能食品两大类:前者主要包括肾上腺皮质激素、性激素和蛋白同化激素等[3];后者具有代表性的即为甾醇酯。
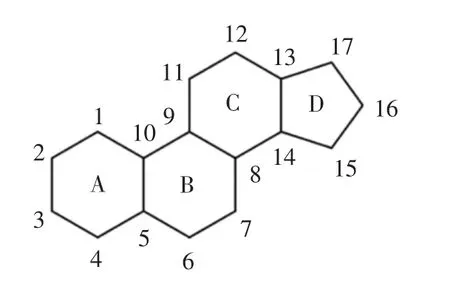
图1 甾体化合物的母核分子结构图Fig.1 The parent structure of steroids
传统上,制备甾体类化合物多采用溶剂提取法或化学合成法。溶剂提取法存在着步骤多、得率低和溶剂毒性等缺陷,以从夏风信子中制备C-27甾体皂苷为例,需要至少7步提取,用到甲醇、氯仿、乙腈等有机溶剂,而得率不足0.05‰[1]。化学合成法弥补了溶剂提取法得率过低的问题,在20世纪中前半叶广受关注,由我国著名化学家黄呜龙研发的薯蓣皂素为原料制备可的松的工艺,在当时不仅填补了我国甾体类药物生产的空白,且使我国在该领域一度处于世界领先地位。该法发展至今,我国甾体类药物中间体的出口量可达1 000 t/年,全球市场达100亿美元[4-5]。然而,化学合成法还是暴露出了步骤多、反应条件苛刻、污染严重、立体选择性差等诸多缺点。因此,具有特异性、环保理念的微生物合成法制备甾体类化合物逐渐进入科学界视眼。
早期的微生物合成法多以植物皂素为原料、以细胞色素P450酶为催化剂,其中植物皂素多为薯蓣皂素、剑麻皂素和番麻皂素等[6]。但自20世纪70年代以来,植物皂素的提取遇到了瓶颈[7-9]:1)薯蓣皂素的重要来源黄姜,不能保证连续产出,资源日渐枯竭;2)提取植物皂素过程中使用的酶、酸和有机溶剂会使排放的废水pH值、生物需氧量和化学需氧量等指标超标;3)提取残渣目前无法二次利用,经填埋处理具有污染地下水的潜在危险性。这些因素促使国内外一些公司开始寻找和开发新的甾体类药物原料。
随着食用油脂工业的发展,毛油经碱炼脱酸、蒸汽脱臭等处理后会产生大量富含甾醇的副产物。甾醇中以植物甾醇最为人所知,它同样以图1的母核为基本结构,且资源丰富,被认为是工业化制备甾体类化合物的理想原料。以米糠油为例,其碱炼后的皂渣(提取谷维素后的皂脚)中植物甾醇含量可达15%~20%,其中β-谷甾醇占62%~72%,而其通过4步生物转化即可制成强心苷元(一类用于治疗心力衰竭的甾体类药物)[1,10]。类似的研究发现,大豆油皂脚中含有毛油中约50%的植物甾醇,是制备五环三萜皂苷(可作为药物或甜味剂)的重要来源[11-12]。除了常见的植物甾醇外,动物胆固醇、真菌甾醇(以麦角甾醇为主)同样被视为珍贵的合成原料[1,13-14]。目前,研究工作主要集中在以甾醇为原料通过微生物法制备甾体类药物(或其中间体)和甾醇酯,但因甾醇和微生物种类繁多,寻求合适的原料以高效合成相应的甾体类化合物成为实现工业化的前提。本文综述了甾体类化合物的主要代表,分析了以甾醇为原料合成甾体类药物和甾醇酯的典型路径,以期为油脂加工副产物的高效利用提出新的途径。
1 以甾醇为原料合成甾体类药物
1.1 甾体类药物的应用
目前,甾体类药物多达400余种,为人熟知的有地塞米松、泼尼松、倍他米松、氢化可的松、黄体酮、睾丸酮及其衍生物等[15],在治疗皮炎、风湿关节炎、内分泌疾病和红斑狼疮等疾病方面有着举足轻重的作用。
1.2 甾体类药物微生物合成法的发展历程
在全球范围内,20世纪中后期处于甾体类药物微生物合成法研发的热潮之中。直至20世纪90年代,我国才认识到以甾醇为原料、以微生物为催化剂合成甾体类药物的迫切性和必要性。中国科学院以此立项,当时浙江省粮食科学研究所作为参加单位配合研发该课题,以米糠油皂脚中提纯的谷甾醇(纯度>90%)为原料进行微生物合成,但该课题未有圆满结果,当时的研发成果成了现时一些小企业生产出口植物甾醇的技术资源。
21世纪初,俄罗斯、中国、泰国等国科学家相继开发出利用分枝杆菌、海洋微生物等催化谷甾醇或混合植物甾醇合成甾体类药物中间体(4-雄烯二酮:4-androstene-3,17-dione,4AD 和 1,4-雄二烯二酮:androsta-1,4-diene-3,17-dione,ADD)的技术,并具备产业化前景[16-18]。目前,该技术已在国内药企投产,且部分企业正在开发以所制备中间体(4AD和ADD)为原料,进一步采用微生物合成甾体类药物的技术,并逐步完成了多种孕激素和糖皮质激素类甾体药物生产原料的切换[19]。
1.3 典型合成研究
以甾醇为原料(底物)、以微生物为催化剂合成甾体类药物这一路径,通常不能直接合成最终药物,而是先合成中间体4AD和ADD,它们的结构式如图2所示,通过中间体再进一步可合成几乎所有的已知甾体类药物。该法的主要过程包括:通过微生物将甾醇C3位的羟基氧化为酮基;再将C5位的双键引入C4位,同时降解C17位的侧链得到AD;在此基础上还原C1位引入双键得到ADD。相关研究主要以谷甾醇、麦角甾醇和混合植物甾醇为原料,见表1。
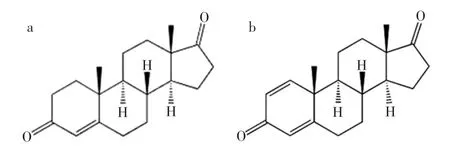
图2 4-雄烯二酮和1,4-雄二烯二酮Fig.2 The structures of 4-androstene-3,17-dione and androsta-1,4-diene-3,17-dione

表1 以甾醇为底物微生物法合成AD和ADD的主要研究Table 1 Microbial synthesis of AD and ADD using sterols
然而,目前通过AD或ADD合成最终药物的多为化学法[14],仅有少数药物可实现全工艺生物法合成。具有代表性的是:通过Mycobacterium sp.NRRL B-3805催化胆固醇合成睾丸酮[6];以谷甾醇为原料合成黄体酮[14];以羊毛甾醇为原料合成C-21甾体或强心苷元[1]。
此外,羽扇豆醇、α-和β-香树脂醇等普通植物油中不常见的甾醇,被发现是合成三萜类化合物的重要底物。例如,β-香树脂醇是合成甘草次酸、齐墩果酸、大豆皂醇、柴胡皂苷的原料;α-香树脂醇是合成熊果酸、乌索酸的原料;羽扇豆醇是合成桦木酸的原料[12,24-29]。
2 以甾醇为原料合成甾醇酯
2.1 甾醇酯的主要应用
甾醇酯被人所认知是从它的降胆固醇功能开始的,随后人们发现它具有降低心血管发病率、抗炎、抗癌等一系列功效,因而开始大力开发这一资源[30]。甾醇酯的使用历史晚于甾体类药物,且其主要被应用于食品和保健品领域。1999年,日本农林省批准甾醇/甾烷醇酯为保健食品FOSHU的添加剂;2000年,美国食品药品监督管理局发布公告称从膳食中摄入甾醇/甾烷醇酯可降低胆固醇;2004年,欧盟委员会批准甾醇酯可以作为黄油涂酱、奶制品的原料;2010年,我国卫生部发布第3号公告批准植物甾醇酯作为新资源食品,对于含量90%的植物甾醇酯建议每日食用量不高于3.9 g(婴幼儿除外)[31]。目前,主要将甾醇酯作为抗氧化剂、乳化剂等应用于食品和保健品之中,以提高该类产品的氧化稳定性和营养功能[32]。
甾醇酯可通过结晶、蒸馏等技术从油脂加工副产物中提取[33],例如可从谷物油脂(米糠油、玉米胚芽油等)的皂脚、脱臭馏出物中提取谷甾醇阿魏酸酯、菜油甾醇阿魏酸酯、24-亚甲基环木菠萝醇阿魏酸酯、环木菠萝醇阿魏酸酯等,其中后两者是谷维素(米糠油的特征营养物质)的主要成分[10,34-35]。然而通过提纯这些天然甾醇酯的产量远远不能满足需求,因而对于甾醇酯合成技术的开发成了目前的研究热点。
2.2 典型合成研究
20世纪70年代,已开发出采用甾醇酰基转移酶催化混合植物甾醇制取甾醇酯的技术[36]。由于微生物法的反应底物基本为从油脂加工副产物中提炼的混合植物甾醇,因此一直以来将研发重点放在酶的改进和脂肪酸的选择上,相关研究见表2。

表2 以甾醇为底物微生物法合成甾醇酯的典型研究Table 2 Microbial synthesis of sterol esters using sterols
然而混合植物甾醇中各单体往往具有各自最适的反应条件,这也限制了甾醇酯的高效合成,故以单一甾醇为原料的合成技术开始受到学者青睐。近年来,随着甾醇单体分离技术的提高,部分单体如β-谷甾醇已经实现工业化生产,相应谷甾醇酯的合成技术也得到不断发展。
然而,甾醇酯的微生物合成最大瓶颈在于酶的高效利用,而这又与酶的存在形式和反应体系息息相关,因此最新研究集中在采用固定化酶,或选择离子液体、超临界流体等新体系[44-45]。
3 结论
甾体类化合物在食品、保健品和药品领域有着举足轻重的作用,按用途主要分为甾体类药物和甾体类功能食品。其中甾体类药物已是仅次于抗生素的第二大类用药;而甾体类功能食品以甾醇酯为代表,近年来在食品、保健品领域颇受关注。传统合成甾体类化合物的方法因存在步骤繁多、污染严重、条件苛刻等问题,逐渐被环保、具特异性的微生物法所取代。合成原料也从日益紧缺的植物皂素资源转为产量丰富的油脂加工副产物甾醇。目前,以甾醇为底物用微生物法合成甾体类药物一般只能合成至中间体AD和ADD,合成最终产物的技术还有待突破;而合成甾醇酯则亟需培育针对不同甾醇(或甾醇混合物)的微生物及选择相应的反应体系,这是实现工业化的前提。
[1]高锦明.植物化学 (第二版)[M].北京:科学出版社,2012:254-285
[2]王敬文.混菌发酵植物甾醇制备11α-OH-ADD的研究[D].上海:上海应用技术大学,2016
[3]张磊.微生物转化法生产雄烯二酮工艺条件优化[D].开封:河南大学,2016
[4]Schmid A,Dordick JS,Hauer B,et al.Industrial biocatalysis today and tomorrow[J].Nature,2001,409(6817):258
[5]Rolf D.Schmid RD,Urlacher VB.Modern Biooxidation:Enzymes,Reactions and Applications[M].Germany:Wiley,2007:155-176
[6]刘夺,张莹,周晓,等.合成生物技术生产甾体激素中间体的研究展望[J].生命科学,2013,25(10):958-965
[7]王庆宇,金凤燮,鱼红闪.薯蓣皂苷元制备方法的研究进展[J].安徽农业科学,2011,39(5):2642-2644
[8]杨磊,肖长文,祖元刚.植物提取物生产过程中废水的治理[J].森林工程,2008,24(4):44-47
[9]孙欣,邓良伟,吴力斌.皂素生产废水污染特点及治理现状[J].中国沼气,2005,23(1):25-2
[10]王瑞元.植物油料加工产业学(下册)[M].北京:化学工业出版社,2009:24-42
[11]吴慧斌.沼液中活性成分的分析及萜类转化机制探究[D].上海:上海海洋大学,2015
[12]张强,李大帅,卢文玉.大肠杆菌异源合成三萜化合物研究进展和前景分析[J].中国生物工程杂志,2016,36(11):83-89
[13]Jin J,Sheraliev G,Xie D,et al.Characteristics of specialty natural micronutrients in certain oilseeds and oils:plastochromanol-8,resveratrol,5-hydroxytryptamine phenylpropanoid amides,lanosterol,ergosterol and cyclolinopeptides[J].Journal of the American Oil Chemists Society,2016,93(2):155-170
[14]王志龙.甾醇侧链切除的微生物转化技术[J].工业微生物,2006,36(3):49-54
[15]Tong WY,Dong X.Microbial biotransformation:recent developments on steroid drugs[J].Recent Patents on Biotechnology,2009,3(2):141-153
[16]Sukhodolskaya GV,Nikolayeva VM,Khomutov SM,et al.Steroid-1-dehydrogenase of Mycobacterium sp.VKM Ac-1817D strain producing 9alpha-hydroxy-androst-4-ene-3,17-dione from sitosterol[J].Applied Microbiology&Biotechnology,2007,74(4):867-73
[17]Saraphanchotiwitthaya A,Sripalakit P.Production of 4-androstene-3,17-dione and 1,4-androstadiene-3,17-dione from rice germ and wheat germ extracts by Mycobacterium sp.[J].Biotechnology Letters,2016,38(9):1-8
[18]周峰.海洋微生物转化2种甾体类化合物的研究[D].杭州:浙江工业大学,2015
[19]中国产业信息.2017年我国甾体药物行业市场现状及发展趋势分析[EB/OL].(2016-12-16)[2017-12-22]http://www.chyxx.com/industry/201612/478199.html
[20]Lee CY,Liu WH.Production of androsta-1,4-diene-3,17-dione from cholesterol using immobilized growing cells of Mycobacterium sp.NRRL B-3683 adsorbed on solid carriers[J].Applied Microbiology&Biotechnology,1992,36(5):598-603
[21]Mahato SB,Mukheiliee A.Steroid transformation by microorganisms[J].Phytochemistry,1984,23:2131-2154
[22]Mahato SB,Garai S.Advances in microbial steroid biotransformation[J].Steroids,1997,62(4):332-345
[23]杨英.微生物转化植物甾醇制备甾体药物关键中间体研究[D].合肥:合肥工业大学,2009
[24]Moses T,Thevelein J M,Goossens A,et al.Comparative analysis of CYP93E proteins for improved microbial synthesis of plant triterpenoids[J].Phytochemistry,2014,108:47-56
[25]Dai Z,Wang B,Liu Y,et al.Producing aglycons of ginsenosides in bakers'yeast[J].Scientific Reports,2014,4(4):doi:10.10.38/srep 03698
[26]Seki H,Sawai S,Ohyama K,et al.Triterpene functional genomics in licorice for identification of CYP72A154 involved in the biosynthesis of glycyrrhizin[J].Plant Cell,2011,23(11):4112-4123
[27]Seki H,Ohyama K,Sawai S,et al.Licorice β-amyrin 11-oxidase,a cytochrome P450 with a key role in the biosynthesis of the triterpene sweetener glycyrrhizin[J].Proceedings of the National Academy of Sciences of the United States of America,2008,105(37):14204-14209
[28]Yu F,Thamm AMK,Reed D,et al.Functional characterization of amyrin synthase involved in ursolic acid biosynthesis in Catharanthus roseus,leaf epidermis[J].Phytochemistry,2013,91(4):122-127
[29]Fukushima EO,Seki H,Ohyama K,et al.CYP716A subfamily mem bers are multifunctional oxidases in triterpenoid biosynthesis[J].Plant&Cell Physiology,2011,52(12):2050-2061
[30]金青哲.功能性脂质[M].北京:中国轻工业出版社,2013:43-45
[31]刘虹蕾,缪铭,江波,等.植物甾醇酯的研究与分析[J].食品工业科技,2012,33(4):434-437
[32]翟鹏贵,彭启辉,姚晖.新资源食品原料植物甾醇和植物甾醇酯的安全与应用[J].中国卫生监督杂志,2011,18(1):51-55
[33]姜绍通,邵平,潘丽军,等.植物油脱臭馏出物中维生素E、甾醇及甾醇酯分离新工艺:CN1693472[P].2005-11-9
[34]Moreau RA,Singh V.Phytosterols in the aleurone layer of corn kernels[J].Biochemical Society Transactions,2000,28(6):803-806
[35]陆柏益,杨佳佳,熊丽娜.甾醇阿魏酸酯的功能、制备及检测方法研究进展[J].现代食品科技,2013,29(12):3063-3069
[36]Bartlett K,Keat MJ,Mercer EI.Biosynthesis of sterol esters in Phycomyces blakesleeanus[J].Phytochemistry,1974,13(7):1107-1113
[37]Shimada Y,Hirota Y,Baba T,et al.Enzymatic synthesis of steryl esters of polyunsaturated fatty acids[J].Journal of the American Oil Chemists Society,1999,76(6):713-716
[38]King JW,Snyder JM,Frykman H,et al.Sterol ester production using lipase-catalyzed reactions in supercritical carbon dioxide[J].European Food Research&Technology,2001,212(5):566-569
[39]胡小加.无溶剂系统中固定化细胞酶催化生产植物甾醇酯的方法:200710168653.0[P].2008-6-18
[40]王殿宇.一种固定化脂质酰基转移酶制备植物甾醇酯的方法:CN104561215[P].2015-4-29
[41]么婷婷,辛嘉英,王艳,等.植物甾醇酯的酶法合成[J].化学工程师,2016,30(9):4-9
[42]Panpipat W,Xu X,Guo Z.Improved acylation of phytosterols catalyzed by Candida antarctica,lipase A with superior catalytic activity[J].Biochemical Engineering Journal,2013,70(2):55-62
[43]Lanctôt AG,Attard TM,Sherwood J,et al.Synthesis of cholesterolreducing sterol esters by enzymatic catalysis in bio-based solvents or solvent-free[J].RSC Advances,2016,6(54):48753-48756
[44]董玲,郑明明,郭萍梅,等.酶法合成植物甾醇酯工艺的研究进展[J].中国油脂,2012,37(6):58-62
[45]于殿宇,王腾宇,陈昊,等.生物酶法合成植物甾醇酯的研究[J].食品工业科技,2011,32(6):318-319

