镇癫开窍颗粒定性定量方法研究
张瑞堂 金永新 张红梅 马肖 何彩虹 田新华 吴玉琼

摘要:目的 建立镇癫开窍颗粒的定性定量方法。方法 采用薄层色谱法鉴别制剂中的龙胆、黄芩、大黄、白芍。采用HPLC对制剂中的龙胆苦苷、芍药苷进行含量测定,色谱柱为Phenomenex C18柱(250 mm×4.6 mm,5 μm),流动相为甲醇-水(12∶88),流速为1.0 mL/min,检测波长为273 nm(龙胆苦苷)、230 nm(芍药苷),柱温为室温。结果 薄层色谱能检出龙胆、黄芩、大黄、白芍。龙胆苦苷在2.396~11.980 ?g范围内呈良好的线性关系(r=0.999 6),平均加样回收率为99.72%(RSD=2.70%);芍药苷在2.728~13.640 ?g范围内呈良好的线性关系(r=0.999 0),平均加样回收率为98.74%(RSD=2.42%)。结论 本研究所建立的方法简便、可靠、重复性好,可用于控制镇癫开窍颗粒的质量。
关键词:镇癫开窍颗粒;龙胆苦苷;芍药苷;龙胆;薄层色谱法;高效液相色谱法
DOI:10.3969/j.issn.1005-5304.2018.04.016
中图分类号:R284.1 文献标识码:A 文章编号:1005-5304(2018)04-0077-05
Abstract: Objective To establish a method for qualitative and quantitative analysis of Zhendian Kaiqiao Granules. Methods Gentiane Radix et Rhizoma, Scuteliariae Radix, Rhei Radix et Rhizoma, Radices Paeoniae Alba in the preparation were identified by TLC. Gentiopicrin and paeoniflorin were determined by HPLC. The analysis was performed on a Phenomenex C18 column (250 mm × 4.6 mm, 5 μm), with the mobile phase of methyl alcohol-water (12:88). The flow rate was 1.0 mL/min and the column temperature was maintained at room temperature; the detection wavelengths were set at 273 nm (gentiopicrin) and 230 nm (paeoniflorin). Results Gentiane Radix et Rhizoma, Scuteliariae Radix, Rhei Radix et Rhizoma, Radices Paeoniae Alba could be detected by TLC. Gentiopicrin showed a good linear relationship at a range of 2.396–11.980 ?g, r=0.999 6. The average recovery was 99.72%, and RSD was 2.70%. Paeoniflorin showed a good linear relationship at a range of 2.728–13.640 ?g, r=0.999 0. The average recovery was 98.74%, and RSD was 2.42%. Conclusion The established method is simple, reliable and reproductive. The method can be used for control quality of Zhendian Kaiqiao Granules.
Keywords: Zhendian Kaiqiao Granules; gentiopicrin; paeoniflorin; Gentiane Radix et Rhizoma; TLC identification; HPLC
镇癫开窍颗粒处方来源于甘肃省第二人民医院(甘肃省精神卫生中心)中医科,为该院经验方,经多年临床使用效果明确、毒副作用小。为使患者携带方便,拟开发为医院院內制剂。该制剂由龙胆、黄芩、白芍、大黄、石膏、生地黄、酸枣仁、龙骨、牡蛎、珍珠母、石决明、琥珀、细辛、茯苓、甘草共15味药组成,具有泄肝潜镇、清泄阳明功效,用于治疗癫狂症。为了控制镇癫开窍颗粒的质量,本研究采用薄层色谱方法对制剂中的龙胆、白芍、黄芩、大黄进行定性鉴别,采用HPLC对制剂中的龙胆苦苷、芍药苷进行含量测定,为将镇癫开窍颗粒开发成安全、有效、价廉的医院院内制剂提供依据。
1 仪器与试药
Agilent1120型高效液相色谱仪(二极管阵列检测器,美国安捷伦公司),WFH-203三用紫外分析仪(上海精科实业有限公司),ALC-210.4型万分之一电子天平(德国赛多利斯公司),JY2002型百分之一电子分析天平(上海精密科学仪器有限公司),RE52CS型旋转蒸发仪(上海亚荣生化仪器厂),SHZ-D(Ⅲ)型循环水式真空泵(天津华鑫仪器厂),B1210E-MT型超声波仪(美国Branson公司,功率80 W,频率50~60 Hz),HH-S26S数显恒温水浴锅(金坛市大地自动化仪器厂)。
龙胆苦苷对照品(含量以97.9%计,批号110736-200731,供含量测定用)、芍药苷对照品(批号110736-201438,供含量测定用)、黄芩苷对照品(批号120955-201309,供含量测定用)、大黄素对照品(批号120984-201202,供含量测定用)、龙胆对照药材(批号121530-200501,供鉴别用)、黄芩对照药材(批号200715-199809,供鉴别用)、大黄对照药材(批号110756-200110,供鉴别用)、白芍对照药材(批号120905-201109,供鉴别用),中国食品药品检定研究院;镇癫开窍颗粒3批(批号分别为20160313、20160315、20160317)、龙胆阴性对照颗粒、黄芩阴性对照颗粒、大黄阴性对照颗粒、白芍阴性对照颗粒,甘肃省第二人民医院药剂科制剂室自制;硅胶G薄层板(批号20140108),青岛海洋化工厂分厂;硅胶GF254薄层板(批号20151013),青岛鼎康硅胶有限公司;甲醇为色谱纯,水为纯化水,其他试剂均为分析纯。
2 方法与结果
2.1 定性分析
2.1.1 龙胆的鉴别
取本品颗粒适量,研细后称取10 g,加甲醇20 mL,超声处理(功率80 W,頻率50~60 Hz)20 min,过滤,滤液于60 ℃水浴蒸干,残渣加甲醇1 mL溶解,作为供试品溶液[1]。称取龙胆苦苷对照品适量,加甲醇制成浓度约为1 mg/mL的对照品溶液[2]。分别取龙胆对照药材约0.3 g、龙胆阴性对照颗粒10 g,按供试品溶液制备方法制得龙胆对照药材溶液和龙胆阴性对照溶液。照薄层法色谱法试验(2015年版《中华人民共和国药典》四部通则0502),吸取供试品溶液、对照品溶液、龙胆对照药材溶液、龙胆阴性对照溶液各10 μL,分别点于同一硅胶GF254薄层板上,以乙酸乙酯-甲醇-水(10∶2∶1)为展开剂,展开,取出,晾干后置紫外灯(254 nm)下检视[3]。在供试品色谱中与对照品、对照药材色谱相应位置显相同颜色斑点,在阴性对照色谱中无相同颜色的斑点,阴性对照无干扰。
2.1.2 黄芩的鉴别
取本品颗粒适量,研细后称取10 g,加乙酸乙酯30 mL、甲醇10 mL,混匀,超声处理(功率80 W,频率50~60 Hz)30 min,过滤,滤液于60 ℃水浴蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液[3]。称取黄芩苷对照品适量,加甲醇制成浓度约为1 mg/mL的对照品溶液。分别称取黄芩对照药材约0.3 g、黄芩阴性对照颗粒10 g,按供试品溶液制备方法制得黄芩对照药材溶液和黄芩阴性对照溶液。照薄层法色谱法试验(2015年版《中华人民共和国药典》四部通则0502),吸取供试品溶液、对照品溶液、黄芩对照药材溶液、黄芩阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-丁酮-甲酸-水(6∶3∶1∶1)为展开剂,展开,取出,晾干,喷以5%三氯化铁乙醇溶液,在105 ℃加热至斑点显色清晰[4-6]。在供试品色谱中与对照品、对照药材色谱相应位置显相同颜色斑点,在阴性对照色谱中无相同颜色的斑点,阴性对照无干扰。
2.1.3 大黄的鉴别
取本品颗粒适量,研细后称取10 g,加乙醚20 mL,超声处理(功率80 W,频率50~60 Hz)20 min,过滤,滤液30 ℃水浴蒸干,残渣加乙醇1 mL使溶解,作为供试品溶液[6-7]。称取大黄素对照品适量,加甲醇制成浓度约为1 mg/mL的对照品溶液。分别称取大黄对照药材约0.3 g、大黄阴性对照颗粒10 g,按供试品溶液制备方法制得大黄对照药材溶液和大黄阴性对照溶液。照薄层法色谱法试验(2015年版《中华人民共和国药典》四部通则0502),吸取供试品溶液、对照品溶液、大黄对照药材溶液、大黄阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以正己烷-乙酸乙酯-冰乙酸(10∶2∶0.1)为展开剂,展开,取出,晾干后置紫外灯(365 nm)下检视[8-9]。在供试品色谱中与对照品、对照药材色谱相应位置显相同颜色斑点,在阴性对照色谱中无相同颜色的斑点,阴性对照无干扰。
2.1.4 白芍的鉴别
取本品颗粒适量,研细后称取10 g,加50 mL水溶解,用水饱和的正丁醇液50 mL萃取2次,合并正丁醇萃取液,用氨试液洗涤2次,每次15 mL,合并正丁醇液,水浴蒸干,残渣加甲醇1 mL溶解,甲醇溶解液作为供试品溶液[10]。称取芍药苷对照品适量,加甲醇制成浓度约为1 mg/mL的对照品溶液。分别称取白芍对照药材约0.3 g、白芍阴性对照颗粒10 g,按供试品溶液制备方法制成白芍对照药材溶液和白芍阴性对照溶液。照薄层色谱法试验(2015年版《中华人民共和国药典》四部通则0502),吸取供试样品溶液、对照品溶液、白芍对照药材溶液、白芍阴性对照溶液各10 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶20∶0.2)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,在105 ℃加热至斑点显色清晰[11-15]。在供试品色谱中与对照品、对照药材色谱相应位置显相同颜色斑点,在阴性对照色谱中无相同颜色的斑点,阴性对照无干扰。
2.2 定量分析
2.2.1 色谱条件
采用Phenomenex C18色谱柱(250 mm×4.6mm,5 μm),预柱为Shimadzu Shim-pack C18柱(10 mm×4.6 mm),流动相为甲醇-水(12∶88),流速为1 mL/min,龙胆苦苷检测波长为273 nm,芍药苷检测波长为230 nm,柱温为室温,进样量为20 μL。
2.2.2 对照品混合溶液的制备
分别精密称取减压干燥至恒重的龙胆苦苷对照品(含量以97.9%计算)6.12 mg、芍药苷对照品6.82 mg,置10 mL棕色容量瓶中,用流动相比例的甲醇水混合液溶解并定容至刻度,即配制成龙胆苦苷、芍药苷浓度分别为0.599、0.682 mg/mL的混合对照品溶液。
2.2.3 供试品溶液的制备
取样品适量,研细,精密称取粉末约10 g,置具塞锥形瓶中,加甲醇20 mL,超声提取(功率80 W,频率50~60 Hz)30 min,过滤,滤液用甲醇定容至100 mL容量瓶中。精密吸取定容溶液10 mL,蒸干,残渣用10 mL水溶解,定量转移至25 mL分液漏斗中,加入水饱和的正丁醇萃取3次,每次5 mL,合并正丁醇液,置水浴上蒸干,残渣用流动相比例的甲醇水混合液溶解,并定容至5 mL棕色容量瓶中,0.45 μm滤膜过滤,取续滤液,作为供试品溶液[16]。
2.2.4 阴性对照溶液的制备
精密称取龙胆阴性对照颗粒、白芍阴性对照颗粒各10 g,混匀,按“2.2.3”项下方法制备,即得阴性对照溶液。
2.2.5 专属性试验
吸取混合对照品溶液、供试品溶液及阴性对照溶液各20 μL,注入高效液相色谱仪,按“2.2.1”项下色谱条件分析,记录色谱图(见图2)。结果表明供试品溶液分别在273、230 nm色谱图中,有与对照品龙胆苦苷、芍药苷保留时间一致的特征峰,保留时间分别为7.5、9.1 min,阴性对照溶液色谱图中无相应特征的吸收峰,表明处方中其他成分对被测成分无干扰,方法专属性较好。各成分分离度均大于2.0,理论塔板数以龙胆苦苷、芍药苷计算均不低于3000。
2.2.6 线性关系考察
分别精密吸取对照品溶液200、400、500、600、700、800、900、1000 ?L,用流动相比例的甲醇水混合液定容至1 mL容量瓶,依次吸取上述溶液各20 ?L,按“2.2.1”项下色谱条件进行分析。以峰面积为横坐标,浓度为纵坐标,绘制标准曲线,得回归方程:龙胆苦苷Y=3.5×10-6X+0.021 2,r=0.999 6;芍药苷Y=1.0×10-6X+2.768 7,r=0.999 0。结果表明,龙胆苦苷和芍药苷分别在2.396~11.980 ?g和2.728~13.640 ?g范围内具有良好的线性关系。
2.2.7 精密度试验
精密吸取同一份供试品溶液20 ?L,重复进样5次,按“2.2.1”项下色谱条件测定,测得龙胆苦苷、芍药苷含量RSD分别为2.09%、2.18%。结果表明仪器的精密度良好。
2.2.8 稳定性试验
分别精密吸取同一份供试品溶液20 ?L,于0、2、4、6、8、10、12、24、36、48 h注入高效液相色谱仪,按“2.2.1”项下色谱条件测定,测得龙胆苦苷、芍药苷含量RSD分别为2.56%、2.42%。结果表明供试品溶液在48 h内稳定性较好。
2.2.9 重复性试验
分别精密称取同一批号样品(批号20160313)6份,分别按“2.2.3”项下方法制备供试品溶液,按“2.2.1”项下色谱条件测定,龙胆苦苷、芍药苷的平均含量分别为3.50、4.20 mg/g,RSD分别为2.42%、2.10%。结果表明本方法的重复性好。
2.2.10 加样回收率试验
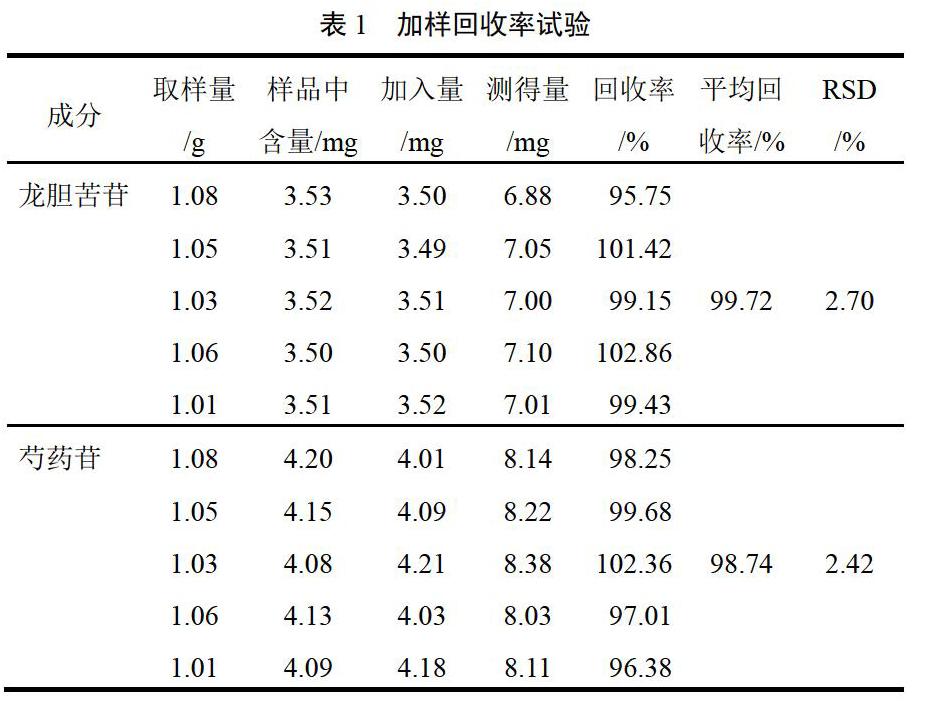
取已知含量的样品(批号20160313)1 g,共5份,精密称定,精密加入一定量的龙胆苦苷、芍药苷对照品,按“2.2.3”项下方法制备并按上述色谱条件进行测定,结果见表1。符合定量分析要求。
2.2.11 样品含量测定
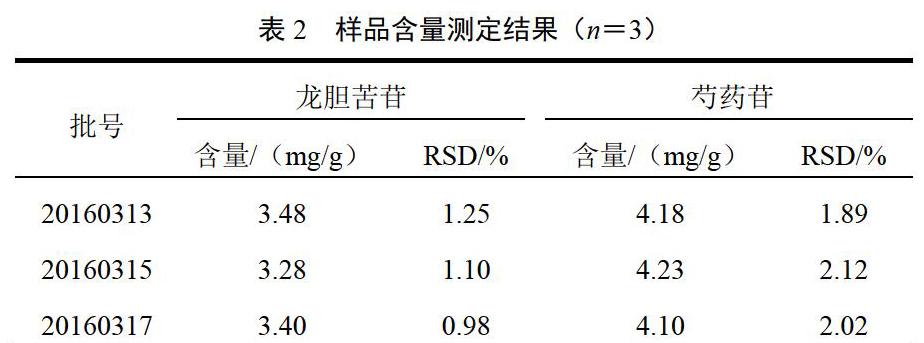
取3批样品,各3份,精密称定,按“2.2.3”项下方法制备供试品溶液,并按“2.2.1”项下色谱条件测定,计算龙胆苦苷、芍药苷含量,结果见表2。3批样品中龙胆苦苷的含量均高于3.0 mg/g,芍药苷的含量均高于4.0 mg/g。本品含龙胆以龙胆苦苷含量的90%计不低于2.7 mg/g,含白芍以芍药苷含量的90%计不低于3.6 mg/g。
3 讨论
黄芩的薄层鉴别曾使用2015年版《中华人民共和国药典》(一部)黄芩项下薄层鉴别的展开剂,供试品溶液斑点分离效果不佳,后采用“2.1.2”项下展开剂,并用5%三氯化铁乙醇溶液显色,较紫外光灯(365 nm)下观察斑点更加清晰,分离效果好。
大黄的薄层鉴别曾使用2015年版《中华人民共和国药典》(一部)大黄项下薄层鉴别的展开剂和以羧甲基纤维素钠为粘合剂的硅胶H薄层板,但供试品溶液色谱中斑点有拖尾现象,后采用“2.1.3”项下展开剂和硅胶G板,置紫外光灯(365 nm)下观察,分离效果好。
白芍鉴别所用的芍药苷对照品溶液应新鲜配制,若放置时间过长,芍药苷对照品薄层色谱会出现2个斑点,这可能与芍药苷在乙醇溶液中不稳定易分解有关。白芍的薄层鉴别曾使用2015年版《中华人民共和国药典》(一部)白芍项下薄层鉴别的提取方法和展开剂,供试品溶液无与对照品相对应的斑点,后用“2.1.4”项下样品处理方法和展开剂,5%香草醛硫酸溶液显色剂显色后斑点清晰,可用于白芍的鉴别。白芍薄层鉴别色谱图中,白芍对照药材色谱由下至上的第一个斑点与阴性对照色谱相对应的位置有相同颜色的斑点,但其主要成分芍药苷与芍药苷对照品色谱在同一位置显相同颜色的斑点,阴性对照在此位置无干扰,故该方法可用于本制剂中白芍的鉴别。
龙胆苦苷、芍药苷含量测定中,我们曾考察了甲醇-水(23∶77)[17]、乙腈-水[18]、乙腈-水-醋酸(10∶80∶1)[19]、乙腈-0.05%磷酸[20-21]的流动相,结果表明,用甲醇-水(12∶88)为流动相时,分离度、峰形均达到比较理想的效果。
本研究对镇癫开窍颗粒中的龙胆、白芍、黄芩、大黄进行了薄层色谱鉴别,并建立了HPLC同时测定龙胆苦苷、芍药苷含量的方法。方法简便、可控,可作为镇癫开窍颗粒质量控制方法。
参考文献:
[1] 吴立宏,官海峰,俞丽,等.红花龙胆质量标准研究[J].中国中药杂志, 2010,35(16):2099-2102.
[2] 赵顺,孙辉,丁野,等.龙胆泻肝丸(大蜜丸)薄层色谱鉴别方法的建立[J].中国药师,2015,18(1):151-153.
[3] 國家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2015:96.
[4] 胡颖菲,陆兔林,毛春芹,等.大柴胡颗粒质量标准研究[J].中成药, 2013,35(1):68-73.
[5] 林绿萍.通窍耳聋丸的质量标准研究[D].广州:广州中医药大学, 2012.
[6] 宋冬梅,顾承刚,吴宁,等.炎可宁片质量标准的建立[J].中国药师, 2011,14(4):569-570.
[7] 舒翔,陈军,林世和,等.止痒洗剂的质量控制[J].中国医院药学杂志, 2012,32(15):1189-1191.
[8] 龚敏阳,伍小燕,莫小林.大黄灌肠液的薄层色谱鉴别方法及土大黄苷的限量检查方法[J].北方药学,2013,10(4):9.
[9] 方文清.三黄清热胶囊质量标准的研究[J].中国医药科学,2012, 2(23):98-100.
[10] 胡丹,刘艳,曹红,等.夏凌养阴颗粒质量控制的研究[J].解放军药学学报,2011,27(1):37-39.
[11] 李艳,胡红艳,黄秋明.白术护肝合剂中当归、白术、芍药的薄层色谱鉴别[J].中醫学报,2012,27(3):343-344.
[12] 沈洁,任世禾.复方银杏叶胶囊质量标准的研究[J].上海中医药杂志, 2007,41(6):79-81.
[13] 孟君,龚云,丁野.妇科调经片质量标准研究[J].中成药,2004,26(7):541-544.
[14] 金永新,郜丽华,顾雪艳,等.反流安无糖型混悬颗粒不同制备工艺制剂质量研究[J].中国中医药信息杂志,2014,21(5):86-90.
[15] 杨怀武,王碧辉,阎玉珍.维血宁颗粒(无糖型)的质量标准[J].中国药师,2010,13(10):1528-1529.
[16] 张瑞堂,石晓峰,张红梅.复方红景天口含片提取工艺优选[J].中国实验方剂学杂志,2011,17(13):42-45.
[17] 刘瑞新.HPLC同时测定龙胆泻肝丸中龙胆苦苷和栀子苷的含量[J].中成药,2007,29(8):1170-1172.
[18] 袁月华,张松青.HPLC法测定栝楼桂枝颗粒中芍药苷含量[J].海峡药学,2013,25(10):89-92.
[19] 魏岚,陈晓辉,王晓辉,等.不同产地龙胆中龙胆苦苷的含量测定[J].沈阳药科大学学报,2004,21(2):114-117.
[20] 马旭伟,韦辉,刘素香,等.HPC法测定强肝胶囊中龙胆苦苷、芍药苷、丹酚酸B[J].中草药,2012,43(6):1125-1128.
[21] 丁文雅,张婷婷,王强.7种龙胆科蒙药药材中龙胆苦苷的含量测定[J].中国药科大学学报,2008,39(1):52-54.
(收稿日期:2017-08-17)
(修回日期:2017-09-14;编辑:陈静)

