荧光增白剂5BM的毒理学数据及其使用安全性(二)
董仲生
(沈阳化工研究院,辽宁沈阳,110021)

(上接第6期第52页)
4. 4 急性吸入毒性
IBT实验室在1971年用FWA 5BM(Ciba-Geigy公司提供)对白化大鼠(5只/性别/组,平均体重290g)进行了一项非- GLP的吸入毒性研究。
实验物质FWA 5BM由高速、清洁、干燥的气流输送。产生的混合物被引入到顶部的有机玻璃接触室(容量70L),通过一个隔板被分散和在底部排出。接触室中FWA 5BM粉尘的浓度通过在动物吸入区域环境的取样进行测定。10只白化大鼠暴露于2.9mg/L FWA 5BM的粉尘中4h,在室内空气中直径为2~5、2~25和大于25mm的颗粒百分数分别为31%、59%和10%[4]。
结果:暴露1~4h,动物普遍表现出不活泼。在之后14天的暴露期动物表现健康和体重增加正常,没有动物死亡。在暴露14天后的全身尸检显示,2只动物的肺发生轻微实变,3只大鼠(性别不详)的肺发生轻微充血,结果LC50>2.9mg/L[5]。
4.5 急性皮肤毒性
(1) Ciba-Geigy公司1974年进行的一项研究报道,FWA 5BM对兔子的经皮LD50值为>2000mg/kg bw[3]。
根据OECD指南402(急性皮肤毒性),Wistar大鼠(5只/性别)在半-封闭的条件下以2000mg/kg bw剂量经皮肤途径暴露于FWA 5BM下24h,然后跟踪给药观察15天。结果没有观察到死亡,其LD50>2000 mg / kg bw[5]。
(2) 1975年毒理学家按照美国食品和药品官员协会(AFDO)的 食品、药品和化妆品中化学品的安全评价(1959)中斑贴技术规程对兔子皮肤的刺激、腐蚀进行了评估[1]。
用俄罗斯兔子(雌性、雄性各3只,体重1.5~2kg),FWA 5BM用量为0.5g,把有FWA 5BM的纱布斑贴2.5cm×2.5cm施用于已备好的有擦伤和无擦伤刮毛的皮肤处,暴露24h后移除纱布。观察3天。同时进行对照实验。
对皮肤刺激立即进行评分和在除去纱布斑贴48h后评分(在实验开始后的24和72h)。
皮肤刺激(包括红斑和焦痂形成以及浮肿形成)的严重性评价标准为:刺激指数平均值小于2表示轻微刺激,2~5表示中等刺激,大于6表示皮肤刺激严重。
结果:本实验的主要刺激指数被评估1.5,因此实验物质FWA 5BM对兔子皮肤造成的刺激为轻微刺激。
上述实验中皮肤反应强度的评分标准与OECD指南中的报道相同。根据CLP法规(欧盟物质和混合物的分类、标签和包装法规)(EC 1272/2008)把FWA 5BM归类为:无皮肤刺激性物质[1]。
(3) 另外,在1975年和1976年,毒理学家按照AFDO的 食品、药品和化妆品中化学品的安全评价”(1959)中斑贴技术规程对兔子皮肤的刺激、腐蚀还分别进行了两项和一项类似的评估实验[1]。
结果:原发刺激指数被分别评估为1.2、0.6(1975年)和1.2(1976年),为轻微刺激。
根据CLP法规(EC 1272/2008)把FWA 5BM归类为:无皮肤刺激性物质。
4.6 眼睛刺激
(1) 1975年毒理学家按照AFDO的 食品、药品和化妆品中化学品的安全评价”(1959)中的规程对兔子眼睛的刺激进行了评估[1]。
眼睛刺激的评级标准为:眼刺激指数0~10:极小;11~25:轻微;26~56:中等;57~84:显著;高于84:极大。
用俄罗斯兔子(雌、雄性各3只,体重1.5~2kg),FWA 5BM用量为0.1g,被放入兔子左眼的结膜囊中,眼睑轻轻地闭合1s,右眼不做处理用于对照。3只兔子的眼睛在施药处理30s后,用10mL温水清洗眼睛。观察时间为7天。
在第1、2、3、4和7天对刺激进行评价,并对每只兔子进行评分。
结果:眼刺激指数被评估为角膜2.8,虹膜0,结膜为2.7;极小的刺激。
讨论和结论:
尽管在AFDO和OECD之间的物质去除时间明显不同(该实验中为30s,OECD中为1h),但结果清晰地表明:来自于24、48和72h的清洗与未清洗所有动物眼睛两者等级的平均值对于角膜的透明度低于1,对于虹膜也低于1,对于两者的结膜红色和水肿低于2。
因此,依据CLP法规,该物质被分类为无刺激。
(2) 另外在1976年几位毒理学家按照AFDO的 食品、药品和化妆品中化学品的安全评价(1959)中的规程对兔子眼睛的刺激进行了3项评估实验[1]。
刺激/腐蚀的相应数据如下:
1976年第一项实验结果:眼刺激指数被评估为角膜0,虹膜0,结膜为1。FWA 5BM对兔子眼睛造成最小的刺激。冲洗的影响(未冲洗的/冲洗的眼睛)被评估为0.4。
1976年第二项实验结果:眼刺激指数被确定为角膜1.4,虹膜0,结膜为2.1;最小的(极微的)刺激。
1976年第三项实验结果:眼刺激指数被确定为角膜0,虹膜0,结膜为0;无刺激。
因此,依据CLP法规,该物质被分类为无刺激。
4.7 皮肤刺激/致敏
(1) 在1965年进行了一项由65人参与的为期3周的人类重复伤害斑贴实验[4],目的是研究FWA 5BM对皮肤的刺激和致敏性。实验物质FWA 5BM(洗涤剂基料溶液中含FWA 5BM 10%)被用于一个系列9个密闭斑贴敷用物(每一个为期24h)中,2周后激发敷用位置。赋形剂作为阴性对照,没进行阳性对照。
洗涤剂基料在通常的商业配方范围内,浓度为0.5%的水溶液。时不时地观察伤害斑贴点,对其进行评分作为原发性刺激[4]。检验结果:
有阳性反应受试者的数量:0
有阴性反应受试者的数量:65有刺激反应受试者的数量:0该物质没有引起刺激或致敏。
(2) 在1970年FWA 5BM以24%的浓度用于光敏实验,有78人参与。除了每周两天在斑贴移除后,实验区域立即在室外阳光下暴露30min外,其他类似于上一实验。
结果显示:上述两个实验,在不同的时间间隔(时间没有说明)对斑贴位置进行刺激评级,FWA 5BM不会引起人体过敏,不是致敏物[4]。
(3) Keplinger等人于1974年进行了一项由自愿者参与的实验。200人用凡士林中含1%和5%的FWA 5BM(Ciba-Geigy公司提供,浓度不详)或50人用0.1%的洗涤剂溶液(类型没有说明)中含0.05%的FWA 5BM进行的斑贴实验。在每周一、三、五(在同一位置施用10次)封闭斑贴。斑贴在24h后移除,然后对斑贴点的初始刺激进行评分。在10~14天的实验后,在同一位置或相邻位置(或两者)进行斑贴激发。24h后移除斑贴。然后立即、24h和48h后对斑贴点的反应进行检查。
结果:人类暴露在任何配方中都没有观察到刺激或致敏[3-4]。
4.8 重复-剂量毒性
4.8.1 经口
(1) 根据OECD 指南407(啮齿动物重复-剂量28-天经口毒性),Wistar 大鼠(5只/性别/组)灌胃剂量0,50,200,1000 mg/kg-bw/day 的FWA 5BM 28天。没有发现死亡。对两个性别的高剂量组,与处理相关的影响是减少了红细胞数(减少了15%~17 %),对两个性别的中和高剂量组血红蛋白浓度减少了(减少了8%~23%),对两个性别的中和高剂量组红细胞比容值略微地减少了(减少了6%~21%),在中和高剂量组动物在绝对和或者相对肝、肾和睾丸重量方面分别发现明显的差异[5]。
结果:观察到有害作用的最低剂量LOAEL=1000mg/kg-bw/day(基于血液学变化主要反映轻微的溶血性贫血)。
未观察到有害作用的剂量N O A E L=2 0 0 mg/kg-bw/day
(2) 在一项非GLP实验中用大鼠对FWA 5BM的重复-剂量毒性进行了研究(IBT实验室在 1973年,Keplinger 等人在1974年,Lyman等人在1975年)。大鼠用含0、40、200和1000mg/kg FWA 5BM的食物喂养2年(约为0、2、8和40mg/kg bw/day)。
结果:FWA 5BM对体重没有影响;对食物的消耗没有明显的影响;没有发现异常行为反应;在动物的死亡总数上没有明显地影响;对测量的血液学、血液化学或尿分析参数没有影响。处理对器官的组织病理学检查方面没有明显的影响。对肿瘤的发生率没有影响。
NOAEL是最大的实验剂量=1000mg/kg[3]。
4.8.2 经皮
(1) 据1956年的研究报告介绍,用老鼠的背部区域进行了亚急性实验[1],FWA 5BM剂量为每5mg/只动物,暴露处理5天。每个性别每个剂量动物数量为5只。FWA 5BM的纯度大于80%。
结果:8天后没有发现异常。无局部刺激,无再吸收毒性。
(2) 另据1956年的研究报告介绍,用老鼠的背部区域进行了亚急性实验[1],FWA 5BM剂量为每只动物20mg,暴露处理5天。每个性别每个剂量动物数量为5只。FWA 5BM纯度大于80%。
结果:8天后没有发现异常。无局部刺激;无再吸收毒性。
(3) 另据1961年的研究报告介绍,在大鼠(重量140~171g)的背部区域进行了亚急性实验[1],FWA 5BM浓度为5%,剂量为0.4mL/只动物,暴露处理5天。每个性别每个剂量动物数量为5只。
结果:8天后没有发现异常。局部刺激轻微;无再吸收毒性。
4.9 遗传毒性
4.9.1 基因突变
(1) 1971年IBT(工业生物-检测实验室)用出生60~70天的12只雄性白化小鼠进行了显性致死实验。小鼠被分成几组:无FWA 5BM处理的阴性对照组;用甲磺酸乙酯处理的阳性对照组;用25、50mg/kg FWA 5B M处理的实验组。
结果:用FWA 5BM处理对交配指数没有影响;对黄体、着床点、早期再吸附和胚胎的数无影响;对末期再吸收数量无影响;对突变速率也没有影响。没有动物死亡或出现出毒性症状。
(2) 1974年Keplinger等人用FWA 5BM对小鼠的显性致死实验呈阴性[3]。
(3) McGregor和Ainsworth于1976年用FWA 5BM对鼠伤寒沙门氏菌株TA1535进行了一项研究,其实验结果为阴性[3]。
(4) 根据OECD指南471(细菌回复突变实验),鼠伤寒沙门氏菌株A 1535、TA 1537、TA 98、TA100和大肠杆菌株WP2uvrA在有或无S9代谢活化物的情况下暴露于0、33、100、333、2500或5000µg/盘的FWA 5BM中,同时进行阴性和阳性对照获得了预期的结果。没有发现细胞毒性。因此,认为FWA 5BM在该实验中不是诱导有机体基因突变的物质[5]。
4.9.2 染色体畸变
4.9.2.1 体外
(1) 据Kilbey B.J.和McGregor D.B等人在1973年、1975年和1976年的实验资料[10-12]介绍,毒理学家用鼠伤寒沙门氏菌TA1535和TA1538菌落,靶基因his(组氨酸),在有或无代谢活化物S9-混合物(雄性大鼠肝脏去线粒体后上层清液和辅酶因子)存在下,进行了细菌回复突变实验(例如Ames test)。
结果和结论:
无论FWA 5BM有没有 活化”,菌株都没有任何诱变活性迹象。
显微镜检验含有FWA 5BM的实验盘,结果显示存在适当的菌苔,微菌落的大小和数量与阴性对照实验盘没有明显的差异。
在用FWA 5BM和对照物处理后,使用鼠伤寒沙门氏菌TA1535和TA1538每盘(3盘平均)获得的突变菌落,见表10。
阳性对照:
二氯甲基二乙胺盐酸盐和2-乙酰胺基芴在每盘突变数量上引起增加。在2-乙酰胺基芴的情况下,增加只发生在代谢活化之后。
结果:无论FWA 5BM有没有活化,菌株都没有任何诱变活性迹象。致基因突变为阴性。
(2) 另有资料介绍[5],根据OECD指南 473(体外哺乳动物染色体畸变实验),中国仓鼠肺成细胞(V79)在有或无活化的情况下暴露于浓度范围在0.1~5mg/mL的FWA 5BM中,FWA 5BM没有引起染色体畸变[5]。
该实验中FWA 5BM对染色体畸变呈阴性。
(3) 1975年Kilbey B.J.等人[11]在 荧光增白剂对微生物的致突变性实验 中介绍,使用酵母菌(酿酒酵母)品系D4和W10,FWA 5BM剂量为100 mg/kg,三平行,对作为二倍体酵母菌细胞质小菌落突变体和有丝分裂基因转换的可能的诱导体的物质活性进行了研究。
结论:结果表明FWA 5BM不能产生诱变或任何遗传物质的变化。
(4) 1975年Kilbey B.J.等人[11]在 荧光增白剂对微生物的致突变性实验 中介绍,代谢活化系统为大鼠S9(肝匀浆液的去线粒体上清液),用靶基因his(多聚组氨酸),鼠伤寒沙门氏菌TA1530,TA1532,TA1535,TA1538在有或无代谢活化进行了细菌回复突变实验。实验浓度为1000mg/kg。实验中沙门氏菌株TA1530,TA1532,TA1535,TA1538被暴露于可见光或保存在暗处1h伴有通风。
结果:在暗处生长后或固定相细胞在光照后,没有迹象表明诱导突变或生存能力受影响。生长正如细胞在固定相的滴度所表明的那样,不受以标准浓度使用的FWA 5BM存在的影响。
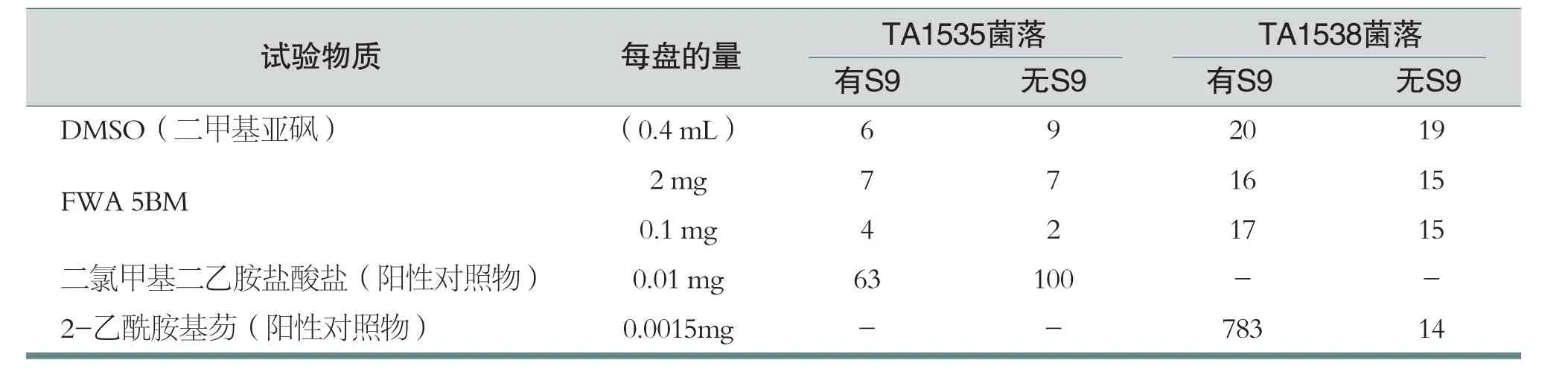
表10 不同试验物质处理后的突变菌落
结论:无论FWA 5BM有没有活化,菌株都没有任何致突变活性迹象。遗传毒性为阴性。
(5) 2014年毒理学家根据OECD指南471进行了细菌回复突变分析实验[1],使用大肠杆菌E.coli WP2 uvr A菌株,靶基因trp(色氨酸)。代谢活化方法为来自于苯巴比妥和b-萘黄酮的S9-混合物诱导大鼠肝脏。实验浓度为33~6666mg/板。同时进行对照实验,实验为三平行。
结果:在实验浓度下用或不用S9混合物,均未发现FWA 5BM的沉淀。在实验条件之下,测交品系回复突变体数量是在历史阴性对照数据范围之内。FWA 5BM被认为是非-诱变性物质。遗传毒性为阴性。
4.9.2.2 体内
(1) 1974年的研究报告介绍,按照OECD指南474(哺乳动物红细胞微核实验),给中国仓鼠(3只/性别/组)经口连续灌胃剂量为1250、2500或5000 mg/kg-bw/day 的FWA 5BM两天。同时进行阳性和阴性对照实验。在最后服药24h后获取骨髓。每只动物检查1000个细胞以寻找细胞核异常,包括单纯的Jolly体、红细胞中的片段、微核和渐进性坏死细胞[5]。
结果:处理对细胞核异常的发生率没有影响。对每一组动物细胞核异常的总的百分数范围是:阴性对照组为0~0.3%,在1250mg/kg组为0~0.4%,在2500mg/kg组为0~0.2%,在5000mg/kg组为0~0.2%。单一的Jolly体(0~0.3%)和其他特殊异常(0~0.1%)的发生率在对照和处理动物之间是相似的。
阳性对照组异常细胞的发生率有明显的增加。在每一个阳性对照中总的异常发生率为7.4%~14.3%。记录在阳性对照组的主要异常是单一的Jolly体 (发生率5.2%~10.2%)、红细胞中细胞核片段(发生率0.7%~1.9%)和有核红细胞(成红细胞)中的微核(发生率0.8%~2.6%)[4]。
结论:在该实验中FWA 5BM不能引起染色体畸变。
(2) 1974年的研究报告介绍,按照OECD指南475(哺乳动物骨髓染色体畸变检验),中国仓鼠(2只/性别/组)经口连续灌胃1250、2500或5000 mg/kg-bw/day剂量的FWA 5BM两天,每天给药一次。同时进行对照实验。仓鼠在最后服药2h后腹腔注射秋水仙胺,在注射秋水仙胺后4h获取骨髓。检查每只动物100个中期板,以寻求染色单体-核染色体-类型畸变、裂隙和粉化[5]。

结果:在最低剂量组的雌性发现每400个细胞(0.25%)有一个出现染色单体型畸变(染色单体断裂)。在赋形剂、2500或5000 mg/kg剂量组没有发现这些染色体畸变。在所有剂量组都没有发现染色体畸变或粉碎。在载玻片上来自于用1250mg/kg(2.25%)、2500mg/kg(0.5%)和 5000mg/kg(1.75%)剂量处理的动物的染色体裂隙发生率与赋形剂对照组的动物(1.25%)没有差别。
这项研究中阳性对照引起了所有畸变类型(染色单体断裂发生率14.25%、染色单体交换发生率17.5% 、染色单体型畸变发生率 1.0%、染色单体裂隙发生率15.25%、粉碎发生率 2.75%)明显的增加[4]。
结论:在该实验中FWA 5BM不能引起染色体畸变。
(3) 为了评价FWA 5BM对雄性生殖细胞的细胞毒性或致突变性,1974年毒理学家按照OECD指南478(遗传毒理学:啮齿动物显性致死实验)进行了FWA 5BM的显性致死实验[1]。实验动物为老鼠(品系NMRI),每个剂量给药动物数为12只雄性。剂量为1650和5000mg/kg,给药途径为经口灌胃。实验持续时间为6周。同时进行对照实验。
交配时间:每组有12只雄性,每组的每一个被处理后立即放入装有3只未处理的雌性老鼠的笼子里。在一周末,将雌性从笼子中移出,换成例外一组3只雌性。该过程持续进行6周。每日对雌性是否成功受孕进行检查,有阴道栓表明成功受孕。观察到阴道栓的那一天被认定为孕 0天”。整个的6个
交配时间 由所有从A-精原细胞到成熟精子的生殖细胞(胚细胞,受精卵)的成熟阶段组成,。
观察和记录雄性在给药之后第一周的全身状况、症状和体重变化。雌性在孕14天被尸检,并对其后代进行检查。
结果:所有实验组,其交配率、着床数量和胚胎死亡有可比性。对雄性没有观察到不适的症状。
结论:FWA 5BM的基因毒性(遗传毒性)为阴性,不会引起染色体畸变,不是致突变物。
(4) 1975年Muller等人用经口浓度高达5000 mg/kg的FWA 5BM对中国仓鼠骨髓的细胞遗传性和核异常性进行了实验,结果呈阴性[3]。

