金丝桃素药理作用以及制备方法研究概况
,2*
1.成都中医药大学药学院,四川 成都 611130;2.中药材标准化标准化教育部重点实验室,四川 成都 611137
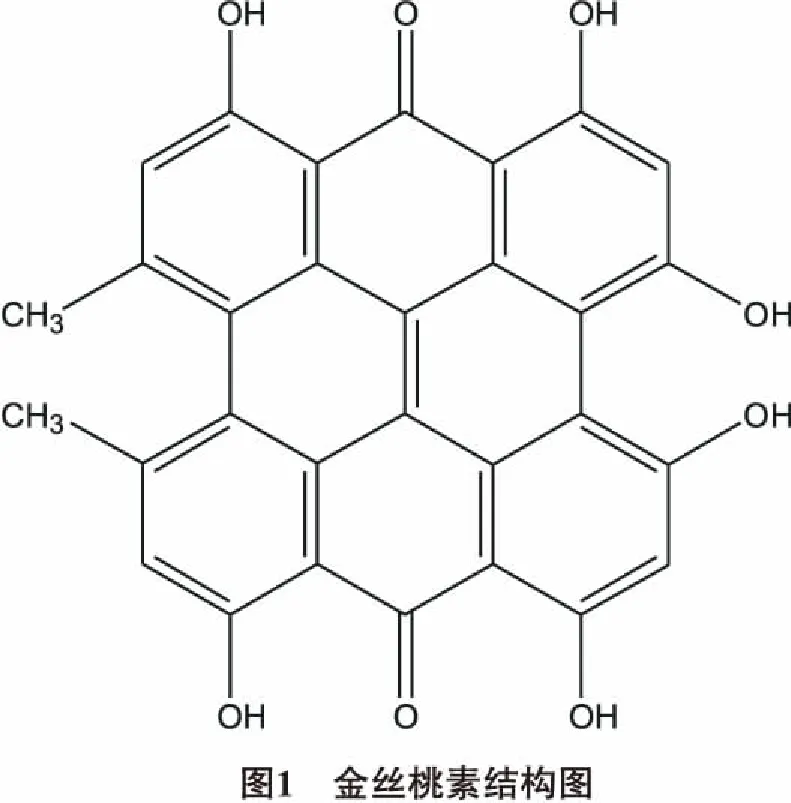
金丝桃素(结构见图1)来源于天然药物贯叶金丝桃,是其中最具有生物活性的成分[1]。原植物主要分布于我国的浙江、福建等省以及西南、西北等地,在我国资源丰富、产量大。金丝桃素分子式:C30H16O8,化学名称为4,4′,5,5′7,7′-六羟基-2,2′-二甲基-中位-萘骈二蒽酮,通过苯环和环外双键形成较大的共轭体系,在590 nm和550 nm处出现2个比较大的吸收峰。经吡啶或含盐酸的甲醇溶液重结晶后呈黑色粉末状晶体,有清香气味,可溶于碱性水溶液、吡啶、有机胺等,溶解后溶液呈樱红色且带有红色荧光[2],见光易分解,需避光保存。多种研究表明,它是一种具有光敏活性且药理作用显著的化合物,包括消炎、抗病毒、抗抑郁、创伤收敛作用等,此外该化合物在兽药方面也有比较广泛的应用。因其药理作用明显,经济价值高,故对金丝桃素药理、制备方法的最新研究进展进行总结,以期为金丝桃素的全面开发提供参考。
1 药理作用
金丝桃素的药理作用显著,主要有抗病毒、抗抑郁、抗肿瘤作用。
1.1 抗病毒 近年来发现金丝桃素在临床上对多种病毒都有抑制作用,如艾滋病、乙肝、疱疹、牛痘等病毒。胡冬华等[3]使用理论计算化学分子动力学模拟的方法,从分子水平上对HIV逆转录酶和金丝桃素的相互作用进行研究,验证了金丝桃素的抗艾滋病病毒在体内的作用机理,促进临床治疗艾滋病的新药开发。范颂等[4]研究金丝桃素与黄芪多糖、清热解毒口服液的联合用药对猪高热病的治疗效果,结果显示其治疗效果显著,为兽药的开发提供新思路。蓝天云等[5]研究金丝桃素的抗乙肝病毒作用并探寻其抗HBV靶点,实验结果显示金丝桃素对HNF3β与HNF4α的表达水平有一定的调控作用,进而抑制PgRNA,初步阐明了金丝桃素对PgRNA的抑制作用以及抗病毒机制。张燕[6]选择1型单纯疱疹病毒(herpes simplex virus 1,HSV-1)作为靶标,结果发现金丝桃素在一定程度尚能够抑制HSV-1病毒复制,证明了金丝桃素具有抵抗该病毒的潜能。
1.2 抗抑郁 金丝桃素抗抑郁作用突出。有研究对比丙米嗪和贯叶连翘两者对抑郁症的治疗效果,结果显示两者疗效接近,证明金丝桃素有治疗抑郁病症的作用[7]。温博等[8]利用抑郁症模型大鼠探寻金丝桃素的抗抑郁作用机制,结果显示该物质可以降低悬尾实验、强迫游泳试验的静止时间,增强5-HT1A受体的表达(P<0.05),升高海马5-HT受体的含量,表明金丝桃素对抑郁症的治疗与海马5-HT的水平以及5-HT1A受体的表达这两者的相关性比较大。翟学佳等[9]采用CUMS模型,对金丝桃素的抗抑郁作用及机制进行探讨,通过行为学试验和相关的生理生化指标可知:金丝桃素对抑郁症症状的减缓有较好的疗效,且数据显示其能够调控代谢物,表明金丝桃素可以减缓CUMS模型的抑郁症状,而且能够调控代谢物紊乱。
1.3 抗肿瘤 金丝桃素作为具有良好光敏活性的物质,是目前被证明的十分有效的天然光敏剂药物。试验证明,金丝桃素对细胞内有关凋亡信号的传导通路有一定的调控作用,作用靶细胞暗毒性低,在许多肿瘤的治疗中都表现出了良好的光化学活性[10],经过光活化的金丝桃素能够抑制酪氨酸激酶、蛋白激酶c以及其他生长因子刺激蛋白激酶的活性[11-12]。邵文丽等[13]对金丝桃素在肿瘤治疗方面的应用极其作用机制进行了全方位的阐述,对肿瘤治疗的研究与开发有一定的参考价值。文献报道,低频率的超声能够激活金丝桃素[14],活化后的金丝桃素可以促进细胞内的Beclin 1和LC3-II的表达,细胞自噬增加,使细胞内促凋亡因子Bax发生转位,从而导致细胞凋亡,进而抑制细胞生长,该发现促进金丝桃素在肿瘤治疗方面的应用,为中药声敏剂[15]的开发提供新思路。
1.4其他 除了上述几种主要的药理活性外,金丝桃素还有抗炎作用,可用于类风湿性关节炎的治疗[16],也有文献提到金丝桃素对鲜红斑痣[17]的治疗效果较好。
2 制备方法
近年金丝桃素的来源包括金丝桃属植物的提取分离以及化学合成。
2.1 天然植物提取
2.1.1 超声提取法 超声提取具有操作方便、耗时短、效率高,尤其适宜于热敏性成分。肖凤艳等[18]采用乙醇提取联合HPLC(高效液相色谱)法对金丝桃素进行定量分析,经过正交试验优化,得到最优提取工艺:70%浓度的乙醇作溶剂,15倍用量,40 ℃的超声温度,提取时间为60 min,提取次数2次,该条件下提取率高达94.66%,证明超声提取效率高、工艺可行,可进行进一步的放大试验。
2.1.2 微波提取法 微波提取法靠使用微波技术来辅助目标成分的提取,目前已得到广泛的应用。杨郭等[19]采用单因素实验,使用二次回归通用旋转组合的方法对影响提取率的各个因素进行考察,实验结果显示:当采用65%的乙醇浓度,17.5倍的溶剂用量,700 W的微波功率,64 min的提取时间作为提取条件时,提取率可以达到4912.79 μg / 10 g。
2.1.3 超临界萃取法 超临界流体萃取(SFE)是近年来应用比较广泛的,涵盖萃取、分离的,集合速度快、选择性好、没有溶剂残留、效率高等优点的新兴提取方法。李玲等[20]采用超临界C02萃取的方法,研究其提取的最佳工艺,获得了比较高的提取率、能耗低、工艺的稳定,使得大规模工业化的生产成为可能。
2.1.4 分子印迹聚合物技术联合法 分子印迹是近年来发展的以某种特定分子为模版进而合成对其具特异性识别能力的聚合材料的新兴技术,因其对特定分子有特异的吸附和识别能力,所以可以有效地富集含量少的特定分子,进而提高相应分子的提取效率。有文献报道,程文霞[21]以金丝桃素为模版分子,以多巴胺作为功能单位和交联剂,使用Fe3O4为基体,进而合成一种具有特异的识别能力和吸附作用的Fe3O4@PDA/Hyp磁纳米球,通过实验验证该聚合材料对金丝桃素模版分子具有良好的印迹效果和识别能力,对金丝桃素的富集提取有启示作用。
前三种方法比较常用,相比之下,超声提取和微波提取更加方便,且溶剂易得,运用较广。此外,还有相关文献报道提取方法还有酶辅助提取法[22]、碱液提取法、大孔吸附树脂吸附法等,联合分光光度法[23]、HPLC-UV-ESI-MS 联用技术[24]检测、荧光检测等方法对金丝桃素进行定性定量分析。
2.2 金丝桃素的化学合成 由于金丝桃素在所属植物中的含量很少,仅靠从天然植物中提取纯化是不能满足其需求的。为了提高金丝桃素的产量,扩大其产业化,化学合成金丝桃素已成为关注的热点。近几年来,金丝桃素的合成大多都以大黄素作为原料。李兆周等以大黄素为起始点,经二氧化锡还原,得到产物加以微波辅助合成金丝桃素,总收率达到74.3%,副产物少,条件简单,收率高,路线图详见图2。汤媛等[25]也采取大黄素作为原料,还原后采用Aldol缩合、经光照反应,最终完成了金丝桃素的合成路线,总收率达到58.6%,该路线在缩合步骤实施改进,通过改进后的工艺操作简便易行、条件温和,可适宜放大生产。胡冬华等[26]同样以大黄素为原料经过催化反应合成了金丝桃素,成本降低,合成时间缩短。还有部分文献指出,金丝桃素的合成也有选择其它更为简单的化合物作原料,夏晶等[27]以2,4-二甲氧基-6-甲基苯甲酸乙酯为原料,经过溴代、水解、氧化、环合、还原这5步反应,合成了3,5-二甲氧基邻苯二甲酸酐,避免使用了传统的水合氯醛等毒性较大地试剂,收率可观。该合成路线获得了金丝桃素的中间体,在一定程度上为金丝桃素的合成提供新思路。

3 小结与展望
金丝桃素的药用价值高,其药理作用方面主要集中在金丝桃素良好的光敏作用,尤其是关注点放在病毒、肿瘤等严重困扰人类健康的疾病上,但是对作用机制的研究尚不透彻,还需要更深层次的探讨。且金丝桃素在动物疫病方面的防治上面也有比较广阔的前景,可以将关注点向兽药的开发上迁移。
金丝桃素的药理作用决定了其需求量的不断扩增,增大金丝桃素的产量成了国内外关注的热点。增大产量可以从两方面入手:①提高提取率。虽然该物质在天然植物中含量低,但提高其提取率增大了对本草的利用率,尽最大可能提高产率。目前对金丝桃素的提取不能只局限与传统的提取分离方法,近些年来新兴技术发展迅猛,如生物技术(可尝试利用生物膜的选择性通透来对目标成分进行筛选)、高分子材料技术、计算机技术等,所以可以将关注点放在各种新兴技术与传统方法联合用以目标成分的获取上。②优化合成路线。因为金丝桃素在植物中的含量低,所以使用化学合成不失为解决其市场供应不足的合理方法。目前金丝桃素主要的成路线是以大黄素为原料,以更为简单、更易获得的简单化合物为原料的研究还不是很完善,因此研究开发路线简单、条件温和、成本低廉的金丝桃素合成路线成为重点及难点。希望能够继续加大对金丝桃素各个方面的研究,以期获得更高收率、更低成本、更加便捷、环保安全、低廉高效的提取合成路线,以便投入工业化大生产,满足市场需求。

