新型罗丹明B-色氨酸荧光探针合成及用于铜离子检测研究
王 鹏
(西华师范大学 a.化学化工学院,b.化学合成与污染控制四川省重点实验室,四川 南充 637009)
在有机生命体中,过渡金属元素扮演着非常重要的角色。铜作为人体必需的微量元素,广泛分布于生物组织中,其中大部分以金属蛋白酶的形式存在并起着重要的功能作用。但是当人体内残存的重金属铜过量时会对人体细胞和组织产生毒性作用,并导致许多神经疾病,例如阿尔茨海默氏症、威尔逊氏病等[1-3]。另外,由于金属铜被广泛的应用工业生产中,作为一种重要的环境污染物,工业废铜排放到环境中也会对环境造成了很大的污染和危害。荧光检测技术是现代分析化学中的一类重要方法,荧光检测技术在生命科学和环境化学领域发挥着不可替代的作用[4-6]。因此采用荧光光谱分析技术检测环境及活体细胞中Cu2+引起了广大科研工作者的广泛兴趣并产生很多了富有成效的工作[7-9]。众所周知,罗丹明衍生物处于螺环结构时既没有荧光也没有颜色;通过金属离子或者其他因素导致的罗丹明开环后,罗丹明衍生物发射出很强的荧光并伴随明显的颜色变化[10]。本文以罗丹明B为荧光团,利用多肽固相合成技术将色氨酸和罗丹明B通过缩合反应连接起来合成了荧光探针RW。相比于其他类型荧光探针,探针RW具有合成简便,水溶性好,灵敏度高,检测限低及响应时间短等优势[11-15]。当探针RW单独存在时,由于螺环结构的形成,探针RW表现出非常微弱的荧光,当向探针RW中加入铜离子之后,由于铜离子诱导的水解反应导致罗丹明开环并释放出强烈荧光,从而在乙腈-HEPES(10-2mol/L;pH=7.4;V/V=2∶8)缓冲溶液中实现了对铜离子的高灵敏高选择性荧光检测,最低检测限为128 nM,同时进行了探针RW荧光性质研究。
1 实验部分
1.1 药品、试剂和仪器
药品与试剂:Fmoc-Rink Amide树脂(0.45 mmol/g),罗丹明 B(97%)和 Fmoc-Trp(Boc)-OH(99%)购置于上海淘普生物科技有限公司。脱Fmoc保护基试剂 (六氢吡啶∶N,N-二甲基甲酰胺=1∶4,V/V),接肽试剂 (二异丙基乙胺∶N,N-二甲基甲酰胺 =174∶826,V/V)和多肽裂解液(三氟乙酸∶三异丙基硅烷∶蒸馏水 =9.5∶0.25∶0.25,V/V/V)在实验室自行配制。氢氧化钠(99%),氯化钠(99%),苯酚(99%),茚三酮(99%),三氟乙酸(99%)吡啶,4-(2-羟乙基)-1-哌嗪乙磺酸(99%),O-苯并三氮唑-四甲基脲六氟磷酸酯(98%),二异丙基乙胺(98%)和三异丙基硅烷(97%)购置于上海九鼎化学有限公司。二氯甲烷,N,N-二甲基甲酰胺,乙腈,无水乙醇,无水乙醚,三乙胺和六氢吡啶等化学试剂均为分析纯,购置于利安隆博华(天津)医药化学有限公司。所有化学试剂直接使用,没有进一步处理。
仪器:精骐牌BC-4201型3D摇床(上海鼎科科学仪器有限公司),25 mL多肽合成管(上海鼎科科学仪器有限公司),FD-1 Ultra-low freeze dryer型冷冻干燥机(北京比朗实验设备有限公司),Agilent 1200液相色谱仪(美国安捷伦科技有限公司),C18半制备分离柱(美国安捷伦科技有限公司),湘仪牌H1850型高速离心机(湖南湘仪实验室仪器开发有限公司),Precisa XB120A型电子天平(上海天美天平仪器有限公司),Bruker Esquire HCT离子阱质谱仪(美国布鲁克公司),岛津RF-5301PC型荧光分光光度计(日本岛津公司)。
1.2 探针RW的合成与表征
探针RW的合成采用多肽固相合成技术与荧光发色团修饰技术,具体合成路线如图1所示。
(1)称取0.20 g Fmoc-Rink Amide树脂,倒入25 mL多肽合成管中,加入10 mL二氯甲烷,浸泡30 min,然后用 N,N-二甲基甲酰胺洗涤3次,向上述含有树脂的多肽合成管加入5 mL脱除Fmoc保护基试剂,在3D摇床上反应30 min;反应完分别用N,N-二甲基甲酰胺,二氯甲烷,无水乙醇,N,N-二甲基甲酰胺各洗涤3次,利用循环水泵抽干树脂,进行K氏检测,若树脂颜色变成蓝紫色,则说明Fmoc-Rink Amide树脂上Fmoc保护基已经完全被脱除,可以进行多肽缩合反应。
(2)称取0.15 g Fmoc-Trp(Boc)-OH和0.20 g HBTU,用 N,N-二甲基甲酰胺溶解,加入到上述多肽合成管中,加入的接肽试剂(40μL),在3D摇床上反应1 h。利用循环水泵抽干,进行K氏检测,若树脂颜色不变,说明缩合反应进行完全。向多肽合成管加入5 mL脱除Fmoc保护基试剂,在3D摇床上反应30 min。然后进行K氏检测,若树脂颜色变成蓝紫色,则进行下一步。
(3)称取0.1 g罗丹明B(过量),用N,N-二甲基甲酰胺溶解,然后加入上述多肽合成管中,加入的接肽试剂(40μL)和三乙胺(40μL),在3D摇床上反应4 h。反应完分别用 N,N-二甲基甲酰胺,二氯甲烷,无水乙醇洗涤3次,利用循环水泵抽干。进行K氏检测,若树脂颜色不变,说明缩合反应进行完全。
(4)现配4 mL的多肽裂解液,加入上述反应完全的多肽合成管中,在3D摇床上反应4 h。将裂解得到的产物倒入25 mL离心管中,加入-20℃无水乙醚,在高速离心机上离心,弃去上清液,即得粗产物。
(5)利用高效液相色谱将粗产物进行纯化,由高效液相色谱纯化图可知产物的纯度达到检测要求。产率:89%;1H NMR(400 MHz,CDCl3,25℃)δ(ppm):8.050-7.850(m,2H),7.707-7.664(m,2H),7.314-7.258(m,2H),7.109-7.080(m,2H),7.040-7.031(m,1H),6.998-6.861(m,3H),6.757(s,1H),6.698-6.548(m,1H),4.450-4.380(m,1H),3.937(br,1H),3.792(br,1H),3.601(q,J=6.4 Hz,8H),3.506-3.390(m,3H),1.306(t,J=6.4 Hz,12H);MS:[RW+H+]+计算值:629.4;测定值:629.2。

图1 探针 R W的合成路线图
2 结果与讨论
2.1 溶液配制及实验条件
利用蒸馏水配置浓度为10-2mol/L的HEPES缓冲溶液,然后以2∶8的体积比向HEPES缓冲溶液中加入乙腈溶液配成乙腈-HEPES(10-2mol/L;pH=7.4;V/V=2∶8)缓冲溶液体系;利用蒸馏水配置 10-3mol/L的探针 RW 溶液和 10-3mol/L的 14种常见过渡金属离子(Ag+,Al3+,Ca2+,Cd2+,Co2+,Cu2+,Fe3+,Hg2+,K+,Mn2+,Na+,Ni2+,Pb2+,Zn2+)溶液。荧光检测实验在室温下进行,荧光检测时,荧光分光光度计的激发和发射狭缝均为10 nm,激发波长为525 nm。所有荧光检测实验所用条件均相同。
2.2 金属离子选择性研究
在荧光比色皿中加入2mL乙腈-HEPES(10-2mol/L;pH=7.4;V/V=2∶8)缓冲溶液,依次分别加入 20 μL,10-3mol/L的探针 RW和 200μL,10-3mol/L(10 equiv.)的 14种常见金属离子,并在荧光分光光度计中检测当14种金属离子存在时探针RW的荧光发射强度变化情况,记录最大发射峰(580 nm)处的荧光发射强度。由图2可知,若用525 nm激发,在含有探针RW的乙腈-HEPES缓冲溶液中加入Cu2+之后,由于铜离子诱导探针RW发生水解反应,导致探针RW开环使荧光发射强度增强,而当其他13种相关过渡金属离子加入探针RW之后,探针RW的荧光发射强度虽然有所增强,但与探针RW单独存在时相差不多,与铜离子相比基本没有任何变化。所以在14种金属离子中,探针RW可以通过“Off-On”型模式特异性检测Cu2+,而其他相关金属离子没有相同模式的响应。这充分说明在525 nm激发下,在乙腈-HEPES(10-2mol/L;pH=7.4;V/V=2∶8)缓冲溶液中,探针RW可实现对Cu2+的高选择性快速检测,而且荧光响应光谱变化明显。
2.3 金属离子竞争性研究
探讨荧光探针RW的荧光检测性质时,必须考察荧光探针抗其他相关金属离子干扰的能力。因此我们做了其他13种相关金属离子对Cu2+检测的荧光竞争性干扰实验。在荧光比色皿中加入2 mL的乙腈-HEPES(10-2mol/L;p H=7.4;V/V=2∶8)缓冲溶液,20μL,10-3mol/L的探针 RW 和 200μL,10-3mol/L(10 equiv.)的Cu2+,记录最大发射峰(580 nm)处的荧光发射强度,然后分别在上述RW-Cu混合溶液中加入200μL,5×10-3mol/L(50 equiv.)其他13种金属离子,记录最大发射峰(580 nm)处的荧光发射强度,然后得到13种相关金属离子荧光竞争性干扰图,由图3可以看出,探针RW在检测Cu2+的过程中,即使其他金属离子过量5倍,几乎对Cu2+的检测不存在竞争性干扰现象。实验现象表明探针RW具有良好的抗干扰能力,可应用于其他金属离子存在的复杂环境中实现对Cu2+的特异性灵敏检测。

图2 探针 R W对 于14种 金属离子的选择检测图

图3 其他13种 相关金属离子存在时,C u2+检测的竞争性柱状图
2.4 Cu2+荧光滴定研究
为了确定检测Cu2+的最大饱和浓度,我们做了Cu2+的荧光滴定实验。在荧光比色皿中加入2 mL的乙腈-HEPES(10-2mol/L;p H=7.4;V/V=2∶8)缓冲溶液和 20μL,10-3mol/L的 RW溶液,然后累计依次加入0~10.0 equiv.(每次0.5equiv.添加)的10-3mol/L的Cu2+进行荧光测量,分别记录20组最大发射峰(580 nm)处的荧光发射强度得到 Cu2+的荧光滴定图(图4)。从荧光滴定图可以看出,在525 nm激发下,探针RW在最大发射峰(580 nm)处的荧光发射强度逐渐增强,并且呈现良好的线性关系。
2.5 Cu2+的检测限研究
通过Cu2+低浓度时荧光滴定数据和线性拟合情况,利用检测限计算公式3σ/k可以计算出Cu2+的检测限。在2mL的乙腈-HEPES(10-2mol/L;pH=7.4;V/V=2∶8)缓冲溶液中,通过逐次等量递增 Cu2+浓度(0.2,0.4,0.6,0.8,1.0,1.2μM),在最大发射峰(580 nm)处测得系列荧光发射强度。重复三组平行实验取最好的一组并求标准偏差得到线性拟合图,从图5可以观察到,在Cu2+浓度为0~1.2μM范围内呈现良好线性曲线(R=0.9863)。最后,利用检测限LOD=3σ/k公式计算出Cu2+的最低检测限为128 nM。该实验结果表明探针RW可以在体外实现对Cu2+的高灵敏检测。

图4 Cu2+荧光滴定光谱图

图5 Cu2+的检测限图
2.6 检测机理探讨
罗丹明B作为荧光染料被广泛应用于荧光探针的设计中,罗丹明荧光探针具有较大的摩尔消光系数,较高的荧光量子产率和较长的发射波长等优良光谱性能。另外,罗丹明类探针通常处于螺环和开环的平衡状态之间,且这两种存在模式能表现出不同的荧光光谱性质,这就使其通常被人们设计成“Off-On”型荧光探针。如图6所示,在本论文中,当探针RW单独存在时,由于罗丹明B螺环的形成,探针RW表现出非常微弱的荧光,当向探针RW中加入铜离子后,由于铜离子诱导的水解反应导致罗丹明开环并释放出强烈荧光,从而在乙腈-HEPES(10-2mol/L;pH=7.4;V/V=2∶8)缓冲溶液中实现了对 Cu2+的高选择性快速特异性检测。
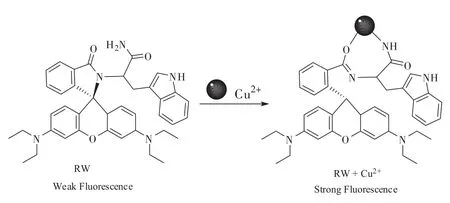
图6 探针 R W的检测机理图
3 结 论
设计并合成了一个新颖的“Off-On”型荧光探针 RW,利用罗丹明衍生物分子“关-开”环原理,在乙腈-HEPES(10-2mol/L;pH=7.4;V/V=2∶8)缓冲溶液体系中实现了对铜离子的高灵敏高选择性荧光检测,通过荧光选择性实验分析发现探针RW对Cu2+具有很好的特异性荧光检测性能;通过Cu2+荧光滴定实验可知探针RW和Cu2+具有良好的线性关系;通过相关金属离子竞争性实验得到其他13种金属离子对Cu2+的检测基本没有干扰作用;最后,通过计算得到Cu2+的最低检测限为128 nM。综上所述,探针RW能够实现对Cu2+高灵敏特异性检测。

