磷在氯气中燃烧实验装置的新设计
张丽敏 刘枚 李兴

摘要: 通过对磷在氯气中燃烧实验的一些研究实例的分析和讨论,认为对该实验有进一步研究和改进的必要性。利用吸滤瓶、具支试管、一次性注射器以及激光笔等器材,通过设计环保一体化的实验装置,减少氯气的制备以及磷在氯气中燃烧时对环境的污染,解决了教材中光有讲述没有实验的实际问题,为培养学生的科学素养和提高化学教学质量创造了条件。
关键词: 红磷; 氯气; 燃烧; 实验改进; 实验探究
文章编号: 1005-6629(2019)12-0065-03 中图分类号: G633.8 文献标识码: B
1 问题提出
磷在点燃的条件下能与氯气反应,是现行高中化学教材[1]中的重要知识点。教材中指出,磷在不充足的氯气中燃燒生成三氯化磷(PCl3),在过量的氯气中燃烧生成五氯化磷(PCl5)。教材中光有这些理论知识,并没有设计实验加以验证和说明。由于大多数教师缺乏有效的实验手段,只能纸上谈兵,常使学生感到枯燥无味,不利于培养学生的感性认识和科学素养。由于学生看不见磷在氯气中燃烧的实验现象,观察不到三氯化磷转化成五氯化磷的过程,学生在好奇心和求知欲的驱使下,往往对生成两种氯化物的生成条件和转化产生怀疑,甚至有的学生提出了一些问题。例如: 教材中给出的结论真的正确吗?磷点燃时真能够在氯气中燃烧吗?三氯化磷真的是无色液体吗?磷在氯气充足时真能生成五氯化磷吗?五氯化磷是什么颜色和状态?由此可见,这些问题虽然不大,但不通过实验是很难解决的。由于教材没有给出相应的实验方法,学生提出的问题再多、再简单,教师也是束手无策,无言以对,只能是书上怎么讲,教师就怎么说,致使教师非常被动和尴尬。针对这种情况,我们利用吸滤瓶、气球、一次性注射器、橡胶塞、激光笔等常见仪器,通过巧妙设计和组合,制作了磷在氯气中燃烧的改进实验装置。
2 研究现状及分析
广大化学教育工作者也曾研究、设计出了磷在氯气中燃烧的一些实验方案。这些实验方案虽然解决了一定的问题,但仍然不尽如人意,具体表现为:
(1) 有的实验方案需要复杂的氯气制备系统,制备、收集氯气时费时费力,不适应当今社会的环保要求,不利于培养学生的环保意识。
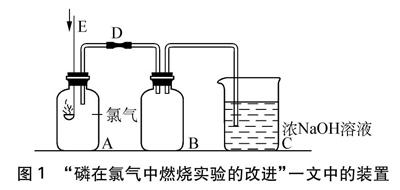
例1 “磷在氯气中燃烧实验的改进”[2]一文(见图1)存在问题有: ①需要一个制备氯气的系统;②点燃红磷时必须在瓶外点燃,既造成了红磷燃烧生成五氧化二磷的粉尘污染,又造成了瓶内氯气外逸的气体污染;③没有指明氯气是干燥的,容易使磷的氯化物发生水解,影响实验效果。
图1 “磷在氯气中燃烧实验的改进”一文中的装置
例2 “红磷在氯气中燃烧实验的改进”[3]存在问题有: ①需要一个制备氯气的系统;②直接将氯气瓶扣在燃烧的红磷上,粉尘污染和气体污染更为严重。
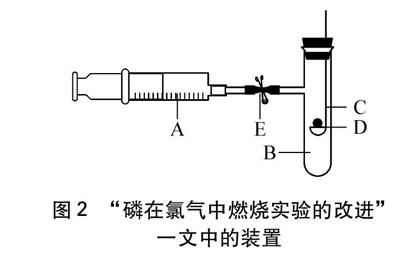
例3 “磷在氯气中燃烧的实验改进”[4](见图2)存在问题有: ①需要一个制备氯气的系统,在注射器内收集氯气,容易使氯气外逸;②点燃红磷时容易造成粉尘污染;③当红磷在氯气中燃烧时由于是放热反应,具支试管上的胶塞很难塞住,容易被顶出,造成室内污染。
图2 “磷在氯气中燃烧实验的改进”
一文中的装置
(2) 有的实验方法很难得到实验现象,失去了化学实验的教学意义。
例4 “红磷在氯气中燃烧实验的改进”[5](见图3)存在问题有: ①点燃红磷时容易造成粉尘污染;②实验现象容易受氯气制备的干扰,因为在反应器内存在大量水蒸气,生成的三氯化磷和五氯化磷容易水解(PCl3+3H2OH3PO3+3HCl、 PCl5+4H2OH3PO4+5HCl),最终很难看到两种产物的生成过程。
图3 “红磷在氯气中燃烧实验的改进”
一文中的装置
上述事实说明,进一步研究红磷在氯气中燃烧实验的方案是很有必要的,通过研究红磷在氯气中燃烧的实验方法,可以完善前人的实验方案,为提高化学教学质量做出贡献。
3 研究理念
根据氯气的制备以及磷在氯气中燃烧的特点,立足于实验的简单化、环保化、一体化,努力保证实验的科学性、安全性、可操作性。制备氯气时,可以用高锰酸钾晶体与浓盐酸反应来完成;可以用浓硫酸干燥氯气;剩余的氯气可以用氢氧化钠溶液来吸收;各种实验仪器通过精心设计、巧妙组合,最终实现氯气制备、磷在氯气中燃烧和有毒气体吸收的一体化,确保实验者能很好地使用该实验装置,顺利完成教学任务。
4 设计方案
依据设计理念,氯气的制备可以利用具支试管作为反应器。具支试管底部盛放高锰酸钾晶体,然后将注射器内的浓盐酸慢慢注入具支试管内,使两者发生反应。生成的氯气通过另一支具支试管内的浓硫酸被干燥,磷和干燥的氯气发生反应是在吸滤瓶内进行,点燃磷的方法是用激光笔照射来完成,有毒物质则利用气球里的氢氧化钠溶液来吸收。使用气球有两个作用: 一是可以平衡吸滤瓶内部与外部的压强;二是防止多余的氯气外逸,不仅保证实验的安全性,而且还可以防止橡胶塞被顶出,造成有毒气体的外泄。
5 反应原理
(1) 高锰酸钾与浓盐酸反应生成氯气
2KMnO4+16HCl(浓)
2MnCl2+2KCl+5Cl2↑+8H2O
(2) 磷在不充足的氯气中燃烧生成三氯化磷
2P+3Cl2点燃2PCl3
(3) 磷在充足的氯气中燃烧生成五氯化磷
2P+5Cl2点燃2PCl5
(4) 反应剩余的氯气被氢氧化钠溶液吸收
Cl2+2NaOHNaCl+NaClO+H2O
(5) 磷的氯化物的水解
① 三氯化磷的水解反应
PCl3+3H2OH3PO3+3HCl
② 五氯化磷的水解反应
PCl5+4H2OH3PO4+5HCl
6 实验用品
吸滤瓶(500mL)1个、大功率激光笔(2W)1支、具支试管(2×20cm, 1.5×15cm)各1支、一次性注射器(50mL)1支、大号气球1个、3号单孔橡胶塞1个、3号橡胶塞1个、6号双孔橡胶塞1个、直角玻璃管2根、细线、硬质橡胶管若干
高锰酸钾晶体、浓盐酸(37%)、干燥红磷、10%氢氧化钠溶液、浓硫酸(98%)、干燥细沙等
7 装置设计
实验装置如图4所示。
A浓盐酸20mL;B浓硫酸5mL;C高锰酸钾晶体5g;D气球;E激光束;F激光笔;G氢氧化钠溶液;H氯气;I红磷;J细沙层0.3cm
图4 实验装置
8 操作过程及现象
(1) 首先按照实验装置(如图4所示),将仪器组装、连接好,所用药品填装好。
(2) 用力下推一次性注射器的活栓,使浓盐酸慢慢滴入盛有高锰酸钾晶体的具支试管内,反应立即进行[2KMnO4+16HCl(浓)2MnCl2+2KCl+5Cl2↑+8H2O],生成的氯气通过另一支具支试管内的浓硫酸干燥后进入吸滤瓶内。
(3) 当吸滤瓶内有淡淡的黄绿色氯气时,用激光笔的绿色光照射红磷,红磷在氯气中立即燃烧(2P+3Cl2点燃2PCl3),发出白光,并在吸滤瓶的内壁上有水珠状无色的液体产生,此无色的液体即为三氯化磷。
(4) 继续用力下推一次性注射器的活栓,当吸滤瓶内有大量黄绿色氯气时,红磷继续燃烧,并可发现有白烟生成(2P+5Cl2点燃2PCl5),然后附着在瓶壁上,由此说明当氯气充足时生成了五氯化磷的晶体。
(5) 红磷燃烧结束后,停止向盛有高锰酸钾晶体的具支试管内加入浓盐酸,吸滤瓶内逸出的氯气被气球内的氢氧化钠溶液吸收(Cl2+2NaOHNaCl+NaClO+H2O)。
(6) 向吸滤瓶内注入氢氧化钠溶液,将生成的三氯化磷、五氯化磷吸收(PCl3+6NaOHNa3PO3+3NaCl+3H2O、 PCl5+8NaOHNa3PO4+5NaCl+4H2O)。
9 幾点说明
(1) 实验所用的红磷也可用白磷代替,效果也佳。
(2) 用浓硫酸干燥氯气可以保证红磷与干燥的氯气发生反应生成磷的氯化物,不至于发生水解而干扰实验现象。
(3) 吸滤瓶底部的干燥细沙层起到隔热的作用,防止红磷燃烧时将瓶底烫裂,造成有毒气体外泄,使实验失败。
(4) 严禁用激光笔照射眼睛,以防造成烧伤。
10 结语
本实验方案具有构思巧妙、简单易行、环保安全、现象明显等诸多特点。通过课堂实验过程中的氯气制备、激光点燃、红磷燃烧、三氯化磷和五氯化磷的生成等,能够有效地帮助学生解惑答疑,进而增大化学理论的可信度,加深学生对有关知识的理解和记忆,培养了学生的创新精神,增强了学生的环保意识,为培养学生的学科素养、提高化学教学质量创造了条件。
参考文献:
[1]人民教育出版社化学室编著. 全日制普通高级中学教科书(必修加选修)·化学(第二册)[M]. 北京: 人民教育出版社, 2003: 5.
[2]李荒生. 磷在氯气中燃烧实验的改进[J]. 湖北中小学实验室, 1977, (1): 13.
[3]王汝坦. 红磷在氯气中燃烧实验的改进[J]. 教学仪器与实验, 1992, (4): 7.
[4]蔡清华. 磷在氯气中燃烧实验的改进[J]. 化学教学, 1998, (1): 7.
[5]李秀波. 红磷在氯气中燃烧实验的改进[J]. 教学仪器与实验, 2001, (1): 11.

