玻璃酸钠滴眼液对PDR患者玻璃体切除术后眼表的保护作用
张妍春,雷春灵,孙朝朝,刘文婷,任秀瑜,康紫薇,宋虎平
0引言
糖尿病视网膜病变是导致工作人群致盲的主要原因,同时糖尿病(diabetes mellitus,DM)也是发生干眼(dry eye syndrome,DES)最主要的系统性危险因素之一[1],研究显示53%~54% DM患者患有临床相关的DES[2-3]。慢性高血糖、糖尿病周围神经病变、胰岛素水平降低、微血管病变以及系统性高渗状态都是糖尿病干眼(diabetes mellitus associated dry eye syndrome, DMDES)的危险因素[4-5]。但是,有些DMDES患者缺乏临床主观症状,这可能与糖尿病周围角膜神经病变导致角膜敏感度下降有关[6]。泪膜破坏不仅会导致干眼的发生,也会导致角膜上皮损害,这在糖尿病患者非常常见[7],因此有学者提出,对于糖尿病患者,除了接受定期的眼底检查外,干眼及眼表的检查也应纳入日常检查项目。
玻璃体切除手术是治疗增殖性糖尿病视网膜病变(proliferation diabetic retinopathy, PDR)的重要手段,20G闭合式玻璃体切除系统仍在多数地区被主要应用。我们前期的研究已经证实与无糖尿病的对照组患者相比,PDR患者泪液分泌量、泪膜质量显著降低,眼表不适显著加重,行20G闭合式玻璃体视网膜手术后PDR患者眼表明显加重并持续存在,甚至术后3mo仍未恢复至术前水平[8]。这与临床常见的PDR患者玻璃体视网膜术后更容易发生严重的角膜并发症,如角膜上皮再生迟缓、持续性的上皮缺失、上皮水肿等眼表异常表现相关,提示我们临床应该关注玻璃体视网膜术后PDR患者的眼表改变。为缓解眼部不适症状和保护患者的视功能,目前主张对干眼的患者根据程度的不同采取不同的治疗方法,其中药物治疗包括人工泪液、润滑膏剂(眼用凝胶、膏剂)、局部抗炎及免疫抑制剂、自体血清以及雄激素、促泪液分泌药物等其它治疗药物[9]。玻璃酸钠滴眼液是广泛应用于各种类型及不同严重程度干眼治疗一线用药的人工泪液之一,本研究拟通过观察比较PDR及应用玻璃酸钠滴眼液的药物对照组患者玻璃体切除手术术前、术后不同时间眼表相关疾病指数(ocular surface disease index, OSDI)、基础泪液分泌量、泪膜破裂时间(BUT)以及角膜共焦显微镜下泪膜、角膜上皮细胞的改变,研究1g/L玻璃酸钠滴眼液对PDR患者20G术后不同时间干眼发病情况的影响,以期为临床治疗提供依据。
1对象和方法
1.1对象经西安市第四医院伦理委员会批准,选取2013-04/2015-12因PDR在西安市第四医院眼科住院行20G玻璃体视网膜手术的2型糖尿病患者作为观察对象,双眼接受手术患者选择第一只手术眼纳入研究。所有患者均自愿参加研究并签署知情告知书确认,能按照研究设计要求按时随诊,完成相关检查。经裂隙灯检查无角膜组织异常情况者纳入研究,PDR的诊断标准及手术指征严格参照ETDRS (Early Treatment of Diabetic Retinopathy Study)标准[10]。手术均由同一术者操作。排除标准:近期(3mo内)超过1wk使用滴眼液史或曾行视网膜光凝治疗,既往眼部外伤或手术史、角膜激光治疗手术史、角膜接触镜配戴史、服用过影响角膜代谢的药物、角膜疾病史以及术中发生意外结膜破裂、角膜上皮损伤或其它并发症者。共90例患者符合病例纳入和排除标准,按照随机分组表随机分为PDR对照组(A组,45例45眼)、玻璃酸钠治疗组(B组,45例45眼),采用单盲研究,即所有指标的检测人员不参与患者的随机分组和治疗过程。
1.2方法
1.2.1检查和评分方法询问研究对象一般情况,包括年龄、性别、症状、既往全身及眼部病史及治疗史、糖尿病病史、近2a血糖水平及药物使用情况;是否有视网膜光凝史;进行全面的眼科检查包括裂隙灯显微镜眼前节检查(眼睑、睑缘及睑板腺改变、结膜和角膜改变等)、裸眼视力、最佳矫正视力(best corrected visual acuity,BCVA)、眼底检查;在手术前、术后1wk,1、3mo由同一医生在同一检查室进行眼表相关检查,检查前至少30min避免使用滴眼液滴眼或进行其它接触眼表的检查;每次眼表检查按以下流程进行:眼表疾病指数量表询问→裂隙灯显微镜检查→泪液分泌试验→BUT→眼表面活体细胞荧光素染色→角膜共聚焦显微镜检查。具体方法如下:(1)患者眼表疾病指数:使用Allergan公司1995年制定的问卷和症状评分系统,内容包括有无眼部异物感、畏光、眼痛等,以及日常生活是否受限和对环境因素的反应,根据调查结果计算眼表疾病相关指数(OSDI),分数0~12分,分数越高症状越重;(2)基础泪液分泌量(Schirmer Ⅰ test,SⅠt):采用泪液检测滤纸条(天津晶明YZB/津0360-2004型标准5mm×35mm),按常规检查方法进行;(3)泪膜破裂时间(break-up time,BUT):使用天津晶明Q/12KF3879-2000标准荧光滤纸条,按常规检查方法进行;(4)角膜荧光素染色(fluorescein cornea staining,FL):使用天津晶明Q/12KF3879-2000标准荧光滤纸条染色,采用12分法进行评分,即将角膜分为4个象限,每个象限为0~3分(总分0~12分),无染色为0分,1~30个点状着色为1分,>30个点状着色但染色未融合为2分,3分为出现角膜点状着色融合、丝状物及溃疡等[11-12];(5)共焦显微镜(LSCM,ConfoScan 4,CS4)非接触下高速扫描泪膜并进行拍摄:20倍镜头,工作距离12mm,非接触式镜头,每只检查眼均采集3次泪膜图像,对所拍设的图像数据选择最佳图像并保存以备分析。参照Stonecipher等[13]的方法将共聚焦显微镜下泪膜图像分为正常(0级,基本均匀一致的脂质层覆盖在黏液层上),轻度损伤(1级,早期的外层脂质层损害表现,表现为泪膜脂质层连续性破坏),中度损伤(2级,脂质层变薄并且出现断裂,更多的蛋白残骸,以及早期上皮细胞脱屑可以看到,随着脂质层变薄,可以看到泪膜的缺失),重度损伤(3级,表现为更严重的细胞脱屑以及泪膜缺失,脂质层几乎不存在,泪膜上可以看到大量上皮细胞脱屑现象,形成鳞片状)4个等级,取3次检查获得等级的平均值;(6)共焦显微镜角膜上皮层高速扫描:待检眼盐酸丙美卡因滴眼液表面麻醉1次后使用40倍物镜镜头在2g/L卡波姆眼用凝胶辅助下自动扫描并记录,扫描范围(x,y)460μm×345μm,40倍放大,扫描频率25Hz(fps),视场最大像素数768pix×576pix,横向分辨率0.6μm/pix,工作距离1.98mm,存储图像以备分析。采集角膜中央上皮表层细胞层、翼状细胞层、基底细胞层图像,盲法选择各层聚焦最佳并具有代表性的3幅图像并保存以备分析。
表1两组一般情况比较
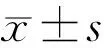

组别例数男∶女平均年龄(岁)视力下降病程(mo)术前眼压(mmHg)空腹血糖(mmol/L)糖尿病病程(a)A组4514∶3156.02±12.455.11±7.3514.18±3.267.06±2.529.56±6.49B组4516∶2955.82±11.966.56±13.3314.22±2.686.65±3.0310.23±6.73 χ2/t0.2000.078-0.641-0.060.697-0.477P0.6550.9380.5230.9520.4880.634
注:A组:PDR对照组;B组:玻璃酸钠治疗组。
表2两组术前最佳矫正视力情况眼(%)

注:A组:PDR对照组;B组:玻璃酸钠治疗组。
表3两组手术耗时及手术方式比较

组别手术耗时(x±s,min)Phaco(联合/未联合,眼)填充物(眼)硅油C3F8空气BSSA组72.44±21.6333/12211923B组74.89±17.2032/13191844 χ2/t-0.5930.0550.1800.0460.7140.155P0.5540.8140.6710.8300.3980.694
注:A组:PDR对照组;B组:玻璃酸钠治疗组。
1.2.2手术及干预方法所有患者均行玻璃体视网膜手术(20G,CX2000),根据患者病情联合或不联合白内障超声乳化及人工晶状体植入术,纪录从开始开睑至手术结束取出开睑器的时间为手术耗时,标准经睫状体扁平部巩膜三通道切口[8],术毕8-0可吸收线8字缝合巩膜切口1针,间断缝合球结膜切口1针。联合白内障手术者于1∶00位使用一次性矛形穿刺刀(19G)行透明角膜辅助切口1.1mm,11∶00位距角膜缘1~1.5mm处用一次性3.2mm金属隧道刀行两平面透明角膜隧道切口,宽3.2mm,长1.75~2mm。术毕使用10-0尼龙线间断缝合透明角膜隧道切口1针,术后3mo拆除尼龙缝线。术中所有病例均使用金属顶压器360度全周顶压辅助基底部玻璃体切除及视网膜光凝,根据病情采用不同的玻璃体填充剂,包括BSS、消毒空气、12%~20% C3F8、硅油。所有术眼于术前2d开始使用3g/L左氧氟沙星滴眼液点眼,术后加用普拉洛芬滴眼液、妥布霉素地塞米松滴眼液点眼,3次/d,复方托吡卡胺滴眼液点眼,2次/d,以上药物持续至术后1mo停药,B组在此基础上于手术后第1d即加用1g/L玻璃酸钠滴眼液滴术眼,3次/d,持续至术后2mo停药。

2结果
2.1一般情况患者的一般情况见表1,共有90例参与研究,其中男30例(33%),女60例(67%)。A组及B组各45例,A组年龄25~82岁,B组年龄23~74岁,两组性别、年龄、视力下降病程、术前眼压比较,差异均无统计学意义(P>0.05)。A组患者糖尿病病程6mo~21a(平均9.56±6.49a),入院空腹血糖7.06±2.52(3.6~16.4)mmol/L;B组糖尿病病程3mo~23a(平均10.23±6.73a),入院空腹血糖6.65±3.03(3.6~14.6)mmol/L,两组比较差异无统计学意义(P>0.05)。将术前最佳矫正视力(BCVA)进行分级,其中HM或CF/眼前5~30cm分别记入HM或CF,经Wilcoxon 秩和检验两组视力比较,差异无统计学意义(Z=-0.196,P=0.844),见表2。
2.2两组手术相关参数比较联合白内障超声乳化手术共65眼,未联合白内障超声乳化25眼,行硅油填充共40眼,行惰性气体填充共37眼,空气填充6眼,7眼BSS填充。两组手术耗时、手术方式比较差异无统计学意义(P>0.05),见表3。
2.3术中明确PDR分期A组增生高危期(Ⅳ期)9例,纤维增生期(Ⅴ期)17例,增生晚期(Ⅵ期)19例;B组增生高危期(Ⅳ期)5例,纤维增生期(Ⅴ期)19例,增生晚期(Ⅵ期)21例。两组术眼糖尿病视网膜病变分期经Wilcoxon 秩和检验,差异无统计学意义(Z=-0.773,P=0.440),见表4。
2.4两组术前及术后不同时间眼表不适症状与泪膜指标比较两组术前、术后1wk,1、3mo OSDI、SⅠt、BUT、FL值见表5。采用重复测量数据的方差分析进行分析两组各时间点测量值的时间差异性,结果表明OSDI、FL评分存在时间差异,差异有统计学意义(P<0.05),采用两两比较的方法(LSD-t检验)对两组术后不同时间与术前该指标差异进行比较,A组术后1wk,1mo FL与术前相比显著增加,差异均有统计学意义(t=-3.430,P=0.001;t=-3.161,P=0.002),至术后3mo FL差异无统计学意义(t=-1.644,P=0.102);术后3mo OSDI评分差异有统计学意义(t=-3.667,P<0.01),术后1wk,1mo OSDI评分差异无统计学意义(t=-1.098,P=0.274;t=0.110,P=0.913);B组FL术后1、3mo与术前比较均有显著改善,差异均有统计学意义(t=2.812,P=0.005;t=3.023,P=0.003);B组OSDI术后1wk,1、3mo与术前比较,差异均有统计学意义(t=2.405,P=0.017;t=6.473,P<0.01;t=7.550,P<0.01)。两组不同检查时间的组间差异结果显示,两组间OSDI、SⅠt、BUT、FL差异均有统计学意义(P<0.05),进一步采用独立样本t检验对各时间点的组间差异进行比较,A、B两组术前OSDI、SⅠt、BUT、FL相比,差异均无统计学意义(P>0.05),术后各项指标除FL 术后1wk两组比较差异无统计学意义(P>0.05)外,其它差异均有统计学意义(P<0.05),见表5,图1。根据角膜共聚焦显微镜下泪膜层的表现将泪膜分为0~3级,共4个等级,两组不同时间点脂质层分级见表6。术前两组90眼中仅有9眼(10%)表现出比较均匀的脂质层覆盖于眼表,14眼(16%)脂质层变薄局部断裂,高达42眼(47%)表现出脂质层断裂缺失,上皮细胞残骸堆积,25眼(28%)脂质层几乎不存在,大量上皮细胞脱屑形成鳞片状,采用Wilcoxon 秩和检验比较术前两组泪膜图像分级差异无统计学意义(P>0.05)。A组术后泪膜脂质层断裂缺失、上皮细胞脱屑较术前更为加重,泪膜质量明显下降,至术后3mo泪膜图像分级仍未恢复。与A组比较,B组术后不同时间点泪膜图像评分较A组明显好转,差异均有统计学意义(P<0.01),两组不同时间泪膜典型照片见图2。
表4两组术眼糖尿病视网膜病变分期构成情况眼(%)

注:A组:PDR对照组;B组:玻璃酸钠治疗组。
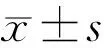

指标组别术前术后1wk术后1mo术后3moOSDI评分(分)A组B组35.68±10.1837.04±14.2140.82±21.2024.94±19.2137.26±20.3716.07±10.5749.87±20.5212.15±9.68F时间=6.729,P时间<0.01F组间=101.873,P组间<0.01F时间×组间=21.613,P时间×组间<0.01 t-0.5182.1745.61310.983P0.6050.032<0.01<0.01SⅠt(mm/5min)A组B组6.98±3.077.89±4.517.33±4.5110.29±6.396.40±3.9711.18±3.965.78±2.7310.18±4.38F时间=2.083,P时间=0.112 F组间=47.826,P组间<0.01 F时间×组间=3.559,P时间×组间=0.020 t-1.120-2.000-5.717-5.885P0.2660.049<0.01<0.01BUT(s)A组B组6.54±3.587.32±3.715.28±2.458.44±2.595.49±2.238.62±2.923.59±1.129.52±2.15F时间=0.688,P时间=0.623 F组间=110.092,P组间<0.01F时间×组间=14.420,P时间×组间<0.01 t-1.005-4.969-5.730-16.380P0.318<0.01<0.01<0.01FL(分)A组B组1.73±1.532.38±1.752.98±1.843.27±2.082.84±2.021.36±1.482.31±1.201.24±1.48F时间=11.822,P时间<0.01F组间=4.144,P组间=0.045 F时间×组间=9.052, P时间×组间<0.01 t-1.8160.1133.9863.630P0.0660.910<0.01<0.01
注:A组:PDR对照组;B组:玻璃酸钠治疗组。
表6两组玻璃体视网膜手术前后不同时间点角膜共聚焦显微镜下泪膜分级眼(%)
注:A组:PDR对照组;B组:玻璃酸钠治疗组。
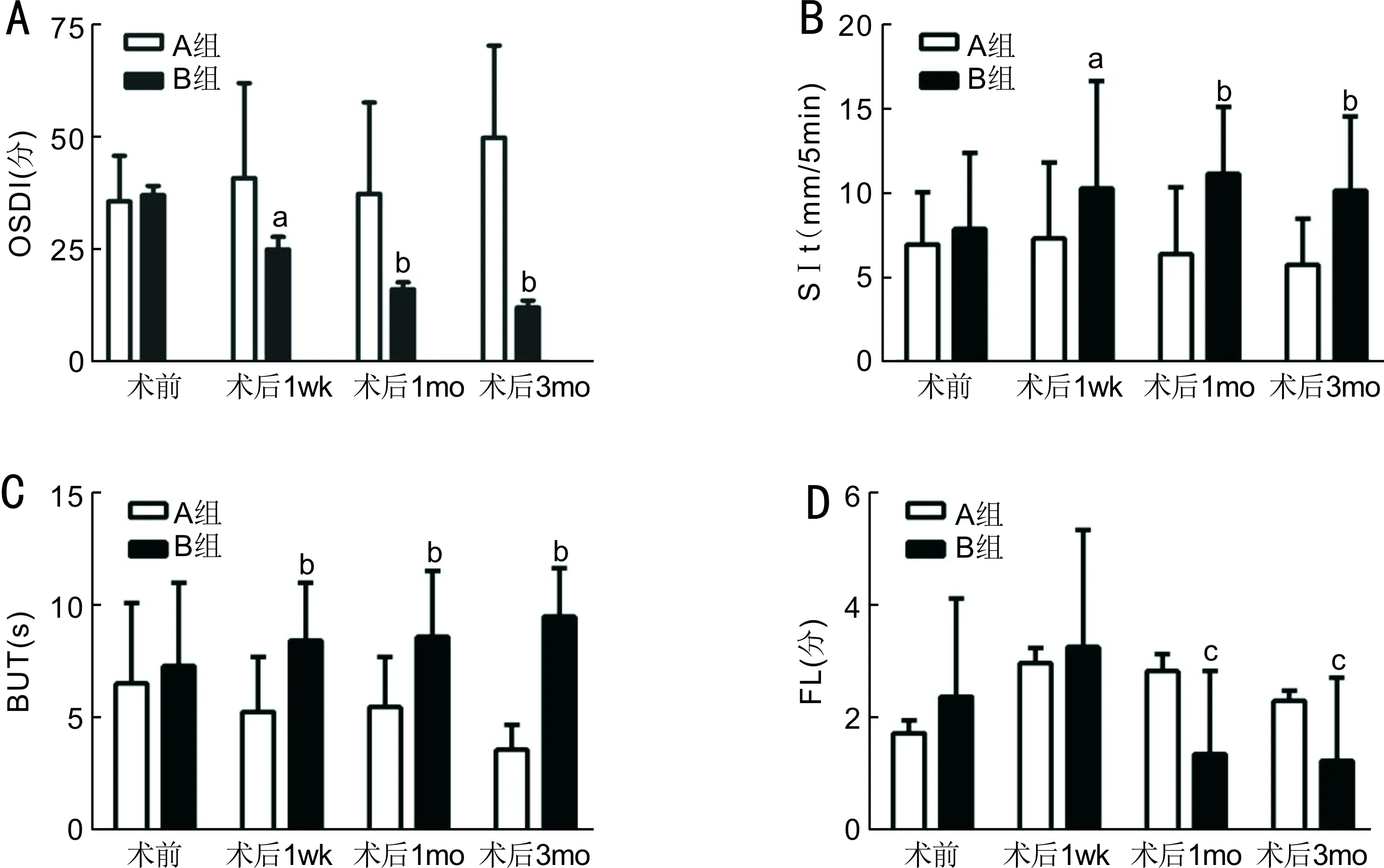
图1不同时间点两组OSDI、SⅠt、BUT、FL的比较A:OSDI;B:SⅠt;C:BUT;D:FL。aP<0.05,bP<0.01vsA组。
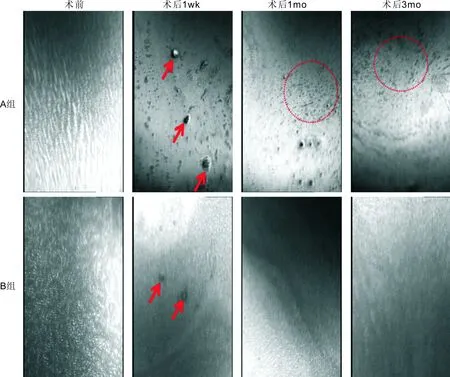
图2不同时间点两组典型角膜共聚焦泪膜图片(×400) A组术后不同时期可观察到脂质层断裂(红圈内),甚至缺失较术前加重,大量上皮细胞脱屑,残骸堆积(红箭头所示)。B组术后偶可见细胞脱屑散在(红箭头所示),泪膜断裂缺失现象明显好转。
2.5两组术前及术后不同时间角膜上皮细胞比较应用LSCM观察两组患眼术前表层上皮细胞(鳞状上皮细胞)大小显著不均,部分细胞边界模糊,上皮细胞脱失致细胞间形成片状暗区,细胞间碎屑状结构堆积呈“废墟状”,伴较多点状高反光物沉积,部分可在更深的细胞层观察到这些现象;翼状细胞形态不规则,大小不一,部分区域细胞结构不可见;基底细胞肿胀,边界模糊,反光减弱,细胞间排列较对照组疏松,细胞形态欠规则,大小不一,部分区域细胞结构不清。A组术后细胞结构破坏较术前更为严重,部分眼甚至无法获取图像进行上皮分层。B组术后部分表层上皮细胞呈鹅卵石状,排列仍较疏松,但细胞边界较术前清晰,细胞间夹杂有少量无结构的暗区及细胞碎屑;翼状细胞形态较前规则,呈小圆形或多边圆形;上皮基底细胞肿胀较轻,细胞大小基本一致,呈蜂窝状排列,随着术后时间延长细胞结构改善更明显。B组同一患者术前及术后1mo LSCM观察到的角膜上皮细胞结构见图3。
3讨论
干眼的发生与泪液分泌不足及泪膜蒸发升高有关,泪膜最深层黏液层是由杯状细胞分泌,玻璃体切除手术过程中巩膜外顶压、结膜切口甚至裂伤造成的结膜创伤会损伤杯状细胞,先前的研究已经显示这种手术对结膜形态的影响[14],我们的研究中所有纳入研究的患者均在术中没有发生结膜及角膜的异常损伤,采用同样的结膜、角膜切口及缝合方式,统一使用金属顶压器并进行全周顶压。前期的研究也证实PDR患者接受20G玻璃体切除手术后眼表异常及泪膜破坏加重,至术后3mo 仍无法恢复[8]。

图3角膜共聚焦显微镜下观察药物治疗组术前及术后1mo角膜上皮细胞变化术前表层上皮细胞肿胀,部分上皮细胞脱失,呈片状黑区,翼细胞层及基底细胞层形态异常,甚至不可见;术后1mo表层上皮细胞、翼状上皮细胞、基底上皮细胞形态均较术前规则。
目前对于糖尿病和非糖尿病患者干眼的治疗方法基本相同,至今仍没有统一标准,但是值得重视的是在DMDES治疗中局部滴眼剂造成的角膜上皮细胞损伤或副作用较没有糖尿病的干眼患者更为严重。局部应用皮质类固醇、环胞霉素等免疫抑制剂类药物可以减轻患者干眼症状及炎症反应[15],但是皮质类固醇药物的副作用如细菌或真菌感染、白内障形成[16]以及免疫抑制剂降低细胞的敏感度,导致上皮细胞溶解均有报道,因此更应慎重应用于DM患者。而自体血清滴眼液能够较为安全有效地治疗DES及持续存在的角膜上皮细胞损害[17],但存在无法保存、潜在的诱发二次感染的风险,因此对该药应用于DMDES患者形成限制。普拉洛芬、溴芬酸钠等非甾体类消炎药(nonsteroidal anti-inammatory drugs,NSAIDs)往往被临床应用来避免激素类药物的副作用[18],能够增加泪液分泌、抑制免疫反应,缓解炎症导致的杯状细胞破坏。玻璃酸钠滴眼液中含有多种成份,可以替代泪液中的有效成份,补充泪液,稀释眼表面的可溶性炎症介质、降低泪液渗透压,增加泪膜稳定性而改善干眼症状[19],其主要成份透明质酸钠是一种线性黏多糖,通过其羧基和极性基团吸附水份,延长泪膜破裂时间,增加泪膜厚度[20],同时玻璃酸钠可与纤维连接蛋白结合,从而促进上皮细胞的连接和伸展、创伤愈合,可有效缓解DES[21-22]、干燥综合征[23]、配戴角膜接触镜[24]、青光眼小梁切除术后[25]等各种原因所致的角结膜上皮损伤。另外,有研究报道玻璃酸钠具有一定的抗氧化作用,当与防腐剂同时使用时,能减少防腐剂所引起的毒性作用[26]。有研究显示玻璃酸钠滴眼液与非甾体类消炎药联合应用可发挥协同治疗干眼的作用[25,27-28],较单独使用玻璃酸钠滴眼液对干眼治疗更为有效[29]。本研究在90例因PDR行20G玻璃体切除患者中随机选取45例,术后在常规抗生素及非甾体类消炎眼药水的基础上给予1g/L玻璃酸钠滴眼液持续滴术眼,采用病例对照观察的方法进行比较。在我们的研究中,术后即使用玻璃酸钠滴眼液点眼的药物治疗组患眼尽管术前眼表相关指标与PDR对照组相比无统计学差异,但术后眼表改善更为明显,术后1wk药物治疗组眼表不适症状、泪膜破裂时间、泪液分泌量及脂质层均较PDR组改善明显,角膜活体荧光素着色至术后1、3mo较对照组显著减少,同时角膜上皮细胞结构也较PDR组改善。以上研究结果表明, 1g/L玻璃酸钠滴眼液能够降低PDR患者术后眼表不适症状,同时能够提高泪膜质量及泪液分泌量,促进眼表修复。遗憾的是,本研究未能监测观察糖化血红蛋白水平,同时限于目前的检查手段及设备所限,我们未能对PDR患者干眼的类型进行更进一步的检查及分类分析,还需要进一步更为深入的观察及研究。
近年来,DMDES发病率越来越高,在临床工作中除了重视高致盲性的糖尿病视网膜病变,也应该重视其最常见的并发症DMDES及玻璃体手术对糖尿病患者眼表的不良影响。分析以上研究结果可以得出结论,20G玻璃体切除术后在常规应用抗生素、皮质类固醇及非甾体类消炎药的基础上加用1g/L玻璃酸钠滴眼液能够明显改善PDR患者眼表不适的临床症状,增加泪液分泌,有效促进泪膜及角膜上皮层的修复,安全性较高。

