水合物研制、结构与性能及其在能源环境中的应用∗
朱金龙 赵予生 靳常青
1)(北京高压科学研究中心,北京 100094)
2)(南方科技大学物理系,深圳 518055)
3)(中国科学院物理研究所,北京 100190)
(2018年9月3日收到;2018年11月20日收到修改稿)
天然气水合物是与能源和环境相关的物质,可以进行甲烷等能源气体的存储和提取,也可以用于对二氧化碳等废气的封存.天然气水合物主要分为三种结构:sI,sII和sH,在本文中对其稳定性、水笼类型和大小以及可俘获气体进行了论述.中子衍射技术是研究水合物的重要手段之一,有着独特的优势.如中子的穿透性可以研究在高压状态下压力腔体内的大块样品;中子对于轻元素的敏感性可以很好地确定水合物当中的碳、氢、氧元素.通过中子衍射和非弹散射可以得到水合物中H/D原子的位置、各向异性振动因子、不同温度压力下的客体分子的水笼占据率、客体分子在水笼中的无序分布、原子核密度分布(通过最大熵方法);通过时间分辨中子,可以检测水合物形成及分解过程的热力学和动力学过程.而利用非弹中子可以得到气体分子平移和旋转振动模式以及分子的量子态转变.通过二氧化碳气体注入对天然气水合物的开采可以实现能源气体甲烷的开采和废气二氧化碳的水合物封存,在减小地质灾害和开采成本上有着独特的优势.
1 引 言
天然气水合物又叫可燃冰,储存在冻土层和300—600 m海底深处的沉积物中,被认为是一种清洁的新型能源.天然气水合物是由水分子通过氢键键合的多面体笼子和各种气体分子填充而形成的一种笼型结构,结构类型取决于水合物所处的压力、温度以及分子气体的类型.根据Villard规则[1],在常压下每个水笼只有一个气体分子填充的情况下,气体分子和H2O分子比例(R)约为1/6.天然气水合物在宇宙中普遍存在,如在地球的冻土层中,在海洋底层的沉积物中以及在外太阳系(木星、星云、气体巨型星的卫星等)中.图1给出了在全世界范围内冻土层和海底沉积物中已经探明和潜在的水合物矿藏区[2-4].水合物当中的能源气体包括甲烷、乙烷、丙烷和一些长碳链的分子气体,其中甲烷所占的比例达到了99.9%,是最常见的天然气水合物包裹气体和潜在的未来新型能源.原则上讲,在标准的温度和压力下,1 m3甲烷水合物可以存储高达164 m3的甲烷气体[5].从能源角度来讲,已探明的天然气水合物中存储的能源气体估计为1019m3,其能量当量是目前包括天然气、石油、煤和森林木材在内的能源的两倍之多;从环境角度来讲,如果天然气水合物矿藏所处位置的温度压力由于地质活动或者人类开采而发生突变的话,如压力突然减小或者温度突然升高,会放出大量的甲烷气体到大气当中,而甲烷气体的温室效应是二氧化碳的26倍之多,因而会加速温室效应和导致全球变暖.

图1 全世界范围内天然气水合物的分布,其中黄色的点是已探知的水合物矿藏,红色的点是可能水合物的矿藏,总共有90个归档的矿藏点(数据来源于参考文献[3,4])Fig.1.The global distributions of natural clathrates worldwide(there are totally 90 documented locations,and the data are from Ref.[3,4]).
经过十几年的勘探调查,我国先后在南海、东海、青藏高原等地发现了储量可观的天然气水合物矿藏.在全球油气工业面临资源劣化、环境复杂化和环保标准严格化的挑战下,天然气水合物这一较清洁的能源类型,正是技术创新需要攻克的主要难题.随着日本、加拿大和美国等在北极地区及我国和日本在海域对天然气水合物实验开发的成功,已经进入天然气水合物商业化开发研究阶段.天然气水合物的开发是一项复杂的系统工程,涉及地质、地球物理、化学、材料、生物、环境、机械工程等诸多领域.全球已有30多个国家对天然气水合物进行了勘查研究,美国、日本、韩国、印度等都制定了雄心勃勃的可燃冰开发计划.美国计划到2020年左右实现小规模实验性开发(2012年已在阿拉斯加进行了第一次试采),到2050年达到每年280亿m3的开发规模.虽然我国在天然气水合物研究方面起步相对较晚,但在天然气水合物的开采技术研究方面也已经进入试开发阶段,2017年我国成功在南海神狐海域(水深1266 m、海底以下203—277 m)试采天然气水合物,创造了持续产气时间最长、产气总量最大的世界纪录.
虽然天然气水合物在勘查和开发技术研究方面都取得了令人瞩目的成果,但是天然气水合物的基础研究相对滞后于开发技术研究,即使现在尚不能回答很多天然气水合物成藏和开发有关的基本问题.这些问题包括天然气水合物在沉积物中的结晶和生长、在沉积物孔隙中的存在形式、水合物形成分解对沉积物物性(渗透率、声波速度、热传导、导电等)的影响、天然气水合物开发过程中水合物的分解机理、释放出的气体在孔隙中的行为、生产系统中的气液多相流、水合物在储层沉积物和生产管柱中的二次生成等.这些问题在相当程度上制约了天然气水合物勘查和生产技术研发.围绕这些科学问题,需要对天然气水合物在高压环境下进行压力(P)-温度(T)*应力(σ)等复杂环境下的模拟与研究.而模拟该复杂渗流环境需要结合固体系统偏应力、液体围压压力、气体孔隙压力、高温/低温条件等,同时,需要在P-T-σ的环境中对水合物进行原位信号测量,进而深入了解天然气水合物的结构与热动力学属性.天然气水合物的研究,特别是开采可行性方面的研究,涵盖了力学、物理、化学、地质学等综合学科的交叉,需要在反应动力学特别是分解动力学方面实现模拟验证性实验.在物质结构的研究中,中子不带电,可以穿透物质而没有破坏性,从而给出物质体相的内力场信息(如应力);中子与原子核的作用并不随原子序数发生有规律的变化,从而可以通过中子散射或成像技术更好地分辨轻元素和相邻的元素;中子衍射具有高的穿透性,可以在特殊的实验环境如高压、低温、强场和不同环境下测试和研究,不仅可用于探索物质的静态微观结构,还可以用于物质动力学过程的研究.因而中子本身特性,对天然气水合物安全高效的开发有着独特的优势,也是必不可少的重要和关键的手段.
通常来讲,水合物中水笼的构型是两个水分子之间通过一个氢原子和氧原子形成氢键而构成的笼状结构;而分子大小尺寸合适便可以被装到笼子当中,并在合适的温度和压力条件下完成气体分子的包覆过程.取决于形成的水笼的构型和连接方式,天然气水合物主要可以形成以下3种不同的晶体结构:结构I(后面用sI表示,空间群为Pm¯3n),结构II(后面用sII表示,空间群为Fd¯3m)和结构H(后面用sH表示,空间群为P6/mmm),如图2所示.

图2 水合物3种主要结构的示意图 512代表12个五元环形成的水笼,51262代表12个五元环和两个六元环组成的水笼(图片来源于文献[6])Fig.2.Three main crystal structures of clathrate hydrates.512means the pentagonal dodecahedra cages and 51262(tetradecahedron)indicates a water cage composed of 12 pentagonal and 2 hexagonal faces.The numbers in squares indicate the number of cage types.The figure is cited from Ref.[6].
sI型水合物的空间群是Pm¯3n,立方结构,晶胞长度约为12 Å,体积约为1700 Å3.理想的单胞组成可以表示为2D·6 T·46 H2O,其中D和T分别代表512和51262笼子,因而其理想的化学计量比分子式为X·5.75 H2O(X为水笼中的气体分子).在气体分子过大而不能装载进小水笼当中时,理想的组分就会变成X·7.67 H2O,此时只有大水笼被占据.可以形成sI型水合物气体分子的尺寸处于4.3和5.3 Å之间,如CH4,CO2,H2S和Xe气体[1].在单胞里面的两个512水笼分别由20个水分子构成,笼子中心到面的距离为4.2 Å[7];51262笼子之间通过六角面相互连接起来形成空间网状结构.从晶体学角度来讲,水分子中的氧原子分布在3个非等价的位置,氢原子占据6个非等价的位置.形成512水笼的水分子的构型与自由水或者Ih六相冰稍微不同.例如,水笼当中O-O-O的夹角和六方冰Ih的四面体夹角相差1.5◦,和自由水当中的夹角相差3.5◦[8].
sII型水合物的晶体结构也是立方的,但其空间群是Fd¯3m,晶胞参数为17 Å,体积为4900 Å3.在一个单胞中有136个水分子,包含16个512水笼和8个51264水笼[7].如果每个水笼被一个分子气体所占据,那么其化学式就可以写成X·5.66 H2O;如果只有大笼子被单分子占据的话,化学式为X·17H2O.在sI和sII型中的512水笼构型上没有大的区别,只是sI结构中的水笼平均半径为3.95 Å,sII结构中的平均半径为3.91 Å.由于512水笼中氧原子处在4个不同的晶体结构点位上,因此512水笼是水合物笼子中偏离球形最多的笼子,呈椭球状.sII结构中由28个水分子构成的51264水笼由于包含着4个六角面,因而其可以装下的分子可以达到6.6 Å.在sII型水合物的单胞里面,512水笼通过共享五边形面在[110]方向链状排布,而大水笼的中心有着金刚石原子排布的构型.大笼子之间按照这种排布方式共享六角面,在大水笼之外的孔隙处形成512水笼.
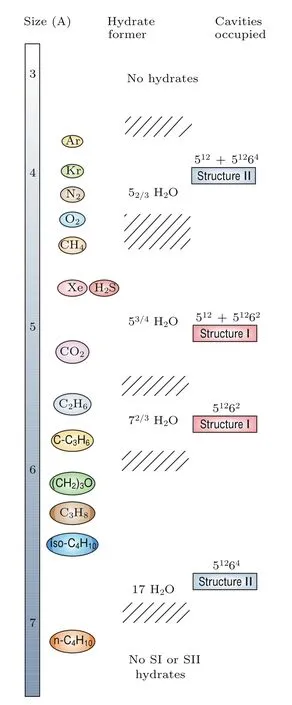
图3 客体分子尺寸和包裹水笼大小之间的关系(图引自文献[6])Fig.3.Relationship of guest molecules versus cage size ranges.Along the line is the sizes(in Å)of the guest molecules in hydrates.The figure is cited from Ref.[6].
如果考虑到外太空的水合物,第三种水合物结构sH[9,10]就会进入到我们的视线.sH水合物是空间群P6/mmm的六方结构,晶胞参数为a≈12.3 Å,c≈9.9 Å,体积V≈1300 Å3.每个单胞中的3个512水笼的构型和sI/sII结构水合物当中的类似.sH结构中的435663水笼会稍微复杂些,具体如图2所示.在该结构中,最大的笼子为51268笼子,可以装下直径大于7 Å的气体分子.sH结构最初被认为只有在大分子和小分子气体混合的情况下才能存在.随着实验的进展,特别是在1 GPa的压力上发现了sH结构水合物,暗示在冰川当中会大量的存在.当所有水笼被填满后,理想的组分为X·3.5H2O.
在3种水合物中,水笼的大小可以从3.9 Å到大于7 Å分布,因而有超过130种化合物可以和水形成水合物[11].原则上讲,分子尺寸小于3.5 Å或大于7.5 Å是进不到sI和sII的水笼当中的[8].图3给出了不同尺寸的气体分子及对应形成的水合物结构.客体分子种类可以是一个原子或者分子,并且其大小是决定形成水合物的重要参数.客体分子极性带来的偶极距的相互作用会对水合物的形成动力学产生微弱的影响.客体分子和主体水笼之间通过范德瓦耳斯力相互作用形成稳定的水合物结构.
2 水合物的中子表征
由于水合物主要由C,H,O等轻元素组成,并且要在一定的压力下稳定或者合成,因而中子衍射是研究水合物热力学和动力学、确定氢原子位置以及客体分子在水笼中无序分布的有力手段,被证明为研究水合物的理想技术.通过中子衍射可以确定特定温度和压力下的水框架结构以及水笼中的分子占据率.作为最轻的元素,氢原子只有一个电子,因而有着最弱的X光散射截面.而中子的散射强弱不随着元素序数单向变化,因而对于轻元素的位置更加敏感(图4),是研究水合物的重要手段.除此之外,中子有着非常强的穿透性,可以研究在高压腔体内的水合物样品,表征水合物中能源气体分子的摄取和释放的过程,并研究客体分子和水笼的相互作用[11,12].下面将详细介绍水合物研究的实验站、样品环境以及数据处理方法.
2.1 中子衍射实验站
原则上讲,中子线站只要有足够的空间和准直系统,并且具备相应的高压环境,就可以从事高压中子水合物的研究.下面介绍原位做水合物研究的几个代表性的中子线站.如图5所示,包括洛斯阿拉莫斯中子散射中心的HIPPO(high pressure,preferred orientation),橡树岭国家实验室的散裂中子中心的SNAP(spallation neutrons and pressure diffractometer)和欧洲的Institute Laue-Langevin的高强度两轴谱仪D20等.

图4 原子序数和中子散射截面的关系,右图给出的是中子与X光散射长度b的比较(图引自文献[11])Fig.4.Atom number and the neutron scattering length amplitude relationship.Right figure shows the comparison of atomic number dependence vs.scattering length,b for X-rays and neutrons.The figure is cited from Ref.[11].
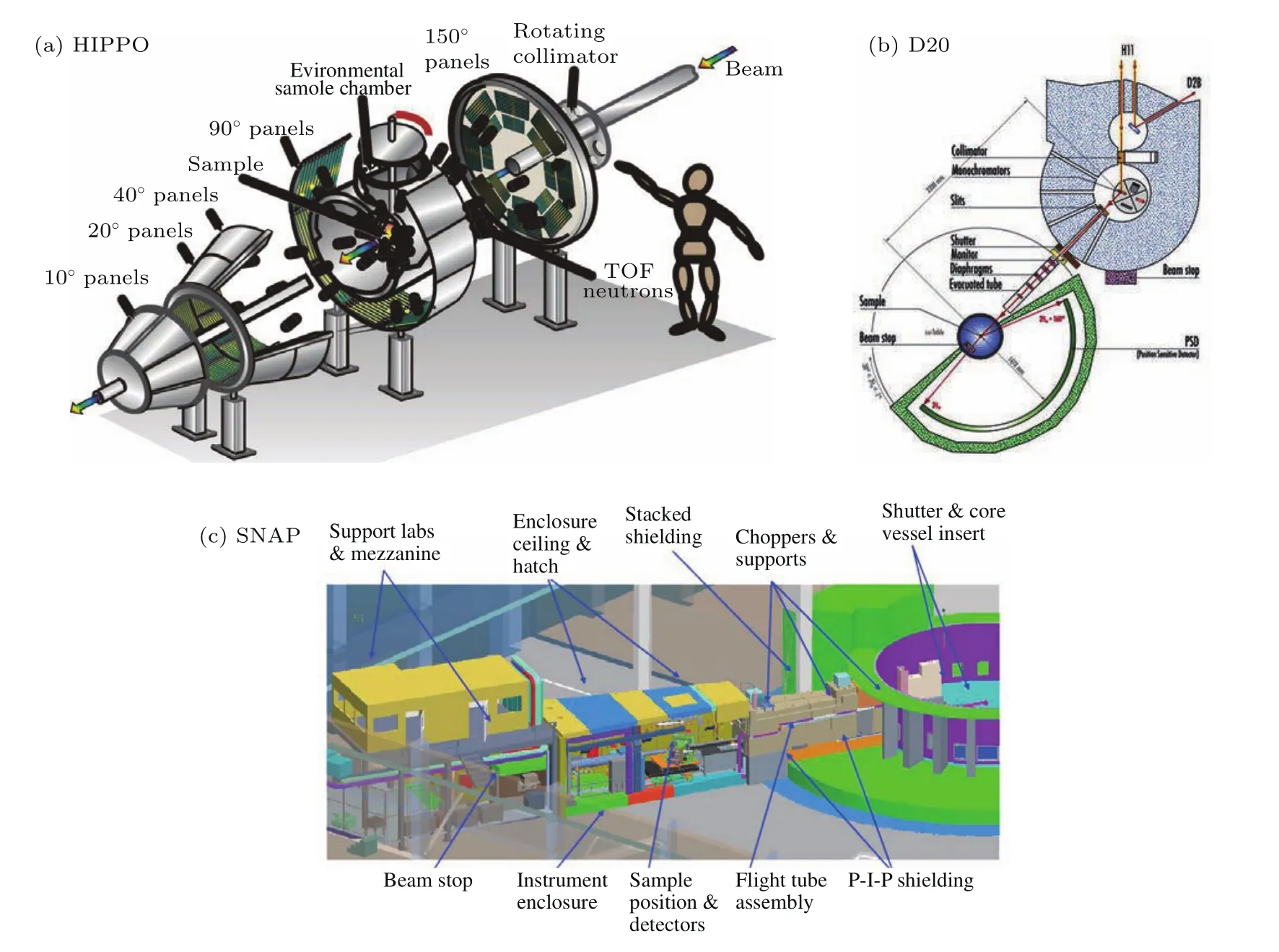
图5 HIPPO,D20和SNAP中子线站的示意图 图片来源于洛斯阿拉莫斯中子中心,ILL和橡树岭散裂中子源Fig.5.Schematic draws of the HIPPO,D20,SNAP neutron beam lines( figures supplied by LANSCE-Lujan Center,ILL and SNS).
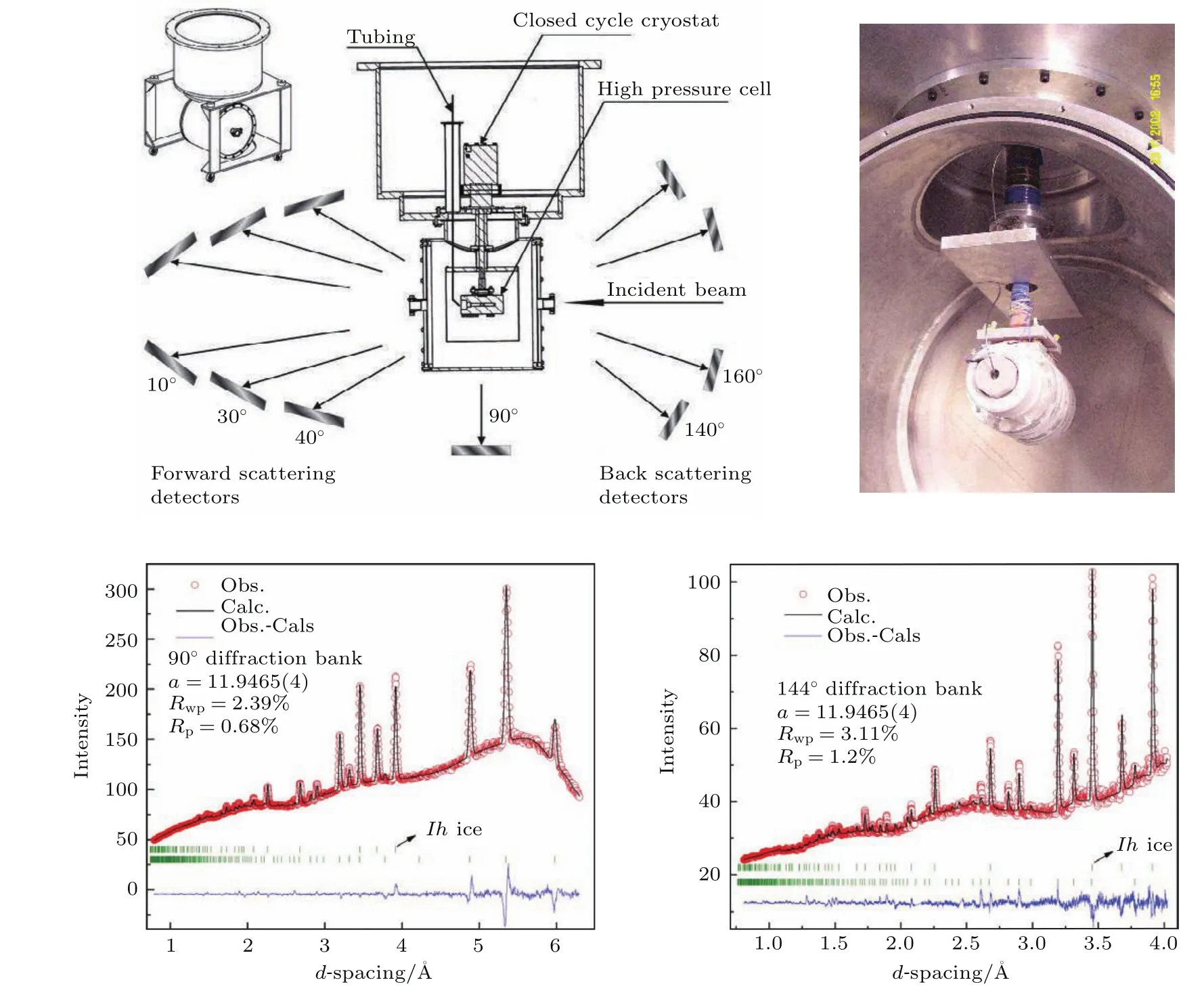
图6 HIPPO实验站的高压低温水合物合成和衍射装置(左上),高压样品腔在低温状态(右上)以及不同角度探测器得到的水合物样品的衍射图Fig.6.Schematic general view(top left corner)and the enlarged section view of the setup designed for high-pressure,low-temperature hydrostatic experiments at HIPPO,LANSCE[13];top right panel is the photo of internal cell at liquid nitrogen temperatures attached to the closed cycle cryostat;lower panel are the representative neutron diffraction patterns of sI methane clathrate at 100 bar and 100 K(2θ=90◦∆d/d∼ 0.01,and 144.45◦,∆d/d∼0.005).
天然气水合物样品可以在低温状态(如液氮温度以下)保存在常压环境中.为了研究水合物的形成、分解动力学和热力学过程以及水合物的相图,必须要在高压的条件下做原位表征.根据压力的不同,水合物的高压腔体材料可以是金属钒(200 bar,at HIPPO,NPDF of LANSCE-LC),铝合金(6000 bar at HIPPO,4500 bar at ISIS)以及钛锆合金(1000 bar at NPDF of LANSCE-LC,5600 bar at ISIS)[13,16].图6给出了HIPPO实验站进行水合物研究的设备和实验方案.
2.2 中子衍射水合物表征
一条高质量的水合物中子衍射谱,除了可以提供晶体结构参数以外,还可以给出以下信息:确切的H/D原子的位置以及C,H,O的各向异性的温度因子;不同温度压力下客体分子在各个水笼中的占据率[12-31];气体分子在水笼中的无序分布以及通过最大熵的方法(maximum entropy model,MEM)[32,33]测定原子的密度分布[34-37];热力学及动力学过程[38-43].在水合物中,水笼的水分子由于无序的取向可以有6种可能的排列,而水分子中的H/D原子位置一般采用Pauling的半氢占据模型[44].图7给出了典型的512和51262水笼在无序和有序下的示意图.D原子的各向异性位移是由于在不同氢键环境下横向和纵向振动[24]引起的水分子的无序引起的.通过氢原子位置的确定可以得到氢氧的键长、键角以及不同水分子中氧原子和氢之间形成氢键的强弱,进而可以评估形成水合物结构的稳定性.例如,形成氢键的氧和氢之间的距离会随着氢键的增强而变大,可以用来确定水分子在不同分子纬度构型中的协同成键效应[24,45].

图7 (a)512和51262水笼中D原子无序排列;(b)3个独特水分子的各向异性热振动椭球面;(c)理论计算给出的512和51262水笼中氢原子的有序排列(图7(a)和(b)来源于文献[24])Fig.7.(a)The 512and 51262cages with D atoms in disordered positions;(b)the con figurations of the three unique water molecules showing the anisotropic ellipsoid surface;(c)the ordered hydrogen position con figuration of 512and 51262cages in theoretical calculation for comparison.Figure(a)and(b)were from Ref.[24].
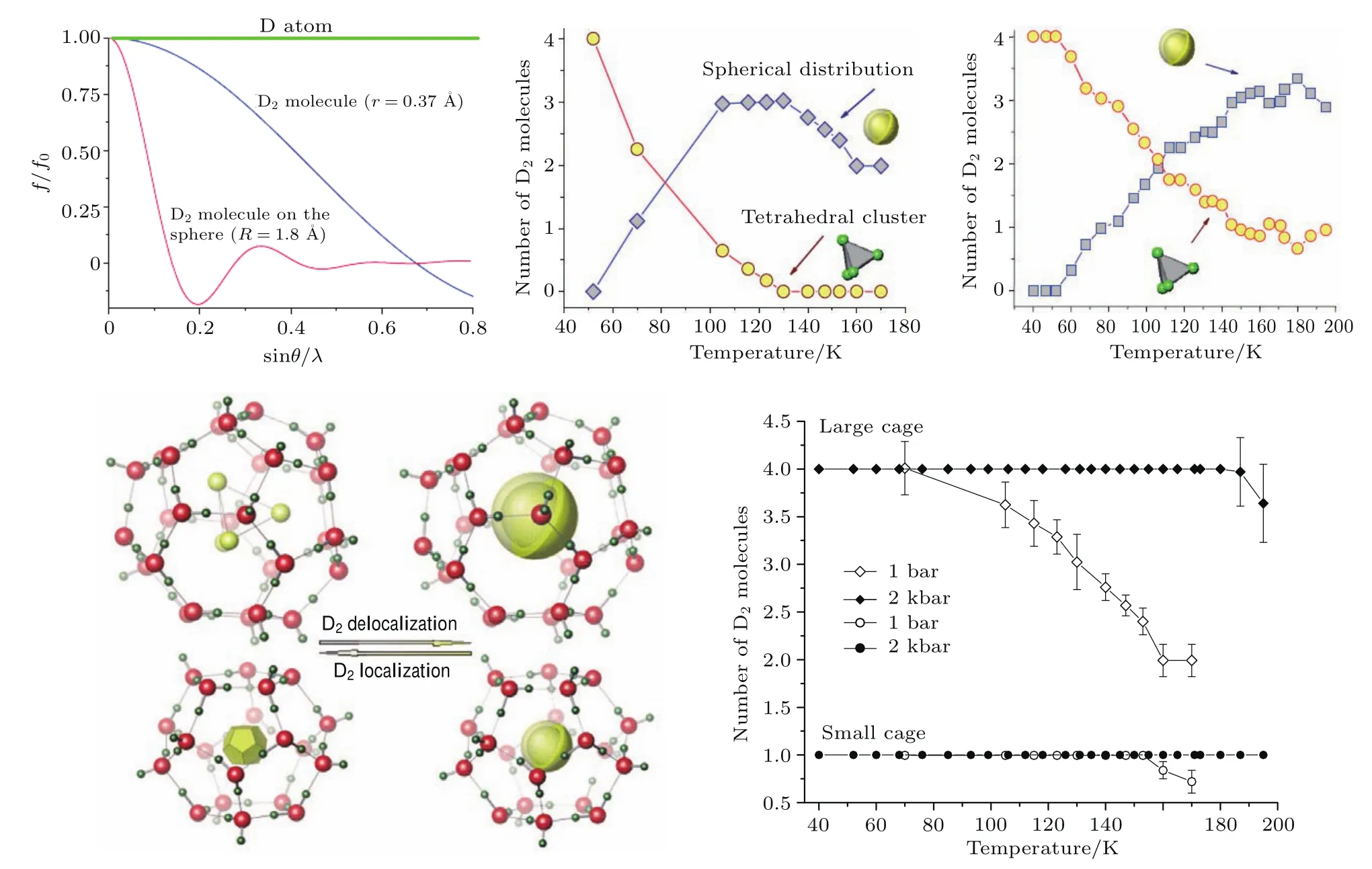
图8 氢气水合物的结构确定,包括D2分子的散射模型、氢分子在水笼中的位置、通过局域化和去局域化模型的线性组合得到在不同温压下的水笼占据率;大水笼中的氢分子占据率在2—4个之间,小水笼在2 kbar压力之前都是单分子占据(图片来源于文献[14])Fig.8.Hydrogen clathrate structural determination,including D2molecular scattering models,re finement of hydrogen molecules in cages,such as linear combination of localized and delocalized models in 51262cages and variation of hydrogen occupancy in the clathrate as functions of temperature and pressure.The large cage occupancy varies between 2 and 4 hydrogen molecules and single occupancy of the small cage at pressure up to 2 kbar.Detailed information can be found in Ref.[14].
通过时间分辨的水笼在不同压力和温度下的占据率可以监测水合物形成和分解的动力学过程[12-31,38-43].水合物研究的一个方向就是研究氢气水合物以及水合物储氢的能力.Wendy等[18]指出氢气水合物的水笼是多重占据的,512水笼可以容纳两个氢,51262水笼中可以放4个氢分子.之后,Konstantin等[14]估算出水合物储氢能力能达到3.77 wt%.通过中子衍射实验给出了氢气水合物的具体结构、温度压力下的水笼占据率,特别给出了在不同温度下氢气在水笼中局域化和非局域化的具体模型(图8).
Kuhs研究组在水合物对不同气体分子的包覆方面做了大量系统的研究,如甲烷水合物、氮气水合物、二氧化碳水合物、氧气水合物和空气水合物等[19,23,29].这些水合物的水笼填充比率通过中子实验来表征,并且和范德瓦耳斯/Platteeuw统计热力学理论以及蒙特卡罗分子动力学模拟来进行比较印证.可以预想,高压下气体有着更高的渗透率,因而会增加水笼的填充概率.然而理论模拟[46-49]和实验结果符合得并不好,暗示着实际情况更加复杂,需要理论模型的进一步完善,如考虑大水笼的双占据状态、实际样品的孔隙率等.中子衍射有可能是探测和定性定量表征水合物相稳定或者亚稳性能的最好的方法[19],可提供精确的参数来改进理论模型.

图9 水合物选定区域的2D衍射图谱(左)以及3个不同样品随着时间的变化不同相的比例变化:氘代冰(?),sII水合物(N),D2O water氘代水(•)(图来自文献[39])Fig.9.2D diffraction patterns of selected region,and phase fraction versus time for three different samples.Symbols:D2O ice(?),sII hydrate(N),D2O water(•).Graphs are from Ref.[39].
通过时间分辨的中子衍射来监测水合物生成和分解过程,可以清楚地理解在不同温度压力下水合物的形位变化,为水合物实际开采提供有效的策略.更为重要的是水合物所处的水文地质条件相当复杂,并且经常是处在多相混合的状态,因而其开采过程很难被预测.而通过大块样品或者实际取样样品在模拟开采条件下进行中子实验有助于理解实际开采过程中的种种问题[43].如图9所示,考虑到二氧化碳水合物和甲烷水合物的稳定区间,可以使用二氧化碳气体注入开采甲烷水合物的方式来实现废气的存储和能源甲烷气体开采的双重目标,这将在最后一个章节进行综合论述.Staykova等[41]指出甲烷水合物和二氧化碳水合物会在气体和冰的界面处生长,并通过时间分辨的中子实验验证了二氧化碳水合物比甲烷水合物的生长速度要快很多,在二者气体有着相似的渗透率和相同的外压力下大概要快3倍,图10给出了不同温度、压力和尺寸下甲烷和二氧化碳水合物的反应动力学.2012年,阿拉斯加的二氧化碳注入水合物开采计划利用原位实验来对开采过程中的参数进行了进一步的模拟.尽管大多数水合物的热稳定相都被比较精确地表征,但是水合物的亚稳定相的研究还是相对较少,特别是在高应力下水合物亚稳相的形成有着特定的实际意义[50-52].除此之外,中子实验还可以追踪到水合物相变过程,特别是水合物相变过程中的中间相,这也是水合物研究的一个前沿科学问题.该研究可以为水合物初步形成过程中的水笼生长和组合提供新的证据和观点.
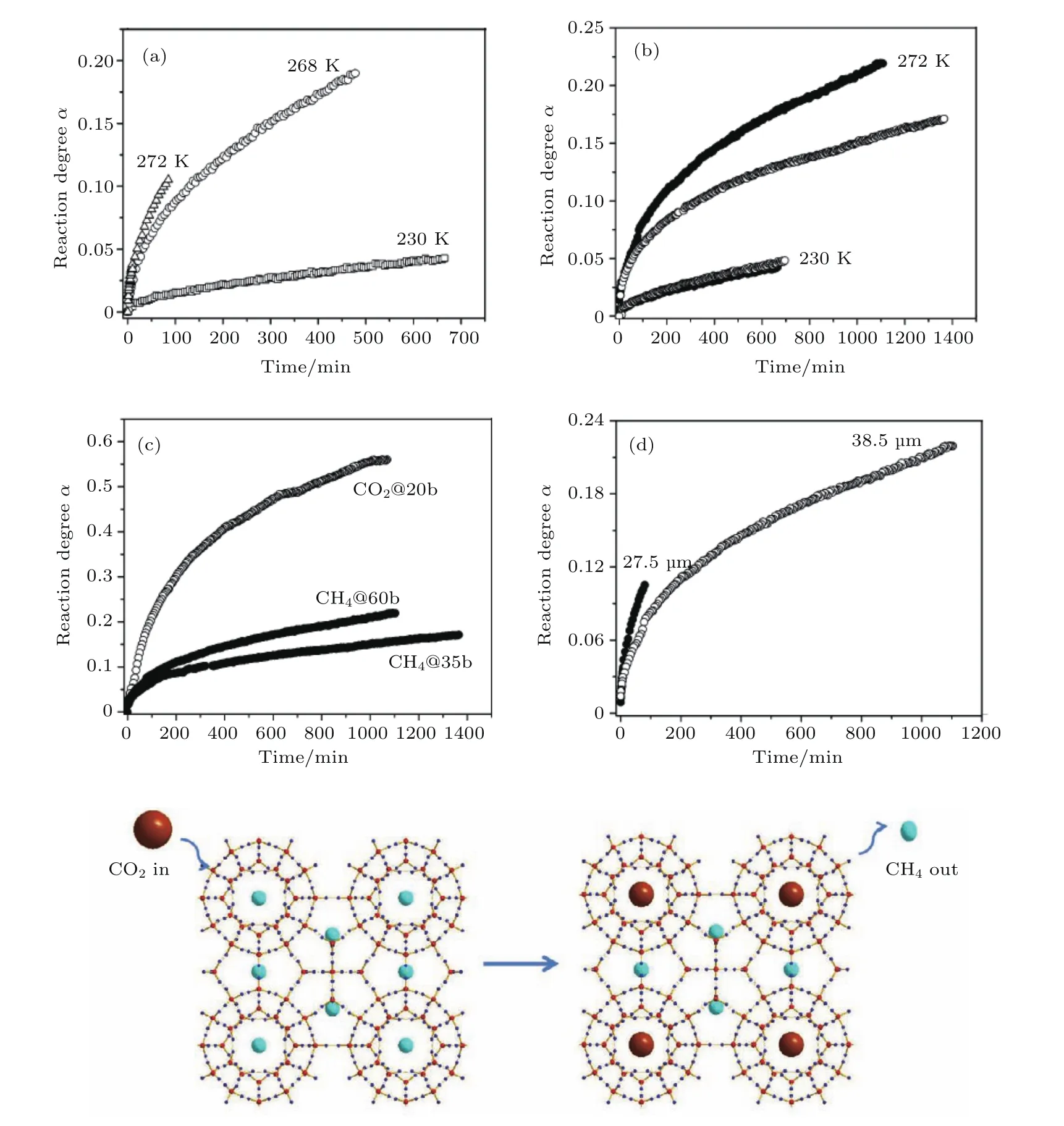
图10 甲烷和二氧化碳水合物反应速率随着温度、压力和尺寸变化的关系;通过示意图给出了CO2取代水合物的过程[41](数据来自参考文献[41])Fig.10.Up panel:temperature,pressure,and size dependency of the reaction kinetics of CH4and CO2 clathrates;lower panel:schematic show of CH4substitution of CO2molecules in the clathrate.Data are from Ref.[41].

图11 (a)TMO(trimethylene oxide)分子在sI型水合物大笼子当中的所有可能位置,温度为173 K[53];(b)NH(neohexane)水合物在sH结构51268水笼中的分布[55];(c)通过不同的无序模型得到氮气水合物中子衍射图谱解析后的气体分布[30];(d)通过分子动力学得到的一氧化碳分子在512水笼中的分布,温度为220 K[54];(e)在sI对称性限定下,二氧化碳分子在512水笼和51262水笼中的分布[55]Fig.11.(a)Trimethylene oxide(TMO)molecule in the large cage of sI clathrate for all allowed positions at 173 K[53];(b)view of hydrates of neohexane(NH)molecules in the structure H large(51268)cage[55];(c)different molecule disordered models using convergence criteria of the re fined neutron diffraction data of N2clathrate[30];(d)the distribution of the CO molecule at different times in the 512cage of sI clathrate at 220 K from molecular dynamic simulation[54];(e)CO2molecules distribution with full symmetry shown in 512cage and 51262cage of sI clathrate hydrate[55].
由于水合物的水笼和内部的包裹气体是通过弱的范德瓦耳斯力相互作用结合在一起,因而气体分子在水笼中的分布处在一个无序的状态.图11总结了在不同水合物笼子中气体的无序分布.对水合物进行单晶样品的衍射是最理想的情况,但实际上很难获得足够大的单晶样品进行中子实验,小块单晶的X光衍射被认为是解决水合物晶体结构和客体分子有序度的第二好的方法[53].例如氧杂环丁烷(TMO)和环氧乙烷(EO)的sI水合物晶体结构和动态信息可通过单晶X射线技术得到进一步的改善,并且可以建立起和这些结构相关的动力学模型来解释2H的NMR数据.而分子动力学是模拟客体分子在水笼中轨迹[54]的有效方式,可以验证Rietveld精修的结果.例如结合分子动力学和中子衍射,Chazallon等[30]通过这两种方式得到了水笼中氮气的分布并进行比较(图11(c)).对水笼中的气体分子无序的正确描述是得到不同压力下水笼填充比例、水合物形成及分解动力学热力学的基本前提.
对于主客体相互作用材料体系,在这里是水合物体系[55],有效描述的另外一种方法是直接空间法[56-58].直接空间法是确定气体分子分布的最有效的方法之一,并且和气体在水笼中的初始位置无关.而通过刚体方法对气体分子以及水分子进行限定可以减少精修的参数,一定程度上克服数据质量不佳或者X光对轻原子不敏感等情形.

图12 氘代Xe气水合物在10 K下的中子衍射图谱和核密度分布图[37];右上是甲烷水合物[34]在7 K及右下二氧化碳水合物[35]在10 K下的核密度分布图Fig.12.Neutron diffraction pattern and nuclear density distribution map of Xe deuteron-hydrate at 10 K[37],nuclear density distribution map of methane clathrate[34]at 7 K and of CO2clathrate at 10 K[35].
由于中子衍射图谱采集在分钟和小时量级,因此给出的是水合物在一定时间范围内分子的平均分布和无序状态,因而是结构模型的一个最佳近似.尽管如此,通过高质量中子衍射数据的精修(大的d空间的覆盖以及高分辨)结合MEM(最大熵方法)可以给出水合物的核密度分布[32-37],如图12所示,因此可以直观地给出客体分子在不同温度和压力下的3D分布图.例如,在洛斯阿拉莫斯中子中心的HIPPO实验站有着5个不同角度的中子探测器可以实现大的d空间的覆盖(0.5—10.5 Å),可以结合高角度衍射的高分辨率将一些靠近的峰给分辨出来.通过这样的数据可以获得精确的傅里叶转换下的图,再得到精确的初始原子位置,进而获得准确的3D核密度分布图.
2.3 中子非弹散射水合物研究
通过非弹中子散射对水合物的研究[59-67]可以给出主客体之间的相互作用和低频动力学,如分子动力学、非简谐振动、主客体振动的耦合、客体分子气体的高频拉伸振动以及水笼的稳定性[59].但是非弹中子散射只能提供水合物晶格动力学等有限信息.非弹中子散射的动量传输,与中子的初始和最终能量相关,因此在小动量传输时只有少量的能量传输[68].通过非弹中子研究的水合物包括甲烷、氢气、氮气、氧气、氩气、氖气水合物等.
3 水合物的开采
如上文所述,天然气水合物处在特定的温度压力条件下,其开采的方法可以通过改变水合物所处环境的温度、压力来打破水合物相平衡,从而分解释放天然气,达到开采的目的.因而天然气水合物的开采主要分为热激发法、降压法、化学试剂法及CO2-CH4置换法.美国、日本、俄罗斯和中国都在水合物开采方面有着不同的进展.去年中国首次海域天然气水合物(可燃冰)试采成功,这标志着中国成为全球第一个实现了在海域可燃冰试开采中获得连续稳定产气的国家——连续产气60天,累计30万立方米.而试采成功只是万里长征迈出的关键一步,要想实现商业化安全开采,后续任务繁重——诸多关键基础科学问题亟需解决.气体水合物通常处于极端复杂的水文地质环境中,且分散存在于沉积物孔隙内.可燃冰开发是一个高压渗流问题,跨越微观、介观与宏观等多个尺度(图13).

图13 天然气水合物开采涉及的不同层面的问题,从上到下为宏观-介观-微观Fig.13.Different scale of nature clathrate exploration,from continuum scale(10 cm–100 m)to pore scale(10 nm–10 cm),and down to nano-scale(<10 nm).
如果开采不当,也没有采取适当措施,可能会诱发地层结构失稳,探井坍塌,甚至引起大规模海底滑坡;大量甲烷的释放可以加速全球变暖,因为温室效应方面甲烷远远高于二氧化碳;如果大气中甲烷含量过高,严重的可以引起生物群体灭绝(图14).
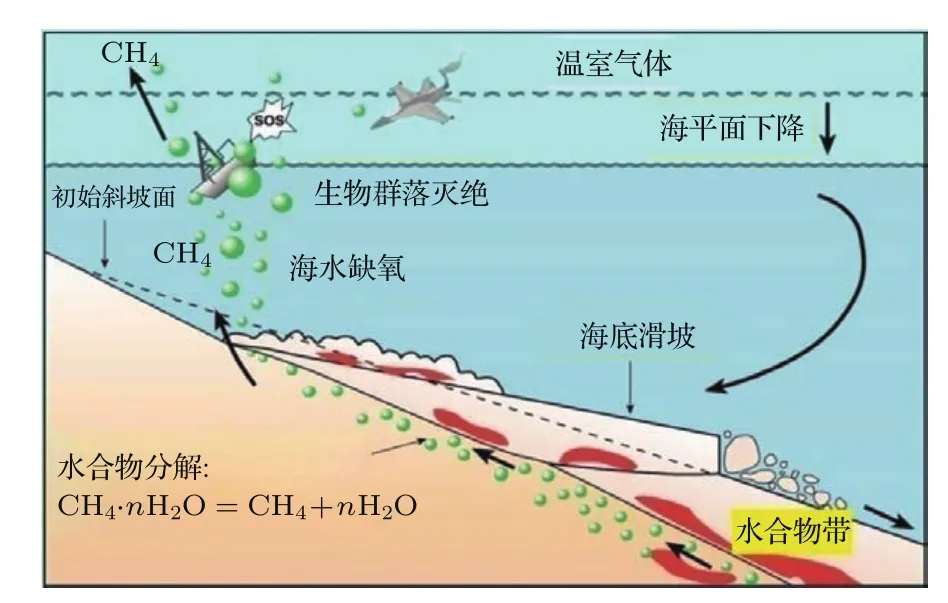
图14 天然气水合物开采不当带来的危害Fig.14.Potential hazards of decomposition of natural clathrates.
在天然气水合物的开采方法中,我们将详细介绍二氧化碳置换法水合物开采(图15)[69].二氧化碳置换法可以实现能源甲烷气体的开采以及废气CO2的水合物封存两个目的,而且实验和理论上证实,该过程在热力学和动力学上是可以自发进行的.在置换开采过程中,由于形成二氧化碳水合物,不会导致大量天然气水合物的分解,保持了地质力学稳定,进而避免了山体滑坡、地震海啸等地质灾害.

图15 二氧化碳注入天然气水合物开采的示意图Fig.15.Schematic show of the concept of gas exchange in natural clathrates.
Ohgaki等[70]第一次实验证实了水合物成藏中二氧化碳置换甲烷的可行性,而对于实际开采,在多孔介质中取代的可能性也进一步得到实验的证实[71],另外还需要考虑水合物中气体分子取代效率和速率问题.在目前的实验中,对二氧化碳甲烷水合物的取代大多是通过宏观物理量的测量来表征整个取代过程,而对于取代的微观机理也大多来自于理论上的模拟,没有实验上的证据.如通过MRI(磁共振成像)和气体渗透率等手段,Ersland等[72]对砂岩介孔当中的水合物CO2取代研究发现该过程的自发进行,暗示在该过程中有甲烷水合物的分解;Jung等[73]通过置换过程中电阻率和硬度的表征,发现取代过程没有明显的硬度改变,但是水合物是否分解没有明确的结论;Ota等[74]通过拉曼光谱确定CO2置换过程中的水合物分解,并指出在取代过程中,CO2取代大水笼的速率要远远高于取代小水笼的速率;Stevens等[75]通过MRI监测了甲烷水合物的生成,并发现在CO2替换过程中没有监测到自由水的生成,但是也排除不了在MRI分辨极限外小范围内的水笼分解和水合物再生成.
对于CO2取代甲烷水合物的普遍共识分为两个步骤:第1步是CO2气体和表面水合物直接接触进行取代,该过程动力学比较快;第2步是进一步的取代,需要CO2气体有一定的渗透率进入水合物的内部对深层的甲烷气体进行取代.因而第2步是决定水合物最终取代效率和整体取代速率的关键步骤.通过上面的工作陈述发现在取代过程中的微观机理并没有得到明确的证明.特别是第1步的过程中是否存在着水合物的分解和再生成,是否会改变表面水合物的形貌而阻止CO2的进一步扩散,进而阻止CO2的进一步取代.Bai等[76]通过分子动力学模拟认为在第二个阶段界面处的甲烷水合物首先是分解,之后在表面处生成了非晶状态的CO2水合物阻止了CO2的进一步扩散,而Geng等[77]也通过分子动力学给出了取代过程中的水合物的二次生成;Schicks等[78]认为取代过程在分子层面上有水合物的分解和生成,而Ota的进一步工作[79]也认为在取代过程中存在分解,并且和水分子的重新排列相关联.除此之外,他们还进一步研究了饱和液体CO2在分子层面与表面水合物的分解.Qi等[80]通过分子动力学给出在取代过程中水合物并不发生分解而是水笼发生了瞬态的破裂;Tung等[81]进一步给出了水合物中CH4和CO2单个水笼瞬态占据过程.
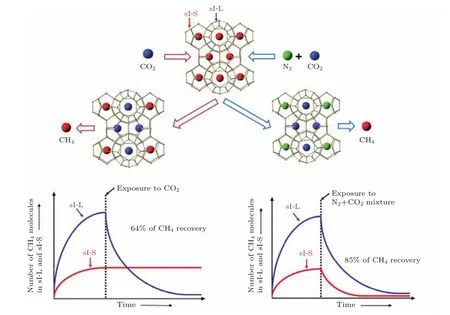
图16 CO2/N2混合气体注入提取甲烷 单独通过CO2气体取代,单独取代sI结构的大水笼,CH4气体的取代效率为64%;通过CO2/N2混合气体取代可以同时取代大水笼和小水笼,因而可以大大提高取代效率Fig.16.Improvement in CH4recovery yield by using CO2+N2mixture.When CO2is solely injected into CH4 hydrate,a maximum 64%CH4recovery yield is anticipated because CH4molecules in 51262(sI-L)cages are mainly recoverable(left).On the other hand,when N2is added,the distinct roles of N2and CO2remarkably enhance CH4 recovery yield(right).
为了进一步提高CO2的取代速率,用N2/CO2混合气体来取代纯的CO2气体进行注入是一个有效的办法.前面提到CO2更倾向于取代大水笼中的甲烷气体,而CO2气体进入小水笼的话需要512小水笼发生较大的扭曲,因而需要较多的能量.而N2气本身可以形成水合物,其分子大小和CH4大小接近,因而可以相对容易地取代sI型水合物512水笼中的甲烷气体.因此,在没有水合物分解的气体取代交换过程中,CO2和N2气体的相互补充作用可以大大提高甲烷的取代效率.在这个推论的基础上,Park等[82]证明在无水条件下用CO2和N2混合气体取代甲烷水合物可以得到85%的取代效率(图16).Liu等[83]进行了相关的实验,并证实N2/CO2混合气体确实可以提高取代速率,但是通过声波监测发现,无论是纯的CO2取代还是N2/CO2混合气体取代,都会造成沉积层硬度的下降,特别是含有N2气的混合气体.
除此之外,CO2注入取代甲烷水合物也可以和减压法相结合,来进一步提高甲烷的产率.Zhao等[84]结合了这两种方法.在CO2注入的第1个阶段,CO2气体和表面的水合物可以很快地反应;当进入到第二个阶段,由于表层水合物对CO2气体传输路径的阻挡,降低CO2的传输和扩散,因而大大降低了取代速率.而此时通过降压法可以使部分甲烷水合物得到分解,提供CO2进一步扩散到内层水合物的路径,进而可以促进进一步的取代,提高甲烷的产率.
4 结论和展望
总而言之,可燃冰作为21世纪最具有价值的能源之一,受到世界各国的瞩目.通过分析可燃冰的结构、实验表征技术以及开采方法和困难,可以对水合物研究有一个整体的掌控.目前中国在可燃冰的开采上取得了长足的进步,对推动能源生产和消费革命具有重要而深远的影响.而我们需要建立大型的包括中子技术在内的实验平台和大科学装置,来全面深入系统地研究在不同水文地质条件下的水合物成藏稳定性和开采技术;通过大量的实验数据和理论模拟来为实际的勘查开采提供保障支持.向地球深部进军,依靠科技进步,保护海洋生态,促进天然气水合物勘查开采产业化进程.
感谢美国能源部支持的洛斯阿拉莫斯实验室的中子散射中心提供部分实验数据.

