SrBPO5∶Ho3+荧光粉的制备、性能及第一性原理计算
姜吉琼,邹正光,李延伟
(1.桂林理工大学 a.化学与生物工程学院;b.材料科学与工程学院,广西 桂林 541006;2.广西大学 化学化工学院,南宁 530004)
0 引 言
近年来,碱土金属硼磷酸盐因具有特殊的结构特征而备受关注[1]。碱土金属离子与稀土离子类似,在各种无机盐中一般都有高于6的配位数,以碱土化合物为基质可以比较容易实现稀土离子的掺杂,从而成为重要的荧光材料和新型闪烁材料[2-4]。此外,硼磷酸盐晶体的光学非线性特征较为突出[5-6],其阴离子基团包含BO4四面体、BO4平面三角形以及PO4四面体,这些阴离子基团以孤岛状、环状、层状、链状相互连接。相对于单纯硼酸盐和磷酸盐,硼磷酸盐更丰富的结构决定了其拥有更加良好的性能[7],在晶体生长、结构解析和光学特性等方面得到了广泛研究。Min等[8]发现Ho3+离子间的电偶极-电偶极作用会导致浓度淬灭。Mu等[9]制备出发射黄光的Sr2TiO4∶Ho3+荧光粉,其满足InGaN基蓝光LED 的要求。但是对于Ho掺杂到SrBPO5基质的发光性能及其第一性原理计算研究尚少有报道。
本文采用高温固相法合成SrBPO5∶Ho3+荧光粉,对其结构、组成及发光性能进行了详细研究,并通过第一性原理计算,获取了SrBPO5∶Ho3+的能带、态密度等理论信息。
1 材料与方法
1.1 试剂与仪器
碳酸锶SrCO3、硼酸H3BO3、磷酸氢二铵(NH4)2HPO4均为分析纯,Ho2O3的纯度为99.99%,以上试剂均购自中国医药集团有限公司。
采用荷兰帕纳科X’pert PRO型X射线衍射仪(辐射源为Cu 靶, X射线波长λ为0.154 056 nm; 工作电压40 kV, 工作电流40 mA, 扫描范围10°~90°)分析材料的微观结构; F-4600型荧光分光光度计分析材料的发光性能(激发源为150 W氙灯, 扫描速度1 200 nm/min, 狭缝10 nm, 分辨率为0.1 nm);日立SU5000场发射扫描电镜分析材料的微观形貌;德国布鲁克xflash6l10型能谱仪表征材料的组分。所有测试均在室温下进行。
1.2 材料制备
采用高温固相合成法制备SrBPO5∶xHo3+(x=0.01、 0.02、 0.03、 0.04、 0.05)系列荧光粉, 按产物的化学计量比称取反应原料, 其中H3BO3按过量10%称取, 弥补高温下硼酸挥发引起的损失。 将称取好的原料置于玛瑙研钵中充分研磨混匀, 然后盛入刚玉坩埚后放入箱式炉, 200 ℃恒温20 min, 继而在1 000 ℃下保温6 h进行合成, 结束后随炉冷却至室温, 取出研磨,制得SrBPO5∶xHo3+荧光粉。
1.3 第一性原理计算
材料的功能性能直接取决于其晶体结构和电子特性,基于密度泛函理论(DFT)的第一性原理计算为在原子水平上探索散装材料的结构和电子性质方面提供了强有力的工具[10-12],可用于探索SrBPO5的能带结构和态密度。
2 结果和讨论
2.1 SrBPO5∶Ho3+的微观结构
图1是SrBPO5∶0.03Ho3+荧光粉的XRD图。实验制备的SrBPO5∶0.03Ho3+荧光粉的衍射数据SrBPO5的标准图谱(JCPDS card No.89-7585)吻合很好, 没有出现杂峰, 且衍射峰的位置也没有明显的移动, 说明少量掺杂Ho对基质的结构没有影响。
2.2 SrBPO5∶Ho3+的组成
图2、 3分别为SrBPO5∶0.03Ho3+荧光粉的元素面分布图和能谱图。 Sr、 B、 P、 O、 Ho均匀分布在样品中, 说明Ho3+成功掺入SrBPO5基质当中。 由于Ho3+是少量掺杂, 含量相对较少。
2.3 SrBPO5∶Ho3+的性能
2.3.1 SrBPO5∶Ho3+的激发光谱和发射光谱 从SrBPO5∶0.03Ho3+荧光粉的激发光谱(图4a)可看出, 当监测波长为692 nm时, 在450~500 nm波长范围出现Ho3+的激发峰, 峰值出现在456 nm波长处, 对应于Ho3+的5I8→5G6跃迁[13]。

图1 SrBPO5∶0.03Ho3+及JCPDS标准卡片 89-7585的XRD图Fig.1 XRD patterns of SrBPO5∶0.03Ho3+ phosphors and JCPDS card(No.89-7585)

图2 SrBPO5∶0.03Ho3+荧光粉中的元素面分布图Fig.2 Element area profile of SrBPO5∶0.03Ho3+ phosphors

图3 SrBPO5∶0.03Ho3+荧光粉的EDS图Fig.3 EDS of SrBPO5∶0.03Ho3+ phosphors

图4 SrBPO5∶0.03Ho3+的激发光谱(a)和发射光谱(b)Fig.4 Excitation(a)and emissison(b)spectra of SrBPO5∶0.03Ho3+
而在发射光谱(图4b)中,在456 nm激发波长下,样品在670~720 nm波长范围出现特征发射,峰值在692 nm波长处,对应于5F5→5I8跃迁[14]。
2.3.2 SrBPO5∶Ho3+的色坐标 根据SrBPO5∶0.03Ho3+在456 nm激发波长下的发射光谱数据,可通过CIE1931软件计算荧光粉的色坐标,并绘制其发光点所在区域。图5给出了SrBPO5∶0.03Ho3+荧光粉的CIE坐标图。计算得到SrBPO5∶0.03Ho3+荧光粉的CIE坐标为(掺杂量在0.287 9、0.483 3),位于绿色区域。
2.3.3 掺杂量对SrBPO5∶xHo3+系列荧光粉的发光性能的影响 系列荧光粉在相同测试条件下所得到的发射光谱如图6所示。随着Ho3+掺杂量的增加,荧光粉的发射强度先增加,在Ho3+掺杂量为0.03 mol时,发光强度最大, 继续增加Ho3+的掺杂量,荧光粉发光强度开始下降,说明在实验研究范围内Ho3+的最佳掺杂量为0.03 mol,继续增大Ho3+的掺杂量,会产生淬灭,发光强度开始降低。
图7是Ho3+的发射强度随Ho3+掺杂量增大的变化趋势图。当掺杂量在0.01~0.03时,Ho3+离子之间距离较大,离子间的交叉弛豫较弱,故其发光强度随着Ho3+掺杂量的增大而增大;当掺杂量在0.03~0.05时,Ho3+之间距离减小,离子间的相互作用不断增强,导致Ho3+之间的无辐射交叉弛豫,因而Ho3+发光强度随着其掺杂量的增大而减弱。根据临界距离(Rc)的计算公式[15-17], 求得Rc=18.045 ×10-10m,远大于5 ×10-10m, 据此判断SrBPO5∶xHo荧光粉的Ho3+之间的能量传递方式应该是电多级-电多级相互作用[18-19]。
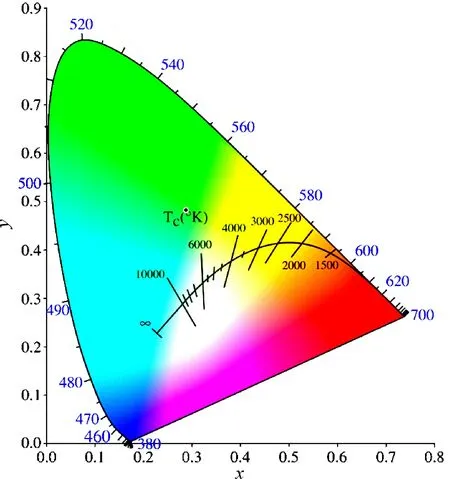
图5 SrBPO5∶xHo3+荧光粉的CIE坐标图Fig.5 CIE 1931 chromaticity diagram of SrBPO5∶xHo3+ phosphors
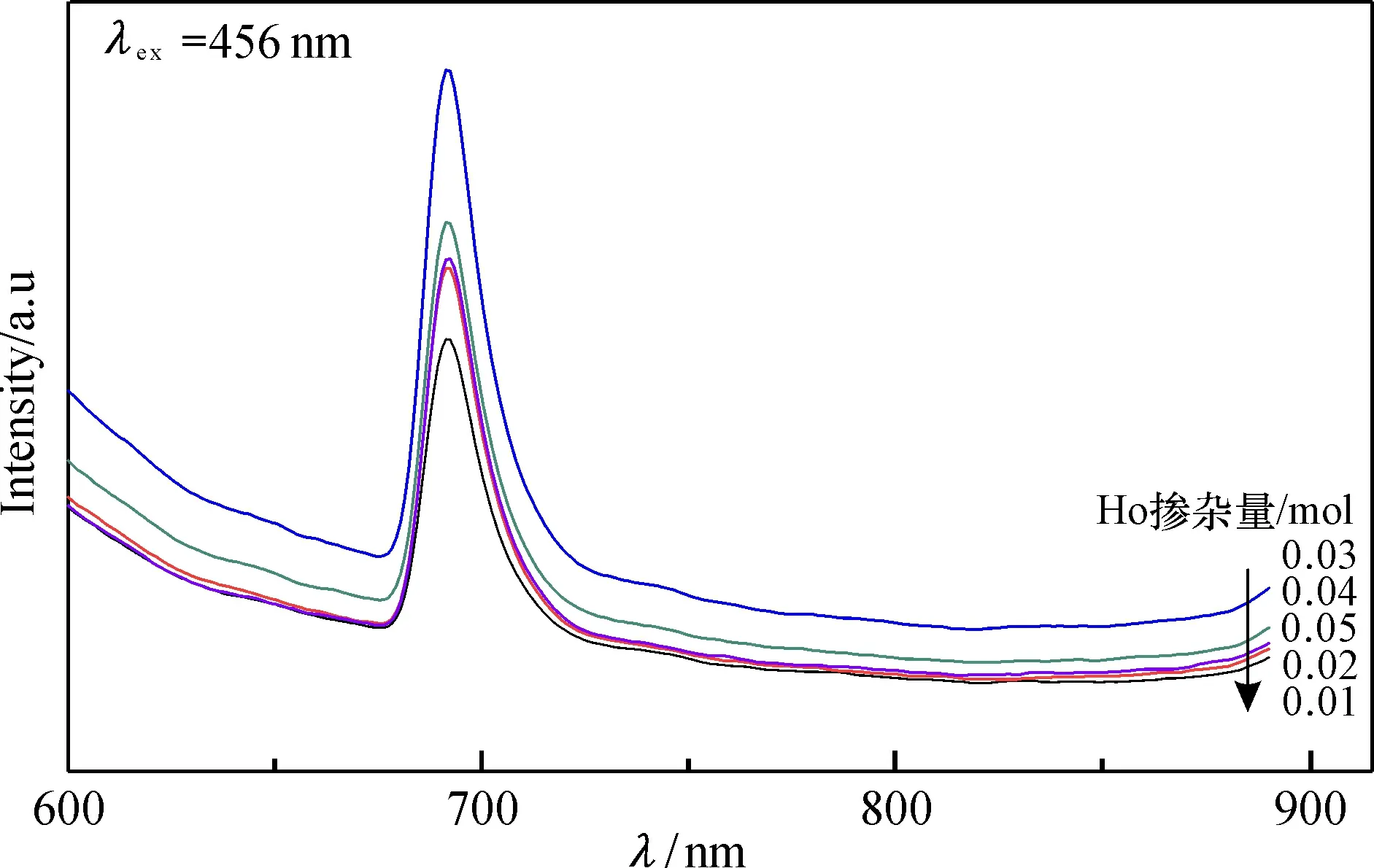
图6 不同HO3+掺杂量的SrBPO5∶xHo3+发射光谱Fig.6 PL emission spectra of SrBPO5∶xHo3+ phosphors

图7 发射强度随Ho3+掺杂量变化Fig.7 Emission intensity varying with Ho3+ doping
2.4 SrBPO5∶Ho3+荧光粉的能带结构
图8为采用GGA/RPEB计算得到的SrBPO5基质和SrBPO5∶Ho3+荧光粉的能带结构, 为了便于比较,费米能级设置在0 eV。 由图8a、 b可知, 价带(VBM)顶和导带(CBM)底都位于K空间G点,这说明SrBPO5是直接带隙半导体。通过计算得到VBM和CBM之间的带隙值为5.57 eV,较实验带隙值6.44 eV小[20]。造成这种情况的原因是:第一性原理计算是通过DFT密度泛函理论方法来计算系统的总能量(包含交换作用能),其中交换作用能的形式通常是不能被精确计算的,这就导致模拟计算的包含交换作用能的系统总能与实际的系统总能量之间存在偏差,从而导致基于密度泛函理论计算得到的带隙值偏低。

图8 SrBPO5(a、b)和Ho掺杂SrBPO5(c)材料 的能带结构Fig.8 Energy band structures of SrBPO5 (a,b)and Ho doped SrBPO5(c)materials
根据图8c计算得到SrBPO5∶Ho3+的VBM和CBM之间的带隙值为5.53 eV, 相对掺杂前略微减少, 且掺杂后的能带结构与未掺时一样, VBM顶和CBM底同处布里渊区G点, 说明SrBPO5∶Ho3+的体系也属于直接带隙结构, 对发光有利。 这是因为直接带隙结构的跃迁几率要大于间接带隙结构(前者的跃迁过程不需要声子参与, 参与跃迁的粒子种类越多,跃迁几率越小)[21]。
2.5 SrBPO5∶Ho3+材料的态密度分析图
研究SrBPO5化合物的电子性能具有深远的意义。通过计算得到SrBPO5、SrBPO5∶Ho3+的总态密度(FDOS)和Sr、B、P、O、Ho原子的分态密度(PDOS)结果如图9所示。为了方便比较,费米能级设定在0 eV处。分析态密度图可知,对于SrBPO5基质,其价带主要由O-2p和Sr-4p轨道贡献, B-2p和P-2p轨道也有少部分贡献;导带主要由Sr-4d轨道贡献, 同样B-2p和P-2p轨道也有少部分贡献;费米能级附近主要是O-2p轨道。O-2p轨道与B-2p和P-2p轨道有明显的一致性,说明在这些轨道间存在共价键。
从图9b可以看出,Ho掺杂后,其价带还是由O-2p和 Sr-4p轨道贡献;导带主要由Sr-4d、B-2p和P-2p轨道贡献。此外还有Ho-4f的贡献;由此也可以看出,掺杂后在费米能级附近出现的新能级为Ho的掺杂引起的。
3 结 论
(1)采用高温固相法合成SrBPO5基质,在200 ℃下预烧20 min后,继而在1 000 ℃下反应6 h合成纯相SrBPO5。产物的衍射数据与国际晶相衍射卡JCPDS089-7585吻合。能谱测试表明,Ho3+成功掺入基质,且均匀分布其中。

图9 SrBPO5和SrBPO5∶Ho3+的总态密度和分态密度Fig.9 Total and partial density and states of SrBPO5 and SrBPO5∶Ho3+
(2)荧光粉SrBPO5∶xHo3+可以被456 nm波长紫光激发,当监测波长为692 nm时,在450~500 nm波长范围出现Ho3+的激发峰,峰值出现在456 nm波长,对应于Ho3+的5I8→5G6跃迁;在456 nm波长激发下,样品在670~720 nm波长范围出现特征发射,峰值在692 nm处,对应于5F5→5I8跃迁。当Ho3+掺杂量为0.03 mol时,发光强度最大,超过此掺杂量会产生淬灭。通过色坐标计算,样品发光区域在绿色区域。通过计算得出,456 nm激发时发光过程的能量传递方式为电多级-电多级机制。
(3)掺杂后体系的带隙值降低,SrBPO5基质和SrBPO5∶xHo3+均为直接带隙结构。态密度图可知,费米能级附近出现的新的能级为Ho的掺杂引起。

