Purex流程铀钚分离工艺单元数学模型研究
于 婷,何 辉,洪 哲,刘占元,李峰峰,叶国安,*
(1.中国原子能科学研究院 放射化学研究所,北京 102413;2.环境保护部 核与辐射安全中心,北京 100082)
Purex流程铀钚分离工艺单元(1B)主要实现来自共去污单元1BF料液中铀钚之间的分离,使用合适的还原剂将Pu(Ⅳ)还原为不易被有机相(30%TBP/OK)萃取的Pu(Ⅲ),因为Pu(Ⅲ)的分配系数很低,几乎全部转入水相中,而绝大多数铀仍保留在有机相中,从而实现铀钚间的分离[1]。
目前,1B工艺单元多采用研究较多且技术上较成熟的U(Ⅳ)-N2H4为还原反萃剂,其已在Thorp厂、阿格厂、欧化厂、西德卡尔斯鲁厄后处理厂、印度塔拉普尔后处理厂和日本东海村核燃料后处理厂应用,并取得了一定的工作实绩[2-3]。在以混合澄清槽为萃取设备的铀钚分离工艺单元操作中,1AP(1BF)料液从1B槽中部引入,并与来自1B槽有机相出口端引入的还原反萃剂1BX2(钚反萃段)接触,同时为提高钚中铀的去除效果,从1B槽水相出口处引入补充萃取剂1BS(萃有一定硝酸的30%TBP/OK,使其与钚反萃段流出的水相逆流接触(该接触段为铀的补充萃取段))[3],被反萃进入水相的铀大部分重新转入有机相。在以U(Ⅳ)-N2H4为还原反萃剂时,由于U(Ⅳ)可被30%TBP/OK萃取,故U(Ⅳ)-N2H4(1BX1)的合适的加料级在1BF之后。
近几十年来,随着计算机技术的发展,计算机模拟技术成为后处理流程设计优化和安全分析的有效工具[2,4-7],为能模拟存在氧化还原反应的1B工艺单元的运行,对1B工艺单元的工艺参数进行优化,编写能实现1B工艺单元过程透视的模拟软件非常必要。本文拟针对以U(Ⅳ)-N2H4为还原剂的1B工艺单元,建立多级逆流混合澄清槽瞬态数学模型,编写该工艺单元计算机模拟软件,使用实验数据对模型和软件进行验证,最后使用模拟软件对影响1B工艺单元运行的工艺参数进行计算分析。
1 铀钚分离工艺单元数学模型及软件实现
1.1 数学模型
为简化多级逆流萃取过程,本研究以混合澄清槽理想模型[8]为基础。在理想的混合澄清槽中,每个萃取单元都由混合室和澄清室构成,两相在混合室能充分接触,而在澄清室中完全分离。对于N级逆流萃取过程,其任一级(第i级)的液流如图1所示。图中i为萃取级数,v为体积或体积流量,L和V分别为第i级所加水相料液和有机相料液的体积或体积流量,x和y分别为水相和有机相中组分的浓度,下标o和a分别表示有机相和水相,t为时间。设每一级的停留时间为1,则t时间进入第i级的液流最多有4股,分别为:1) 下一级第i+1级、上一时间t-1的水相液流xi+1,t-1,流量为va,i+1,t-1;2) 上一级i-1级、上一时间t-1的有机相液流yi-1,t-1,流量为vo,i-1,t-1;3) 第i级加入水相料液XF,体积为LF;4) 第i级加入有机相料液YF,体积为VF。

图1 逆流萃取第i级物料出入示意图Fig.1 Stream of i stage in multistage counter-current extraction
在第t停留时间中,第i级发生相际间传质反应以及相应的氧化还原反应,经过1个停留时间后,水相和有机相料液分别从第i级流出,其中水相xi,t流入i-1级(或为产品),有机相yi,t流入第i+1级(或为产品)。在1个停留时间内,流经混合澄清槽的液流可通过物料守恒方程来描述,且流出第i级的料液符合相平衡,具体如下式所示:
yi-1,t-1vo,i-1,t-1+xi+1,t-1va,i+1,t-1+XFLF+
YFVF=xi,tva,i,t+yi,tvo,i,t
(1)
yi,t=Dxi,t
(2)
因萃取过程中液体体积会因体积膨缩效应而发生变化,可使用体积膨缩模型进行计算,如下式所示:
vo,i,t=f(VF+vo,i-1,t-1)
(3)
va,i,t=f(LF+va,i-1,t-1)
(4)
分配比D可使用先前研究所得到的分配比模型[8]计算求得。利用以上4个关系式即可求得第i级水相及有机相中各组分的浓度。
1B工艺单元混合澄清槽数学模型以铀钚分离工艺单元单级数学模型[9]和混合澄清槽瞬态数学模型为基础,设定混合澄清槽一级停留时间为1,级效率为100%,在混合澄清槽开始时,即t=0时刻,假定1B槽中所有级都按照确定的流比充满水相和有机相,萃取槽的4股进料从相应的进料口开始,此时,各级出口水相和有机相各组分的浓度均为0。两相在相应的各级萃取单元停留1个停留时间,达到发生氧化还原反应、萃取平衡后,再从相应出口流出,除第1级的1BP和第N级的1BU两股液流外,其余出口液流均流入各自的相邻级,之后又在相应的萃取单元停留,发生氧化还原反应和传质反应,在第2个停留时间后流出作为下一停留时间各自相邻级的入口液流或作为产品流出,如此循环进行,直至t=x时间,两相中各级出口各组分的浓度不再发生变化,则混合澄清槽达到动态平衡,具体如图2所示。

图2 1B工艺单元混合澄清槽瞬态数学模型Fig.2 Transient model of counter-current mixer-settler in 1B
1.2 软件实现
使用Visual Basic 6.0语言编写以U(Ⅳ)-N2H4为还原反萃剂的铀钚分离工艺单元计算机模拟程序,所有的参数输入和计算结果输出均在图3所示的界面下完成,程序在Intel Core i5-5200U CPU 2.2GHz处理器、8.00 GB内存的计算机中调试通过。
2 模型验证
2.1 铀和酸的平衡浓度剖面
因铀钚分离工艺单元1BF料液中铀和酸的浓度较大(分别为90 g/L和0.18 mol/L),钚的含量相对较低,在实际工艺中不会大于2 g/L,则钚基本不会对铀和酸的分布造成影响。因此选用文献[10]的数据,以30%TBP/OK为萃取剂,室温下以1B操作工艺条件作为输入参数,将计算结果与实验结果进行比对。具体工艺条件列于表1,实验值与计算值的对比示于图4、5。由图4、5可知,水相中硝酸浓度、铀浓度,有机相中硝酸浓度、铀浓度实验值和计算值符合良好。
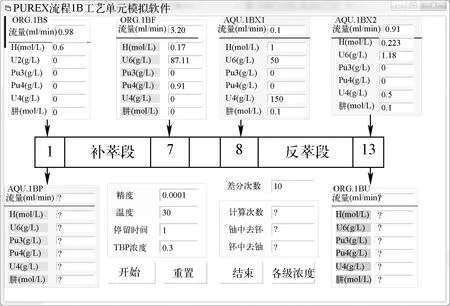
图3 1B单元模拟软件输入输出图形界面Fig.3 Graphic interface for I/O of parameter of 1B

表1 工艺条件Table 1 Flowsheet condition of 1B

图4 HNO3的平衡浓度剖面Fig.4 Concentration of HNO3 in each stage
2.2 钚的平衡浓度剖面
使用含0.91 g/L Pu(Ⅳ)的1BF模拟料液按照表2的工艺条件运行,运行温度为30 ℃,计算所得的平衡浓度剖面与实验结果的对比示于图6、7。

图5 铀的平衡浓度剖面Fig.5 Concentration of U in each stage

料液流比组成及浓度加料级1BX10.03150 g/L U(Ⅵ)、150 g/L U(Ⅳ)、1 mol/L HNO3、0.1 mol/L N2H4HNO381BX20.2781.18 g/L U(Ⅵ)、0.5 g/L U(Ⅳ)、0.223 mol/L HNO3、0.1 mol/L N2H4HNO3131BS0.330%TBP/OK、0.6 mol/L HNO311BF187.11 g/L U(Ⅵ)、0.91 g/L Pu(Ⅳ)、0.17 mol/L HNO37
由图6、7可知,计算得到的平衡浓度剖面和实际平衡浓度剖面趋势一致,接近两相出口端的计算值和实验值符合良好,在4~8级钚浓度的计算值与实验值的相对偏差较大,主要是靠近第7级2BF进料口,1BP槽实际运行工况级效率一般为80%,而模拟计算是以级效率为100%的理想平衡态为计算前提,存在一定的偏差,且通过对这几级逐级进行物料衡算,发现4~8级物料不衡算,表明实验值并不准确,导致最终的计算值与实验值相对偏差较大。1BP槽运行、取样操作以及样品分样分析等是这些显著偏差的主要原因。
对混合澄清槽达到动态平衡后的1BP和1BU中各组分的计算值和实验值进行对比,即两相出口浓度进行对比,结果列于表3。由表3可知,1BP和1BU中各组分的计算值和实验值符合良好,1BP中铀和钚的相对偏差分别为7.55%和-6.75%,酸的相对偏差低于1%,肼浓度的实验值与计算值差别相对较大,原因是数学模型并未考虑1B工艺单元中的亚硝酸等与肼发生氧化还原反应,导致计算值较实验值大。
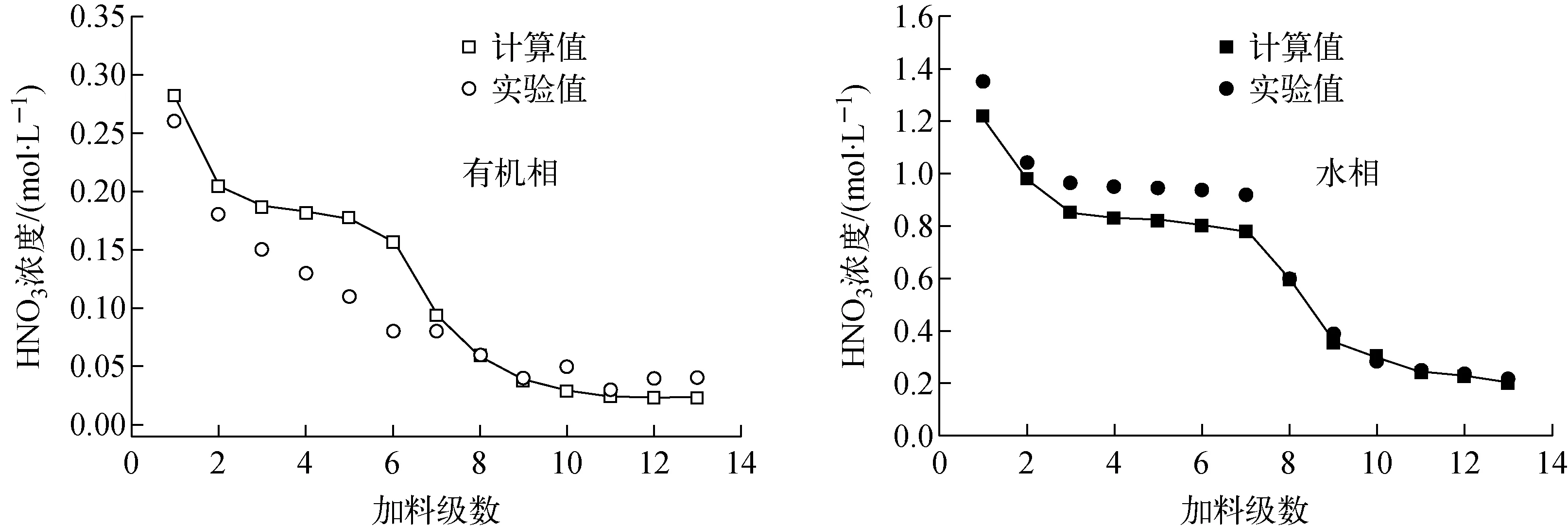
图6 硝酸的平衡浓度剖面Fig.6 Concentration of HNO3 in each stage

图7 钚的平衡浓度剖面Fig.7 Concentration of plutonium in each stage

料液U浓度/(g·L-1)Pu浓度/(g·L-1)H+浓度/(mol·L-1)肼浓度/(mol·L-1)计算值实验值计算值实验值计算值实验值计算值实验值1BP11.8311.002.903.111.351.360.10.0551BU69.3270.1904.52×10-60.0230.04—
3 工艺参数对铀钚分离段的影响计算分析
使用表4中1B工艺单元的工艺参数作为模拟软件的输入参数,每次变化1个工艺参数以考察该工艺参数对工艺单元的影响。设定每级停留时间为1 min、反应温度为30 ℃、级效率为100%,分别考察U(Ⅳ)-N2H4(1BX1)加料级数、补萃段级数、1BS酸度和1BX2酸度对铀钚分离过程的影响。

表4 1B工艺单元工艺条件Table 4 Flowsheet condition of 1B
3.1 U(Ⅳ)加入位置的影响
表4中其他条件不变,使用模拟程序计算1BX1加料级数为6~11级对钚的反萃率以及对钚中去铀系数(SFU/Pu)的影响,结果示于图8。由图8可知,在U(Ⅳ)过量的情况下,1BX1在反萃段加入位置对钚的反萃率不构成影响,即对有机相和水相出口级的钚浓度无影响,但对SFU/Pu有所影响,随着1BX1加料级数逐渐靠近1BX2,SFU/Pu逐渐下降,但影响并不明显。

图8 钚的反萃率和SFU/Pu随1BX1加料级数的变化Fig.8 Rate of Pu back-extraction and SFU/Pu with 1BX1 feed position
3.2 补萃段级数的影响
表4中其他条件不变,使用模拟程序计算补萃段级数分别为2~6级时钚的反萃率和铀的SFU/Pu,结果示于图9。由图9可知,钚的反萃率不受补萃段级数的影响。而SFU/Pu随着补萃段级数的增加而增加,在补萃段级数为2时,SFU/Pu仅为59,而在补萃段级数为4时,SFU/Pu则超过104,在实际工艺中一般选补萃级数为6。实际过程中,SFU/Pu>104难以达到,模型计算结果超过104,主要是因为该模型假设混合澄清槽为级效率100%的理想状态,而实际过程中级效率一般为80%~90%。
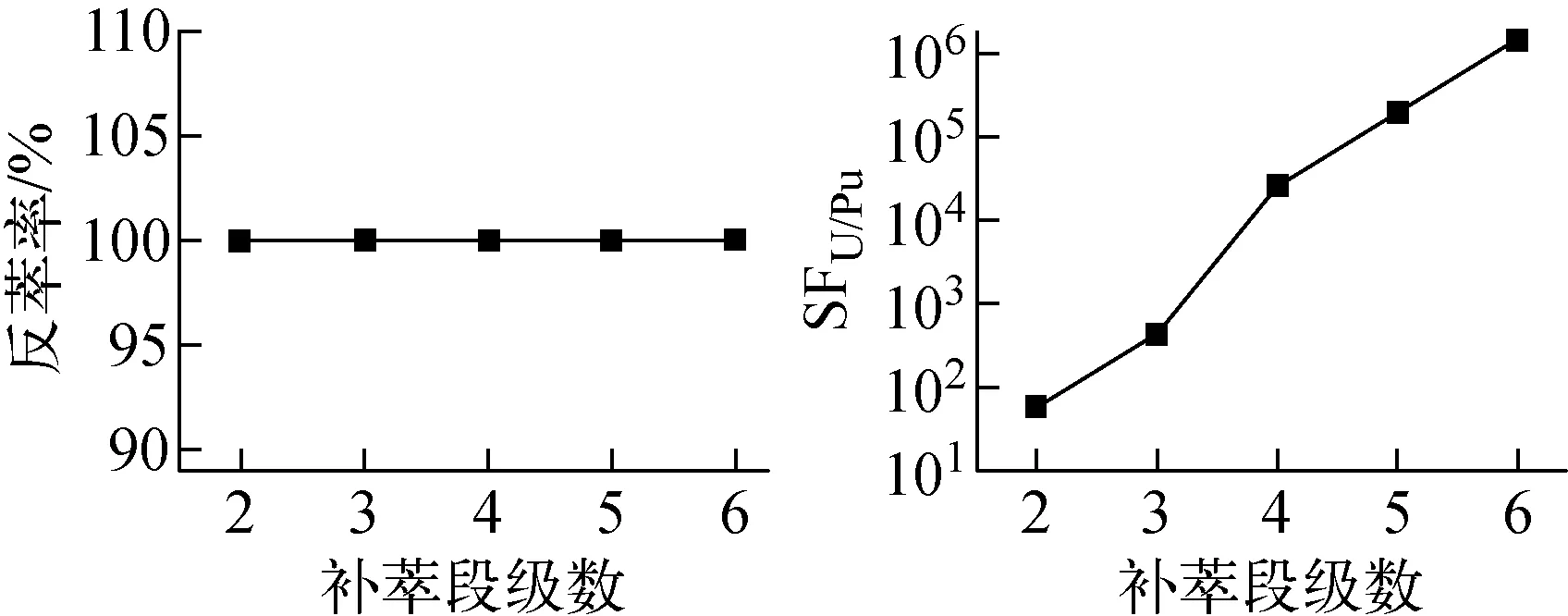
图9 钚的反萃率和SFU/Pu随补萃段级数的变化Fig.9 Rate of Pu back-extraction and SFU/Pu with stage of supplement extraction
3.3 1BS硝酸浓度的影响
表4中其他条件不变,使用模拟程序分别计算1BS中硝酸浓度为0、0.1、0.2、0.3、0.4、0.5 mol/L时钚的反萃率和SFU/Pu,其中SFU/Pu的计算结果示于图10。由计算可知,钚的反萃率不受1BS中硝酸浓度的影响。由图10可知,SFU/Pu随1BS中酸度的增加而增加,但在硝酸浓度为0 mol/L时,SFU/Pu已大于104,故在实际工艺中无需考虑1BS中硝酸浓度对工艺单元运行的影响。
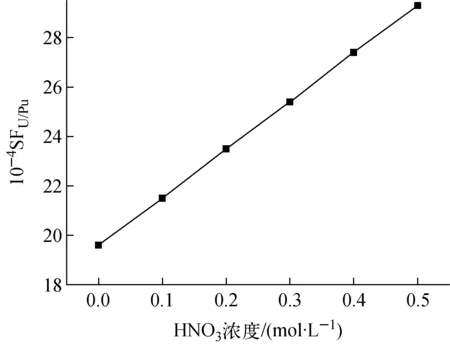
图10 SFU/Pu随1BS中硝酸浓度的变化Fig.10 SFU/Pu with HNO3 concentration in 1BS
3.4 1BX2硝酸浓度的影响
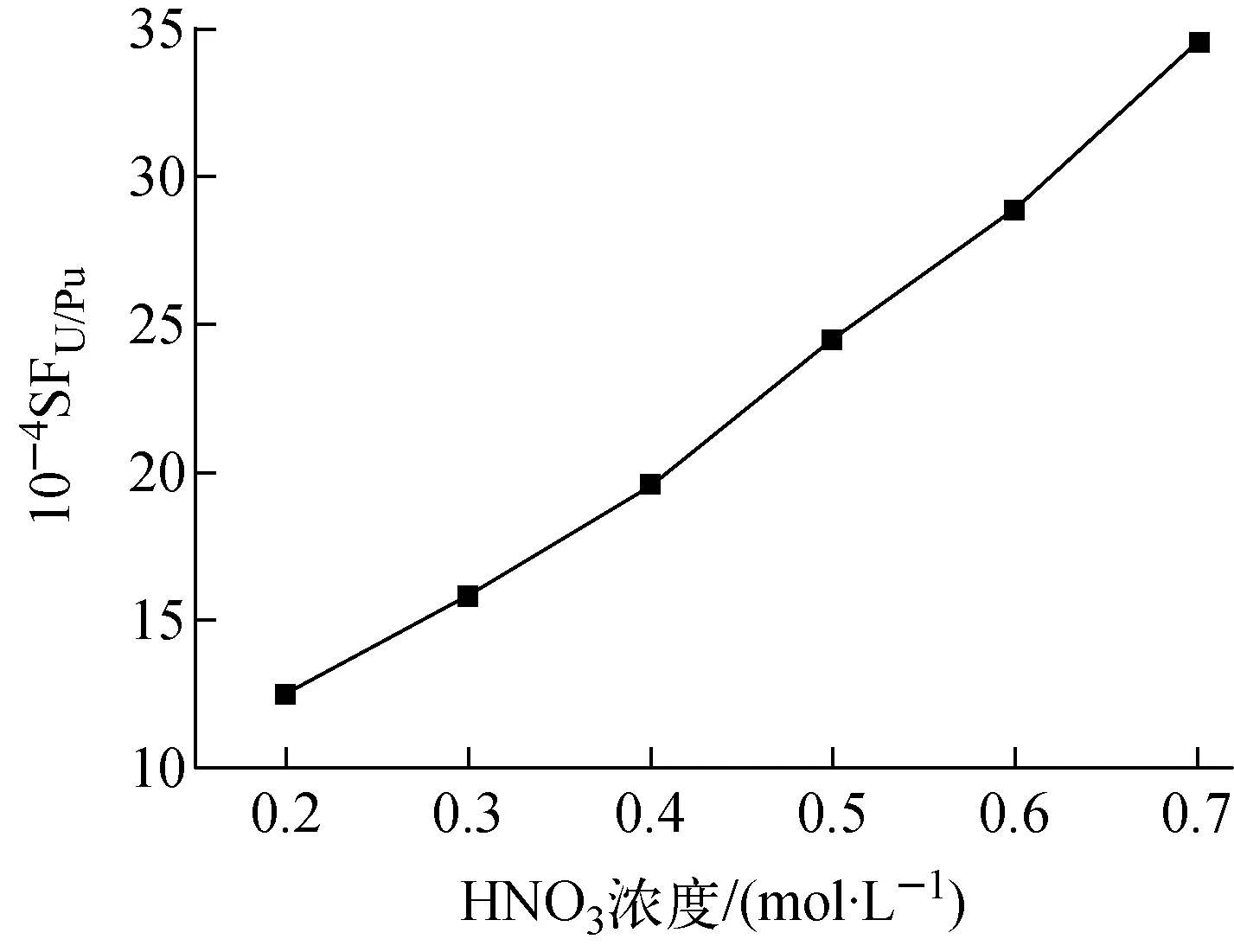
图11 SFU/Pu随1BX2中硝酸浓度的变化Fig.11 SFU/Pu with HNO3 concentration in 1BX2
表4中其他条件不变,使用模拟程序分别计算1BX2中硝酸浓度为0.2、0.3、0.4、0.5、0.6、0.7 mol/L时的SFU/Pu和钚的反萃率,其中SFU/Pu的计算结果示于图11。计算结果显示,钚的反萃率不受1BX2中硝酸浓度的影响。由图11可知,SFU/Pu随1BX2中酸度的增加而增加,但在硝酸浓度为0.2 mol/L时,SFU/Pu已大于104,故可认为1BX2中硝酸浓度对工艺运行的影响不大。
4 结论
通过对Purex流程中以U(Ⅳ)-N2H4为还原剂的铀钚分离工艺单元的分析,建立了以混合澄清槽为萃取设备的1B工艺单元数学模型,编写了该工艺单元的计算机模拟软件,使用台架实验数据对程序进行了验证,最后对影响该工艺单元运行的工艺参数进行了计算分析,得到以下结论。
1) 本研究建立的数学模型的计算值与台架实验结果符合良好,模拟程序可用于模拟1B工艺单元的运行。
2) 使用编写的1B单元模拟软件工艺参数对1B工艺单元的影响进行了计算分析,计算结果表明,在U(Ⅳ)过量的情况下,1BX1在反萃段的加入位置对钚的反萃率不构成影响,对SFU/Pu有一定影响,但影响有限;SFU/Pu随补萃段级数的增加而增大;1BS和1BX2中的酸度对钚反萃率和SFU/Pu影响不大。
感谢中国原子能科学研究院信息中心刘强副研究员在程序编写上提供的技术支持!

