基于371例儿童紫癜性肾炎的临床与病理分型的相关性分析
宋纯东 代思雨 宋 丹 任献青 王小飞 郭庆寅 张 霞 杨 濛 张 建 翟文生 丁 樱
紫癜性肾炎(HSPN)是过敏性紫癜(HSP)最重要的并发症之一[1],根据临床表现可分为单纯血尿型、单纯蛋白尿型、血尿和蛋白尿型、急性肾炎型、慢性肾炎型、急进型肾炎型和肾病综合征(NS)型等[2]。HSPN的肾脏病理改变主要为肾小球系膜细胞增殖和基质增生,系膜区以IgA免疫复合物沉积为主要特征,属于继发性IgA肾病[3]。肾脏受累的严重程度及其转归,是决定HSP预后的重要因素,也是导致慢性肾功能不全的主要病因[4]。本文回顾性分析河南中医药大学第一附属医院(我院)儿科HSPN患儿的临床及病理资料,旨在了解HSPN的发病规律。
1 方法
1.1 HSPN诊断标准和临床分型 诊断标准[2]:①有明确的皮肤紫癜病史,伴或不伴有关节、肌肉或消化道症状;②尿检异常,包括血尿(肉眼血尿或镜下血尿)和蛋白尿。临床分型如下。Ⅰ型:单纯性血尿或单纯性蛋白尿型;Ⅱ型:血尿和(加)蛋白尿型;Ⅲ型:急性肾炎型;Ⅳ型:NS型;Ⅴ型:急进性肾炎型;Ⅵ型:慢性肾炎型。
1.2 纳入标准 2016年1月1日至2018年12月31日在我院儿科肾病病区住院并有肾活检病理报告、年龄<18周岁的HSPN患儿。
1.3 排除标准 ①有家族性尿检异常史;②有其他肾脏疾病;③有其他免疫系统疾病,如干燥综合征、系统性红斑狼疮和风湿病等。
1.4 病理分型
1.4.1 光学显微镜分级 按照国际儿童肾病研究会(ISKDC)分类标准[5],将HSPN病理表现分为六级。Ⅰ级:轻微病变;Ⅱ级:单纯性系膜增生;Ⅲ级:系膜增生伴<50%肾小球新月体形成和(或)节段损害;Ⅳ级:系膜增生伴50%~75%肾小球新月体形成(或)节段损伤;Ⅴ级:系膜增生伴>75%肾小球新月体和(或)节段损伤;Ⅵ级:膜性增殖性肾炎。
1.4.2 免疫荧光分型 肾小球系膜区是免疫复合物沉积的主要部位,严重者可延伸至毛细血管壁,根据沉积的免疫复合物的不同,HSPN免疫荧光分型可分为IgA型、IgA+IgG型、IgA+IgM型、IgA+IgG+IgM型[6]。
1.4.3 肾小管病理分级 Ⅰ级:间质基本正常,轻度小管变性扩张;Ⅱ级:间质纤维化,小管萎缩<20%,散在炎性细胞浸润;Ⅲ级:间质纤维化,小管萎缩20%~50%,散在和(或)弥漫性炎性细胞浸润;Ⅳ级:间质纤维化,小管萎缩>50%,散在和(或)弥漫性炎性细胞浸润。
1.5 资料截取 从病历资料中截取患儿的性别,年龄,病程,关节,肌肉、消化道症状,皮肤紫癜后发现尿检异常时间,临床分型,24 h尿蛋白定量(≥50 mg·kg-1·d-1为大量蛋白尿),肾小球及肾小管病理分型、免疫荧光分型。
1.6 随访 对大量蛋白尿患儿在治疗8周末进行复诊随访,检测尿常规和24 h尿蛋白定量。
1.7 统计学方法 采用SPSS 20.0软件进行分析。计量资料数据呈正态分布者,以xˉ±s描述,组间比较采用t检验;如呈非正态分布,以中位数(P25,P75)描述,组间比较采用秩和检验。计数资料以构成比或百分比描述,组间比较采用McNemar检验,新月体分组与24 h尿蛋白水平的关系采用单因素方差分析;计数资料组间的相关性采用Spearman秩相关检验。以双侧α=0.05为检验水准。P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 符合本文纳入标准HSPN患儿457例,排除有家族性尿检异常史者11例,有其他肾脏疾病者52例,有其他免疫系统疾病者23例,371例HSPN患儿进入本文分析。男223例、女148例,年龄2~18岁,中位年龄10(7,12)岁,住院时间5~50 d,中位数19(16,23)d;其中,单纯皮肤紫癜77例(20.8%),伴关节、肌肉症状80例(21.6%),伴消化道症状75例(20.2%),同时伴消化道和关节症状139例(37.5%);皮肤紫癜后发现尿检异常时间:<1周123例(33.2%),~1个月194例(52.3%),~3个月29例(7.8%),~6个月10例(2.7%),~1年6例(1.6%),>1年9例(2.4%)。
2.2 临床分型 Ⅰ型中单纯性蛋白尿型和单纯性血尿型各12例(3.2%,12/371),其中单纯性蛋白尿型有2例有大量蛋白尿(16.7%,2/12);Ⅱ型291例(78.4%),其中大量蛋白尿者103例(35.4%,103/291);Ⅳ型56例(15.1%),均有大量蛋白尿。
肉眼血尿18例,其中Ⅱ型11例(3.8%,11/291),Ⅳ型7例(12.5%,7/56),χ2=28.4,P<0.01。
有消化道症状者214例中大量蛋白尿98例(45.8%);无消化道症状者157例中大量蛋白尿63例(40.1%);两组间进行McNemar检验,χ2=15.6,P<0.001。
2.3 病理分型
2.3.1 光学显微镜分级 Ⅰ型8例(2.2%),Ⅱ型79例(21.3%),Ⅲ型278例(74.9%),Ⅳ型5例(1.4%),Ⅴ型1例(0.3%)。
2.3.2 免疫荧光分型 IgA型309例(83.3%),IgA+IgG型10例(2.7%),IgA+IgM型52例(14.0%);伴C3沉积132例(35.6%),伴FIB沉积364例(98.1%),未见伴C1q沉积者。
伴C3沉积的132例(35.6%)中109例为IgA型,3例为IgA+IgG型,20例为IgA+IgM型。对免疫荧光分型与补体C3沉积的关系进行Spearman秩相关检验,r=-0.16,P=0.759。
2.3.3 肾小管病理分级 Ⅰ级44例(11.8%),Ⅱ级160例(43.1%),Ⅲ级165例(44.5%),Ⅳ级2例(0.2%)。
2.3.4 光学显微镜分级与其他病理分型的关系 表1 Spearman秩相关检验显示,光学显微镜分级与免疫荧光分型(r=0.061,P=0.241)和补体C3沉积(r=-0.072,P=0.168)均无明显相关性,与肾小管病理分级间有相关性(r=0.366,P<0.001)。
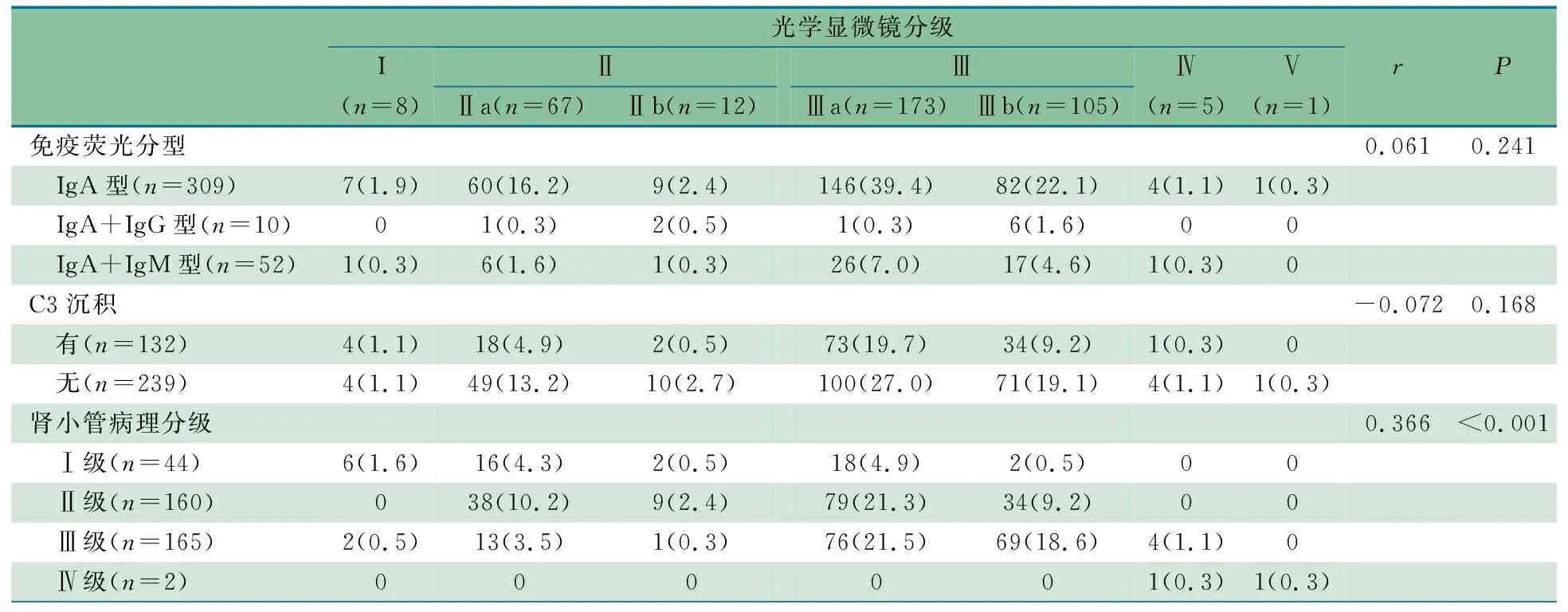
表1 光学显微镜分级与其他病理分型的关系[n(%)]
2.3.5 新月体含量分级及其与尿蛋白水平的关系 表2显示,根据新月体含量比例分组,将其与24 h尿蛋白量进行单因素方差分析,F=3.980,P=0.001,说明新月体的比例与24 h尿蛋白量有相关性。
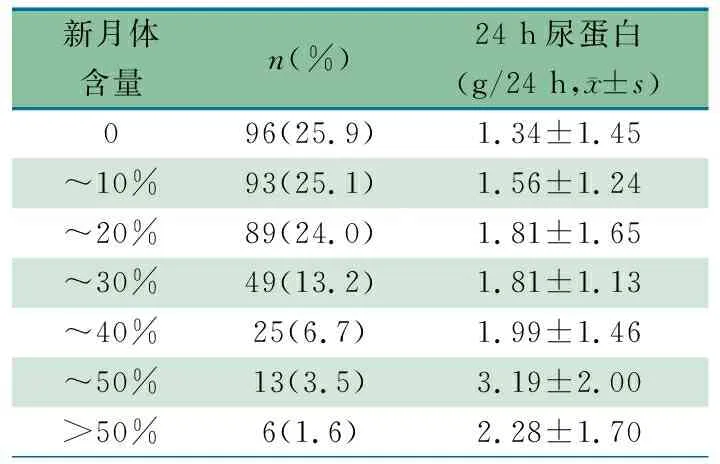
表2 不同比例新月体患儿24 h尿蛋白定量水平
2.5 临床分型与病理分型的关系 表3 Spearman秩相关检验显示,临床分型与光学显微镜分级相关(r=0.264,P<0.001),与免疫荧光分型无明显相关性(r=0.087,P=0.241),,与肾小管病理分级间有相关性(r=0.246,P<0.001)。
2.6 随访情况 治疗8周后对161例大量蛋白尿患儿进行随访,有48例24 h尿蛋白定量未降至正常,或尿蛋白及尿红细胞未转阴性,光学显微镜病理分级:Ⅰ型1例(2.1%)、Ⅱa型5例(10.4%)、Ⅱb型6例(12.5%)、Ⅲa型12例(25.0%)、Ⅲb型20例(41.7%)、Ⅳ型3例(6.2%)、Ⅴ型1例(2.1%);临床分型:血尿和(加)蛋白尿型32例(66.7%),NS型16例(33.3%)。

表3 临床分型与病理(光学显微镜、免疫荧光、肾小管)分型的关系[n(%)]
3 讨论
HSPN是儿童时期最常见的继发性肾小球肾炎。几乎所有的HSP患儿肾活检均能发现肾脏损伤[7],约85%发生在起病的4周内,97%发生在起病的6个月内[8]。免疫反应可导致肠道黏膜肿胀、狭窄,患儿出现腹痛、便血,有消化道症状者大量蛋白尿的发生率增加[9]。
本文371例患儿中,仅伴消化道症状者75例(20.2%),同时有消化道、关节和肌肉症状者139例(37.5%)。McNemar检验显示,有消化道症状者出现大量蛋白尿的可能性增加(χ2=15.6,P<0.001)。临床分型以血尿加蛋白尿型最多(78.4%),其次为NS型(15.1%),其余为单纯血尿型和单纯蛋白尿型(各占3.2%),无急性肾炎型、急进型肾炎综合征型、慢性肾炎型者,与文献[9]报道一致。本文共18例出现肉眼血尿,其中NS型7例,血尿加蛋白尿型11例,两组差异有统计学意义,说明NS型发生肉眼血尿比例较高,与文献[10]报道一致。病理分型以Ⅲ级为主(74.9%),其次为Ⅱ级(21.3%),与文献[11]报道一致,但也有文献中报道Ⅱ级比Ⅲ级多[12],可能与病例来源地域不同有关。
有研究报道,52.8%的HSPN患儿系膜区同时有IgA+IgG+IgM沉积[13],且肾组织C3沉积与HSPN患儿的免疫损伤明显相关[14]。本文患儿免疫荧光分型中未见到IgA+IgG+IgM型,35.6%的患儿可见有补体C3沉积,C3沉积主要集中于Ⅲ级病变。有研究显示,C3在HSPN肾组织中沉积可能与补体旁路途径调节异常有关[15]。对免疫荧光分型与补体C3、光学显微镜分级之间进行Spearman秩相关分析,结果无统计学意义。然而,有文献报道,免疫荧光分型与光学显微镜分级有一定的相关性,单纯IgA沉积以Ⅱb、Ⅲb为主,IgA+IgM+IgG型和IgA+IgM型在Ⅳ~Ⅴ型有增多趋势[16]。肾小球疾病的发展不仅与肾小球本身受损相关,更与肾小管病变程度密切相关[17],本文患儿病理检查都存在不同程度的肾小球和肾小管病变,对肾小管病变与光学显微镜分级行Spearman秩相关分析,差异有统计学意义(P<0.05),说明肾小管病变程度与光学显微镜分级呈正相关。
HSPN患儿的临床及病理表现多样,轻重不一。本研究临床表现为单纯性血尿型和单纯性蛋白尿型者光学显微镜分级以Ⅱ级为主,血尿加蛋白尿型以Ⅱ级和Ⅲ级为主,NS型以Ⅲ级为主。对患儿的临床分型与光学显微镜分级进行Spearman相关性分析,P<0.01,说明HSPN患者的临床症状的严重程度与肾脏病理分级相关,即临床表现越重,肾脏病理分级越高[18]。但也有临床与病理表现不一致的情况,如本组病理Ⅴ级的临床表现为单纯血尿型。因此,不能单凭患儿的临床症状去推断病理类型,否则会误判误治。
在许多肾小球疾病中,新月体的形成与肾功能进行性恶化、大量蛋白尿等有关,对预后起关键作用,HSPN新月体均见于病理Ⅲ级以上的患儿[19]。本文显示,随着新月体比例的增加,24 h尿蛋白水平有增多的趋势。
尿蛋白水平是非糖尿病性肾脏疾病进展的一个危险因素[20-21],大量蛋白尿是影响肾功能及病程的重要因素,因此对161例大量蛋白尿患儿进行随访,发现治疗8周24 h尿蛋白定量未降至正常、或尿蛋白及尿红细胞未转阴性者48例,以血尿加蛋白尿型最多(32/48,66.7%),病理以Ⅲb级(20/48,41.7%)为主。
综上所述,根据本文病例HSPN临床以血尿加蛋白尿型最常见,病理以Ⅱ级和Ⅲ级多见;临床与病理、消化道症状与大量蛋白尿、NS型和肉眼血尿、肾小管病变程度与病理分型、新月体含量与24 h尿蛋白水平等均有一定相关性。对于HSP初发的患儿,在发病后的第1个月内应积极接受治疗,减少紫癜反复及HSPN的发生,尤其是应注意个别病理分级与临床分型之间不一致的情况存在,对反复迁延的单纯血尿型要适时进行肾活检。

