捧兴通脉颗粒对高脂乳剂致高脂血症大鼠的影响
陈昱晓, 韦立群, 张宇薇, 许立拔, 蒋伟哲, 付书婕
(广西医科大学药学院,广西南宁 530021)
随着人们生活水平的提高,肥胖已成为全球广泛存在的健康问题,它常伴有高脂血症,是动脉粥样硬化、脑卒中、冠心病、心肌梗死、猝死等疾病的重要诱因。肝脏负责脂质和脂蛋白代谢,是机体营养代谢的重要器官,脂质摄入过量时会导致肝损伤,继而引发脂质代谢紊乱[1]。
捧兴通脉颗粒是广西壮要方医院的医疗机构制剂,已获医疗机构制剂注册批件 (桂药制字M20170005),由玉郎伞、姜黄、广山楂、决明子等广西特色壮药材组成,具有护肝降脂的作用,主要用于高血脂症、脂肪肝等疾病的治疗,临床疗效显著,已列入科技部-中央引导地方科技发展专项资金项目、广西创新驱动发展专项-科技重大专项。研究表明,玉郎伞多糖、总黄酮、皂苷等成分具有护肝降脂的作用[2-6],而姜黄素、山楂总黄酮、决明子总蒽醌等具有治疗脂肪肝的作用[7-9]。本实验采用高脂乳剂建立大鼠高脂血症模型,观察捧兴通脉颗粒降血脂和改善肝功能的作用,为其临床应用和深入研究提供理论和实验依据。
1 材料
1.1 动物 雄性Wistar大鼠,SPF级,体质量180~200 g,由广西医科大学实验动物中心提供,生产许可证号SCXK(桂)2009-0002,饲养于广西医科大学药学院标准实验室,自由饮水摄食。
1.2 试药 捧兴通脉颗粒 (6 g/袋)购自广西壮要方医院,批号20130301;血脂康胶囊购自北京北大维信生物科技公司,批号2013072。胆固醇购自广州威佳科技有限公司,批号20130826;丙硫氧嘧啶购自上海朝晖药业有限公司,批号1401F11;精制猪油为自制;胆固醇 (TC)、甘油三酯 (TG)、高密度脂蛋白胆固醇 (HDLC)、低密度脂蛋白胆固醇 (LDLC)、载脂蛋白A1(ApoA1)、ApoB、谷丙转氨酶(ALT)谷草转氨酶 (AST)试剂盒购自上海执诚生物科技有限公司,批号 NOVL017、NOVL011、AUGK008、NOVL009、 DECL008、 OCTL012、 NOVL002、 NOVL012。
1.3 仪器 7100型全自动血生化分析仪 (日本日立公司);Micro17R型高速低温离心机、FORMA991型-80℃超低温冰箱、Multiskan G0型全波长酶标仪 (美国赛默飞世尔科技公司);EL602型电子天平 (0.01 g,瑞士梅特勒-托利多公司);UW620H型电子天平 (0.001 g,日本岛津制作所)。
2 方法
2.1 药液配制 取颗粒3袋 (18 g),加纯净水至60 mL,充分混匀,即得高剂量药液 (300 mg/mL),同法倍比取颗粒,配制低、中剂量药液 (75、150 mg/mL)。
2.2 分组及给药 大鼠适应性饲养7天后取80只,随机选取其中12只作为空白组,按10 mL/kg剂量灌胃给予等体积纯净水,其余大鼠按相同剂量灌胃给予高脂乳剂 (配方参考余学钊等[10]报道,即20%猪油+6%胆固醇+0.2%丙硫氧嘧啶+10%吐温-80+63.8%水,机械混合,冷冻保存,使用前水浴融溶),每天1次。21 d后,大鼠眼眶后静脉丛采血,测定TC水平。
选取TC水平在2.8~6.0 mmol/L之间的模型大鼠60只,随机分为模型组、血脂康组 (0.2 g/kg)及捧兴通脉颗粒低、中、高剂量组 (0.8、1.5、3.0 g/kg),每组 12只。每天早上除空白组大鼠按10 mL/kg剂量灌胃给予纯净水外,其余大鼠按相同剂量灌胃给予高脂乳剂;每天下午除空白组、模型组大鼠按相同剂量灌胃给予纯净水外,其余大鼠按相同剂量灌胃给予相应药液,每天上、下午各灌胃1次,每周称定大鼠体质量并调整给药量,连续6周。
2.3 血清生化指标检测 给药3、6周,大鼠眼眶后静脉丛采血,通过全自动血生化分析仪进行检测。
2.3.1 血脂 测定TCHO、TG、HDLC、LDLC水平。
2.3.2 血脂综合指数和动脉硬化指数 根据血脂水平,计算血脂综合指数 (LCI, TC×TG×LDLC/HDLC)、 动脉粥样硬化指数 [AI, (TC-HDLC) /HDLC][11-12]。
2.3.3 血清载脂蛋白 测定载脂蛋白A1(ApoA1)、载脂蛋白 B (ApoB) 水平,并计算两者比值 (ApoA1/ApoB)[13]。
2.3.4 血清肝功能指标测定ALT、AST水平。
2.4 肝脏组织病理学检查 末次采血结束后处死大鼠,取出部分肝组织,10%中性福尔马林固定,苏木素-伊红(HE)染色,光镜下检查肝组织病理变化。
2.5 统计学分析 通过SPSS17.0软件进行处理,数据用±s)表示,符合正态分布和方差齐性者,采用One-Way ANOVA分析,差异有统计学意义则组间采用LSD-t进行两两比较分析;不符合正态分布或方差齐性者,采用Kruskal-Wallis H分析,差异有统计学意义则组间采用Mann-Whitney U进行两两比较分析。P<0.05为差异具有统计学意义。
3 结果
3.1 体质量 表1显示,与空白组比较,模型组大鼠体质量显著降低 (P<0.01);与模型组比较,捧兴通脉颗粒组大鼠体质量无明显变化 (P>0.05)。
表1 捧兴通脉颗粒对大鼠体质量的影响 (g,n=12)

表1 捧兴通脉颗粒对大鼠体质量的影响 (g,n=12)
注:与模型组比较,▲▲P<0.01
组别 剂量/(g·kg-1) 给药前 给药后3周 给药后6周空白组 — 345.2±25.4▲▲ 381.8±26.9▲▲ 407.2±32.8▲▲模型组 — 300.4±12.7 298.2±17.9 280.0±19.6血脂康组 0.2 301.9±15.2 298.1±18.6 280.4±25.3捧兴通脉颗粒组 0.8 305.5±12.3 300.6±20.6 279.6±28.8捧兴通脉颗粒组 1.5 303.4±15.4 301.0±17.1 292.7±30.1捧兴通脉颗粒组 3.0 295.0±8.2 286.8±12.2 272.0±23.2
3.2 血脂指标 表2~3显示,与空白组比较,模型组给药后第3、6周大鼠血清TC、TG、LDLC水平显著升高(P<0.01), HDLC水平显著降低 (P<0.01); 与模型组比较,捧兴通脉颗粒组给药后第3周TC、TG、LDLC水平显著降低 (除低剂量组TC水平外) (P<0.05,P<0.01),同时高剂量组HDLC水平显著升高 (P<0.05),给药后第6周四者水平均有明显变化 (P<0.05,P<0.01)。
表2 捧兴通脉颗粒对大鼠血脂指标的影响 (第3周) (mmol/L,, n=12)

表2 捧兴通脉颗粒对大鼠血脂指标的影响 (第3周) (mmol/L,, n=12)
注:与模型组比较,▲P<0.05,▲▲P<0.01
组别 剂量/(g·kg-1) TC TG HDLC LDLC空白组 — 1.63±0.28▲▲ 0.46±0.16▲▲ 2.93±0.53▲▲ 0.46±0.15▲▲模型组 — 5.66±0.85 0.76±0.24 1.96±0.66 3.97±0.93血脂康组 0.2 4.54±0.99▲ 0.63±0.19▲ 2.55±0.50▲ 2.68±0.79▲▲捧兴通脉颗粒组 0.8 4.55±1.35 0.56±0.19▲ 2.19±0.38 3.28±0.56▲捧兴通脉颗粒组 1.5 3.63±1.38▲▲ 0.43±0.10▲▲ 2.27±0.49 2.91±0.58▲▲捧兴通脉颗粒组 3.0 4.28±1.47▲ 0.57±0.25▲ 2.45±0.54▲ 3.03±0.44▲▲

表3 捧兴通脉颗粒对大鼠血脂指标的影响 (第6周) (mmol/L,x±s, n=12)
3.3 血脂综合指数和动脉硬化指数 表4~5显示,与空
白组比较,模型组给药后第3、6周大鼠血清LCI、AI显著升高 (P<0.01);与模型组比较,捧兴通脉颗粒组给药后第3、 6周两者显著降低 (P<0.05, P<0.01)。
表4 捧兴通脉颗粒对大鼠血脂综合指数和动脉硬化指数的影响 (第3周)s, n=12)

表4 捧兴通脉颗粒对大鼠血脂综合指数和动脉硬化指数的影响 (第3周)s, n=12)
注:与模型组比较,▲P<0.05,▲▲P<0.01
组别 剂量/(g·kg-1) LCI AI空白组 — 0.12±0.05▲▲ -0.44±0.11▲▲模型组 — 10.12±6.35 2.18±1.11血脂康组 0.2 3.57±3.42▲▲ 0.84±0.57▲▲捧兴通脉颗粒组 0.8 4.13±2.71▲▲ 1.16±0.80▲捧兴通脉颗粒组 1.5 1.94±0.74▲▲ 0.64±0.66▲▲捧兴通脉颗粒组 3.0 3.57±2.64▲▲ 0.83±0.69▲▲
表5 捧兴通脉颗粒对大鼠血脂综合指数和动脉硬化指数的影响 (第6周), n=12)

表5 捧兴通脉颗粒对大鼠血脂综合指数和动脉硬化指数的影响 (第6周), n=12)
注:与模型组比较,▲▲P<0.01
组别 剂量/(g·kg-1) LCI AI空白组 — 0.19±0.08▲▲ -0.09±0.50▲▲模型组 — 13.82±11.22 2.05±1.01血脂康组 0.2 0.83±0.48▲▲ 0.36±0.52▲▲捧兴通脉颗粒组 0.8 1.90±1.12▲▲ 0.59±0.79▲▲捧兴通脉颗粒组 1.5 1.72±1.14▲▲ 0.57±0.53▲▲捧兴通脉颗粒组 3.0 1.07±0.95▲▲ 0.43±0.88▲▲
3.4 血清载脂蛋白 表6~7显示,与空白组比较,模型组给药后第3周大鼠血清ApoA1水平无明显变化 (P>0.05), ApoB 水平显著升高 (P<0.01), ApoA1/ApoB 显著降低 (P<0.01),而给药后第6周三者均有明显变化 (P<0.05,P<0.01);与模型组比较,捧兴通脉颗粒组给药后第3周三者无明显变化 (P>0.05),给药后第6周均有明显变化 (除中剂量组ApoA1水平外) (P<0.05,P<0.01)。
表6 捧兴通脉颗粒对大鼠血清载脂蛋白的影响 (第3周)(mg/dL, s, n=12)
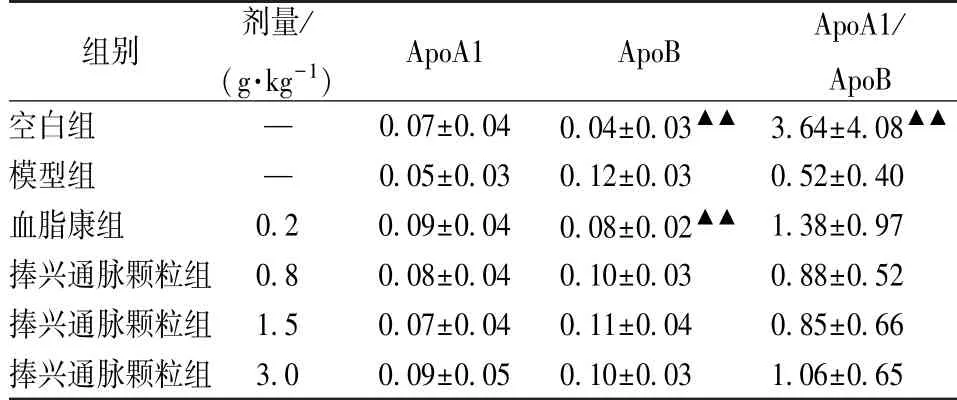
表6 捧兴通脉颗粒对大鼠血清载脂蛋白的影响 (第3周)(mg/dL, s, n=12)
注:与模型组比较,▲▲P<0.01
组别 剂量/ApoA1 ApoB ApoA1/(g·kg-1) ApoB空白组 — 0.07±0.04 0.04±0.03▲▲ 3.64±4.08▲▲模型组 — 0.05±0.03 0.12±0.03 0.52±0.40血脂康组 0.2 0.09±0.04 0.08±0.02▲▲ 1.38±0.97捧兴通脉颗粒组 0.8 0.08±0.04 0.10±0.03 0.88±0.52捧兴通脉颗粒组 1.5 0.07±0.04 0.11±0.04 0.85±0.66捧兴通脉颗粒组 3.0 0.09±0.05 0.10±0.03 1.06±0.65
表7 捧兴通脉颗粒对大鼠载脂蛋白指标的影响 (第6周)(mg/dL, s, n=12)

表7 捧兴通脉颗粒对大鼠载脂蛋白指标的影响 (第6周)(mg/dL, s, n=12)
注:与模型组比较,▲P<0.05,▲▲P<0.01
组别 剂量/ApoA1 ApoB ApoA1/(g·kg-1) ApoB空白组 — 0.15±0.04▲▲ 0.04±0.02▲▲ 6.52±4.82▲▲模型组 — 0.04±0.02 0.14±0.03 0.34±0.19血脂康组 0.2 0.08±0.05▲ 0.10±0.03▲▲ 0.92±0.59▲▲捧兴通脉颗粒组 0.8 0.07±0.03▲ 0.08±0.04▲▲ 0.95±0.77▲▲捧兴通脉颗粒组 1.5 0.09±0.04 0.08±0.02▲▲ 1.17±0.61▲▲捧兴通脉颗粒组 3.0 0.08±0.04▲ 0.09±0.03▲▲ 1.14±1.00▲▲
3.5 血清肝功能指标 表8显示,与空白组比较,模型组给药后第3、6周大鼠血清ALT、AST水平显著升高 (P<0.01);与模型组比较,捧兴通脉颗粒组给药后第3周两者水平显著降低 (除中剂量组ALT水平外) (P<0.05,P<0.01), 给药后第 6周亦然 (P<0.05, P<0.01)。
表8 捧兴通脉颗粒对大鼠肝功能指标的影响 (U/L, n=12)

表8 捧兴通脉颗粒对大鼠肝功能指标的影响 (U/L, n=12)
注:与模型组比较,▲P<0.05,▲▲P<0.01
组别 剂量/(g·kg-1)第6周ALT AST ALT AST第3周空白组 — 53.2±23.9▲▲ 111.9±24.0▲▲ 63.8±20.4▲▲ 114.9±13.7▲▲模型组 — 112.0±16.7 151.1±26.3 128.3±18.3 179.7±52.1血脂康组 0.2 98.7±11.5 131.2±12.6 106.9±22.6▲▲ 128.2±17.9▲捧兴通脉颗粒组 0.8 95.2±18.8▲ 123.0±23.3▲ 110.8±16.8▲ 136.3±28.0▲捧兴通脉颗粒组 1.5 98.8±13.7 121.4±12.6▲▲ 100.8±21.7▲ 124.9±16.2▲捧兴通脉颗粒组 3.0 93.2±15.9▲ 122.8±12.3▲▲ 103.9±27.1▲▲ 121.5±12.7▲▲
3.6 肝脏结构改变 图1显示,空白组大鼠肝体表面光滑,颜色暗红,无颜色、质地、体积异常,光镜下细胞大而结构完整,核圆居中,呈放射状分布,中央静脉区未见异常;模型组大鼠肝体呈粉黄色,包膜粗糙无光泽,肿胀而富有油腻感,光镜下肝细胞大小不一,排列不规则,肿胀核不居中,空泡增多,肝细胞脂肪样变性增多,部分细胞变性坏死;血脂康组、捧兴通脉颗粒组大鼠肝体颜色明显改善,颜色暗红,表面光滑,肿胀、坏死明显减轻,光镜下肝细胞排列有序,核圆居中,细胞结构轮廓清晰,未见空泡、肿胀和坏死,以血脂康组、捧兴通脉颗粒高剂量组肝细胞形态改善最为明显。
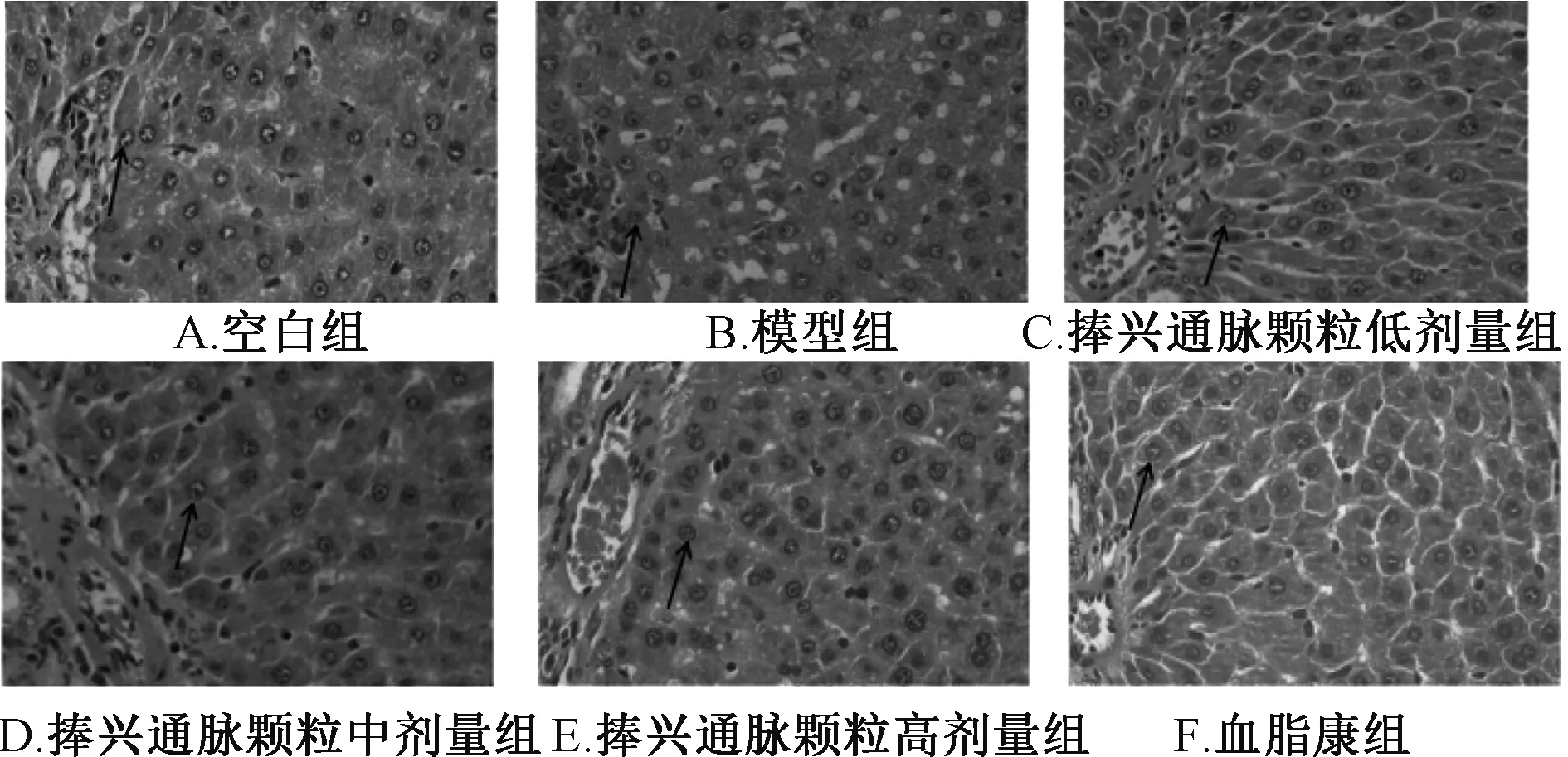
图1 各组大鼠肝组织病理学变化 (HE,×400)
4 讨论
高脂乳剂建立高脂血症大鼠模型时,具有省时省力、模型稳定等特点,可避免饲喂高脂饲料时大鼠食量不均、厌食症等问题[14]。另外,配方中加入丙硫氧嘧啶可增加胆固醇合成,诱发高脂血症,同时具有一定肝细胞毒性,可导致肝小叶损伤坏死,影响脂质、胆固醇、脂蛋白代谢[15];加入猪油和胆固醇可增加脂质、胆固醇摄入量,快速稳定地建模。本实验发现,模型组大鼠血清TC、TG、LDLC、ApoB水平及LCI、AI显著升高,HDLC、ApoA1水平及ApoA1/ApoB水平显著降低,ALT、AST水平显著升高,肝组织细胞出现显著脂肪变性,表明建模成功。
结果表明,捧兴通脉颗粒治疗3、6周后,大鼠血清TC、TG、LDLC水平及LCI、AI降低,HDLC水平升高,以6周效果最佳,表明它具有良好的调节血脂作用。ApoA1和HDLC是抗高脂血症的积极因素,而ApoB是一种含糖的血浆载脂蛋白,主要负责运输胆固醇,使胆固醇沉积于动脉血管壁,促进动脉粥样硬化的形成[15],捧兴通脉颗粒可升高血清 ApoA1水平,降低 ApoB水平,提高 ApoA1/ApoB,表明它可通过激活载脂蛋白功能,加速TC、TG、LDLC排泄,降低高脂血症对机体的损伤。同时,捧兴通脉颗粒可有效降低大鼠血清AST、ALT水平,明显改善肝组织细胞形态,减少肝细胞脂肪变性和肝小叶的结构变异,表明它对丙硫氧嘧啶、脂质、胆固醇造成的肝损伤具有一定的保护作用。
根据 《保健食品检验与评价技术规范》[16]结果判定标准,在血清TC、TG、HDLC 3项指标中TC、TG呈阳性即可判定样品具有辅助降血脂功能,而捧兴通脉颗粒对三者的作用均呈阳性,可认为它具有良好的调节血脂作用。
综上所述,捧兴通脉颗粒可明显降低血脂水平,改善肝功能及肝组织病理损伤,其机制可能与激活载脂蛋白功能及护肝作用有关。虽然高脂乳剂可建立高脂血症模型,但并不能建立肥胖模型,可能与肝损伤影响营养物质吸收和代谢有关,具体机制有待进一步研究,同时捧兴通脉颗粒是否对肥胖模型有效也尚需深入探索。

