以氯化血红素作为指示剂的Hg2+电化学传感器的制备与应用
陈碧娇,李晓燕,牛燕燕,谢 慧,罗贵铃,习亚茹,熊 懿,孙 伟
(海南师范大学 化学与化工学院 海口市功能材料与光电化学重点实验室,海南 海口 571158)
汞是一种有毒元素,易被皮肤和呼吸道吸收,严重危害人体健康[1-2]。近年来随着工业的发展,汞污染日趋严重[3-4],因此对快速精准检测Hg2+的方法提出了更高的要求。适配体能与相应的靶分子进行高亲和力和强特异性的结合,被称为“化学抗体”,具有靶分子范围广、易化学合成、便于修饰及稳定性好等优势[5]。氯化血红素(hemin)是一种天然的金属铁卟啉化合物[6],具有较强的吸附能力,可作为电活性分子,生物催化剂等。
图1 适配体传感器的实验原理示意图
Fig.1 Schematic diagram of experimental principle of aptamer sensor
本文将hemin作为指示剂构建一种可检测Hg2+的电化学适配体传感器。图1为该电化学传感器的工作原理示意图,将氮掺杂石墨烯(NG)通过滴涂法得到NG/CILE,再将纳米金(AuNPs)通过电沉积法[7-9]在NG/CILE表面沉积得到AuNPs/NG/CILE,通过自组装法[10]将适配体(aptamer)修饰在AuNPs/NG/CILE表面,制得aptamer/AuNPs/NG/CILE。将制得的aptamer/AuNPs/NG/CILE经硫代乙醇酸(TGA)处理后保持aptamer链处于直立状态。在没有Hg2+的情况下垂直平行的aptamer链能够有效防止hemin吸附到电极表面,而Hg2+存在时,碱基胸腺嘧啶(T)与Hg2+特异性结合可改变aptamer的排列形式,形成多孔结构[11]。Hemin可以通过这些孔隙吸附在修饰电极表面,其电活性中心Fe(Ⅲ)与电极表面之间会发生电子转移而产生电信号。采用循环伏安法(CV)和差分脉冲伏安法(DPV)研究该传感器对Hg2+的测定,结果表明其具有灵敏度高、特异性强、微型化等优点。
1 实验部分
1.1 仪器与试剂
CHI1210A型电化学工作站(上海辰华仪器公司),三电极系统:以修饰电极为工作电极,Ag/AgCl电极为参比电极,铂丝电极为辅助电极。
氯化血红素(hemin,合肥博美生物科技有限责任公司),硫代乙醇酸(TGA,上海阿拉丁生化科技股份有限公司),三羟甲基氨基甲烷(Tris,山东西亚化学工业有限公司),氮掺杂石墨烯(NG,南京先丰纳米材料有限公司),硝酸汞(Hg(NO3)2,广州化学试剂厂),氯金酸(HAuCl4,天津凯玛生化有限公司),N-己基吡啶六氟磷酸盐(HPPF6,兰州雨陆精细化工有限公司),适配体序列为:5'-SH-C6-TTT-TTT-TTT-TT-3'(上海生工生物工程有限公司),其他试剂均为分析纯,实验用水均为二次蒸馏水。
1.2 电化学适配体传感器的制备
离子液体修饰碳糊电极(CILE)的制备方法见文献[12]。
取8 μL NG溶液(0.5 mg/mL)均匀涂布在CILE表面自然晾干后,在2.0 mmol/L HAuCl4和0.5 mol/L KNO3的混合溶液中进行恒电位沉积实验,沉积电位为-0.3 V,沉积时间为300 s,静置100 s后取出电极轻洗,自然晾干得到AuNPs/NG/CILE。将AuNPs/NG/CILE置于4 ℃条件下于适配体溶液(2 μmol/L)中自组装60 min后,表面清洗后再用0.1 mmol/LTGA浸泡后即可得到aptamer/AuNPs/NG/CILE。
2 结果与讨论
2.1 适配体传感器中hemin的循环伏安图
适配体修饰电极在含有5 μmol/L hemin的二甲基亚砜(DMSO)[11]溶液中浸泡60 min后在10 mmol/L Tris-HCl缓冲液(pH值=7.4)进行循环伏安测试,如图2A所示,无Hg2+存在时可观察到弱的还原峰;含有5 μmol/L Hg2+时出现明显的还原峰(曲线b)。对照实验为适配体修饰电极在不含hemin的DMSO溶液中处理后,在10 mmol/L Tris-HCl缓冲液(pH值=7.4)中的循环伏安图(如图2B)。显然,在没有Hg2+(曲线a)和有Hg2+(曲线b)的情况下均没有观察到明显的氧化还原峰。结果表明Hg2+的存在可增强hemin在电极界面的吸附作用,从而增大电化学检测信号。
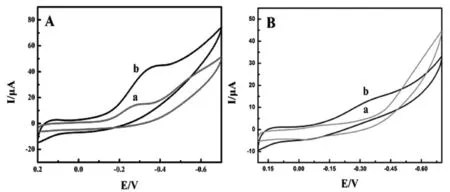
(A)有hemin对适配体修饰电极;(B)无hemin对适配体修饰电极
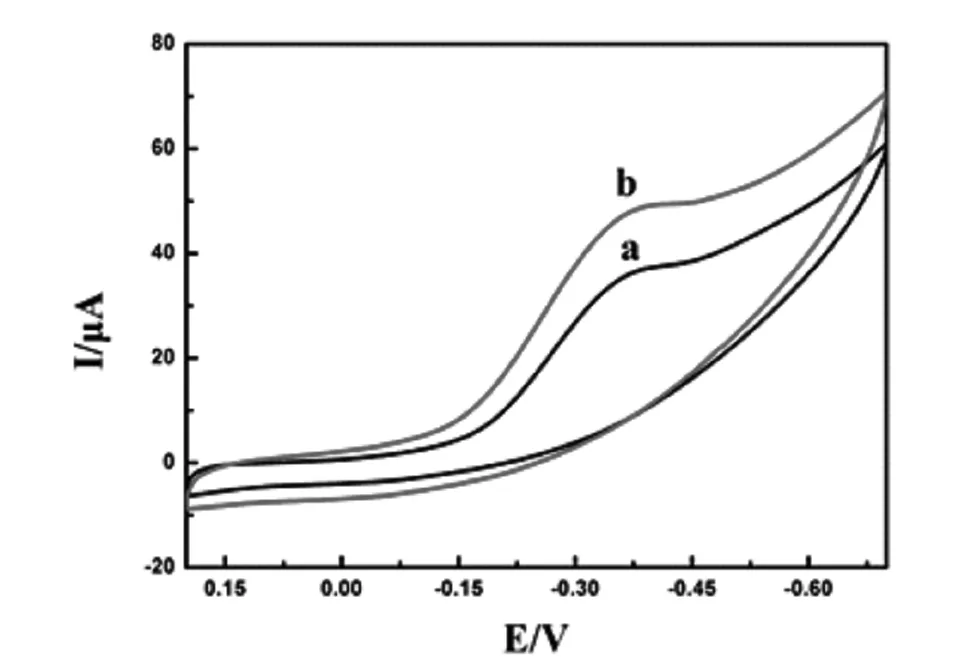
a-b:Hg2+/aptamer/AuNPs/CILE,Hg2+/aptamer/AuNPs/NG/CILE
利用循环伏安法(CV)对修饰了NG的适配体传感器进行电化学行为研究(如图3)。Hg2+/aptamer/AuNPs/CILE(曲线a)上出现了还原峰,其电流值为26.49 μA;修饰NG后,Hg2+/aptamer/AuNPs/NG/CILE(曲线b)的还原峰电流明显增大为37.13 μA,高比表面积NG能够提高aptamer在电极表面上的负载量,有效地加快电子转移速率,从而提高导电速率。
2.2 实验条件的优化
采用自组装法将适配体序列固定在修饰电极表面上,自组装时间是影响适配体传感性能的重要因素。自组装时间对电化学信号的影响如图4所示。当自组装时间从20 min向60 min变化时,随着组装时间的增加,峰电流逐渐增加;当组装时间在60 min到120 min之间,峰电流开始下降,因此选择最佳的自组装时间为60 min。

a-f: 20 min,40 min,60 min,80 min,100 min,120 min
图4 (A)不同组装时间下,Hg2+/aptamer/AuNPs/NG/CILE在Tris-HCl(pH值=7.4)
混合溶液中的循环伏安图;(B)不同组装时间与峰电流的关系曲线
Fig.4 (A)Cyclic voltammograms of Hg2+/aptamer/AuNPs/NG/CILE in Tris-HCl (pH=7.4) solution with different assembly times;(B)Relationship of different self-assembly time and the peak current
2.3 工作曲线
在10 mmol/L Tris-HCl (pH值7.4)缓冲液中采用DPV研究不同浓度Hg2+溶液(含2 μmol/L hemin)对aptamer/AuNPs/NG/CILE电化学行为的影响,结果如图5A所示。随着Hg2+浓度的增加,峰电流值也逐渐增大,这是由于Hg2+浓度的增大使电极表面形成的T-Hg2+-T数量增加,适配体膜的孔隙增多,从而导致hemin在电极界面的吸附量增大,峰电流值也随之增大。还原峰电流(Ipc)与Hg2+浓度的对数呈现良好的线性关系(如图5B),线性回归方程为Ipc(μA)=6.115+48.021 lg C(mol/L) (γ=0.995),检测限为1.67×10-8mol/L (3σ),线性范围为5.0×10-8~5.0×10-6mol/L。

a-f: 5.0×10-8,1.0×10-7,5.0×10-7,1.0×10-6,2.0×10-6,5.0×10-6mol/L
图5 (A)不同浓度Hg2+在aptamer/AuNPs/NG/CILE上的DPV曲线;(B)Hg2+浓度的对数与峰电流值的线性关系曲线
Fig.5 (A)DPV of Hg2+detection on aptamer/AuNPs/NG/CILE;(B)Linear relationship between logarithm of Hg2+concentration and the peak current value
2.4 干扰测定
探究其他非特异性金属离子(如浓度均为1 mmol/L Na+、K+、Co2+、Cd2+和Ba2+)对本实验所制备的Hg2+电化学适配体传感器的干扰实验。通过对比实验结果(图6),发现非特异性的金属离子对该适配体传感器的干扰很小,这是由于本方法所采用的适配体只能与Hg2+发生特异性结合而不和其它金属离子发生相互作用,因此该修饰电极对Hg2+具有较好的特异性识别能力。
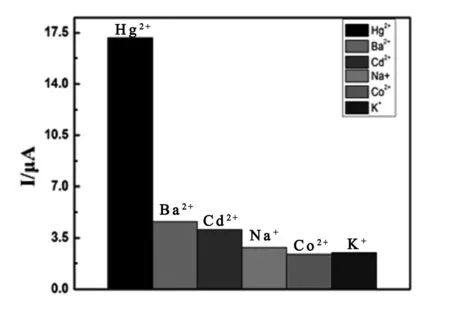
图6 Hg2+和干扰离子(Na+、K+、Co2+、Cd2+和Ba2+)
3 结论
本文研究了一种以hemin作为指示剂的Hg2+电化学适配体传感器。Hg2+存在时,胸腺嘧啶T碱基与Hg2+的特异性结合可改变aptamer的排列形式,使其形成多孔结构。此时,hemin可以通过这些孔隙吸附在修饰电极表面产生电化学信号。将所构建的适配体传感器应用于微量Hg2+的检测,具有良好的应用前景。

