胃癌患者的E-钙黏蛋白、波形蛋白、甲胎蛋白表达水平及其临床意义研究
陈恒,江立千
(河南圣德医院临检中心,河南 信阳 464100)
流行病学研究证实,2010-2017年每年部分地区胃癌的平均发病率可达274~593/10万人左右[1]。临床上胃癌的发生不仅能够导致患者生活质量的显著下降,同时患者的五年生存率和中位生存时间可明显的恶化[2]。
在胃癌发生过程中的相关分子机制研究中,可以发现不同的分子或者蛋白水平的改变,均能够促进胃癌的发生,加剧胃癌患者病情的进展速度。E-钙黏蛋白的表达能够通过促进上皮细胞间质成分的分解,促进癌细胞侵袭能力的增加,进而促进了癌细胞对于胃黏膜基底膜组织的浸润和突破过程[3];波形蛋白的表达,能够通过维持上皮细胞的极性,稳定上皮细胞的增殖过程,降低癌细胞的扩散和转移的风险[4];甲胎蛋白是消化道重要的生物学肿瘤标志物,在胃肠道黏膜上皮细胞的持续性DNA分裂的过程中,甲胎蛋白的表达浓度可明显的上升[5]。为了揭示E-钙黏蛋白、波形蛋白、甲胎蛋白的表达与胃癌患者的关系,从而为临床上胃癌的病情评估提供参考,为胃癌患者的血清学筛查提供分子标志物,本次研究选取2016年5月-2017年8月在我院接受治疗的胃癌患者为研究对象,探讨了E-钙黏蛋白、波形蛋白、甲胎蛋白的表达及其与胃癌患者临床病理特征的关系,报道如下。
1 资料与方法
1.1 患者一般资料 选取2016年5月-2017年8月在我院接受治疗的胃癌患者为研究对象。纳入标准:⑴年龄18~80岁;⑵手术病理诊断为胃癌者;⑶无其他系统严重疾病者;排除标准:⑴临床资料不全者;⑵合并其他部位原发肿瘤者。根据纳入排除标准共纳入研究对象100例,其中男62例,女 38例,年龄 42~75岁,平均 50.18±6.12岁。对照组纳入排除标准:⑴年龄18~80岁;⑵经活检确诊为胃炎者,排除恶性病变者,根据纳入排除标准共纳入病例数100例,男50例,女50例,年龄42~76岁,平均50.22±5.79岁。两组患者年龄、性别等一般资料比较无差别,具有可比性。
1.2 检测方法 所有组织标本经石蜡包埋后作连续切片,厚度约为4um采用免疫组化链霉卵白素一生物素复合体法 (strep avidin-biotin complex,SABC法)染色,二氨基联苯胺(diamionben zidene,DAB)显色。E-钙黏蛋白、波形蛋白、甲胎蛋白通用型二抗以及SP试剂盒和DAB显色盒均购自北京中杉金桥生物技术开发公司。以阳性片及PBS代替一抗分别作为阳性及阴性对照,高倍显微镜下观察E-钙黏蛋白、波形蛋白、甲胎蛋白的表达情况,具体染色步骤严格按照SP试剂盒说明书进行操作。
1.3 评价指标 观察两组患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况,比较不同特征胃癌患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况的差异,分析影响胃癌患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况的因素。
1.4 统计学处理 数据录入后,采用SPSS 11.5软件进行分析。计数和计量资料分别采用例和均数±标准差表示。两组患者、不同特征胃癌患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况的比较采用卡方检验进行分析。采用Logistic回归分析法分析影响胃癌患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况的因素。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况的比较 胃癌患者的E-钙黏蛋白阳性表达率高于胃炎组,波形蛋白阳性表达率低于胃炎组,两组患者的甲胎蛋白阳性表达率无差别。见表1。
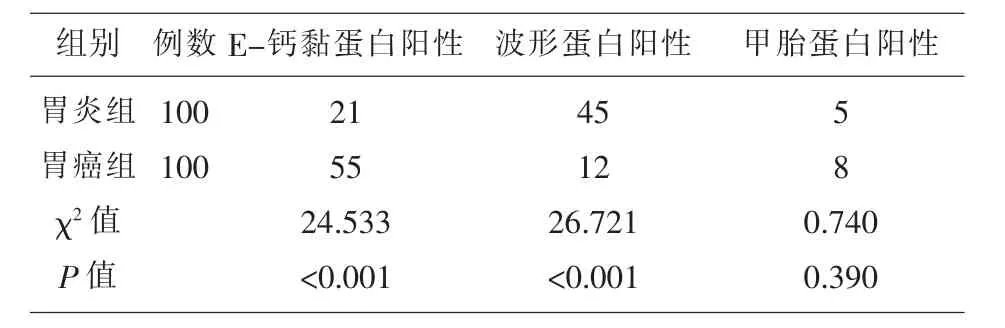
表1 两组患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况的比较
2.2 不同特征胃癌患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况的比较 分化程度为中低分化、有淋巴结转移、有肝转移、TNM分期为Ⅲ+Ⅳ的胃癌患者的E-钙黏蛋白和甲胎蛋白阳性表达率较高,波形蛋白阳性表达率较低,不同年龄、性别胃癌患者的E-钙黏蛋白、波形蛋白、甲胎蛋白阳性表达率无差别。见表2。
2.3 影响胃癌患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况的因素分析 将单因素分析有意义的因素作为自变量,将胃癌患者E-钙黏蛋白、波形蛋白、甲胎蛋白阳性表达作为因变量,进行回归分析,结果显示分化程度和淋巴结转移是影响E-钙黏蛋白、波形蛋白表达的因素,肝转移和淋巴结转移是影响甲胎蛋白表达的因素。见表3、表4、表5。

表2 不同特征胃癌患者E-钙黏蛋白、波形蛋白、甲胎蛋白表达情况的比较

表3 影响胃癌患者E-钙黏蛋白阳性表达率的因素
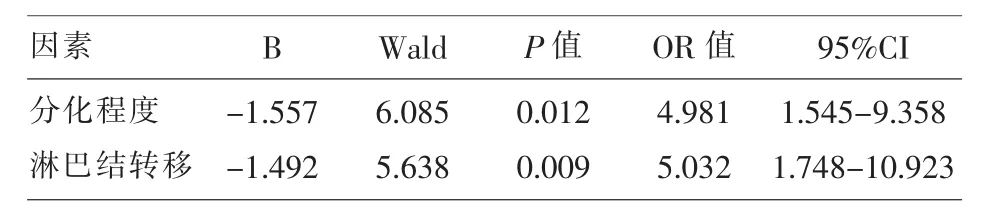
表4 影响胃癌患者波形蛋白阳性表达率的因素

表5 影响胃癌患者甲胎蛋白阳性表达率的因素
3 讨论
幽门螺杆菌感染能够显著促进胃黏膜上皮细胞的病变,增加胃癌的发生风险,特别是在合并有慢性萎缩性胃炎或者胃肠道上皮化生的患者中,胃癌的发生风险可进一步的上升[6]。现阶段临床上主要通过手术治疗胃癌,但包括手术及术后放疗治疗后,胃癌患者的临床病情缓解率仍然较低,治疗后的患者无进展生存期仍然无明显的改善。而免疫靶向性治疗,能够在胃癌患者的辅助治疗过程中发挥重要作用,本次研究对于胃癌患者体内的E-钙黏蛋白、波形蛋白、甲胎蛋白的表达分析研究,不仅能够深入揭示胃癌的发生机制,同时还能够为胃癌患者的免疫靶向性治疗提供参考靶点。
E-钙黏蛋白是上皮间质转化因子的成员,其能够通过促进癌细胞间质成分的分解,促进金属基质蛋白酶的激活,从而降低癌细胞间的粘附程度,促进了癌细胞的扩散和转移过程。同时基础方面的研究还证实,E-钙黏蛋白能够通过提高癌细胞上游转录活性的增加,进而提高癌细胞纺锤体的复制和分裂速度,促进癌细胞的持续性自我扩增[7];波形蛋白是上皮间质转化过程中的重要负性调控因子,其能够维持上皮细胞的极性和形态,抑制癌细胞间质成分的过度分解,降低癌细胞的变形能力[8]。波形蛋白还能够稳定癌细胞间缝隙连接蛋白的浓度,提高癌细胞间缝隙连接的数量,进而进一步稳定癌细胞的生物学特征[9];甲胎蛋白是评估消化系统肿瘤发生的重要标志物,在肝癌患者中具有明显上升趋势,虽然部分研究者探讨了甲胎蛋白的表达与胃癌的关系,认为甲胎蛋白的表达上升与胃癌患者的临床转归的恶化密切相关[10,11],但对于E-钙黏蛋白、波形蛋白与胃癌患者临床病理特征的分析研究不足。
本次研究通过免疫组化方法,探讨了E-钙黏蛋白、波形蛋白、甲胎蛋白的表达与胃癌患者的关系,发现在病例组患者中,E-钙黏蛋白的表达明显的上升,而波形蛋白的表达明显的下降,提示E-钙黏蛋白、波形蛋白的异常表达均能够促进胃癌的发生过程。通过汇集不同的相关文献,笔者认为这主要由于E-钙黏蛋白、波形蛋白的下列几个方面的作用有关[12,13]:⑴E-钙黏蛋白的上升能够促进上皮间质转化病理过程的进展,促进金属基质蛋白酶对于癌细胞间质成分的分解,为癌细胞的迁移和对于基底膜组织的浸润提供前提;⑵波形蛋白水平的下降失去了其对于癌细胞生物学特征的稳定作用,导致癌细胞间细胞连接蛋白的不足,促进了癌细胞的扩散。王红山等[14]研究者也认为,在胃癌患者中,E-钙黏蛋白的表达阳性率可平均上升30%以上,特别是在合并有明显的肌层浸润或者局部引流淋巴结转移的患者中,E-钙黏蛋白的表达阳性率可进一步的上升。但本次研究并未发现在胃癌患者中甲胎蛋白的表达阳性率的上升,这与王雅坤等[15]研究者的结论存在一定的差别,这可能与本次研究中胃癌患者的临床分期多数为早期患者,同时可能与甲胎蛋白的检测灵敏度的不同有关。在探讨相关指标与胃癌患者临床病理特征的关系中,可以发现中低分化、有淋巴结转移、有肝转移、TNM分期为Ⅲ+Ⅳ的胃癌患者的E-钙黏蛋白和甲胎蛋白阳性表达率较高,而波形蛋白的表达阳性率较低,提示了相关肿瘤蛋白的表达与胃癌患者的临床病理特征关系较为密切,这主要由于E-钙黏蛋白、甲胎蛋白的上升,能够提高胃黏膜上皮癌细胞对于淋巴结内皮的粘附能力,导致胃黏膜腺体细胞的分化成熟过程的异常;而波形蛋白的下降,能够影响到胃黏膜上皮细胞的形态学的改变,并增加了癌细胞的浸润和畸变的风险,从而促进了相关临床病理特征的进展。危险因素的分析也可见,分化程度和淋巴结转移是影响E-钙黏蛋白、波形蛋白表达的风险因素,而肝转移和淋巴结转移是影响甲胎蛋白的风险因素,进一步提示了相关蛋白的表达与胃癌患者的病情关系。
综上所述,在胃癌患者中,E-钙黏蛋白的表达明显上升,而波形蛋白的表达明显下降,同时E-钙黏蛋白、波形蛋白、甲胎蛋白的异常表达,均能够促进胃癌患者临床病理特征的进展。后续临床相关研究,可以继续探讨E-钙黏蛋白、波形蛋白、甲胎蛋白的表达与胃癌患者临床预后转归的关系。

