阿维菌素纳米乳剂的研制及其检测
穆永才 罗天瑶

摘要:为了研制成阿维菌素纳米乳制剂,筛选出由油酸乙酯、吐温80、1,2-丙二醇、纯水组成的空白纳米乳体系。经溶解试验,该体系对阿维菌素的溶解性良好,可达1.6%以上。选取1%的阿维菌素纳米乳剂,进行质量和安全性评价,结果表明:这种阿维菌素纳米乳剂理化指标合格,无刺激性、无过敏性、无溶血性,稳定,安全可靠。
关键词:纳米乳;阿维菌素;新剂型;研制;检测
中图分类号:S859.5 文献标识码:A
文章编号:2095-9737(2019)03-0001-04
阿维菌素是大环内酯类抗生素,具有结构新颖、农畜两用的特点。目前,在市场上销售的阿维菌素原药是以abamectin为主要杀虫成分,并以B1a的含量来标定[1]。這种抗生素在兽医临床上主要用于畜禽的消化道线虫和外寄生虫的驱杀。常用的剂型有粉剂和注射剂等。这些剂型一度满足防治畜禽相应寄生虫的需求,但也存在着持效期短、需多次给药、药效不稳定等缺点。纳米乳剂是由油相、水相、乳化剂和助乳化剂组成的相对稳定体系,制成药剂具有生物活性高、缓释、刺激性小、毒性低、稳定的特点[2]。为了克服现有阿维菌素制剂的诸多不足,笔者研制成一种阿维菌素纳米乳制剂,并对其特性进行测定,现报道如下。
1 材料
1.1 仪器设备
激光粒度仪(winner802型),由济南微纳颗粒仪器股份有限公司生产;运动黏度自动测定仪(ZTND2000型),由上海平轩科学仪器有限公司生产;电导率仪(DDSJ-318型),由上海仪电科学仪器股份有限公司生产;恒温磁力搅拌器(S10-2型),由上海司乐仪器有限公司出品;ZYP-320偏光显微镜,上海兆仪光电有限公司生产,HT7700透射电镜,日本日立公司生产;MiniSpan Plus微型高速离心机,杭州奥盛仪器有限公司生产;WAY-2W阿贝折射仪,上海精科实业有限公司生产;LC-20AT液相色谱仪,日本岛津公司生产;FAT2104电子天平,常州万得天平仪器有限公司生产。BR120-4固液比重计,百荣精密仪器有限公司生产。
1.2 主要试剂
阿维菌素原药(B1≥90%),大庆志飞生物化工有限公司生产;油酸乙酯、乙酸乙酯,江西阿尔法高科药业有限公司生产;聚氧乙烯氢化蓖麻油(Cremophor RH40),德国巴斯夫公司(BASF)生产;Transcutol.V(二乙二醇单乙基醚兽用型),法国嘉法狮公司(Gattefossé)生产;吐温80、1,2-丙二醇、正丁醇、无水乙醇,天津富宇精细化工有限公司生产;色谱甲醇,购自天津赛孚瑞科技有限公司;阿维菌素色谱标准样品,沈阳化工研究院生产。纯化水,检验研究室自制。
1.3 实验动物
健康状况良好的成年大耳白兔4只,雌雄各半,购于富裕县华美养兔场;体重50 kg绵羊20只购自于齐齐哈市北郊养羊户。这些实验动物均为舍饲,自由采食,自由饮水,实验前进行临床健康观察。
2 方法
2.1 阿维菌素纳米乳剂的制备
2.1.1 增溶体系的选择
以各组分均为医药级产品、对阿维菌素增溶能力强、形成稳定的纳米乳剂为标准,进行增溶体系的选择。预选的体系有油酸乙酯、水、聚氧乙烯氢化蓖麻油、二乙二醇单乙基醚体系[2],油酸乙酯、水、吐温80、1,2-丙二醇体系[3],乙酸乙酯、水、吐温80、无水乙醇体系[4],油酸乙酯、水、吐温80、正丁醇体系[5]。
筛选方法采取2种方式。方式1是将每个预选体系的油相、乳化剂、助乳化剂及主药按一定质量依次混合后,再逐滴加入水相,观察体系状态。油相与总表面活性剂的比例分别是1∶9;1∶8;1∶7;1∶6;1∶5;1∶4。乳化剂与助乳化剂的比例(Kim值)分别为3∶1;2.5∶1;2∶1;1∶1。方式2是预先将油相与主药混合制成油药溶液。混合的次序是乳化剂、助乳化剂、油药溶液。逐滴加水,观察体系状态。油药与总表面活性的比例和乳化剂与助乳化剂的比例(Kim值)同方式1。采用以上两种方式在4种体系中筛选出油酸乙酯、水、吐温80、1,2-丙二醇体系为最佳增溶体系。经反复多次试验,形成浓度高达1.6%以上阿维菌素纳米乳。
2.1.2 1%阿维菌素纳米乳的制备
称取21.50%的乳化剂于制药烧杯底部,再称取8.68%的助乳化剂置于乳化剂之上,然后再称取3.77%的油药溶液置于助乳比剂之上。将转子和温度探头置于制药烧杯内,设定转数为120 r/min,温度为35℃,开启磁力搅拌器开关。边搅拌,边逐滴加入纯化水,滴水速度控制在60滴/min,当加入水量达到66.05%时,关闭滴定管阀门,停止滴水,继续搅拌至溶液透明为止。
将上述药液过滤除菌后,分装于高温干燥灭菌的青霉素瓶中,用于各项检测之用。
2.2 纳米乳剂的检测
2.2.1 理化性质的检测
2.2.1.1 粒度检测
使用光相关纳米粒度仪进行检测。测试条件:分散介质为水,折射率为1.333,粘度为8.904E-04Pa.S,测试温度为25℃,延迟单位时间是25μs。
2.2.1.2 纳米乳类型检测
采取如下两种方法[6]:①稀释法,将少量的乳状液分别加入油和水中轻轻摇动,看乳状液在油中还是在水中容易分散。当乳状液加入油中容易分散,则油为连续相,说明乳状液为W/O型;当乳状液加入水中容易分散时,则水为连续相,乳状液为O/W型。②滤纸法,将一滴乳状液滴于滤纸的中心,如果乳状液为O/W,即水为连续相时,水容易在滤纸上通过毛细作用而向外扩散,最终在滤纸的中心剩余1个小油点。但如果是W/O型乳状液时,乳状液几乎在滤纸上不扩散。
2.2.1.3 粘度检测
采用运动粘度测定仪进行检测。测试前参数设置:样品号码:0001#,当前粘度计1#,1#粘度计系数为0.8,预置温度25℃,温度微调-0.5℃,打开自动控温,开启打印,设置好日期和时间。将药剂按要求吸入毛细管粘度计内,并将毛细管粘度计置于恒温槽中,即可检测,每样品检测3次,取其均值。
2.2.1.4 密度检测
选用固液比重计进行检测。用100 g标码进行校正,设定常用参数,选择测量模式,按照液体比重测量的操作方法进行。
2.2.1.5 电导率检测
开机后在仪器的起始状态进行设置操作。在测量模式中勾选电导率选项和连续测量模式;在系统设置中进行操作编号;在设置电导常数中设置与电导电极上标注的同样的电导常数。按要求安装好电导电极以及温度传感器,准备好待测溶液后,即可开始测量。
2.2.1.6 双折射现象检测
采取偏光显微镜法检测。经过调节亮度、调焦、调整载物台和物镜中心重合、孔径光阑中心调节、正交偏光观察等几个步聚,观察被检样品有无双折射现象的发生。
2.2.1.7 pH值检测
采用pH计法测定。准备:按使用说明进行相关准备,仪器标定:打开电源开关,仪器进入pH测量状态。调节温度使温度显示值和溶液温度一致。按“标定”键,任选两种标定液进行标定。测量:用蒸馏水及被测溶液清洗电极后即可对被测液进行测量。
2.2.1.8 稳定性检测
采取了恒温储存试验。即将药品试样分别储存在高温(40℃)和常温(20~25℃)的环境中,随时观察药样的外观变化,并按一定时间间隔进行药样粒度和主药含量检测。
2.2.2 阿维菌素含量的测定
采用液相色谱分析方法。色谱条件:高效液相色谱仪(具有紫外可变波长检测器);色谱柱:150 mm×3.9 mm(id)不锈钢柱,内装Nova-PakC18、5 μs填充物;流动相:甲醇+乙腈+水=38+38+24,经过滤、脫气处理;流量控制在1.0 mL/min;柱温:置室温下,其温差变化不能大于2℃;检测波长:245 nm;进样体积:5 μL;保留时间:B1a 15.6 min,B1b 11.3 min。
2.2.3 纳米乳剂的溶血试验
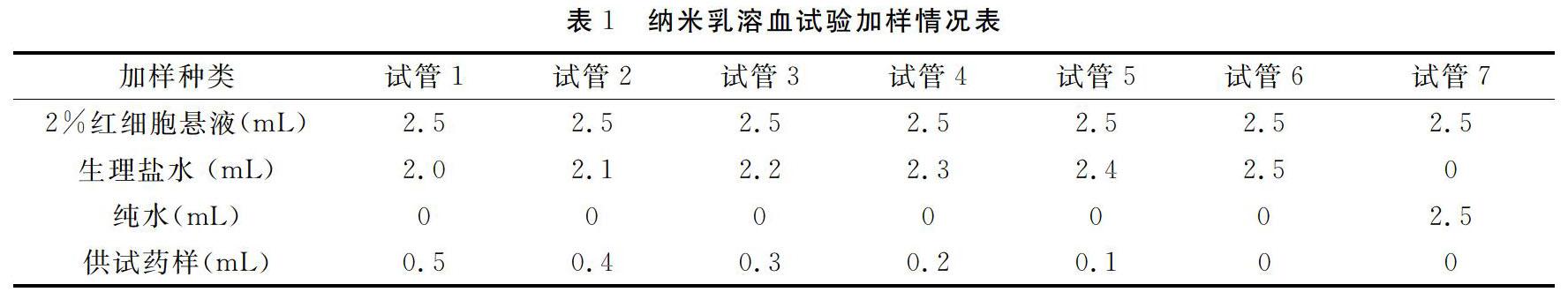
按有关文献[7]介绍的方法进行。首先制成2%兔红细胞悬液。再用生理盐水对1%阿维菌素纳米乳制剂进行稀释(稀释比为1∶3)后当作供试药液。然后取7支10 mL试管,分别编号为1~7号,将1~5号管作为试样品管,将6号管作为阴性对照管,将7号管作为阳性对照管。各试管加样种类、次序及加样量见表1。
按上表依次加样,混匀后置37℃恒温箱中温育。记录0.25 h,0.5 h,1 h,2 h,3 h的结果。当阴性对照管(凝聚和无溶血发生)和阳性对照管(有溶血)条件成立的情况下,在3 h内,如果试样管中的溶液不发生凝聚和溶血,则受试药液可以注射使用;若试样管中的溶液发生凝聚和(或)溶血,则受试药液不宜注射使用。
2.2.4 纳米乳剂对家兔的刺激性试验
遵循有关文献[8]进行。利用白兔背部皮肤脱毛处理后,分成左右、前后四区。将生理盐水和伊维菌素微乳制剂一次性涂抹于指定的皮肤区域,剂量均为0.5 mL.观察皮肤接触受试物后是否引起红肿、充血、渗出等局部反应,根据制定的“皮肤刺激反应评分标准”和“皮肤刺激强度评价标准”评定药物对家兔皮肤的刺激性。同时将受试物滴于家兔眼结膜囊内,观察虹膜、角膜和结膜是否出现浑浊、充血、水肿等局部反应,依据“眼刺激试验评分标准”和“眼刺激程度评价标准”评价药物对家兔眼睛的刺激性。
2.2.5 对靶动物绵羊的安全性试验
将20只绵羊随机分成4组,设1倍量、3倍量、5倍量、空白对照、处理,每组的给药剂量分别为0 mg/kg、0.2 mg/kg、0.6 mg/kg、1.0 mg/kg体重肌注给药,二次用药24 h后,于静脉采血进行血液生化和血液学的检测,以及病理学检查。整个试验期间每天定时观察试验羊的精神、饮食和临床症状的改变并记录死亡情况。
3 试验结果
3.1 理化性质检测结果(见表2)
3.2 稳定性检测结果(见表3)
3.3 溶血试验结果
在试验观察期内,阳性对照组可见完全溶血现象,其他各组未见溶血和凝集现象的发生,说明1%阿维菌素纳米乳注射液可供注射使用。
3.4 刺激性试验结果
破损皮肤试验区24 h后已无刺激性,完整试验区30 min后无刺激性。对照组破损皮肤试验区在去除受试物30 min后对皮肤无刺激性。根据评分标准将该注射液对皮肤的刺激性定为无刺激。
受试兔双眼角膜、结膜、虹膜均正常。该注射液对家兔的眼部无明显影响。依据眼的刺激反应评分统计结果判定该制剂对家兔眼睛无刺激性。
3.5 安全性试验结果
整个试验期内,试验、对照各组羊健康状况良好,精神、饮水、采食未见异常。无中毒和死亡的现象发生。
血液、生化及病理学检测结果表明,1%阿维菌素纳米乳注射液对羊的血细胞生成无不良影响,对羊的肝、肾功能和各物质代谢均无不良影响,未发现各组羊的实质器官有异常和可疑的病变。
4 讨论与分析
阿维菌素已广泛应用于农业和畜牧业病虫害的防治。在兽医临床上主要用于畜禽消化道线虫和体外寄生虫的驱杀。对于如此重要的抗寄生虫病药物新剂型的研究和探索一直是业内人士的热点课题。目前的研究和生产实践表明,用于防治植物病虫害的阿维菌素纳米乳剂已有市售。在防治畜禽寄生虫病方面,兽用伊维菌素纳米乳的研制已有报道[2],但兽用阿维菌素纳米乳剂尚未见报道。伊维菌素与阿维菌素,虽为同类药物,结构相似,药效相同,但阿维菌素的价格较伊维菌素低。本项研究的难点主要在于对阿维菌素溶解性好、稳定、毒性低或无毒的纳米乳基质的研制及生产工艺的建立。
在研制过程中,结合国内外已有报导和多年从事纳米乳兽药研究经验,在四种医用纳米乳基质中,筛选出油酸乙酯、吐温80、1,2-丙二醇、纯水为组分的阿维菌素纳米乳增溶体系。经特殊工艺处理后,对阿维菌素的增溶浓度可达到1.6%以上,此浓度高于常规注射剂(1%),加之纳米乳剂具有微量高效的特性,因此完全满足临床需求。研制的另一个难点是纳米乳剂主药浓度的测定。为了使B1a和B1b与杂质完全分离,项目组经多次试验发现以38%乙腈、38%甲醇与24%纯水(均为体积百分比)组成流动相,可以解决这一问题。这种定量方法简便可行,准确度和精密度较好。
按照《中国兽药典》[9]、《化学药物刺激性、过敏性和溶血性研究技术指导原则》[10],参考有关文献方法进行了1%阿维菌素纳米乳剂理化性质、安全性以及刺激性、过敏性和溶血性的试验。结果表明,该制剂稳定(稳定期在2年以上),理化指標符合相关规定,对靶动物安全,无刺激性、过敏性和溶血性。
上述试验结果为该制剂的临床应用打下了良好的基础。
参考文献:
[1] 邹磊,张玉华.阿维菌素的发展趋势展望[J].黑龙江医药,2006,19(3):200.
[2] 罗天瑶,穆永才,兰世捷.伊维菌素纳米乳剂的研制及其评价[J].黑龙江畜牧兽医,2017(12):156-158,296.
[3] 张继瑜,李剑勇,周绪正,等.一种伊维菌素纳米乳药物组合物及其制备方法:中国,2008101503549[P].2010-01-13.
[4] 芮亚培,欧阳五庆,邱刚,等.红霉素纳米乳的制备及其药效学的研究[J].西北农林科技大学学报(自然科学版),2008,36(3):59-63.
[5] 刘根新,张继瑜,吴培星,等.伊维菌素纳米乳注射液的研制与质量安全性评价[J].畜牧兽医学报,2011,42(8):1161-1167.
[6] 王军,杨许召.乳化与微乳化技术[M].1版.北京:化学工业出版社,2012.
[7] 邢守叶,周绪正,李冰,等.伊维菌素微乳制剂的溶血性试验[J].黑龙江畜牧兽医,2015(6):98-99.
[8] 刘磊,张继瑜,周绪正,等.伊维菌素微乳剂的家兔刺激性试验[J].江苏农业科学,2013,8:197-199.
[9] 中国兽药典委员会.中华人民共和国兽药典(2015年1部)[M].北京:中国农业出版社,2016.
[10] 中华人民共和国卫生部药政局.化学药物刺激性、过敏性和溶血性研究技术指导原则[M].2005:208-209.

