褪黑素固体脂质纳米粒的制备及其体外透皮吸收研究Δ
王锡辉,王亚平,王向宇,宋宜蕾,王兴荣,王建泽,郝吉福(山东第一医科大学/山东省医学科学院药学院,山东泰安 271016)
褪黑素(Melatonine,MT)是由脑松果体分泌的一种内源性神经激素,又名松果体素、褪黑色素,具有改善睡眠质量、调整人体昼夜节律、抗氧化及调节免疫等生理作用[1]。然而,由于MT的半衰期短,吸收差且不稳定,口服存在不可避免的首关效应,因此设计合适的药物递送系统以提高该药的吸收效率是目前药剂学领域亟待解决的问题之一[2]。固体脂质纳米粒(SLNs)是以天然或合成的固态类脂为材料,将药物包裹或镶嵌在类脂核中,制成的具有缓释性和靶向性的且粒径<1 000 nm的纳米递送系统[3]。由于SLNs的粒度效应可明显提高药物的透皮吸收程度,故常被作为药物经皮递送系统的载体[4-5]。为此,本研究以MT为模型药物,山嵛酸甘油酯为油相,泊洛沙姆188(F188)为乳化剂,通过熔融乳化法[6]制备MT固体脂质纳米粒(MT-SLNs),并采用Franz扩散池法考察该制剂的体外透皮行为,以期为后续MT经皮递送系统的深入研究提供理论支持。
1 材料
1.1 仪器
VP-10A型高效液相色谱仪、IRAFFINITY型红外光谱仪(日本Shimadzu公司);Nano-S 90型激光粒度分析仪(英国Malvern公司);RYJ-6A型药物透皮扩散试验仪(上海黄海药检仪器有限公司);JEM-1200EX型透射电镜(日本JEOL公司);JY92-2D型超声细胞粉碎机(宁波新芝生物科技股份有限公司);EYELA FDU-1200型冻干机(日本EYELA公司);K30型高速冷冻离心机(美国Sigma公司);ME104T型分析天平[梅特勒-托利多仪器(上海)有限公司]。
1.2 药品与试剂
MT原料药(上海阿拉丁生化科技股份公司,批号:20170923,纯度:98%);MT对照品(中国食品药品检定研究院,批号:520023-201301,纯度:99.8%);山嵛酸甘油酯(批号:20161226)、F188(批号:20170118)均购自北京凤礼精求商贸有限公司;超滤离心管(30 kDa,美国Millipore公司);聚山梨酯80(Tween-80,天津巴斯夫化工股份有限公司);甲醇为色谱纯,其余试剂均为分析纯,水为双蒸水。
1.3 动物
清洁级昆明种小鼠,雌雄各半,6周龄,体质量(20±2)g,购自济南朋悦实验动物繁育有限公司,动物生产许可证号:SCXK(鲁)20140007。
2 方法与结果
2.1 MT-SLNs与空白SLNs的制备
采用熔融乳化法[6]制备MT-SLNs。精密称取MT原料药50 mg、山嵛酸甘油酯500 mg,溶于无水乙醇5 mL中,水浴加热至85℃至熔融,作为油相;另取乳化剂F188 0.2 g,溶于水20 mL中,作为水相,水浴加热至上述相同温度,将水相与油相混合并搅拌均匀,于85℃保温条件下置超声细胞粉碎机中超声(功率:400 W,频率:20 kHz)5 min,直至反应体系由白色乳浊液变为淡蓝色澄清液体,继续搅拌以挥干有机溶剂,随后将其迅速转移至冰水浴中进行固化,即得MT-SLNs(含MT原料药2.5 mg/mL、山嵛酸甘油酯25 mg/mL、F188 1%)。同法制备不含MT的空白SLNs,备用。
2.2 MT-SLNs的表征

图1 MT-SLNs的透射电镜图(×20 000)Fig 1 TEM image of MT-SLNs(×20 000)

图2 MT-SLNs的粒径分布Fig 2 Particle size distribution of MT-SLNs
2.2.1 形态观察与粒径检测 取“2.1”项下MT-SLNs适量,用水稀释后,使用透射电镜观察其形态,使用激光粒径分析仪检测其粒径分布。结果,所得MT-SLNs呈圆球状,且未见聚集现象发生;其平均粒径为(67.88±0.17)nm,多分散指数为0.188±0.001,详见图1、图2。
2.2.2 红外光谱检测 取“2.1”项下MT-SLNs适量,经冷冻干燥后,取冻干粉末2 mg,加入干燥的溴化钾10 mg,研磨后压片,置于红外光谱仪下进行扫描,记录红外光谱图,并同法测定MT原料药。结果,MT原料药在3304 cm-1处可见N—H伸缩振动的特征吸收峰,在1 624 cm-1处可见N—H弯曲振动的特征吸收峰,在2 989、2 927 cm-1处可见饱和C—H伸缩振动的特征吸收峰,在1 587、1 440 cm-1处可见苯环C—H伸缩振动的特征吸收峰。制成SLNs后,上述N—H伸缩、弯曲振动的特征吸收峰消失,且苯环C—H伸缩振动的特征吸收峰红移至1 750 cm-1,详见图3。

图3 MT-SLNs和MT原料药的红外光谱图Fig 3 IR spectra of MT-SLNs and MT raw material
2.3 MT含量检测方法的建立
2.3.1 色谱条件 色谱柱:Aquasil C18柱(250 mm×4.6 mm,5µm);流动相:甲醇-水(50∶50,V/V);流速:1 mL/min;柱温:25 ℃;检测波长:223 nm;进样量:20 μL。
2.3.2 溶液的配制 精密称取MT对照品5.0 mg,用甲醇溶解并定容至10 mL,得MT质量浓度为0.5 mg/mL的对照品溶液。取“2.1”项下MT-SLNs 0.1 mL,用甲醇溶解并定容至10 mL,超声(功率:200 W,频率:40 kHz)15 min后,经0.22 μm微孔滤膜滤过,即得供试品溶液。取空白SLNs适量,按供试品溶液配制方法制备阴性对照溶液。
2.3.3 系统适用性试验 取“2.3.2”项下对照品溶液、供试品溶液、阴性对照溶液各适量,按“2.3.1”项下色谱条件进样分析,记录色谱图。结果,MT的保留时间为5.8min,理论板数按MT计不低于2 000,空白SLNs不干扰待测物的测定,详见图4。
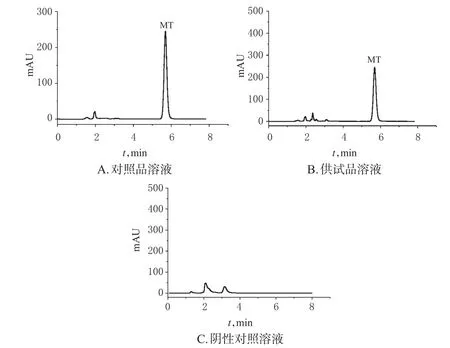
图4 高效液相色谱图Fig 4 HPLC chromatograms
2.3.4 标准曲线的绘制及定量限、检测限的考察 精密称取MT对照品25.0 mg,置于10 mL量瓶中,加入甲醇适量,振摇使溶解,以流动相定容至刻度,配制成质量浓度为2.5 mg/mL的标准溶液。取上述标准溶液适量,以流动相稀释,配制成质量浓度分别为0.78、3.9、7.8、19.5、39.06、78.125 μg/mL的系列对照品溶液,按“2.3.1”项下色谱条件进样测定,记录峰面积。以待测物质量浓度(c,μg/mL)为横坐标、峰面积(A)为纵坐标进行线性回归,得回归方程为 A=127.47c-4.30(R2=0.999 9)。结果,MT检测质量浓度的线性范围为0.78~78.125 μg/mL;定量限为0.78 μg/mL(信噪比为10∶1),检测限为0.236 μg/mL(信噪比为3∶1)。
2.3.5 方法学考察 精密吸取“2.3.2”项下供试品溶液20 μL,按“2.3.1”项下色谱条件重复测定5次,记录峰面积。结果,MT峰面积的RSD为1.38%(n=5),表明该方法精密度良好。按“2.3.2”项下方法配制供试品溶液(MT质量浓度为5.0 μg/mL),分别于室温下放置0、2、4、8 h后,按“2.3.1”项下色谱条件进样测定,记录峰面积。结果,各质量浓度样品MT峰面积的RSD为2.73%(n=4),表明其室温放置8 h内稳定性良好。按“2.3.2”项下供试品溶液制备方法平行制备供试品溶液5份,再按“2.3.1”项下色谱条件进样测定,记录峰面积。结果,MT峰面积的RSD为2.47%(n=5),表明该方法重复性良好。按“2.1”项下方法制备不含MT的空白SLNs,分别加入低、中、高质量浓度(1.0、5.0、25.0 μg/mL)的MT对照品溶液,按“2.3.2”项下供试品溶液制备方法处理后,再按“2.3.1”项下色谱条件进样分析,记录峰面积,并计算空白回收率。每质量浓度平行操作5次。结果,各样品的平均空白回收率分别为101.17%、98.92%、99.13%,RSD分别为3.56%、2.96%、1.36%(n=5)。
2.4 包封率(EE)和载药量(DL)的测定
采用超滤离心法测定MT-SLNs的包封率及载药量。精密量取“2.1”项下MT-SLNs 0.5 mL,置于超滤离心管中,4 000×g离心15 min,收集滤液,按“2.3.1”项下色谱条件进样测定,计算未被包封(即游离)的褪黑素质量(m游离);再精密量取“2.1”项下MT-SLNs 0.5 mL,置于10 mL量瓶中,加入甲醇定容,超声(功率:200 W,频率:40 kHz)15 min,经0.22 µm微孔滤膜滤过后,按“2.3.1”项下色谱条件进样测定,计算褪黑素总质量(m总),按公式计算EE和DL:EE=[(m总-m游离)/m总]×100%,DL=[(m总-m游离)/m酯]×100%(式中,“m酯”为处方中山嵛酸甘油酯的质量)。结果,本研究所得MT-SLNs的EE为(87.54±5.31)%,DL为(8.42±0.78)%。
2.5 MT-SLNs的体外经皮渗透试验
2.5.1 离体皮肤制备 于小鼠腹部涂抹脱毛膏行脱毛处理后,用生理盐水洗净,饲养24 h后处死,剥离无毛的腹部皮肤,去除皮下脂肪,用生理盐水洗净,以滤纸吸干水分,再用磷酸盐缓冲液(PBS,pH 7.4)漂洗至洗液澄清,用滤纸吸干后,备用[7]。
2.5.2 体外透皮吸收试验 在直立式Franz扩散池中进行透皮吸收试验,扩散池置于药物透皮扩散试验仪中,于37℃恒温循环水浴中保温。将“2.4.1”项下处理好的小鼠离体皮肤固定在供给池和接收池中间,角质层部分朝向供给池,其有效渗透面积为3.5 cm2。以0.1%Tween-80-生理盐水溶液作为接收液,接收池容积为6.5mL。取“2.1”项下MT-SLNs 1.0 mL,加至供给池小鼠离体皮肤(5张)的角质层表面,以相同质量浓度的MT原料药(将MT原料药5.0 mg分散到水2.0 mL中所得的混悬液)作为对照(离体皮肤5张),在300 r/min的搅拌条件下,分别于0.5、1、2、3、4、6、8、10 h时吸取接收液0.5 mL,并于取样后补加相同体积的接收液。吸出的接收液经0.22µm微孔滤膜滤过后,按“2.3.1”项下色谱条件进样分析,根据回归方程计算MT的质量浓度,并按如下公式计算单位面积的累积渗透量(Q):

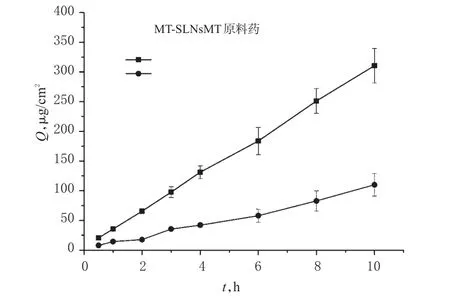
图5 MT-SLNs和MT原料药的体外渗透曲线(n=5)Fig 5 Percutaneous penetration curves in vitro of MTSLNs and MT raw material(n=5)
式中,“S”为有效渗透面积,“V”为接收室中接收液的体积,“Vi”为每次取样的体积,“ci”为第i次至上次取样时接收液中药物的累积质量浓度;“cn”为该次取样时接收液中药物的质量浓度。采用Excel 2007软件以Q对时间t作图,并进行线性回归,得动力学拟合方程。该方程的斜率即为稳态透过速率[Jss,µg/(h·cm2)],回归曲线与x轴的交点即为滞后时间(t1ag,h)。采用Prism 6.0软件对数据进行统计分析。数据均以±s表示,组间比较采用t检验。P<0.05为差异有统计学意义。结果见图5、表1。
表1 MT-SLNs和MT原料药的经皮渗透动力学拟合方程及渗透参数(±s,n=5)Tab 1 Percutaneous penetration kinetic fitting equations and parameters of MT-SLNs and MT raw material(±s,n=5)
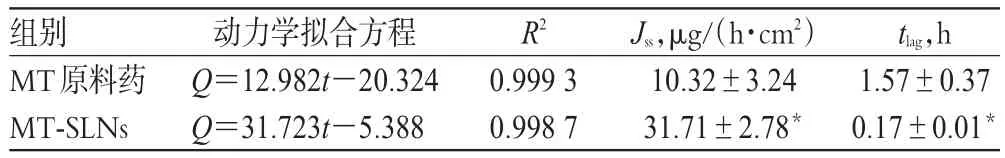
表1 MT-SLNs和MT原料药的经皮渗透动力学拟合方程及渗透参数(±s,n=5)Tab 1 Percutaneous penetration kinetic fitting equations and parameters of MT-SLNs and MT raw material(±s,n=5)
注:与MT原料药组比较,*P<0.01Note:vs.MT raw material group,*P<0.01
tlag,h 1.57±0.37 0.17±0.01*组别MT原料药MT-SLNs动力学拟合方程Q=12.982t-20.324 Q=31.723t-5.388 R2 0.999 3 0.998 7 Jss,μg/(h·cm2)10.32±3.24 31.71±2.78*
由图5、表1可见,MT-SLNs及其原料药的透皮吸收行为均符合零级动力学释放规律。其中,MT-SLNs的Jss为(31.71±2.78)µg/(h·cm2),显著高于 MT 原料药的(10.32±3.24)µg/(h·cm2);MT-SLNs的tlag为(0.17±0.01)h,显著短于MT原料药的(1.57±0.37)h,差异均有统计学意义(P<0.01)。
3 讨论
MT作为一种广泛存在于动物体内的生理节律性调节因子,主要由脑松果体在夜间分泌,在睡眠过程中发挥重要作用,有助于改善存在睡眠延迟、睡眠障碍人群的睡眠质量,亦有助于调整旅行者、宇航员或夜班工作人员的时差[8]。然而由于MT的半衰期较短(t1/2<45 min)、口服吸收影响因素较多(如胃的排空及排空速率、食物及胃肠道代谢等),加之其不可避免的首关效应,使得MT口服给药效果欠佳[9]。皮肤作为机体最大的器官,经皮递送系统可明显减轻MT的肝消除程度,并提高其生物利用度,使其更接近于内源性MT的释放水平[3]。尽管经皮给药有许多优点,然而由于皮肤角质层具有“砖泥结构”的屏障特性,故如何有效克服角质层的屏障作用是经皮递送系统研究领域需要解决的问题[10]。考虑到MT的分子量较小(分子量为232),易于透过皮肤角质层,同时在MT的分子结构中含有亲水和亲脂基团,有利于其透过皮肤的生物膜而被吸收,故该药可被设计为经皮递送系统药物[11-12]。有研究表明,可将脂质体、醇质体、聚合物纳米粒等作为MT的载体用于其经皮递送系统的制备,但上述载体具有一定的流动性,容易导致药物的泄漏[11]。SLNs采用生物相容性好的脂质材料,药物可被镶嵌或包载于固态的脂质颗粒中,可使药物泄漏减少、经皮递送系统稳定性提高[3]。因此,本课题组将MT设计为SLNs以更好地改善其透皮吸收特征。
本研究采用熔融乳化法制备SLNs。首先,将油相加热,当超过脂质熔点后,油相可变为均一的液体;随后将药物溶解于液态的油相中,在乳化剂的作用下,使油相与同温度的水相形成水包油型乳剂;最后快速降温使液态的油相固化成固态的微粒,从而将药物包裹于脂质中,最终制得澄清、透明且带有微蓝色乳光的MT-SLNs。粒径检测结果显示,本研究制得的MT-SLNs的平均粒径为(67.88±0.17)nm,多分散指数为0.188±0.001,提示所制备的MT-SLNs分布比较均匀。红外光谱检测结果表明,MT的特征吸收峰消失或红移,提示其已被包括在固体脂质中。经HPLC法检测,本研究制得的MT-SLNs的EE为(87.54±5.31)%,DL为(8.42±0.78)%。由于MT具有较高的脂溶性,而所用到的脂质材料山嵛酸甘油酯能够和模型药物MT之间具有较好的相容性,可将MT镶嵌或包裹在脂质材料所形成的骨架中,故EE和DL较高,提示SLNs可作为模型药物MT经皮递送系统的载体。
透皮试验结果显示,将MT制备成SLNs后,Jss较MT原料药提高了约3.07倍,tlag缩短至0.17 h左右,表明将MT制成SLNs可显著提高其透皮性能,并能缩短滞后时间,从而有助于其疗效的发挥。笔者分析原因可能包括:首先,SLNs颗粒更易黏附在皮肤的角质层上,形成具有封闭效应的药物存贮库,在皮肤内外两侧维持较高的浓度梯度,使得所包载的药物分子可扩散至更深的皮肤层;其次,粒径大小在100 nm以下的SLNs具有更强的黏附性以及更大的接触面积,可进一步促进药物透过皮肤内流;此外,SLNs可与给药部位的角质层发生相互作用,引发脂质重排,从而减小药物分子渗透过皮肤角质层的阻力[13]。由此可见,将MT制成SLNs后,该药的体外透皮效果得到明显提高。
综上所述,本研究可为MT经皮递送系统的制备和优化提供理论基础,在后续的工作中将开展经皮给药后体内药动学的相关研究。

