多非利特对兔右心房快速起搏模型的影响
屠叶平 侯月梅 金晓媛 张晓雅
(1上海市奉贤区中心医院老年科,上海 201499;2南方医科大学)
心房颤动(房颤)是临床上最常见的心律失常之一,目前仍主要依靠药物转复,开发安全有效的抗房颤药物是研究的热点〔1〕。多非利特是一种新型的纯Ⅲ类抗心律失常药物,通过特异性阻断快钾通道使心肌细胞复极延长〔2〕。研究表明多非利特具有较好的转复心房扑动(房扑)、房颤维持窦性心律作用,在国外已应用于临床房扑和房颤的治疗,但在应用过程中通过延长动作电位可导致尖端扭转型室性心动过速(室速)的发生,且与浓度相关〔3,4〕。本研究应用微电极阵(MEA)技术结合心腔内电生理技术,研究不同浓度多非利特对兔右心房快速起搏(RAP)模型电生理特性的影响,以探索出更严格的药物使用安全范围。
1 材料和方法
1.1实验动物和分组 纯种新西兰大白兔40只,不限雌雄,体重2.0~3.0 kg,均购自南方医科大学实验动物中心,合格证号:SYXK(粤)2011-0074。随机分成5组各8只,对照组、起搏组、多非利特A组(10-5μmol/L)、多非利特B组(10-4μmol/L)、多非利特C组(10-3μmol/L)。
1.2实验试剂、溶液成分和仪器 改良台氏液成分(mmol/L):NaCl 144;KCl 5.0;CaCl21.8;MgCl21;NaH2PO4;HEPES 5.0;葡萄糖10〔5〕(NaOH 滴定至pH 值为7.4)。多非利特(批号:F6331,美国Sigma公司),以上均为国产分析纯。MEA系统(Microeletrode arrays MEA64 System,MCS Gmbh,德国),主要配置为柔性电极(64位点),余包括MC-Rack软件包、USB-ME64转换卡、Stimulus Generator刺激仪、PGA64 放大器等。
1.3建立兔快速心房起搏模型 将戊巴比妥钠(3%)按照剂量30 mg/kg,通过兔耳缘静脉注射麻醉,再静推800 U肝素抗凝。将兔固定在兔台上,沿颈部正中做切口,分离右侧颈内静脉后切开,结扎近头端〔6〕。使用电生理仪LEAD-7000(四川锦江电子科技)同时记录兔体表心电图(Ⅱ导联)和高右房心腔内电图,插入一根6F的两极电极导线至右心房做起搏和记录。当心腔内电生理图出现高大A波、小V波时,记录图形较理想,此时固定电极导线〔7〕。以600次/min的固定频率进行RAP 24 h。正常对照组仅植入起搏电极导线,不做高位右心房快速起搏〔8〕。
1.4标本制备 RAP 24 h后,开胸取出心脏,迅速放置于充氧的4℃改良台氏液中,挤压心脏排出心腔内多余积血,对心脏进行简单修剪〔6〕。启动离体心脏灌流系统,改良台氏液流速设为12 ml/min,使用数控恒温循环水槽ALC-CWB将温度控制在37℃,台氏液中通以95%O2+5%CO2的混合气体(pH<7.5)〔9〕。分离后提住主动脉,将灌注管道插至冠状动脉开口上方处,用丝线打结固定后开始灌注。使用Stimulus Generator刺激仪做驱动刺激,刺激强度大于2倍阈值,波宽2 ms,频率1 Hz,选择25号为刺激电极导线正极34号为负极。心脏稳定30 min后开始记录心房肌场电位和兴奋传导的变化。
1.5给药方法 多非利特经双蒸水溶解后按照设定的最终药物浓度(10-5μmol/L、10-4μmol/L和10-3μmol/L)混入改良台氏液中。改良台氏液中加入多非利特后pH会发生改变,借助台氏pH剂,使用NaOH/HCl 重新将pH 滴定至7.4。
1.6MEA系统 MEA系统柔性电极由MEA1、MEA2组成,是在柔性塑料片基质头部1.8 mm×1.8 mm的区域,以6×6分布形式植入32个金电极。记录电极直径50 μm,相邻间隔300 μm。原理:柔性电极记录的原始电信号,通过放大器PGA64增益100倍后,由模数转换卡USB-ME64数字化,最后使用软件MC-Rack处理〔9〕。场电位参数(FPmin)第一个负向波峰值(FPmin)、最后一个正向波峰值(FPmin),fAPD:从FPmin到FPmax 的时间〔10〕。兴奋传导速度=距离÷时间,32电极之间距离固定,兴奋的时间差即为兴奋传播所需时间。
1.7统计学方法 采用SPSS22.0统计软件进行t检验和单因素方差分析,方差齐时采用LSD-t,方差不齐时采用Dunnettt检验。
2 结 果
2.1兔RAP模型 RAP时,当体表心电图变得紊乱,P波消失,R-R间期不等,f波出现,频率达450~600次/min(图1),且持续时间超过10 s,表明AF模型制作成功,本实验成功率达95%。

Ⅱ:体表Ⅱ导联心电图; HRA:高右房心腔内电图图1 RAP兔房颤
2.2起搏组兔心房肌fAPD、CV与HR的变化 兔离体心脏成功行Langendroff灌流后,对25号(+)和34号(-)电极施加2 V电压,2 ms脉宽,延时100 ms连续刺激右房30 min。实验过程中25号和34号均显示为一条直线,无生物电信号产生。因兔心肌大小和柔性电极放置位置存在差异,会对数据造成一定影响,故各组所有数据采用场电位信号稳定、清晰的35号为原始研究数据。相较于对照组,起搏组fAPD明显缩短,CV明显减慢,HR明显加快,差异均有统计学意义(P均<0.05),见表1。
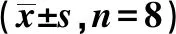
表1 各组fAPD、CV和HR的比较
与对照组比较:1)P<0.05;与起搏组比较:2)P<0.05
2.3多非利特组兔心房肌fAPD、CV与HR的变化 相较于起搏组,多非利特组fAPD与HR分别呈浓度依赖性延长与减慢,差异有统计学意义(P<0.05),CV则无明显变化,差异无统计学意义(P>0.05),见表1,图2。

1~5:对照组、起搏组、多非利特A组、非利特B组、多非利特C组图2 各组场电位时限变化
3 讨 论
MEA技术在抗心律失常药物研发和药物梯度浓度研究中都可取得理想效果,其通过多位点实时、同步记录多细胞群的电活动,利用用药后组织细胞fAPD、CV、自主节律等参数的变化来评价其药物效应及药物不同浓度的作用效果〔11,12〕。柔性电极问世后,能够应用MEA技术进行离体小动物整体心脏电生理方向的研究。在药物研发过程中,离体心脏实验相较于在体心脏实验具有明显优势,能够消除神经、体液等内环境调节作用对药物效果的干扰。本实验应用MEA结合心内电生理技术,在Langendorff改良台氏液灌流条件下,可清楚、稳定地在较长时间内观察到兔离体心脏在基础状态、RAP后和多非利特干预下 fAPD、CV和自主节律的变化,并且能够快速、敏感地显示出不同浓度多非利特(10-5、10-4、10-3μmol/L)的作用差异。
迄今为止,国内外关于房颤模型的研究较多,已建立了较多的房颤模型,包括以犬等大型动物为代表的房颤模型和以兔等中型动物为代表的房颤模型〔13〕。使用RAP方法制作的兔房颤模型与临床观测的房颤在结构和功能上均具有一定共性,房颤诱导后能够维持,不会自行终止,进行干预后能有效被终止〔14,15〕。因而RAP在房颤的电生理研究领域得到了广泛应用。本实验应用MEA结合心内电生理技术进行多非利特对RAP模型干预的研究是一次创造性地尝试,不仅房颤模型稳定性、重复性好且贴近临床,在尽可能消除外界其他干扰条件下,直观抗房颤药物对房颤模型的影响,为今后抗心律失常尤其是抗房颤药物的研发构建了典范平台。
抗心律失常药物在对抗心律失常的同时往往能诱发心律失常的发生,药物引起QT间期延长是目前安全药理学中关注的主要问题。尽管多非利特已在国外上市用于房扑、房颤的治疗,但因其具有延长QT间期而导致尖端扭转型室速的副作用,且呈浓度相关性〔16〕,因此多非利特的药物安全剂量范围仍需进一步研究。本研究显示,10-5、10-4、10-3μmol/L 多非利特在短时间内均可延长fAPD、减慢HR,对CV则无明显影响。浓度在10-5~10-4μmol/L时,对fAPD、HR影响相对较小,浓度达10-3μmol/L时,可使fAPD明显延长、HR明显减慢,故浓度低于10-3μmol/L是相对安全的药物剂量范围。由于多非利特不影响CV,所以其减慢HR主要与抑制自主节律有关,且与fAPD呈负相关。因此,在临床上应用多非利特时,要严格把握药物安全剂量范围,注意观察HR与QT间期的变化,防止因QT间期延长引发尖端扭转型室速等心律失常发生。
应用MEA结合心内电生理技术在RAP模型中进行抗心律失常药物的研究是一种行之有效且理想的技术手段,将为推进该研究领域的进一步发展起到重要作用。在兔RAP模型中,多非利特可浓度依赖性地延长fAPD与减慢HR,对CV则无影响,显示出较好的抗房颤作用,浓度低于10-3μmol/L是相对安全的药物剂量范围。本研究对该药今后在国内的上市具有重要参考意义。

