气溶胶辅助法合成球形氧化镁及其吸附性能研究
柴政泽 ,叶俊伟,2,田其哲 ,史 磊 ,宁桂玲 ,2
(1.大连理工大学化工学院,精细化工国家重点实验室,辽宁大连116024;2.辽宁省硼镁特种功能材料制备与应用技术工程实验室)
中国拥有丰富的盐湖镁资源,其中察尔汗盐湖是中国最大的镁盐集中地,也是世界上镁盐储量最大的盐湖。在盐湖综合利用过程中,目前每年副产约3 000万t氯化镁,利用率不高,因此基于氯化镁为镁源,开发镁基功能材料具有重要战略意义[1]。
氧化镁是一种用途广泛的多功能材料,可以用于耐火[2]、吸附[3-5]、抗菌[6]和催化[7]等领域。 目前合成氧化镁的方法主要有沉淀法、水热法、静电纺丝法、热解法和微波辅助水热合成等方法。G.Tian等[8]以天然黏土和富含Mg(Ⅱ)的盐水为原料,以氨水为沉淀剂制备了棒状的 MgO;P.Gao 等[9]用 Mg(NO3)2·6H2O和尿素为原料,乙醇为溶剂,采用水热的方法制备了球形花状 MgO;S.Makhluf等[10]以乙酸镁和乙二醇为原料,采用微波水热的方法制备了纳米晶MgO;Z.Shen等[11]通过热解氯化镁的方法制备了块状 MgO;A.Almasian 等[12]以硝酸镁为原料采用静电纺丝的方法制备了介孔MgO纳米线。但是,这些方法通常由于操作步骤过于繁杂、需要加入表面活性剂等缺点制约了MgO功能材料的制备,而随着气溶胶技术的出现及不断发展可以良好地解决以上问题,气溶胶法操作步骤简单、无需使用表面活性剂、可以连续化生产[13]。本文利用气溶胶的优势辅助合成球形氧化镁。通过各种技术手段表征了不同反应温度下形成的前驱体颗粒和MgO,并研究了MgO对有机染料刚果红的吸附性能。
1 实验部分
1.1 试剂
六水氯化镁(MgCl2·6H2O)、尿素(CN2H4O)、刚果红(C32H22N6Na2O6S2),以上化学试剂均为分析纯,且购买后未经任何纯化。
1.2 气溶胶法辅助合成球形MgO
将100 mL 1 mol/L的尿素水溶液加入到100 mL 2 mol/L的氯化镁水溶液中,混合均匀,然后加热到85℃反应6 h,促使尿素水解。反应结束后,以N2作为载气,携带前驱体溶液进入管式炉(温度分别为600、700、800、900 ℃)进行热解,不同温度下收集到的前驱体颗粒分别命名为P-600、P-700、P-800和P-900。收集到的前驱体颗粒在N2氛围下以5℃/min的升温速率升温,并在达到600℃时保温2 h,制备得到产品,分别命名为 M-600、M-700、M-800 和 M-900。
1.3 样品表征
采用X射线粉末衍射仪(XRD,Rigaku-DMax 2400)对样品进行晶相分析。用扫描电子显微镜(SEM,TESCAN VEGA3)观察样品的形貌。样品对有机染料刚果红的吸附性能采用紫外可见分光光度计(U-4100,HITACHI)测定其在 500 nm 处的吸光度确定浓度。采用红外光谱仪(FT/IR-4100,JASCO)对样品的有机官能团进行分析。
1.4 刚果红吸附性能测试
配制100 mL质量分数为1×10-4的刚果红水溶液搅拌均匀,分别称取10 mg MgO加入到7个剧烈搅拌的 10 mL 刚果红溶液中,在 5、10、20、30、40、50、60 min时,取混合溶液8 mL在8 000 r/min的离心机中离心1 min,取上清液在紫外可见分光光度计下测定吸光度,确定其浓度。测试数据采用伪一级动力学和伪二级动力学进行拟合。
1)伪一级动力学

式中,qe和qt分别是在平衡时和时间t(min)下的吸附量,mg/g;k1是伪一级动力学的速率常数,min-1。
2)伪二级动力学
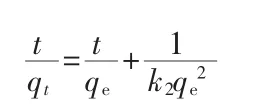
式中,k2是伪二级动力学模型的速率常数,g/(mg·min)。
吸附等温线实验。配制质量分数分别为1×10-4、2×10-4、4×10-4、6×10-4、8×10-4、1×10-3的 10 mL 刚果红溶液,分别称取10 mg MgO样品加入到不同浓度的溶液中,搅拌12 h后离心取上清液测试。测试数据采用Langmuir和Freundlich模型进行拟合。
3)Langmuir模型

式中,ρe是平衡时的质量浓度,mg/L;kL表示与结合位点的亲和力相关的Langmuir常数,L/mg;qm是单层表面被完全覆盖时的吸附容量的理论极限,有助于比较吸附性能,mg/g。
4)Freundlich 模型

式中,kF和n是Freundlich常数,分别代表吸附容量和吸附强度。1/n的量级量化了吸附的有利性和吸附剂表面的不均匀性程度。
2 结果与讨论
气溶胶法辅助合成球形MgO的反应流程如图1所示。首先将MgCl2·6H2O和尿素混合均匀的水溶液在85℃下加热,当尿素水解达到一定的pH时,迅速释放出CO2和NH3,并产生大量的OH-,与镁离子反应形成溶胶,随后跟随载气进入管式炉在不同温度下进行热解并且聚集生成球形前驱体颗粒,然后在600℃下煅烧生成球形产品。

图1 实验过程示意图
图2 a为不同温度下前驱体颗粒的XRD谱图。由图2a 可以看出, 在 2θ为 13.0、18.3、22.5、22.9、26.4°处分别对应 NH4MgCl3·6H2O 的(020)、(200)、(220)、(022)和(040)晶面;在 2θ为 22.6、32.3、57.9°处分别对应 NH4Cl的(100)、(110)和(211)晶面。 在2θ为 15.5、31.4、32.5、56.6°处分别对应 Mg(OH)Cl的(003)、(101)、(012)和(113)晶面。 在 2θ为 36.5、42.5、61.8、73.8、78.4°处 分 别 对 应 MgO 的 (111)、(200)、(220)、(311)和(222)晶面。 由图2a 可知,样品 P-600 和 P-700 包含 NH4MgCl3·6H2O、NH4Cl和MgO,P-800 包含 Mg(OH)Cl、NH4Cl和 MgO,P-900包含MgO和NH4Cl。随着反应温度的升高,前驱体颗粒倾向于向MgO晶型转化,但是并不能完全转化为MgO,前驱体中依然包含NH4Cl。
为了进一步佐证生成的物质,研究了前驱体颗粒的红外光谱(图2b),尽管不同温度下的谱图十分相似,但是仍然可以看到细微的变化。由图2b可知,样品P-900在438、795 cm-1处出现 Mg—O基团的拉伸和弯曲振动吸收峰,在其他反应温度下的样品同样存在,这也佐证了XRD图中每个反应温度下的样品都存在MgO的晶型;在1 356、3 259 cm-1处出现N—H基团的振动吸收峰,并且同样在其他温度下的样品中出现,这是氯化铵中N—H基团的振动吸收峰,同样也是六水氯化铵镁中的铵根离子中的N—H基团的振动吸收峰,与XRD图中的氯化铵和六水氯化铵镁相对应。在581、1 617、3 441 cm-1处出现水的振动吸收峰,1 480 cm-1处的峰是属于吸附的二氧化碳的振动吸收峰。

图2 不同反应温度下前驱体颗粒的XRD(a)和IR(b)谱图
经过煅烧之后,对样品进行XRD表征,从XRD图(图3)可以看出,前驱体颗粒经过煅烧之后都具有良好的晶型,并且没有其他杂峰。图3a为M-600的 XRD 图,可以看到在 35.6、42.5、61.9、74.3、78.3°处分别对应 MgO 的(111)、(200)、(220)、(311)和(222)晶面。在前驱体颗粒中所包含的氯化铵和六水氯化铵镁也完全找不到出峰位置,这表明在经过煅烧之后,前驱体颗粒完全转化为MgO。

图3MgO的XRD谱图
图4 是不同反应温度下的前驱体颗粒和MgO的SEM图。从图4可以看出,前驱体颗粒表面光滑平整(a、b、c和 d),但是 MgO 颗粒表面凹凸不平,是由一些小颗粒聚集而成(e、f、g和 h),这是由于沉积在前驱体颗粒表面的氯化铵完全挥发造成的。

图4 不同反应温度下前驱体颗粒和MgO的SEM图
图5为MgO的等温线和孔径分布图。MgO的等温线均符合H3型,从孔径分布图可以看出,不同反应温度下制备的MgO的孔径分布主要集中在两处介孔区域,一处是集中在3~4 nm;另一处则有所不同,在 600℃时(图5a),孔径集中在 10~14 nm,在700 ℃时(图5b),孔径主要集中在 29~33 nm,在800 ℃时(图5c),孔径主要集中在 58~62 nm,在900℃时(图5d),孔径主要集中在58~62 nm。随着温度的升高孔径逐渐增大,但当增大到一定程度后增大幅度减小。 M-600、M-700、M-800、M-900 的比表面积分别为 36、32、31、26 m2/g; 孔容分别为 0.26、0.30、0.35、0.39 cm3/g,随着反应温度的升高,比表面积逐渐减小,孔容逐渐增大,符合一般规律。

图5 MgO的等温线和孔径分布图
对于制备的氧化镁,研究了其对刚果红的吸附性能。由于煅烧温度对MgO的吸附性能影响较大,随着温度的升高,MgO的活性逐渐降低,另外,根据氮吸附数据的综合考虑,选用反应温度为600℃时制备的MgO对质量分数为1×10-4的刚果红进行吸附性能研究。图6a为不同时间下的刚果红浓度变化,在0 min时刚果红为鲜艳的酒红色,5 min后溶液已经基本变为澄清透明的溶液。图6b为刚果红的紫外吸收光谱,5 min之后刚果红的出峰位置已经消失,这表明刚果红已经被MgO完全吸附。对于吸附动力学,吸附数据采用伪一级(图6c)和伪二级(图6d)动力学公式拟合。伪一级动力学拟合后R12=0.999 97,k1=0.975 8 min-1,qe1=100.015 mg/g;伪二级动力学拟合后的R22=1.000 00,k2=0.246 6 g/(mg·min),qe2=100.20 mg/g;因为R12小于R22,所以符合伪二级动力学公式。对于吸附等温线采用Freundlich和Langmuir模型进行拟合,Freundlich模型拟合R32=0.861 2,kF=378.05,n=6.718 4;Langmuir模型拟合后R42=0.980 2,饱和吸附量qm=764.91 mg/g,吸附常数kL=2.000 3 L/mg;R32小于R42,所以等温线符合Langmuir模型(图6e)。

图6 MgO吸附刚果红
3 结论
通过气溶胶辅助的方法成功制备了球形氧化镁。本方法步骤简单,无需采用表面活性剂或模板剂。通过XRD表征确定生成的MgO晶型良好,SEM图片显示MgO颗粒表面是由小的颗粒聚集而成。氮吸附-脱附数据表明在反应温度为600℃时制备的MgO比表面积为36 m2/g,平均孔径为34 nm,总孔容为0.26 cm3/g,对有机染料刚果红的吸附符合伪二级动力学,5 min内达到吸附平衡,吸附速率较快;吸附等温线符合Langmuir模型,饱和吸附量为764.91 mg/g。

