共聚物增黏剂在超临界CO2中的微观结构与性能
孙文超, 孙宝江, 汪海阁, 孙文霞, 卓鲁斌, 曾义金, 相 华
(1.中国石油大学(华东)石油工程学院,山东青岛266580; 2.中国石油集团工程技术研究院有限公司,北京 102206;3.中国石化胜利石油工程公司地质录井公司,山东东营 257100; 4.中国石油化工股份有限公司石油工程技术研究院,北京100101; 5.俄罗斯国立古勃金石油天然气大学,莫斯科 119991)
作为一种绿色溶剂,超临界二氧化碳(SC-CO2)因其良好的扩散性、传热性和传质性而被应用于许多工业过程。在页岩气开发中,SC-CO2被认为是一种有望替代水基压裂液的清洁压裂液[1]。SC-CO2具有较强的造缝能力,对储层无污染,易返排。同时,由于它与页岩中有机质的相互作用强于CH4,CO2可以置换储层中的甲烷,提高天然气的采收率[2-3]。SC-CO2压裂产生的微裂缝可以为CO2的地质埋存提供巨大的潜力[4],利用从工业烟气中捕获的CO2开发页岩气,可能是实现碳捕集、利用和埋存的手段。作为压裂液,CO2的主要功能之一就是将支撑剂输送到裂缝的深处,防止裂缝闭合。但由于其黏度低、支撑剂输送能力差,加砂压裂技术一直未得到突破[5-6]。实现SC-CO2加砂压裂的关键技术是通过添加增黏剂来提高其黏度。Enick等[7]合成的半氟化三烷基氟化物在质量分数为4%时仅能使CO2的黏度增大3.3倍。Eastoe等[8]评价半氟化的F7H4类表面活性剂在超临界CO2中的增黏性能,在40 ℃、40 MPa条件下,质量分数为4.4%的K-F7H4、Li-F7H4、Na-F7H4分别可使 CO2黏度增加10%、23%、100%。由于在CO2中的低溶解性,使用聚合物作为CO2增黏剂一度被认为是非常困难的。在聚合物-CO2体系中,较强的聚合物-CO2相互作用和较弱的聚合物-聚合物相互作用有利于聚合物的溶解。Tapriyal等[9]的研究表明,电荷偏离和四极矩使得CO2既可以作为受电子的路易斯酸又可作为供电子的路易斯碱,能够与特定的官能团产生有利的相互作用。O′Neill等[10]发现具有较低表面张力的聚合物的分子间相互作用较弱,这有利于聚合物在SC-CO2中溶解。Sarbu等[11]发现,具有高自由体积、高链柔性的聚合物,通常具备较低的玻璃转化温度,表现出与CO2的较好混溶性。过弱的聚合物-聚合物相互作用并不利于聚合物提高CO2的黏度。例如聚氟化丙烯酸酯虽然在CO2中具有相当好的溶解性,但并不能有效提高其黏度,这正是由于聚合物链间过弱的相互作用使其无法在CO2中有效缔合[12]。Beckman和Enick等[13-14]认为,通过设计特定的分子结构,将亲CO2单体和疏CO2单体共聚得到的共聚物可以在溶解于CO2的同时,通过π-π堆积、氢键或疏溶剂缔合作用有效地提高CO2的黏度。因此,保证足够的聚合物-CO2相互作用前提下,保持适当的聚合物间相互作用,使两者达到平衡,可能是开发在SC-CO2中溶解并有效提高其黏度的聚合物的策略。开发新型CO2聚合物增黏剂需要分子结构对分子间相互作用及其在CO2中性能的影响机制的支撑。但由于时间和经济成本,机制研究很难完全通过实验得到。分子模拟技术为研究聚合物-CO2体系中分子间相互作用机制提供了新的途径,并被用于研究微观结构对宏观性质的影响。Johnson等[15]通过量子力学方法计算了聚合物结构单元与CO2之间的成键模式和相互作用能,但计算结果与实验结果并不一致。量子力学计算尺度较小,只能模拟聚合物的结构单元,且无法评价温度、压力、聚合物-聚合物相互作用和聚合物-CO2相互作用的影响。与之相比,全原子分子动力学模拟的计算尺度更大,可以模拟温度、压力和体系中分子间相互作用的影响,其结果更加可信。刘涛等[16-18]通过全原子分子动力学模拟研究共聚物结构对其溶解性的影响,并得到了良好的结果。笔者通过实验与分子模拟相结合的方法研究共聚物与其在SC-CO2中的溶解性和增黏性之间的结构-性能关系。以甲基丙烯酸甲酯、丙烯酸乙酯单体分别与1H,1H,2H,2H-全氟癸基丙烯酸酯单体合成共聚物作为增黏剂,进行结构表征及物性测量,并评价其在SC-CO2中的溶解性和增黏性能。通过分子模拟分析CO2-共聚物体系的分子间相互作用能、径向分布函数等参数,以评价体系的微观结构和分子间相互作用特性。在此基础上探讨影响共聚物在SC-CO2中溶解性能和增黏性能的主要因素,揭示共聚物分子结构和组成与其性能之间的关系。
1 实验方法
1.1 合成与表征
1.1.1 合成方法
所用试剂为甲基丙烯酸甲酯(MMA,99.8%,TCI)、丙烯酸乙酯(EAL,99%,Alfa Aesar)、1H,1H,2H,2H-全氟癸基丙烯酸酯(HFDA,98%,Alfa Aesar)、2,2′-偶氮二异丁腈(AIBN,99%,Aldrich)、甲醇(99.9%,Aldrich)和1,1,2-三氯三氟乙烷(99.8%,Aldrich)。引发剂AIBN通过从甲醇中重结晶2次纯化后使用。
共聚物样品通过自由基聚合反应得到[19-20]。将MMA单体和EAL单体分别与HFDA单体在玻璃安瓿中混合,向其中加入作为自由基引发剂的2,2′-偶氮二异丁腈(相对于单体物质的量分数为1.0%)。经过3次冻融循环彻底去除氧气后,将玻璃安瓿减压密封,在60 ℃条件下反应24 h。停止反应后将产物溶解在1,1,2-三氯三氟乙烷中,然后在甲醇中沉淀2次进行纯化,将过滤后收集的反应产物真空干燥得到无规共聚物样品。图1为P(HFDA-co-MMA)与P(HFDA-co-EAL)的合成路线,其中a、b分别为两种共聚物中HFDA基团的物质的量比;x、y分别为两种共聚物中MMA基团和EAL基团的物质的量比。

图1 P(HFDA-co-MMA)与P(HFDA-co-EAL)共聚物的合成路线Fig.1 Synthetic procedure of copolymers P(HFDA-co-MMA) and P(HFDA-co-EAL)
1.1.2 表征方法
使用Bruker-400MHz核磁共振波谱仪,以氘代氯仿为氘代试剂,以400 MHz共振频率记录共聚物的1H NMR谱。通过光谱中的化学位移峰的积分相对强度分析共聚物的共聚比[21-22]。
将共聚物样品溶解在1,1,2-三氯三氟乙烷中分别制备6种不同浓度的待测溶液,通过0.8 μm的过滤器过滤后,使用Wyatt DAWN HELEOS多角度静态光散射仪测量共聚物的相对分子质量[23-25]。
使用Mettler-Toledo差示扫描量热仪在氮气气氛下测量共聚物的玻璃化转变温度[26-28]。加热速率和冷却速率均为10 ℃/min。
将共聚物样品溶于1,1,2-三氟三氯乙烷制成10%的溶液,将其以2 000 r/min转速旋涂在玻璃基材上制备聚合物膜。在25 ℃条件下使用KRUSSDSAHT型接触角测量仪来测量水和正十六烷与共聚物膜的接触角[29-31],重复5次取平均值,通过二液法计算得到共聚物的表面张力。
1.2 浊点压力及黏度测量
如图2所示,浊点压力和黏度测量实验装置的核心部分为高压可视单元,材质为316L不锈钢。视窗为耐高压石英玻璃,尺寸为95 mm×15 mm,最大工作压力为30 MPa,最高工作温度150 ℃。移动柱塞可以改变高压可视单元的容积。实验装置顶部有投球装置,可以向可视单元内投放铝球。通过奥林巴斯I-TR高速摄像机拍摄铝球降落过程。

图2 超临界二氧化碳浊点压力及黏度测量实验装置Fig.2 Experimental equipment of cloud point pressure and viscosity measurement for SC-CO2
(1)利用二次蒸馏水进行可视单元体积标定,根据实验设计浓度,称取一定质量的增黏剂样品,加入可视单元中。
(2)对可视单元抽真空,温度稳定后充入CO2气体,压力稳定后使用磁力搅拌装置搅拌30 min。
(3)静置1 h后,缓慢改变柱塞位置使可视单元的容积增大,体系压力降低,直至出现白雾,此时的压力为浊点压力[32],即聚合物完全溶解于CO2所需的最低压力。
(4)改变柱塞位置使可视单元内体系的压力超过浊点压力,向可视单元内投放铝球,利用高速摄像机以2 000帧/s速度拍摄铝球降落过程。
CO2及CO2-聚合物体系的黏度计算公式[33-34]为

(1)
式中,η为待测溶液的黏度,Pa·s;A为31 6L不锈钢的热膨胀系数,K-1;B为316 L不锈钢的压缩系数,Pa-1;T和T′分别为实际温度和参考温度,K;p和p′分别为实际压力和参考压力,Pa;ρs、ρa分别为CO2-聚合物溶液和铝球的密度,kg/m3;t为铝球降落时间,s;K为根据实验数据回归得到的常数,Pa-1。
将利用式(1)得到的CO2-聚合物体系的黏度值ηsol与相同温度、压力条件下测得的纯CO2的黏度值ηCO2进行比较,根据公式ηR=ηsol/ηCO2[20]得到相对黏度ηR,用来评价增黏剂的增黏性能,ηR越大,表示增黏性能越好。
2 分子模拟方法
使用Material Studio 7.0软件进行CO2-聚合物体系的分子动力学模拟。构建的共聚物分子通过Discover模块中的Smart Minimizer进行结构优化。在此基础上利用Amorphous Cell模块构建不同体系的盒子。然后通过Forcite模块中的Anneal进行300 K到500 K共5个循环的退火计算,以有效地迟豫体系。最后使用NPT系综在25 MPa、308.15 K条件下进行2 000 ps的MD模拟。静电相互作用采用Ewald算法计算,范德瓦尔斯相互作用采用Group based算法计算,温度和压力控制均采用Andersen方法[16-18]。最后500 ps的平衡构象用于数据分析。所模拟的体系列于表1中。

表1 利用分子模拟构建的体系
3 结果分析
3.1 共聚物的结构表征与物性测量
所合成的5种共聚物的1H核磁谱如图3所示。通过计算不同基团特征峰的化学位移峰面积之比[21-22],得到产物中两种单体的共聚比。以图3(a)所示P(HFDA0.79-co-EAL0.21)的1H核磁谱图为例,EAL基团甲基H原子a的化学位移在(1.2~1.4)×10-6内,

图3 5种共聚物的1H核磁谱图Fig.3 1H NMR spectrum of five copolymers
HFDA基团亚甲基H原子h的化学位移范围为(4.3~4.5)×10-6。两种基团中特征H原子的化学位移峰面积之比等于两种单体的物质的量比,据此得到x∶y=21∶79。其他4种共聚物的共聚比通过相同的方法获得。
所合成共聚物的表面张力、玻璃化转变温度和相对分子质量测量结果如表2所示。与P(HFDA0.26-co-EAL0.74)相比,P(HFDA0.28-co-MMA0.72)的表面张力和玻璃化转变温度明显更大。对于4种P(HFDA-co-EAL)共聚物,随着EAL所占物质的量比的增加,表面张力和玻璃化转变温度逐渐增大。相对分子质量测量结果表明,共聚物样品之间的相对分子质量差异较小。

表2 共聚物P(HFDA-co-EAL)与P(HFDA-co-MMA)的物性Table 2 Results for properties of P(HFDA-co-EAL) and P(HFDA-co-MMA)
3.2 共聚物在SC-CO2中的溶解性能
质量分数为1%的共聚物样品在SC-CO2中的浊点压力与温度之间的关系如图4所示,所有共聚物在SC-CO2中的浊点压力均随着温度的升高而增加。随着温度从35升至50 ℃,P(HFDA0.28-co-MMA0.72)的浊点压力从24 MPa增加到29.9 MPa,增加了5.9 MPa。对于4种P(HFDA-co-EAL)共聚物,随着温度从35 ℃升至55 ℃,浊点压力的增大了约5 MPa。显然,温度对共聚物在SC-CO2中的溶解性有显著影响。原因在于随着温度的升高,CO2的密度和介电常数降低[35],对聚合物的溶解能力随之下降,此时必须提高压力以增加CO2与共聚物的分子间相互作用,平衡共聚物-CO2体系的分子间相互作用。

图4 共聚物在SC-CO2中的浊点压力与温度的关系Fig.4 Cloud point pressures of copolymers in SC-CO2 versus temperature
35 ℃条件下,共聚物样品在SC-CO2中的浊点压力与质量分数之间的关系见图5。可以看出,所有共聚物的浊点压力均随质量分数的增大而升高。图5(a)中P(HFDA0.28-co-MMA0.72)在相同质量分数条件下的浊点压力高于P(HFDA0.26-co-EAL0.74)。这两种共聚物溶解性能的明显差异应源于其结构区别。虽然MMA和EAL是同分异构体,但与HFDA聚合得到的两种共聚物的分子结构却有所区别。P(HFDA0.28-co-MMA0.72)的主链和侧链MMA基团上各有一个甲基,而P(HFDA0.26-co-EAL0.74)的主链上没有甲基,侧链EAL基团上则存在一个甲基和一个亚甲基(图1)。与P(HFDA0.26-co-EAL0.74)相比,P(HFDA0.28-co-MMA0.72)主链甲基的存在降低了其自由体积和分子链柔顺性,使其表面张力和玻璃化转变温度增大(表2),造成不利的混合焓和混合熵[21-22]。对于P(HFDA-co-EAL)共聚物,相同质量分数条件下,随着EAL含量的增加,共聚物在SC-CO2中的浊点压力升高,如图5(b)所示。根据表2的测量结果,随着EAL含量的增加,共聚物的表面张力和玻璃化转变温度逐渐增大,分子间相互作用变大,链柔性变差,因而溶解性能下降。与共聚物质量分数相比,EAL基团的含量在决定浊点压力时起了更大的作用。

图5 共聚物在SC-CO2中的浊点压力与质量分数的关系Fig.5 Cloud point pressures of copolymers in SC-CO2 versus mass fraction
通过分子动力学模拟计算了共聚物与CO2之间的相互作用能,其绝对值越大,聚合物与CO2的相互作用越强。CO2与共聚物之间的相互作用能可由下式[18]得到:
Einter=Epolymer+CO2-(Epolymer+ECO2).
(2)
式中,Einter为CO2与共聚物之间的相互作用能,kJ/mol;Epolymer+CO2为CO2-共聚物体系的总能量,kJ/mol;ECO2为CO2的能量,kJ/mol;Epolymer为共聚物的能量,kJ/mol。
共聚物与CO2之间的相互作用能见表3。P(HFDA0.28-co-MMA0.72)和P(HFDA0.26-co-EAL0.74)与CO2的相互作用能大致相当,表明这两种共聚物与CO2相互作用的强度相差不大,因此其溶解性能的差异主要受共聚物分子间相互作用和链柔顺性的影响。对于P(HFDA-co-EAL)共聚物,随着EAL基团含量的增加以及HFDA基团含量的减少,相互作用能变小,意味着共聚物与CO2之间的相互作用减弱。这与前文所述的共聚物链间相互作用增强、链柔性变差共同导致了共聚物溶解性能的降低。结果也表明,亲CO2的HFDA基团有助于提高共聚物在SC-CO2中的溶解性能。

表3 共聚物与CO2之间的相互作用能Table 3 Interaction energy between copolymer and CO2 kJ/mol
3.3 共聚物在SC-CO2中的增黏性能
在聚合物能够溶解于CO2的条件(35 ℃、30 MPa)下,测量了共聚物-CO2体系的相对黏度与质量浓度之间的关系。在实验温度压力条件下,纯CO2的黏度为0.098 86 mPa·s。如图6所示,这5种共聚物均能提高SC-CO2的黏度。增黏性能最好的为P(HFDA0.26-co-EAL0.74),在质量分数为5%时可以使SC-CO2的黏度提高87倍,强于P(HFDA0.28-co-MMA0.72)的51倍,如图6(a)所示。与P(HFDA0.26-co-EAL0.74)相比,P(HFDA0.28-co-MMA0.72)主链上甲基的存在使其空间位阻增大,降低了其在SC-CO2中的分子间缔合程度。对P(HFDA-co-EAL)共聚物而言,EAL的含量越大,相对黏度越大,在质量分数为5%时可以使SC-CO2的黏度提高34~87倍,如图6(b)所示。P(HFDA-co-EAL)分子中的EAL作为缔合基团使共聚物具备了较强的增黏性能。
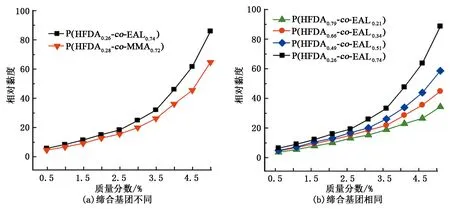
图6 共聚物-CO2体系的相对黏度与质量分数之间的关系Fig.6 Relative viscosities of polymer-CO2 systems versus mass fraction
图7为共聚物质量分数为4%并完全溶解于CO2的条件下,共聚物-CO2体系的相对黏度与温度及压力的关系曲线。可以看出,在30 MPa条件下,随着温度的升高,体系的相对黏度逐渐变小。在35 ℃条件下,随着压力的增大,体系的相对黏度逐渐变大。温度的升高使CO2对共聚物的溶解能力下降,共聚物在溶液中的舒展性变差,流体力学尺寸变小,链间缔合程度相应下降,导致其增黏性能下降。在更高压力下,CO2的溶解度参数增大[36-37],溶解能力提高,共聚物在溶液中的流体力学尺寸增大,使其可以通过更高程度的链间缔合产生更强的增黏性能。由于压力的变化对CO2和CO2-共聚物体系的黏度均有影响,故本文中在分析压力对相对黏度的影响时并未考虑压缩的增黏作用。

图7 共聚物-CO2体系的相对黏度与温度及压力之间的关系Fig.7 Relative viscosities of five polymer-CO2 systems versus temperature and pressure
径向分布函数常用于分析体系的微观结构并评价分子间相互作用,其峰位和峰值能够间接表明分子间相互作用的强弱。径向分布函数表示以A粒子为中心,周围B粒子的球对称径向分布概率,其表达式[16]为

(3)
式中,gAB(r)为径向分布函数;ρAB为AB粒子对的数密度;NAB(r)为在r到r+Δr的距离区间内的粒子对的平均数目。
为评价CO2-共聚物体系中共聚物的不同基团对其增黏性能的贡献,统计了共聚物中缔合基团的C-C对和HFDA基团的F-F对的分子间径向分布函数。径向分布函数的峰位越小,峰值越高,相互作用就越强。P(HFDA-co-EAL)的EAL基团和P(HFDA-co-MMA)的MMA基团C-C对的分子间径向分布函数结果如图8所示。

图8 共聚物缔合基团中C-C对的分子间径向分布函数Fig.8 Radial distribution functions of intermolecular carbon-carbon pairs of associative groups
图8(a)中,P(HFDA0.26-co-EAL0.74)和P(HFDA0.28-co-MMA0.72)的曲线上均可观察到明显的峰,峰位均在4.3 Å处。但后者的峰值小于前者,说明EAL基团的分子间相互作用强于MMA基团,其分子间缔合能力也较强,因而增黏性能更好。图8(b)中4条曲线的峰值和峰位有明显的不同。P(HFDA0.26-co-EAL0.74)的径向分布函数曲线峰值最高,P(HFDA0.49-co-EAL0.51)次之,两者的峰值出现在4.3 Å处。P(HFDA0.66-co-EAL0.34)不仅峰值较低,峰位也更远,在4.8 Å处。在P(HFDA0.79-co-EAL0.21)的曲线中则没有观察到明显的峰值。随着EAL基团含量的增大,共聚物分子可以在较近距离内产生更高程度的分子间缔合,从而使其增黏性能提高。
共聚物的HFDA基团中F-F对的分子间径向分布函数如图9所示。所有的曲线显示出类似的趋势,均未观察到明显的峰,径向分布函数值均小于1。说明共聚物中的HFDA基团分子间相互作用较弱,不足以使共聚物产生有效的分子间缔合。这与HFDA基团中氟原子的强电负性和氟斥力有关。分子间径向分布函数分析结果表明,共聚物在SC-CO2中的增黏性能应归功于疏CO2的缔合基团。
4 结 论
(1)随着EAL含量的增加,P(HFDA-co-EAL)共聚物在SC-CO2中的浊点压力逐渐上升,溶解性变差。这与共聚物分子间相互作用的增大和分子链柔顺性降低有关。但与此同时,其增黏性能逐渐提高,质量分数为5%的P(HFDA0.26-co-EAL0.74)可以使SC-CO2的黏度提高87倍,这源于共聚物在SC-CO2中分子链间缔合程度的增强。
(2)与P(HFDA0.26-co-EAL0.74)相比,在相同质量分数条件下,P(HFDA0.28-co-MMA0.72)在SC-CO2中的溶解性较差,增黏性能也较弱,最高仅可以使SC-CO2的黏度提高51倍。虽然EAL与MMA是同分异构体,但是两类共聚物的分子结构有较大差异。P(HFDA-co-MMA)主链上连接的甲基使其自由体积和柔顺性下降,并削弱了其在SC-CO2中的分子间缔合程度,降低了其溶解性能和增黏性能。
(3)共聚物结构和组成的差异影响了CO2-共聚物体系的分子间相互作用和共聚物分子间缔合能力,从而使共聚物的溶解性能和增黏性能产生了较大差别。增黏剂结构-性能关系的研究有助于SC-CO2增黏剂分子的设计。

