氮杂环卡宾催化的α,β-不饱和醛的直接催化氧化
Ingrid Rakielle Tsapy Takia,李洁妤,韩小瑜,曾晓飞
(1. 浙江科技学院生物与化学工程学院,浙江 杭州 310023; 2. 杭州师范大学材料与化学工程学院,浙江 杭州 311121)
0 引言
α,β-不饱和酸作为一类重要的有机合成中间体,常见的如巴豆酸和肉桂酸等化合物,在食品添加剂、医药、农药、化妆品及功能材料等多种精细化学品领域有着广泛的应用[1].由α,β-不饱和醛氧化制备α,β-不饱和酸的合成方法已有大量文献[2-3]报道.传统的合成方法主要采用当量的氧化剂对醛进行氧化,如CrO3、KMnO4及Ag2O等.采用此类氧化剂进行反应时,反应条件较为苛刻,一些氧化环境耐受性差的底物难以适用.此外,大量氧化剂的使用往往会造成大量的固废以及金属残留等问题,造成较大环境污染.因此开发环境友好的催化氧化体系仍是该氧化反应需要解决的问题.
氮杂环卡宾(NHC)是一类重要的有机杂环化合物,其不仅可以和金属配位催化各种偶联反应、烯烃复分解反应及环合反应等[4-5],还可以作为小分子催化剂,在碱性条件下与羰基化合物作用形成Breslow中间体,应用于各种复杂分子的构建中[6-7].近年来,国内外研究学者报道了通过卡宾直接催化氧化相应的芳香醛制备羧酸化合物的合成方法,为传统的金属参与的醛氧化制备羧酸化合物提供了新的研究思路[8].该合成方法以氧气作为氧化剂,在非手性卡宾催化剂的催化条件下,普通的芳香醛可以被直接催化氧化生成相应的羧酸,随后可进一步与O-、N-等亲核试剂反应,得到相应的羧酸酯及酰胺.反应条件温和,催化高效,化学收率优异,是一种制备羧酸及其衍生物的有效合成方法.
而当该反应应用于α,β-不饱和醛如由肉桂醛制备肉桂酸的反应时,则发现该反应产物并非肉桂酸,而是氢化肉桂酸.原因是由于卡宾与肉桂醛发生作用之后生成homoenolate中间体,之后发生分子内的质子转移,最终生成氢化肉桂酸衍生物(图1a)[9].整个反应涉及分子内的氧化还原反应(Redox),并不能实现肉桂酸化合物的有效合成.因此,研究如何在卡宾的催化作用下,直接将肉桂醛氧化成相应肉桂酸化合物,并广泛适用于α,β-不饱和酸的合成,有着重要的科学意义及潜在的应用价值.

图1 卡宾对α,β-不饱和醛的催化转化Fig.1 NHC-catalyzed transformations of α,β-unsaturated aldehyde
我们设想在氮杂环卡宾催化剂与α,β-不饱和醛发生作用形成氢原子转移中间体后,能否原位引入氧气作为氧化剂,这样就可以形成α,β-不饱和酰基唑中间体,进一步水解即可实现α,β-不饱和羧酸衍生物的合成(图1b).因此,本课题研究了氮杂环卡宾在氧气或空气下直接催化氧化合成肉桂醛的有机反应(图1),通过对卡宾催化剂、反应溶剂及催化剂用量等条件优化,得到制备合成肉桂酸的最佳反应条件.并在此基础上,考察了该氧化反应的底物适用范围,制备合成了一系列含有多取代基的α,β-不饱和酸类化合物.
1 实验部分
1.1 试剂、仪器与测试方法
α,β-不饱和醛及催化剂制备所需试剂均购自上海安耐吉化学,其余试剂均为分析纯,卡宾催化剂参考文献[10-11]报道方法制备合成.
核磁共振氢谱采用Bruck-500型核磁共振谱仪进行测定;熔点通过WRS-1B熔点仪进行测定.
1.2 α,β-不饱和酸2a-2m的合成
以肉桂酸2a化合物的合成为例(图2).向干燥的5 mL圆底烧瓶中,依次加入催化剂a(0.01 mmol, 3.6 mg),DMAP (0.4 mmol, 44.9 mg), THF溶剂2 mL,在搅拌状态下加入α,β-不饱和醛1a(0.4 mmol),在室温条件下进行反应,TLC跟踪反应进行.待反应结束后,加入稀盐酸, 析出固体,抽滤,干燥,得到目标化合物2a.
化合物2b—2m制备方法参考化合物2a的合成.

图2 卡宾对α,β-不饱和醛的直接催化氧化Fig.2 NHC-catalyzed direct oxidation of α,β-unsaturated aldehyde
2 结果及讨论
2.1 反应条件优化
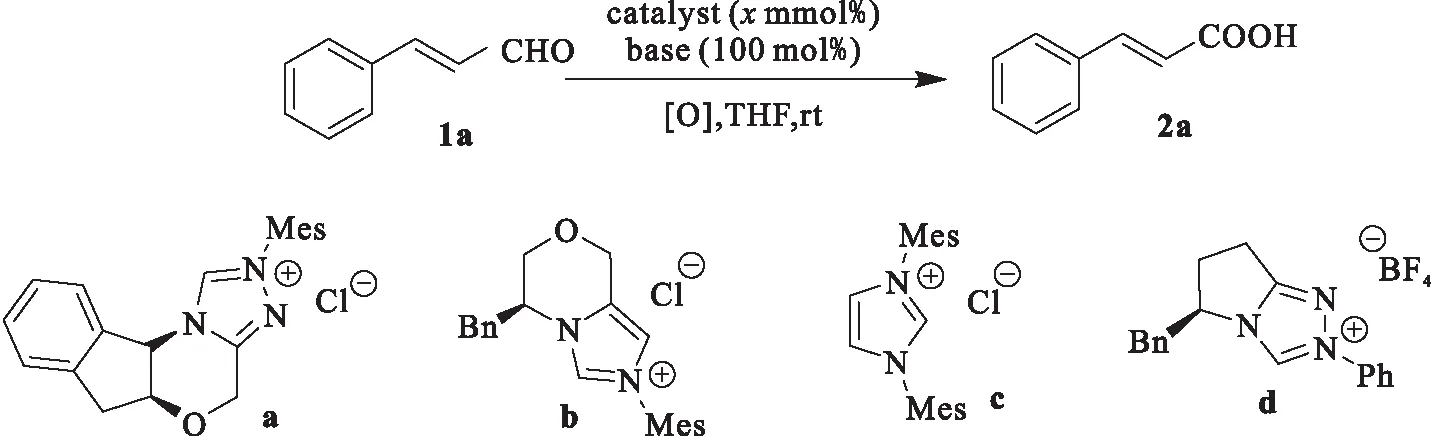
以肉桂醛1a的氧化为模板反应,在氮杂环卡宾作为催化剂,空气中对此反应进行了尝试.研究发现,空气中的氧气可以使氮杂环卡宾催化剂与肉桂醛发生作用形成氢原子转移中间体氧化,进一步水解后顺利得到了肉桂酸.我们进一步对反应条件进行了优化,结果见表1.实验结果表明,该反应在以卡宾做催化剂碱性条件下均能顺利进行,且以不同的收率得到肉桂酸2a.催化剂的种类与当量会对反应产生较大的影响.通过内标法,经核磁共振氢谱来计算优化条件过程中的反应产率.即反应结束后加入等物质的量的1,3,5-三甲氧基苯作为内标物质,以氘代氯仿为溶剂作核磁共振氢谱表征,根据两者特征峰的面积积分比例计算出实验产率.由表1可知,所有的N-杂环卡宾催化剂都表现出较好的催化性能.结果表明, 最佳催化剂为a.同时碱对反应有较大影响,采用10 mol% 的催化剂用量及100 mol% 的DMAP作为碱时,反应的化学收率可高达94%.不同的溶剂对该氧化反应也产生影响.THF作为反应溶剂,反应化学收率最好.综合上述实验结果最终确定最佳反应条件为:a(10 mol%)作为反应的催化剂,DMAP作为碱,在THF中室温下空气中进行反应.
表1 反应条件的优化
Tab.1 Optimization of reaction conditions
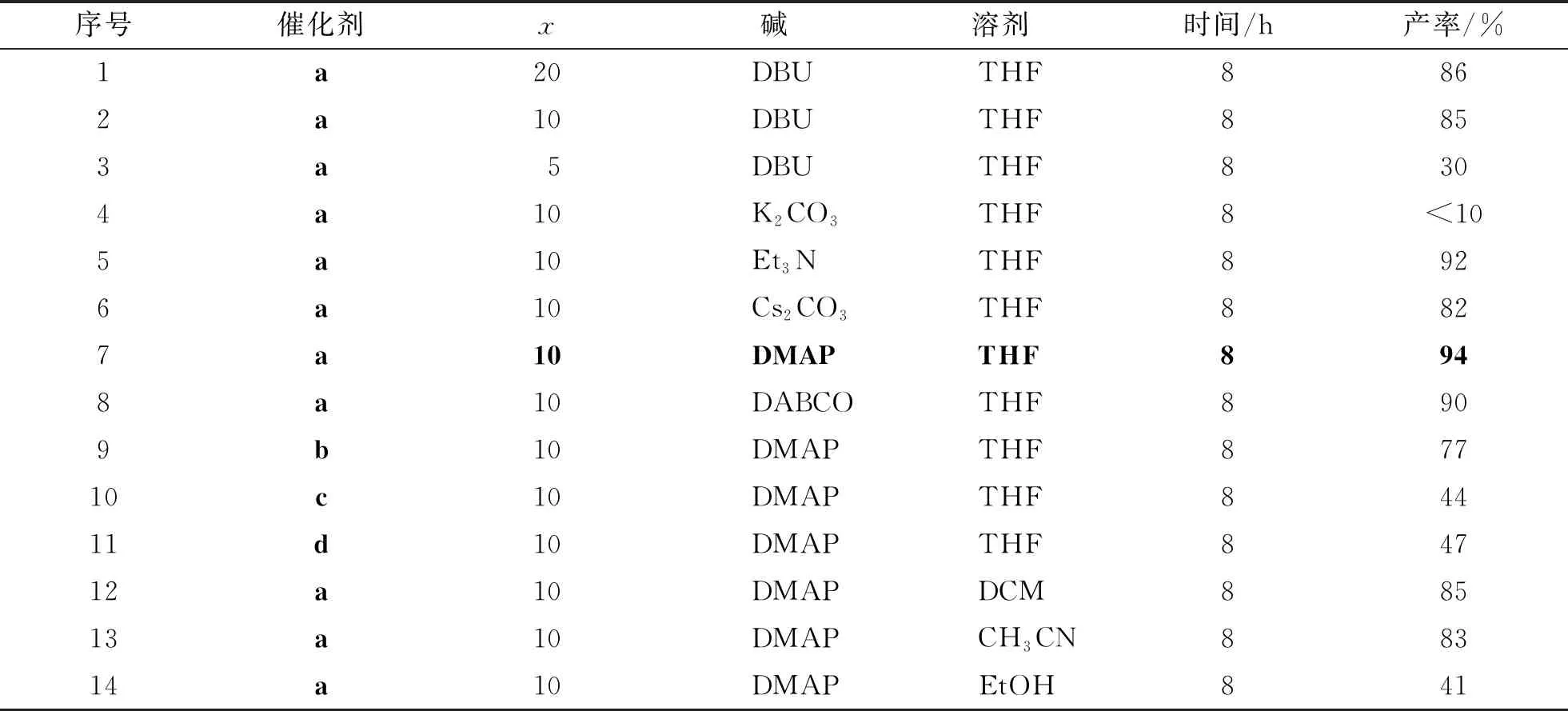
序号催化剂x碱溶剂时间/h产率/%1a20 DBU THF8862a10 DBU THF8853a5 DBU THF8304a10 K2CO3 THF8<105a10 Et3N THF8926a10 Cs2CO3 THF8827a10 DMAP THF8948a10 DABCO THF8909b10 DMAP THF87710c10 DMAP THF84411d10 DMAP THF84712a10 DMAP DCM 88513a10 DMAP CH3CN88314a10 DMAP EtOH841
2.2 底物拓展
在最佳反应条件下,进一步考察了底物的普适性(图3).实验结果表明,肉桂醛类衍生物都可以被卡宾催化剂高效直接催化氧化得到相应的羧酸化合物,且化学收率优异.该反应对于α,β-不饱和醛类化合物有很好的普适性.各种肉桂醛衍生物对该反应都表现出良好的兼容性.肉桂醛的苯环上无论连有吸电子基团或者供电子基团,该氧化反应都进行良好,反应时间短,且化学收率高.含有杂原子取代基α,β-不饱和醛2e也可以通过该直接氧化方法得到相应的酸,且化学收率高达95%.另外,β-烯基取代或者链状烷烃取代的α,β-不饱和醛都可以实现α,β-不饱和酸类化合物的合成, 且化学收率优异.另外,肉桂醛的α-位连有取代基时,反应无法进行.可能的原因是不饱和醛在与氮杂环卡宾催化剂结合后,α-位取代基的存在阻止了氢转移过程,从而使该反应无法进行.
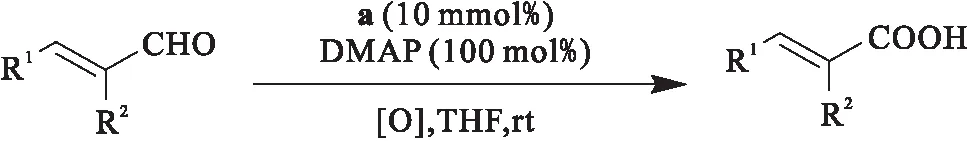
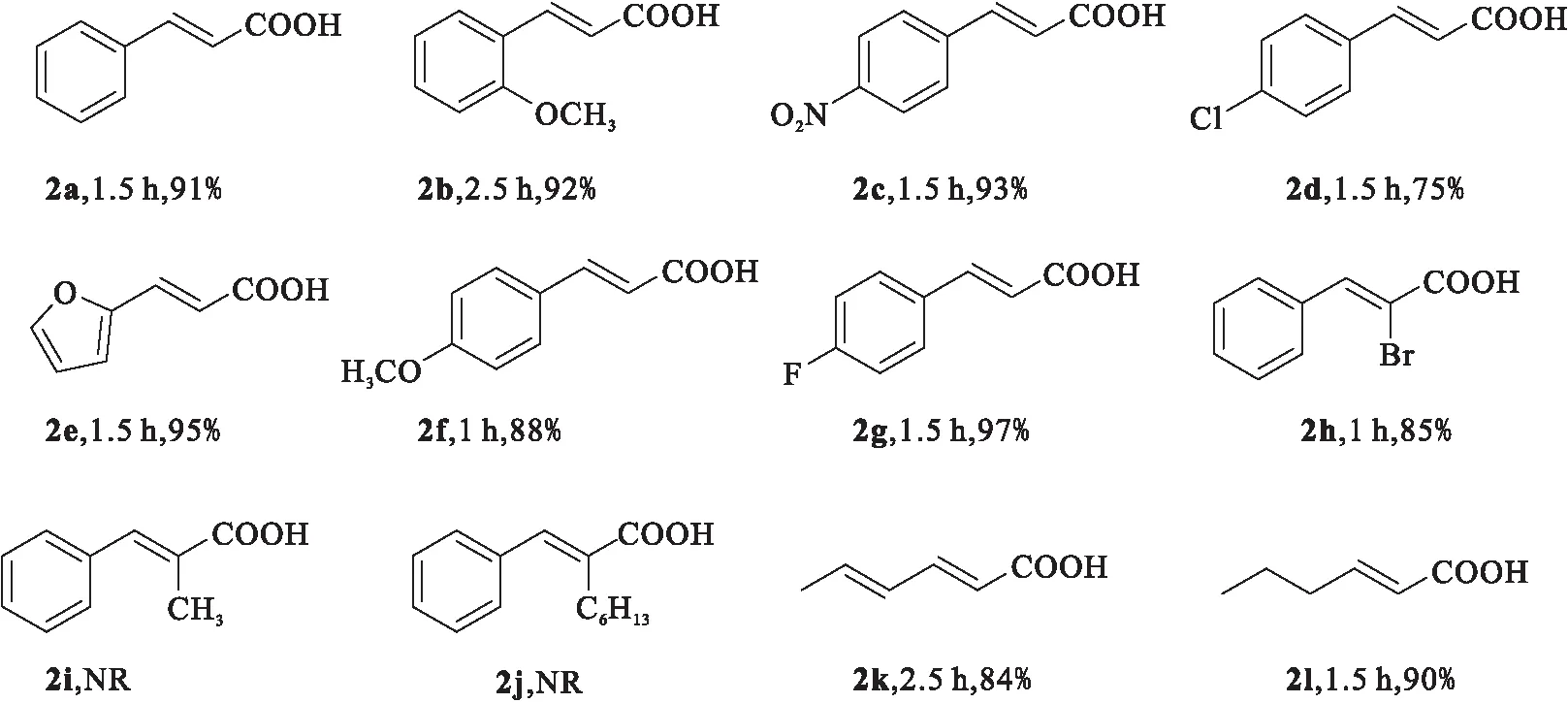
图3 底物扩展Fig.3 Substrate scope extension
2.3 核磁共振氢谱的分析
2a:白色结晶粉末,收率91%,mp:133.4~134.5 ℃;1H NMR (500 MHz,DMSO)δ 7.73~7.55 (m, 3H), 7.42 (dd,J= 6.5,3.7 Hz,3H), 6.54 (d,J=16.0 Hz,2H).
2b:白色结晶粉末,收率92%,mp:181~183 ℃;1H NMR (500 MHz,DMSO)δ 7.84(d,J=16.2 Hz,1H),7.68(dd,J=7.7,1.4 Hz,1H),7.44~7.38(m,1H),7.09(d,J=8.2 Hz,1H),6.99(t,J=7.5 Hz,1H),6.51(d,J=16.1 Hz,1H),2.54~2.47(m,4H).
2c:白色晶体粉末,收率93%,mp:287~289 ℃;1H NMR(500 MHz,DMSO)δ 8.18(dd,J=27.7,8.8 Hz,2H),7.90(d,J=8.8 Hz,2H),7.49(d,J=16.0 Hz,1H),6.68(d,J=16.0 Hz,1H),2.66(s,1H).
2d:白色晶体粉末,收率75%,mp:238~240 ℃;1H NMR(500 MHz,DMSO)δ 7.73(d,J=8.5 Hz,2H),7.59(d,J=16.1 Hz,2H),7.48(d,J=8.5 Hz,2H),6.56(d,J=16.0 Hz,1H).
2e:白色针状粉末,收率95%,mp:134~136 ℃;1H NMR(500 MHz,DMSO)δ 7.84(s,2H),7.40(d,J=15.8 Hz,1H),6.93(d,J=3.4 Hz,1H),6.64(dd,J=3.3,1.8 Hz,1H),6.16(d,J=15.8 Hz,1H).
2f:白色晶体粉末,收率88%,mp:172~173.5 ℃;1H NMR(500 MHz,DMSO)δ 7.65(d,J=8.7 Hz,2H),7.55(d,J=16.0 Hz,1H),6.98(d,J=8.7 Hz,2H),6.38(d,J=16.0 Hz,1H),3.80(s,4H).
2g:白色晶体固体,收率97%,mp:210~211.5 ℃;1H NMR(500 MHz,DMSO)δ 7.14(dd,J=15.3,10.0 Hz,1H),6.25(d,J=9.4 Hz,1H),6.22(d,J=6.0 Hz,1H),5.76(d,J=15.3 Hz,1H),1.81(d,J=5.8 Hz,3H).
2h:白色结晶状粉末,收率85%,mp:131~132.5 ℃;1H NMR(500 MHz,DMSO)δ 7.69(dd,J=6.5,2.8 Hz,2H),7.59(d,J=16.0 Hz,1H),7.44~7.39(m,3H),6.53(d,J=16.0 Hz,1H).
2k:白色结晶状粉末,收率84%,mp:132~133 ℃;1H NMR(500 MHz,CDCl3)δ 12.52(dd,J=8.7,5.6 Hz,2H),12.35(d,J=16.0 Hz,1H),12.01(t,J=8.8 Hz,2H),11.25(d,J=16.0 Hz,1H),8.47~7.79(m,2H).
2l:无色液体,收率90%,mp:29~32 ℃;1H NMR(500 MHz,DMSO)δ 6.81(dt,J=15.5,7.0 Hz,1H),5.76(d,J=15.6 Hz,1H),2.20~2.11(m,2H),1.52~1.34(m,3H),0.92~0.85(m,3H).
3 结论
本课题以清洁、廉价的空气作为氧化剂,通过使用氮杂环卡宾催化,可实现多种α,β-不饱和醛的直接催化氧化反应.该合成方法无需金属参与,原料廉价易得,实验操作简便,反应条件温和,底物适用范围较广,化学收率优异,可与传统使用重金属或昂贵的催化剂体系相媲美,为α,β-不饱和酸类化合物的高效合成提供了新的研究策略.

