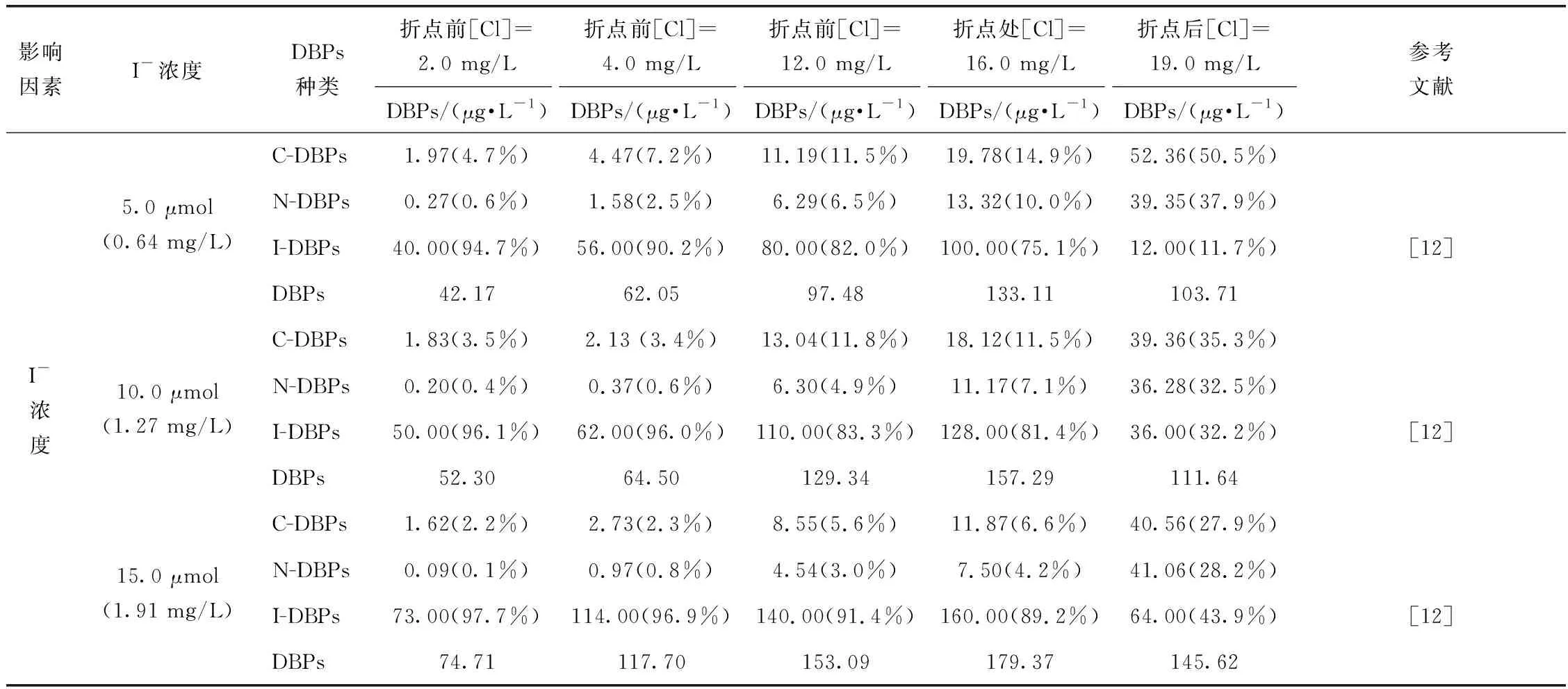
含碘水折点加氯过程中消毒副产物的生成影响机制
张肸同,徐 斌,2,*,张天阳,刘 志,朱静萍,高 炜,沈玉琼,芮 旻
(1.同济大学污染控制与资源化研究国家重点实验室,长江水环境教育部重点实验室,上海 200092;2.上海污染控制与生态安全研究院,上海 200092;3.上海城投水务〈集团〉有限公司制水分公司,上海 200080;4.上海市政工程设计研究总院〈集团〉有限公司,上海 200092)
氯化消毒作为水厂最常用的消毒方式,具有高效、经济、运用广泛等优点。而折点现象又是氯化消毒中常见的现象,当原水中含有较多氨氮或含氨基类有机化合物时,折点加氯能达到更好的消毒效果,且满足余氯量要求[1]。但是,氯化消毒也存在弊端,除了能够消灭水中病原体外,氯还可以与水中基质化合物,例如天然有机物(NOM)、无机化合物(Br-和I-等)反应生成各种DBPs[2]。大量研究表明,加氯消毒后饮用水的致突变性显著增强。短期生物学试验、动物致癌试验以及流行病学调查结果均表明,DBPs对人体健康构成威胁[3]。国际癌症研究机构(IARC)将TCM和BDCM列为2B类致癌物质,即可以对人类致癌物质[3]。在众多DBPs中,卤乙腈(HANs)类的含量排在DBPs的第三位,仅次于THMs和卤乙酸(HAAs)。WHO规定,DCAN的浓度不得超过20.0 μg/L,DBAN不得超过70.0 μg/L[4]。大多数运用啮齿类动物检测DBPs 致癌性的试验表明,DBPs引起肝癌的概率大于膀胱癌、结肠直肠癌;此外,BDCM 和TCM可以引起肾肿瘤; BDCM和TBM可以引起小肠肿瘤,TBM和BDCM可以诱发大肠肿瘤,其中,BDCM 致肿瘤的剂量要低于其他THMs的剂量[3]。HANs的毒性研究多集中于遗传毒性,对于其致癌性的研究尚未报道。但早期体内致畸试验研究显示,HANs具有胚胎毒性,可使围产期仔鼠存活率下降及生长发育迟滞,TCAN显示出最强的发育毒性[5]。
次氯酸与氨的反应主要受温度、pH和加氯量等因素的影响[6]。研究发现,含有氨氮或氨基类有机化合物的水在进行氯化消毒时,当氨氮浓度为0.5~1.0 mg/L、氯浓度为1.0~10.0 mg/L时将产生折点现象[7-8]。在中性条件下,氯氨水系统反应通常涉及3个阶段:第一阶段缓慢氧化阶段(Cl/N<1.0),涉及化学反应式(1)和式(2),由于该阶段次氯酸的量小于氨的量,氨不能被充分氧化,产物主要是一氯胺;第二阶段过渡阶段(1.0
Cl2+H2O→HOCl+H++Cl-
(1)
HOCl+NH3→NH2Cl+H2O
(2)
HOCl+NH2Cl→NHCl2+H2O
(3)
HOCl+NHCl2→NCl3+H2O
(4)
3HOCl+2NH3→N2+3H++3Cl-+3H2O
(5)
地表水中I-浓度通常在0.5~20.0 μg/L,有些情况下(如海水倒灌等)I-浓度可能超过50 μg/L[10-11]。当这些含碘水作为水源水,且用氯、氯胺和臭氧等进行消毒时,I-可以被氧化成HIO,从而与水中的有机物反应生成碘代消毒副产物(I-DBPs)。作者所在团队前期研究了含碘水折点加氯过程中I-DBPs的生成特性[12]。研究发现:沿折点加氯曲线,折点之前生成的I-DBPs主要是CHI3和CHI2Cl,且随着加氯量的增加,生成的I-DBPs总浓度逐渐增加;折点之后生成的I-DBPs主要是CHICl2,且随着加氯量的增加,生成的I-DBPs总浓度逐渐减少[12]。然而,在I-存在的情况下,氯化消毒折点加氯过程中除I-DBPs以外,C-DBPs和N-DBPs的生成特性以及DBPs产量与折点位置关系如何目前尚不清楚。因此,本研究重点探究了含碘水在折点加氯过程中C-DBPs和N-DBPs的生成特性以及DBPs产量与折点位置的关系,并深入探究了不同I-浓度、Br-/I-摩尔比、NOM浓度和pH对C-DBPs和N-DBPs生成的影响。
1 材料与方法
1.1 药品
本试验所用药品均为分析纯,且没有经过再一次纯化。碘化钾(KI≥99.0%)、溴化钾(KBr≥99.0%)、次氯酸钠(NaOCl, 4.00%~4.99%)、氯化铵(NH4Cl)、氢氧化钠(NaOH)、硫酸 (H2SO4)、磷酸二氢钾(KH2PO4)和腐植酸I(HAI)均购于Sigma-Aldrich (USA);甲醇、甲基叔丁基醚(MTBE)购于 J.T. Baker (USA);Suwannee River 腐植酸(HAⅡ)和富里酸(FA)购于国际腐殖质协会(IHSS)。试验所用纯水均来自 Milli-Q 纯水机。C-DBPs标准品(包括CH3Cl、CH2Cl2、CHCl3和CCl4),N-DBPs标准品(包括CH3NO2、C2H2ClN、C2HCl2N、C2HClBrN和C2HBr2N)均购于CanSym Chemical Corp.(Canada)。
1.2 试验方法和分析方法
1.2.1 折点加氯试验
用NH4Cl试剂预氨化5.0 mg C/L NOM(HAI)样品,使氨氮浓度达到1.4 mg/L,然后立即在样品中加入NaOCl溶液,使样品氧化剂浓度在1.0~20.0 mg/L (0.014~0.280 mmol),室温下[(25.0±1.0) ℃]反应2.0 h。反应后的溶液用DPD滴定法测总氯和自由氯浓度[13-14]。
1.2.2 DBPs生成试验和分析方法
DBPs的生成是以40 mL棕色玻璃瓶在无顶空室温[(25.0±1.0) ℃]条件下反应。试验中探究的4个影响因素,分别是I-浓度(5.0、10.0、15.0 μmol)、Br-/I-摩尔比(0.5、1、5)、NOM浓度(3.0、5.0、7.0 mg C/L)和pH值(6.0、7.0、8.0)。pH的测量用pH计(FE20-FiveEasy, Mettler Toledo, Switzerland)。NOM浓度的测量用 Shimadzu TOC-VCSH analyzer (Shimadzu, Japan)测可溶性有机碳(DOC)的浓度,该仪器的检测限是0.1 mg C/L。Br-和I-的测量用离子色谱仪(ICS-2000, Dionex, USA),配AS11-HC分析柱和 AG11-HC防护柱。
DBPs的检测方法采用USEPA551.1检测方法[15]。2.0 mL 甲基叔丁基醚(MTBE)萃取10.0 mL样品,震荡3 min,静置4 min,取上层溶液700~1 000 μL到棕色小瓶里,然后用气相色谱仪(GC-2010, Shimadzu, Japan)分析。GC-2010气相色谱仪配电子捕获器(ECD)和HP-5毛细管柱(30 m×0.25 mm i.d., 0.25 μm膜厚度, J&W, USA)。射入口温度为200.0 ℃,检测器温度为290.0 ℃,载气氮压力为69.8 kPa,流速为30.0 mL/min,温度程序设置为40.0 ℃持续10 min,然后以 15.0 ℃/min增加到260.0 ℃,持续10 min。
2 试验结果与讨论
2.1 I-浓度对折点加氯过程中C-DBPs和N-DBPs生成的影响
在本研究中,当Cl2/NH3-N摩尔比为2.3、反应时间为2.0 h时,反应样品中氧化剂出现折点现象。Sylvia等[16]研究发现,折点加氯折点值出现在Cl2/NH3-N摩尔比为1.4~3.2时,本试验与之相符。
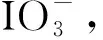

([NH4Cl]=1.4 mg N/L (0.1 mmol),[DOC]=5 mg C/L,pH值=7.0,反应时间为2.0 h,反应温度为25.0 ℃)图1 I-浓度对折点加氯过程中C-DBPs和N-DBPs生成的影响Fig.1 Effect of I- Concentration on C-DBPs and N-DBPs Formation during Breakpoint Chlorination
表1不同I-浓度条件下各种消毒副产物在折点以及折点前后的生成量
Tab.1 Production of DBPs in Pre-Breakpoint Zone and Post-Breakpoint Zone during Different I-Concentration
影响因素I-浓度DBPs种类折点前[Cl]=2.0 mg/L折点前[Cl]=4.0 mg/L折点前[Cl]=12.0 mg/L折点处[Cl]=16.0 mg/L折点后[Cl]=19.0 mg/LDBPs/(μg·L-1)DBPs/(μg·L-1)DBPs/(μg·L-1)DBPs/(μg·L-1)DBPs/(μg·L-1)参考文献I-浓度5.0 μmol(0.64 mg/L)10.0 μmol(1.27 mg/L)15.0 μmol(1.91 mg/L)C-DBPs1.97(4.7%) 4.47(7.2%)11.19(11.5%)19.78(14.9%)52.36(50.5%)N-DBPs0.27(0.6%) 1.58(2.5%)6.29(6.5%)13.32(10.0%)39.35(37.9%)I-DBPs40.00(94.7%)56.00(90.2%)80.00(82.0%)100.00(75.1%)12.00(11.7%) [12]DBPs42.1762.0597.48 133.11 103.71C-DBPs1.83(3.5%)2.13 (3.4%)13.04(11.8%)18.12(11.5%)39.36(35.3%)N-DBPs0.20(0.4%) 0.37(0.6%) 6.30(4.9%) 11.17(7.1%)36.28(32.5%)I-DBPs50.00(96.1%)62.00(96.0%)110.00(83.3%)128.00(81.4%)36.00(32.2%)[12]DBPs52.3064.50129.34 157.29 111.64C-DBPs1.62(2.2%) 2.73(2.3%)8.55(5.6%)11.87(6.6%)40.56(27.9%)N-DBPs0.09(0.1%)0.97(0.8%)4.54(3.0%) 7.50(4.2%)41.06(28.2%)I-DBPs73.00(97.7%)114.00(96.9%)140.00(91.4%)160.00(89.2%)64.00(43.9%) [12]DBPs74.71117.70153.09 179.37 145.62
注:1.C-DBPs主要是TCM,N-DBPs主要是DCAN,其他类含量较少,本研究忽略不计;2.I-DBPs主要是试验中生成的各种碘代三卤甲烷,包括CHI3、CHClI2、CHCl2I,具体数值见参考文献[12];3.DBPs的总量为C-DBPs、N-DBPs和I-DBPs的和;4.(%)表示该种类DBPs的量占总DBPs的量百分比
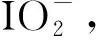
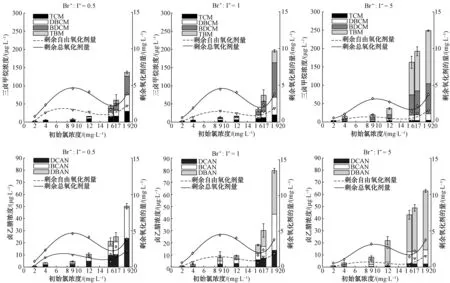
([NH4Cl]=1.4 mg N/L (0.1 mmol),[DOC]=5.0 mg C/L,[I-]+[Br-]=1.27 mg/L,pH值=7.0,反应时间为2 h,反应温度为25.0 ℃)图2 Br-/I-摩尔比对折点加氯过程中C-DBPs和N-DBPs生成的影响Fig.2 Effect of Br-/I- Molar Ratio on C-DBPs and N-DBPs Formation during Breakpoint Chlorination
2.2 Br-/I-摩尔比对折点加氯过程中C-DBPs和N-DBPs生成的影响
在本研究中,当Cl2/NH3-N摩尔比为2.3、反应时间为2.0 h时,反应样品中氧化剂出现折点现象。
氯、溴、碘以及NOM共存体系中,涉及的化学反应主要有式(6)~式(12)。
HOCl+I-→HOI+Cl-k1=4.3×108mol-1·L·s-1
(6)[18]
HOCl+Br-→HOBr+Cl-k2=1 550 mol-1·L·s-1
(7)[21]

(8)[22]

(9)[22]
HOCl+NOM→产物k5=0.7-5 mol-1·L·s-1
(10)[23]
HOBr+NOM→产物k6=15-167 mol-1·L·s-1
(11)[23]
HOI+NOM→产物k7=0.1-0.4 mol-1·L·s-1
(12)[19]
由图2可知,在不同Br-/I-摩尔比条件下,折点均出现在初始氯浓度为16.0 mg/L时。当Br-/I-=5时,剩余总氧化剂和剩余自由氧化剂浓度均较低。本试验生成的C-DBPs主要类型为TBM、TCM、DBCM、BDCM;生成的N-DBPs主要类型为DBAN、BCAN、DCAN。对仓鼠卵细胞基因毒理性的研究发现,慢性仓鼠卵细胞细胞毒性等级排序为:TBM>DBCM>TCM>BDCM[20]。与Cl-THMs不同,Br-THMs易被转基因株沙门氏菌谷胱甘肽S转移酶-θ(GSTP1-1)诱变,因此,与Cl-THMs相比,Br-THMs具有更高的细胞毒性[17, 20]。HANs消毒副产物的细胞毒性排序为:TCAN>DBAN>BCAN>DCAN[20]。相同加氯量,随着Br-/I-的增加,Br-DBPs浓度逐渐增加,且具有更高基因毒性的TBM浓度水平增加最多,逐渐成为主要物质,DBCM浓度略有降低,BDCM浓度变化不大,TCM浓度水平减少最多,逐渐成为低浓度水平物质。对于N-DBPs,相同加氯量,随着Br-/I-的增加,具有更高细胞毒性的DBAN浓度水平增加最多,逐渐成为主要生成物质,BCAN浓度略微有所降低,DCAN浓度水平减少最多,逐渐成为低浓度水平物质。这可能是因为随着Br-增多,水溶液中HOBr浓度升高,HOBr比HOCl具有更强的电子取代能力,生成更多的Br-THMs[12,24-25];另外,相同Br-/I-,沿着折点加氯曲线,THMs类和HANs类物质浓度含量均随之增加。同时,沿着折点加氯曲线折点之后浓度增加更明显,可能是因为折点之后水中剩余氧化剂主要是自由氯,自由氯具有更强的氧化性,能够氧化更多的NOM生成DBPs,这也造成折点后THMs类和HANs类含量增加较明显[26]。

表2 不同 Br-/I-摩尔比条件下各种消毒副产物在折点以及折点前后的生成量Tab.2 Production of DBPs in Pre-Breakpoint Zone and Post-Breakpoint Zone during Different Br-/I- Molar Ratio
注:1.C-DBPs主要包括TCM、DBCM、BDCM和TBM,N-DBPs主要包括DCAN、BCAN和DBAN,其他类含量较少,本研究忽略不计;2.I-DBPs主要是试验中生成的各种碘代三卤甲烷,包括CHI3、CHClI2、CHCl2I、CHBrI2、CHBr2I、CHClBrI,具体数值见参考文献[12];3.DBPs的总量为C-DBPs、N-DBPs和I-DBPs的和;4.(%)表示该种类DBPs的量占总DBPs的量百分比
由表2可知,折点前低加氯量生成的DBPs总量远小于其他位置,折点前高加氯量生成的DBPs总量略小于折点处,远小于折点后,折点后生成的DBPs总量大约是折点前低加氯量的4倍,折点前高加氯量的2倍。另外,与其他影响因素相比,Br-的存在大大增加了DBPs的生成量,这是因为,由式(11)可知,与HOI和HOCl相比,HOBr与NOM的反应活性更高,Br-C键比Cl-C键更易形成,更易与NOM发生反应生成Br-DBPs[18]。随着Br-浓度的增加,具有更高细胞毒性和基因毒性的TBM和DBAN占比大大增加。因此,对于Br-、I-共存的水体,在氯化消毒过程中采用加大氯投加量来降低I-DBPs的方法是不可行的。Br-的存在仅加大了I-DBPs的生成,对C-DBPs和N-DBPs的生成量影响不大。这是因为,此时生成了新型I-DBPs,包括CHBrI2、CHBr2I和CHClBrI。在2.0~4.0 mg/L低氯投加量时,DBPs的生成量远小于高加氯量,此时的氧化剂主要是NH2Cl,证明对Br-、I-同时存在的水体用氯胺消毒能减少DBPs的生成,且随着Br-占比的增大,DBPs生成量变化不大。
2.3 NOM浓度对折点加氯过程中C-DBPs和N-DBPs生成的影响
在本研究中,当Cl2/NH3-N摩尔比为2.3、反应2.0 h时,样品中氧化剂出现折点现象。
由图3可知,不同DOC浓度条件下,折点均出现在初始氯浓度为16.0 mg/L时,且不同DOC浓度对折点曲线影响不大。当DOC浓度相同时,沿折点加氯曲线,在折点之前,DOC浓度对TCM和DCAN生成的影响较小,且相对于折点之后,生成的TCM和DCA浓度水平较低。折点处以及折点之后,TCM和DCAN生成量增加明显。折点之后([Cl]=19.0 mg/L),TCM和DCAN生成量是折点处的2倍左右。

([NH4Cl]=1.4 mg N/L (0.1 mmol),[I-]=10.0 μmol,pH值=7.0,反应时间为2 h,反应温度为25.0 ℃)图3 NOM浓度对折点加氯过程中C-DBPs和N-DBPs生成的影响Fig.3 Effect of NOM Concentration on C-DBPs and N-DBPs Formation during Breakpoint Chlorination
表3不同DOC浓度条件下各种消毒副产物在折点以及折点前后的生成量
Tab.3 Production of DBPs in Pre-Breakpoint Zone and Post-Breakpoint Zone during Different NOM Concentration

影响因素DOC浓度/(mg C·L-1)DBPs种类折点前[Cl]=2.0 mg/L折点前[Cl]=4.0 mg/L折点前[Cl]=12.0 mg/L折点处[Cl]=16.0 mg/L折点后[Cl]=19.0 mg/LDBPs/(μg·L-1)DBPs/(μg·L-1)DBPs/(μg·L-1)DBPs/(μg·L-1)DBPs/(μg·L-1)参考文献DOC浓度3.05.07.0C-DBPs1.68(4.0%) 3.68(6.6%)7.79(7.0%)18.79(16.9%)36.54(40.1%)N-DBPs0.14(0.3%)1.73(3.1%)3.03(2.7%)2.64(2.4%)34.60(38.0%)I-DBPs40.00(95.7%)50.00(90.2%)100.00(90.2%)90.00(80.7%) 20.00(21.9%)[12]DBPs41.8255.41110.81 111.43 91.13C-DBPs1.89(4.7%)3.38(5.4%)10.19(8.1%)23.89(15.0%)56.12(35.3%)N-DBPs0.29(0.7%)1.60(2.5%)6.30(5.0%)11.17(7.0%)44.93(28.2%)I-DBPs38.00(94.6%)58.00(92.1%)110.00(86.9%)124.00(78.0%)58.00(36.5%) [12]DBPs40.1862.98126.49 159.07 159.05C-DBPs2.28(3.8%) 2.22(3.0%)9.39(5.4%)19.04(7.8%)51.84(40.1%)N-DBPs0.24(0.4%)0.76(1.0%)5.80(3.3%)17.97(7.3%)43.35(38.0%)I-DBPs58.00(95.8%)70.00(96.0%)160.00(91.3%)208.00(84.9%)58.00(21.9%) [12]DBPs60.5272.98175.19 245.02 153.19
注:1.C-DBPs主要是TCM,N-DBPs主要是DCAN,其他类含量较少,本研究忽略不计;2.I-DBPs主要是试验中生成的各种碘代三卤甲烷,包括CHI3、CHClI2、CHCl2I,具体数值见参考文献[12];3.DBPs的总量为C-DBPs、N-DBPs和I-DBPs的和;4.(%)表示该种类DBPs的量占总DBPs的量百分比
相同初始氯浓度,随着DOC浓度的升高,TCM和DCAN的生成量逐渐升高。但当DOC浓度达到7.0 mg C/L时,TCM和DCAN的生成量几乎不再增加。可能原因是天然有机物中的酚类化合物、β-二酮类化合物和一些能转化为酮酸(如柠檬酸)的羧酸是生成THMs的主要前驱物质,当DOC浓度达到一定时,溶液中能与消毒剂结合生成DBPs的前驱物质达到极限,DOC浓度继续增大时,DBPs生成量几乎不变[27]。

([NH4Cl]=1.4 mg N/L (0.1 mmol),[I-]=10.0 μmol(1.27 mg/L),[DOC]=5.0 mg C/L,反应时间为2.0 h,反应温度为25.0 ℃)图4 pH值对折点加氯过程中C-DBPs和N-DBPs生成的影响Fig.4 Effect of pH Value on C-DBPs and N-DBPs Formation during Breakpoint Chlorination
由表3可知,折点前低加氯量生成的DBPs总量远小于其他位置,约是其他位置DBPs总量的0.5倍。在高加氯量条件下,折点后生成的DBPs总量略小于折点处和折点前。折点前I-DBPs含量占总DBPs的90%左右,而折点后I-DBPs含量降低到总量的30%左右。因此,对于DOC含量较高的含碘水进行氯化消毒时,加大氯投加量减少I-DBPs的生成量是可行的,同时,由2~4 mg/L低氯投加量可知,NH2Cl作为消毒剂可以较少DBPs的生成,因此,氯化消毒过程中可以适当投加氨氮。同时,DOC浓度越高,DBPs生成量越高,但是DOC浓度的影响作用没有其他因素大。
2.4 pH对折点加氯过程中C-DBPs和N-DBPs生成的影响
由图4可知,不同pH条件对折点曲线影响较大,折点出现的初始氯浓度也不相同。pH值=7.0条件下,折点出现在初始加氯量为16.0 mg/L时;pH值=6.0条件下,折点出现在初始加氯量为17.0 mg/L时;pH值=8.0条件下,折点加氯量为19.0 mg/L时。同时,在相同pH条件下,TCM和DCAN的浓度均随折点加氯曲线呈明显增加的趋势,且在曲线折点之前浓度增加量小于折点之后。同一加氯量条件下,pH值=6.0时,TCM的浓度最低,可能是由于
在酸性条件下,卤仿反应机制和动力学的变化,或其他与有机氯中间体有关的反应[28]。在pH值=8.0时,DCAN的浓度最低,这可能是因为,DCAN只有在pH值=5.0时才稳定存在,在pH值=7.0时会随时间增加而降解,在pH值=9.0时几乎不生成DCAN[29]。同时,一氯胺在pH值=7.0时能够水解成HOCl,从而更加有利于TCM和DCAN的生成;而在酸性条件下,一氯胺容易降解;碱性条件下,一氯胺不能生成HOCl,不利于TCM和DCAN的生成[12, 30]。
由于pH对折点加氯现象影响较大,不同pH条件下,折点出现位置不同。为了与前述其他影响因素相互对照,不同pH条件下各种DBPs产量考察点仍然选取[Cl]=4.0、12.0、16.0、19.0 mg/L。由表4可知,酸性条件生成的DBPs总量最小,碱性条件下生成总量最大,约是酸性条件下的2~5倍。pH值=8.0时,形成的I-THMs总量最大,这可能是由中间产物的水解和THM前体的烯醇化造成的[12]。在碱性条件下,氧化能力强于NHCl2的NH2Cl更有利于I-THMs的形成,同时,NH2Cl在酸性条件下易水解或转化为NHCl2和NCl3,碱性条件下I-DBPs的生成量大于中性和酸性[12, 30]。因此,在碱性条件下通过加大氯投加量来控制I-DBPs的生成是不可行的。在2.0~4.0 mg/L低加氯量条件下,与高加氯量相比,DBPs的生成量最小,但pH值=8.0时,DBPs生成量约是中性条件下的1.5倍,证明碱性条件会促进氯胺消毒过程中DBPs的生成。

表4 不同pH条件下各种消毒副产物在折点以及折点前后的生成量Tab.4 Production of DBPs in Pre-Breakpoint Zone and Post-Breakpoint Zone during Different pH Value
注:1.C-DBPs主要是TCM,N-DBPs主要是DCAN,其他类含量较少,本研究忽略不计;2.I-DBPs主要是试验中生成的各种碘代三卤甲烷,包括CHI3、CHClI2、CHCl2I,具体数值见参考文献[12];3.DBPs的总量为C-DBPs、N-DBPs和I-DBPs的和;4.(%)表示该种类DBPs的量占总DBPs的量百分比
3 结论
本试验主要研究了含碘水在折点加氯过程中,I-浓度、Br-/I-摩尔比、NOM浓度和pH对C-DBPs和N-DBPs生成的影响以及DBPs生成量与折点位置关系。借助氯与氨氮共存体系产生的折点现象,分析不同加氯量造成的折点不同位置处DBPs的生成状况。对比几个影响因素可知,Br-/I-摩尔比是影响DBPs生成的最主要影响因素,Br-的存在使DBPs生成量在同等条件下远大于只存在I-的水体。同时,虽然高水平的I-DBPs在实践中可能是罕见的,但在以氯作为消毒剂的水厂的实际生产中,增加氯剂量是控制I-DBPs生成的一种可行方法,该方法在Br-、I-共存水体和碱性水体中是无效的。在高含碘水中,氯胺作为消毒剂要比氯更有优势,但是在碱性条件下氯胺又能促进I-THMs的形成,因此,对于碱性含碘,控制pH可能是更有效的措施。同时,反应温度、反应时间等因素均可能对结果产生影响,实际生成过程中应考虑各种可能影响条件。

