牛黄清胃丸中化工染料检查及天然色素成分分析
刘静,刘汇,2,何轶,戴忠*,马双成*
1.中国食品药品检定研究院,北京 100050;2.延边朝鲜族自治州食品药品检验所,吉林 延吉 133002
牛黄清胃丸是由牛黄、大黄、黄芩、黄柏和番泻叶等17味药组成的中药复方制剂,具有清胃泄火、润滑通便之功效。用于心胃火盛、头晕目眩、口舌生疮、牙龈肿痛、乳蛾咽痛、便秘尿赤[1]。处方中含有的黄芩、黄柏药材是市场上常见的染色中药,其可能存在的合成染料主要有金胺O,但其他黄色系染料如柠檬黄、日落黄、亮黄、金橙Ⅱ等也可能用于染色[2-7]。中药安全问题一直备受关注,从近年国家药品评价抽验质量分析情况来看,在经济利益的驱使下,中药染色掺伪现象时有发生[2-3]。由于中药染色常采用化工染料,这些合成染料大都具有一定毒性,对人体健康存在严重安全隐患,有的甚至有致癌性,在食品领域被禁止使用或严格控制使用量[8]。中药染色危害公众用药安全,欺骗消费者,是严重的违法行为。因此,国家药品监管部门高度重视,相继审核批准了多种中药中化工染料补充检验方法,主要有黄芩、蒲黄、红花等,有力地打击了中药使用合成染料染色的违法行为[9]。因此,为更好地保障用药安全性。本研究首先研究建立了牛黄清胃丸中柠檬黄、日落黄、亮黄、金橙Ⅱ和金胺O的HPLC检查方法。同时,针对本品处方药味多,所含化学成分复杂多样,且处方中栀子、大黄等药材中含有一些天然色素成分的情况[10-11],笔者进一步研究建立了这些天然色素成分指纹图谱,为更全面地评价本品质量提供了参考。
1 材料
1.1 仪器
Waters高效液相色谱仪(配备DAD检测器);Mettler XS105DU十万分之一天平、AE 3240 万分之一电子天平(瑞士梅特勒-托利多仪器有限公司);KQ-300DA型数控超声波清洗仪(昆山市超声仪器有限公司,超声功率:300 W,频率:40 kHz);Milli Q纯水机(美国Millipore公司)。
1.2 试药
金胺O、柠檬黄、日落黄、金橙Ⅱ对照品(中国食品药品检定研究院,批号分别为111770-201603、510004-201602、510005-201602、111769-201302);亮黄(美国Sigma-Aldrich公司);黄芩苷、西红花苷Ⅰ、西红花苷Ⅱ、大黄酸、盐酸小檗碱、芦荟大黄素、大黄素、大黄酚、大黄素甲醚(中国食品药品检定研究院,批号分别为110715-201619、111588-201701、111589-201705、110757-201607、110713-2016113、110795- 201710、110756-201512、110796-201621、110758- 201616);乙腈、醋酸铵为色谱纯;冰醋酸为分析纯;水为超纯水。
牛黄清胃丸共49 批,来源于18 个生产企业,覆盖山西、辽宁、吉林等 18 个省区,分别为A企业(3批,样品编号1~3,批号分别为:A17033、A16239、A17046),B企业(2批,样品编号4~5,批号分别为:17360701、17360401),C企业(3批,样品编号6~8,批号分别为:17013559、17013558、17013549),D企业(3批,样品编号9~11,批号分别为:17031009、111001、17041005),E企业(3批,样品编号12~14,批号分别为:1706153、1709126、1709130),F企业(3批,样品编号15~17,批号分别为:20161201、20170702、20170401),G企业(3批,样品编号18~20,批号分别为:170302、161205、170301),H企业(3批,样品编号21~23,批号分别为:1705021、1712033、1705026),I企业(3批,样品编号24~26,批号分别为:171002、170302、170301),J企业(3批,样品编号27~29,批号分别为:20170803、20170801、20170802),K企业(3批,样品编号30~32,批号分别为:111171212、11170329、11180208),L企业(3 批,样品编号33~35,批号分别为:117002、117003、118001),M企业(3 批,样品编号36~38,批号分别为:20151102、20170601、20170602),N企业(3批,样品编号39~41,批号分别为:170801、160703、170501),O企业(3批,样品编号42~44,批号分别为:170801、170301、170901),P企业(2批,样品编号45~46,批号分别为:20170901、20170201),Q企业(1批,样品编号47,批号:20170101),R企业(2批,样品编号48~49,批号分别为:20170701、20160602)。
2 方法与结果
2.1 对照品溶液制备
取柠檬黄、日落黄、亮黄、金橙Ⅱ、金胺O对照品适量,用甲醇溶解,制成每1 mL中约含100 μg的混合对照溶液,用0.45 μm微孔滤膜滤过,即得。
取大黄酸等9种对照品适量,用甲醇溶解,分别制成每1 mL中约含200 μg的对照溶液,用0.45 μm微孔滤膜滤过,即得。
2.2 供试品溶液制备
取牛黄清胃丸2丸,加硅藻土6 g粉碎,研细,精密称取9 g,加甲醇溶液30 mL,超声处理30 min,放冷,取续滤液,用0.45 μm微孔滤膜过滤,即得。
2.3 色谱条件
色谱柱:Phenomenon Luna C18(250 mm×4.6 mm,5 μm) 柱;流动相:乙腈 (A) 和0.05 mol·L-1醋酸铵(冰醋酸调pH 4.5)(B) 梯度洗脱[梯度程序I(化工染料检查):0~30 min,2%~70%A;30~40 min,70%~95%A;40~50 min,95%A;梯度程序Ⅱ(天然色素成分分析):0~35 min,15%~55%A;35~45 min,55%~95%A;45~50 min,95%A];流速:1 mL·min-1;柱温:40 ℃;检测波长:490 nm (I)、430 nm (Ⅱ);进样体积:10 μL。
2.4 结果
2.4.1HPLC检查5种黄色系化工染料
2.4.1.1样品检测 样品按2.2项下制备供试品溶液,按2.3项下色谱条件梯度洗脱程序I,进样测定,记录色谱图(图1)。49批牛黄清胃丸样品中均未检出与上述5种黄色系对照品保留时间一致的色谱峰。

注:A.混合对照(1.柠檬黄;2.日落黄;3.亮黄;4.金橙Ⅱ;5.金胺O);B.供试品。图1 混合对照品和供试品HPLC图(490 nm)
2.4.1.2检出限 取不同浓度对照试剂溶液,按2.3项下色谱条件梯度洗脱程序I进样。在490 nm检测波长下测定,以信噪比3∶1为检出限,结果见表1。

表1 5种化工染料对照试剂检测结果
2.4.2天然色素成分分析
2.4.2.1方法学考察 精密度试验:取同一供试品溶液(批号:A17033),按2.3项下色谱条件Ⅱ重复进样6次,记录色谱图。以盐酸小檗碱为参照峰,计算色谱图中特征峰的相对保留时间和相对峰面积。结果表明,各特征峰的相对保留时间和相对峰面积的RSD分别为0.04%~0.5%、0.3%~2.9%,表明仪器精密度良好。
重复性试验:取同一批次牛黄清胃丸(批号:A17033),按2.2项下方法制备6份供试品溶液,按2.3项下色谱条件Ⅱ进样测定,记录色谱图。以盐酸小檗碱为参照峰,计算色谱图中特征峰的相对保留时间和相对峰面积。结果表明各特征峰的相对保留时间和相对峰面积的RSD分别为0.04%~0.5%、0.3%~2.9%,表明方法重复性良好。
稳定性试验:取同一供试品溶液(批号:A17033),分别于0、6、12、18、24 h按2.3项下色谱条件Ⅱ进样测定,记录色谱图。以盐酸小檗碱为参照峰,计算色谱图中特征峰的相对保留时间和相对峰面积。结果表明各特征峰的相对保留时间和相对峰面积的RSD分别为0.03%~0.5%、0.4%~3.3%,表明供试品溶液在24 h内稳定。
2.4.2.2共有模式的建立与分析 取49 批牛黄清胃丸样品,按2.2项下方法制备供试品溶液,按2.3项下色谱条件梯度洗脱程序Ⅱ进样测定,记录色谱图,见图2。将结果导入Chem Pattern软件,以所有变量作为共有峰筛选条件,采用高斯曲线模拟的方法生成共有模式,包括14个共有峰,见图3。经与对照品、对照药材比对,鉴定其中9 个共有峰并明确其主要药材来源,见表2。
2.4.2.3统计学分析 相似度分析:利用Chem Pattern软件,以HPLC (430 nm) 指纹图谱共有模式为参照图谱,采用夹角余弦法计算各样品的相似度,见图4。所有49批样品与共有模式的相似度为0.68~0.99,其中C企业样品相似度高,均一性好;仅B企业样品相似度低于0.7,分析发现其样品部分色谱峰含量较其他企业样品存在一定差异。

图2 牛黄清胃丸样品天然色素HPLC指纹图谱(430 nm)

注:3.黄芩苷;4.西红花苷-I;5.西红花苷-Ⅱ;6.大黄酸;7.盐酸小檗碱;11.芦荟大黄素;12.大黄素;13.大黄酚;14.大黄素甲醚。图3 牛黄清胃丸天然色素指纹图谱共有模式(430 nm)
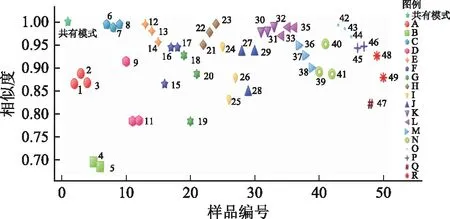
图4 牛黄清胃丸样品相似度
主成分分析:主成分分析(PCA)是根据实际需要从中抽取出几个来尽可能多地反映原来变量信息的一种多元统计分析方法。利用Chem Pattern软件将样品测定数据标准化后进行主成分分析,见图5。第一主成分(PC1) 的贡献率为40.28%,第二主成分(PC2) 的贡献率为25.21%,第三主成分(PC3) 的贡献率为18.27%,累计达到83.76%,说明其能较全面地反映样品间的差异。PCA散点图显示,不同企业生产样品基本可以各自聚为一类,其中B企业样品明显偏离其他样品。主成分载荷图给出各色谱峰在主成分中所占的比例,其中离X=0 轴距离越远的点对PC1的贡献越大,如西红花苷Ⅰ和大黄酚;而离Y=0轴距离越远的点对PC2的贡献越大,如大黄酚和西红花苷Ⅰ;而离Z=0轴距离越远的点对PC3的贡献越大,如西红花苷Ⅰ和盐酸小檗碱。以B和C企业为例,两者样品主要沿PC2、PC3得到分离,因而对PC2、PC3贡献大的成分是其主要差异性成分;因B位于PC2<0,PC3<0的位置,C位于PC3>0,PC3>0的位置,所以与PC2负相关、与PC3正相关的成分大黄酚在B样品中含量较高;与PC2、PC3均正相关的成分盐酸小檗碱在B样品中含量较低。

注:A.得分图;B.载荷图。图5 牛黄清胃丸样品PCA分析结果
3 讨论
3.1 提取方法考察
采用超声提取方式,分别考察不同提取溶剂(甲醇、80%甲醇-水)、提取时间(超声30、45、60 min)等条件,结果发现,提取时间影响不大,甲醇提取样品中天然色素成分信息丰富,基线分离情况良好。
3.2 色素成分分析
实验过程中发现,尽管所有样品在490 nm下均未检出5种黄色系化工染料,但在430 nm波长下可见色谱峰信息丰富,因此研究建立了这些天然色素成分指纹图谱,并进一步分析鉴定其中9个主要共有峰,结果表明,这些成分主要来源于处方中大黄、番泻叶、黄柏、黄芩和栀子等5味药材。此外,通过Chem pattern软件分析,49批样品与共有模式的相似度为0.68~0.99,其中仅B企业样品相似度低于0.7,分析发现其样品部分色谱峰含量较其他企业样品存在一定差异;主成分分析能够明确不同企业产品中差异较大的成分,其在一定程度上也反映了不同企业相关药材的质量及投料情况。此外,个别企业样品批间存在一定差异,分析表明因部分色谱峰含量不同所致。
3.3 结论
所有样品均未检出柠檬黄、日落黄、亮黄、金橙Ⅱ和金胺O这 5种黄色系化工染料。同时,研究建立的天然色素成分指纹图谱准确、可靠、简便,能够反映不同企业产品的质量,为更好地控制制剂质量提供了参考。

