颅内血管外周细胞瘤的特点及复发的影响因素分析
王传伟 宫杰 赵文国 范晓勇 刘志国 王建刚 刘玉光
血管外周细胞瘤(hemangiopericytoma,HPC)是一种较少见的间质性肿瘤,常发生于四肢、盆腔及腹膜后等部位,也可发生于中枢神经系统中,占颅内肿瘤总发病率的0.5%[1-5]。1942 年Stout 和Murray[2]首次为其命名,Begg 和Garret[3]于1954 年明确定义了该种肿瘤,之后陆续有散发及综合病例报道[4]。颅内HPC 归类于具有恶性倾向的肿瘤,但影像学上却有类似良性脑膜瘤的表现,与脑膜瘤在诊断上容易混淆。由于HPC 在诊断上容易与脑膜瘤相混淆,手术难度较大,预后较脑膜瘤差,神经外科医师需充分重视。随着病理技术及影像学的发展,2007 年世界卫生组织(World Health Organization,WHO)正式明确了HPC 的概念及其病理级别,并与脑膜瘤划清界限[4]。本文总结了本院近10 年收治的42 例HPC 患者的病例资料,分析其特点并研究其复发的影响因素,现报道如下。
资料与方法
一、研究对象
选取山东大学齐鲁医院神经外科自2008 年1 月至2018 年10 月经手术病理证实的颅内HPC 患者42例,其中男性18 例,女性24 例,年龄范围24~72 岁,平均46 岁。病程5 d~21 年。临床症状包括头痛22 例,视力模糊16 例,头晕9 例,恶心12 例,呕吐6 例,肢体乏力12 例,肢体或面部麻木7 例,癫痫4 例,耳鸣1 例,颈部肿胀1 例,月经停止1 例。体征包括视乳头水肿24 例,肌力下降10 例,感觉障碍9 例,病理征4 例,视神经萎缩5 例,听力下降1 例,走路不稳2 例。本研究符合2013 年修订的《赫尔辛基宣言》(www.wma.net/en/30publications/10policies/b3/index.htm)。
二、治疗方法
所有患者均接受外科手术,术前均采用CT 及MRI 检查,手术方式根据肿瘤部位不同而采取经额入路、经翼点入路、经枕入路、经乙状窦后入路、经矢状窦旁入路。部分患者术后接受放射治疗与化学治疗。采用电话及门诊进行随访,随访时间24~144 个月,患者均行脑CT 或MRI 检查。
三、病理检查
所有肿瘤标本均行HE 染色及免疫组化染色,指标包括但不限于Ki-67、CD34、CD31、Bcl-2、Vimentin、EMA、GFAP、S100。
四、资料收集
收集患者的临床资料包括性别、年龄、病程、肿瘤影像学特点(包括瘤周水肿、静脉窦受侵袭情况、肿瘤成分、肿瘤边界、肿瘤大小、肿瘤位置)、手术切除程度、Ki-67 指数、WHO 病理分级。
五、统计学分析
采用SPSS16.0 软件进行统计学分析,通过初步分析将各变量均转变为分类变量,利用Kaplanmeier 单因素生存分析和Cox 多因素回归分析判断相关因素对患者随访期内复发情况的影响。P<0.05为差异有统计学意义。
结果
一、影像学特点
本组患者经CT 及MRI 检查显示,肿瘤直径范围1.3~7.2 cm,34 例患者呈类球形,8 例患者呈分叶状。CT 信号可呈等密度、高密度、低密度,甚至不均一密度。MRI 上T1 像呈等信号或稍高信号,T2 像呈稍高信号或等信号(少数呈低信号),压水像呈稍高信号,强化像可呈均匀强化或不均匀强化,DWI 弥散加权像多数呈高信号,少部分呈等或低信号。32例肿瘤在影像学上有较清晰的边界,10 例肿瘤边界不清。囊性或囊实性肿瘤为8 例,实性肿瘤为34 例。瘤周水肿明显者32 例,不明显者10 例。肿瘤位置包括大脑凸面8 例,大脑镰旁10 例,矢状窦旁10 例,幕孔区2 例,中颅窝底4 例,镰幕交界处2 例,岩斜区2 例,鞍区及鞍旁4 例(图1)。
二、术后及随访结果
术后结果显示:肿瘤质地均较韧,主要分布于凸面、镰窦旁及颅底,手术入路根据肿瘤位置及与周边结构的关系等特点而定。手术时间2~13 h(平均4.5 h),术后住院时间为10~45 d(平均18 d),其中静脉窦受侵犯者18 例。42 例患者中,14 例患者接受全切除治疗,28 例患者接受非全切治疗。术后24 例患者肿瘤复发,其中2 例肺部转移,1 例骨转移。单纯颅内原位复发患者21 例,10 例选择于我科再次手术治疗,5 例选择肿瘤科治疗,3 例选择外院手术,3 例采取保守处理。3 例远处转移而复发的患者均未进一步治疗,其中2 例在随访时已死亡;1 例拒绝再次手术。
三、病理结果
免疫组化染色结果示:Ki-67 比值为1%~40%;CD34 阳性者39 例;Bcl-2 阳性者32 例;波形蛋白(Vimentin)阳 性者36 例;CD31、EMA、GFAP、S100均为阴性。免疫组化染色与HE 染色结果见图2。8例属于WHO Ⅲ级,34 例属于WHO Ⅱ级。

图1 3 种位置的HPC 的影像学图像

图2 血管外周细胞瘤的免疫组化及HE 染色图(200×)
四、肿瘤复发的相关因素分析
Kaplan-meier 单因素生存分析结果显示,肿瘤位置、肿瘤大小、肿瘤切除程度、Ki-67 指数是肿瘤复发的相关因素(表1)。结合临床经验,静脉窦受侵袭情况对肿瘤复发也有一定的影响。进一步将单因素分析中差异有统计学意义的因素与静脉窦受侵袭情况纳入Cox 多因素分析,结果显示肿瘤切除程度、静脉窦受侵袭情况是肿瘤复发的独立影响因素(表2)。
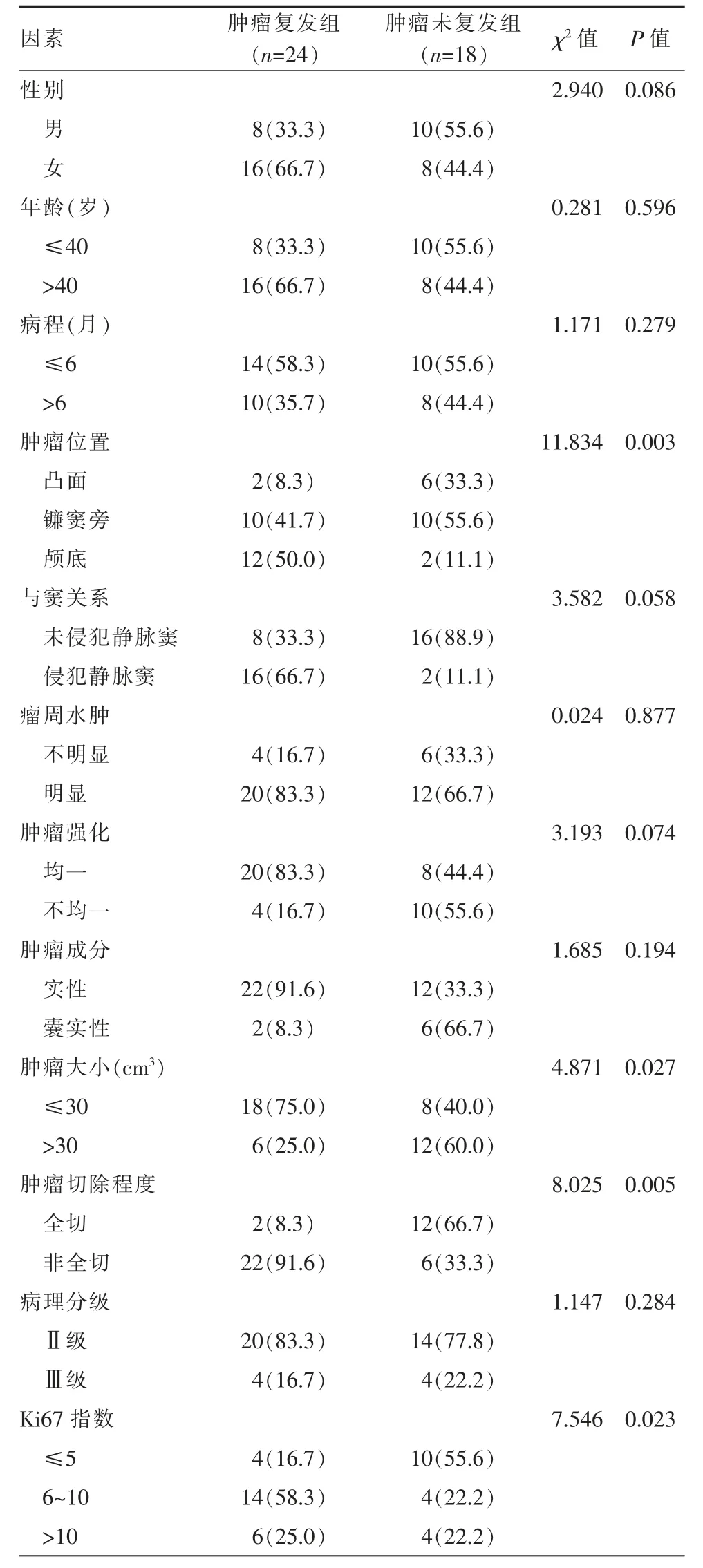
表1 血管外周细胞瘤患者复发的单因素分析
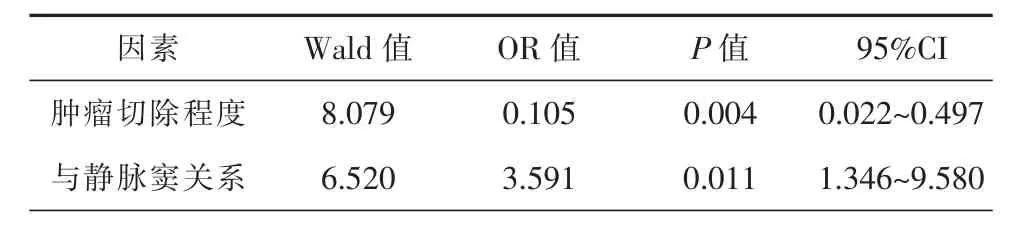
表2 影响血管外周细胞瘤患者复发的Cox 多因素分析
讨论
早在2007 年之前,HPC 被认为是脑膜瘤的一个亚类即血管母细胞性脑膜瘤,由于二者在病理学和生物学特性上有一定相似,有时也会与间变型脑膜瘤混淆[1-3]。随着免疫组化、分子病理等技术和影像学的发展以及临床经验的积累,HPC 的概念逐渐被正式认可,2007 年WHO 把中枢神经系统HPC 从脑膜瘤的诊断中彻底分离开来[4]。最新的2016 年WHO中枢神经系统肿瘤分类标准定义一类肿瘤,称为孤立性纤维性肿瘤/血管外皮细胞瘤[5]。
病理学是诊断HPC 的根本标准。CD34、reticulin、Bcl-2 及Vimentin 等 是HPC 的 代 表 性 指标[5]。本组HPC 组织中CD34、Bcl-2 及Vimentin 阳性率很高,而EMA、CD31、GFAP、S100 几乎均为阴性;与此对应,血管母细胞性脑膜瘤EMA 阳性率较高,而CD34、Bcl-2 等均阳性率较低,可资鉴别[5]。HPC的Ki-67 普遍较高,本组患者中24 例在5%以上,16例在10%以上(其中6 例为20%,2 例为30%,1 例为40%),说明本组病例肿瘤细胞的增殖活性十分高。随着分子病理学的发展,更深层的HPC 病理学特征被发现,如荧光原位杂交确认HPC 细胞中染色体12q13 存在倒置,基因NAB2 与STAT6 存在融合等[6-7]。病理学结果是金标准,直接决定预后并指导下一步治疗,然而如何在术前对手术难度及预后做出预判并指导临床,还需影像学及临床表现的总结。
本组病例中,临床症状主要是头痛、视力模糊、头晕恶心,多为肿瘤所致颅内高压引起,为非特异性症状,而且症状本身还依赖于肿瘤发生部位。笔者认为病程的长短对诊断有一定的参考意义:本组患者中有24 例病程≤6 个月,其中20 例病程更短,在3个月以内。阳性率最高的体征为视乳头水肿(24例);而20 例病程最短(3 个月内)的患者中,14 例体检发现明显的视乳头水肿,可见HPC 在短时间内可以迅速引起瘤周水肿和颅内压增高,说明HPC 进展相对较快。HPC 也有局灶性体征如一侧肌力下降、感觉障碍等。而脑膜瘤一般进展较慢,病程多在数年至数十年不等,尚有相当一部分脑膜瘤为外伤检查或健康体检时发现,有些甚至终身变化不大。
笔者研究认为,HPC 具有以下特点:CT 上多表现为稍高密度占位性病变,但钙化少见,部分瘤周水肿明显,基底多位于硬脑膜;肿瘤强化明显;MRI上可见肿瘤呈T1WI 等或稍高信号,T2WI 稍高或混杂信号,T1WI 增强扫描往往强化非常明显,不均匀强化、混杂信号、囊性改变、形状不规则较脑膜瘤多见,瘤内常有更多的血管流空影,皮质扣压征可见,脑膜尾征少见。除上述基本特点外,CT 灌注成像(computed tomography perfusion,CTP)、磁共振波谱成像(magnetic resonance spectroscopy,MRS)和弥散加权成像(diffusion weighted imaging,DWI)在某种程度上可资与脑膜瘤鉴别。Righi 等[8]报道,与脑膜瘤相比,MRS 显示HPC 中胆固醇、肌醇、葡萄糖和谷胱甘肽含量相对高,而肌酸、谷氨酰胺、丙氨酸、甘氨酸和乙酰胆碱含量相对低甚至缺如。Shuang 等[9]报道CTP 上显示HPC 实质中的脑血容量比较高。Liu等[10]与邝欢等[11]发现DWI 中ADC 值对于鉴别诊断有一定意义,HPC 的ADC 值明显高于间变型脑膜瘤。本研究显示14 例HPC 在DWI 上呈低信号,16例呈混杂信号,8 例呈略高信号,4 例呈等信号。混杂信号及不均匀强化可能的原因为肿瘤生长过快、瘤内出血或肿瘤本身成分所致。
本研究对影响肿瘤复发的单因素分析结果显示,肿瘤位置、肿瘤大小、肿瘤切除程度、Ki-67 指数、静脉窦受侵袭情况与肿瘤的复发具有相关性,进一步多因素分析认为肿瘤切除程度、静脉窦受侵袭情况是肿瘤复发的独立影响因素。本组病例中,肿瘤全切除14 例,其中2 例在随访期间复发;未全切除28 例,22 例复发。究其原因可能为仅切除肿瘤而对附着的硬脑膜或骨质不作处理,或仅电灼附近基底而不做彻底切除,对于HPC 这种高增殖性高侵袭性的肿瘤是不可靠的,笔者建议在不带来较大风险及伤害的情况下尽可能“激进切除”,彻底去除肿瘤及周边硬脑膜及骨质,甚至瘤周黏连的少部分脑组织,将明显降低HPC 的复发率。位于功能区或位置深在的HPC 需谨慎,需注意保护血管及脑组织,原则上尽可能保护蛛网膜,而实际上常见肿瘤边界黏连明显,无法像脑膜瘤一样较容易地分离蛛网膜。笔者观点与国际上一些学者的“根治性切除”(radical resection)治疗HPC 的理念一致,有些学者称之为“Simpson 0 级切除”[12-13]。肿瘤位置是影响HPC 复发的因素之一,位于凸面的或未侵袭静脉窦的HPC 更易获得彻底切除,而位于颅底如岩斜区或侵犯颅底较严重的肿瘤往往难以全切,更容易导致复发。静脉窦受侵袭情况虽在本次单因素分析时统计学差异不明显,但结合临床情况考虑,侵袭静脉窦的HPC 难以真正全切,因此容易复发,实际上也与切除程度和肿瘤位置有关系。Ki-67 指数≤5 的患者复发率明显低于6~10 及>10 的患者,因为Ki-67 指数较大者增殖旺盛、恶性度相对较高,少量肿瘤细胞残余就可能引起快速复发,以往文献也强调了HPC 中Ki-67 在判断复发的重要性[14]。对于放射治疗、化学治疗是否可以显著降低HPC 复发率并改善预后,目前有研究认为术后辅助放射治疗对于减少复发有明显作用,也有研究显示放射治疗对于术后及复发性HPC 无明显帮助[12-17]。本研究术后仅部分患者遵医嘱接受放射治疗与化学治疗,考虑到统计学对数据的要求,应本组未把放射治疗和化学治疗列入讨论因素,但结合笔者经验及以往文献,应支持术后积极采用放射治疗与化学治疗。
综上所述,手术是治疗HPC 的首选措施,肿瘤切除程度、静脉窦受侵袭情况是肿瘤复发的独立影响因素,因此争取首次手术做到完全切除对于降低复发率至关重要。
利益冲突所有作者均声明不存在利益冲突

