HPLC波长切换法同时测定黄芩-甘草药对中9种成分含量
彭勍,孟硕,苗兰,林力,刘光宇,张鹏,刘建勋
HPLC波长切换法同时测定黄芩-甘草药对中9种成分含量
彭勍,孟硕,苗兰,林力,刘光宇,张鹏,刘建勋
中国中医科学院西苑医院基础医学研究所,中药药理北京市重点实验室,国家中澳中医药国际联合研究中心,北京 100091
建立HPLC同时测定黄芩-甘草药对中芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素含量的方法,探讨黄芩-甘草配伍前后这9种主要成分含量变化规律。采用Phenomenex Synergi Polar-RP 80A色谱柱(4.6 mm×250 mm,4 μm),流动相为乙腈-0.1%磷酸,流速1.0 mL/min,柱温35 ℃,通过梯度洗脱和多波长切换技术,测定黄芩-甘草药对配伍前后9种主要成分的含量。芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素的线性范围分别为0.032 5~1.040 0 μg(=0.999 9)、0.050 9~1.630 0 μg(=0.999 9)、0.007 8~0.248 0 μg(=0.999 9)、0.436 9~13.980 0 μg(=0.999 8)、0.040 3~1.290 0 μg(=0.999 9)、0.078 4~2.510 0 μg(=0.999 9)、0.025 4~0.812 0 μg(=0.999 9)、0.085 6~2.740 0 μg(=0.999 7)、0.004 3~0.139 0 μg(=0.999 7)。黄芩和甘草配伍后,芹糖甘草苷含量升高(<0.01),甘草苷含量降低(<0.01),其他成分含量无明显变化。本研究建立的方法稳定、准确,可为黄芩-甘草药对及其制剂的质量评价和控制提供依据;黄芩-甘草配伍后部分成分含量发生变化。
黄芩;甘草;含量测定;高效液相色谱法;波长切换
药对是在中医理论指导下,临床相对固定的2味中药配伍,具有协同增效或配伍减毒作用,为中医药发展过程中的特色产物之一[1]。黄芩味苦,性寒,功效清热燥湿、泻火解毒[2]301;甘草味甘,性平,功效补脾益气、清热解毒、祛痰止咳、缓急止痛、调和诸药[2]86。黄芩-甘草是常用配伍药对,见于小柴胡片、芩连片等多种制剂中,多发挥清热解毒作用。本课题组根据临床经验方,研发了具有宣肺平喘、祛风止咳、清热化痰功效的麻荆颗粒,主要用于外寒内热证的感冒后咳嗽、急性支气管炎、慢性支气管炎发作期等,由麻黄、黄芩、甘草、牡荆油组成,其中黄芩与甘草为1∶1配伍[3]。目前,针对黄芩-甘草药对的配伍研究较少,对于黄芩和甘草配伍后主要化学成分的含量变化尚未见报道。因此,本试验建立HPLC多波长切换法同时测定黄芩-甘草药对中芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素9种成分含量的方法,比较黄芩和甘草配伍前后主要成分的含量变化,为中药复方配伍机制及黄芩-甘草药对的临床合理应用提供依据和参考。
1 仪器与试药
Agilent1200型高效液相色谱仪(美国安捷伦公司),MS205DU型十万分之一电子分析天平(瑞士梅特勒-托利多公司),KH-300E型超声波清洗器(昆山市超声仪器有限公司)。
对照品黄芩苷、甘草苷(中国食品药品检定研究院,批号分别为110715-201720、111610-201005,纯度均大于98%),芹糖甘草苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷(成都曼斯特生物科技有限公司,批号分别为MUST-18112701、MUST-19030102,纯度均大于98%),异甘草苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素(上海诗丹德生标准技术服务有限公司,批号分别为6387、5014、5699、5559、5325,纯度分别为99%、99%、98%、96%、98%)。乙腈(色谱纯,Fisher公司),磷酸(色谱纯,Fisher公司),其他试剂均为分析纯,水为娃哈哈纯净水(杭州娃哈哈有限公司)。
3批黄芩(产地河北,批号1606011、1704012、1805011,编号为黄芩1、2、3)、3批甘草(产地新疆,批号1606012、1704011、1805022,编号为甘草1、2、3),购于河北百草康神药业有限公司,经中国中医科学院中药研究所生药标本室何希荣药师鉴定,分别为唇形科植物黄芩Georgi的干燥根和豆科植物甘草Fisch.的干燥根和根茎,品种、性状均符合2015年版《中华人民共和国药典》(一部)的有关规定,标本存于本实验室。
2 方法与结果
2.1 色谱条件
色谱柱为Phenomenex Synergi Polar-RP 80A柱(4.6 mm×250 mm,4 μm),流动相为乙腈-0.1%磷酸水溶液,流速1.0 mL/min,柱温35 ℃,梯度洗脱程序见表1,波长切换(0 min,276 nm;30 min,360 nm;34 min,280 nm;45 min,352 nm;49 min,275 nm;62 min,237 nm;66 min,274 nm),进样量10 μL。在此色谱条件下,各成分均达到基线分离,理论塔板数均大于6000。
表1 流动相梯度洗脱程序(%)
时间乙腈0.1%磷酸水溶液 0 min1882 19 min1981 20 min2377 34 min2377 35 min2575 50 min2773 75 min5545
2.2 溶液制备
2.2.1 混合对照品溶液
分别取芹糖甘草苷、甘草苷、异甘草苷和甘草酸对照品适量,精密称定,加70%甲醇,配制成浓度分别为1.040、1.630、0.248、2.740 mg/mL的对照品贮备液;分别取黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素和汉黄芩素对照品适量,精密称定,加甲醇配制成浓度分别为13.980、1.290、2.510、0.812、0.139 mg/mL的对照品贮备液。精密吸取各对照品贮备液适量,置10 mL棕色容量瓶中,甲醇定容至刻度,摇匀,得每1 mL含芹糖甘草苷104.0 μg、甘草苷163.0 μg、异甘草苷24.8 μg、黄芩苷1398.0 μg、千层纸素A-7-O-β-D-葡萄糖醛酸苷129.0 μg、汉黄芩苷251.0 μg、黄芩素81.2 μg、甘草酸274.0 μg和汉黄芩素13.9 μg的混合对照品溶液。
2.2.2 供试品溶液及单味药对照溶液
取黄芩、甘草粉末(过3号筛)各0.1 g,精密称定,置具塞锥形瓶中,精密加入70%乙醇25 mL,称定质量,超声提取(功率300 W,频率40 kHz)30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,静置,0.45 μm微孔滤膜过滤,取续滤液,即得供试品溶液。取黄芩样品粉末(过3号筛)0.1 g,精密称定,按上法制备,即得黄芩对照溶液。取甘草粉末(过3号筛)0.1 g,精密称定,按上法制备,即得甘草对照溶液。
2.3 方法学考察
2.3.1 专属性试验
取混合对照品溶液、供试品溶液、黄芩对照溶液和甘草对照溶液,按“2.1”项下色谱条件测定,色谱图见图1。在供试品溶液色谱图中,与混合对照品色谱图的芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素相应色谱峰位置上均有相同保留时间的色谱峰,而黄芩对照溶液中不含芹糖甘草苷、甘草苷、异甘草苷和甘草酸的色谱峰,甘草对照溶液中不含黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素和汉黄芩素的色谱峰,表明黄芩和甘草中的特征成分在此测定方法下不相互干扰。
2.3.2 线性关系考察
取“2.2.1”项下混合对照品溶液,逐级等倍稀释,得6个浓度的混合对照品溶液,按上述色谱条件分别测定,以各成分浓度(μg/mL)为横坐标,以峰面积为纵坐标,计算回归方程,结果见表2。芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素在各自的线性范围内均有良好的线性关系。
2.3.3 精密度试验
精密吸取同一混合对照品溶液,按“2.1”项下色谱条件,连续进样6次,记录峰面积,结果芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素的峰面积RSD分别为1.19%、0.65%、0.14%、0.10%、0.04%、0.03%、0.10%、0.11%和0.14%,表明仪器精密度良好。
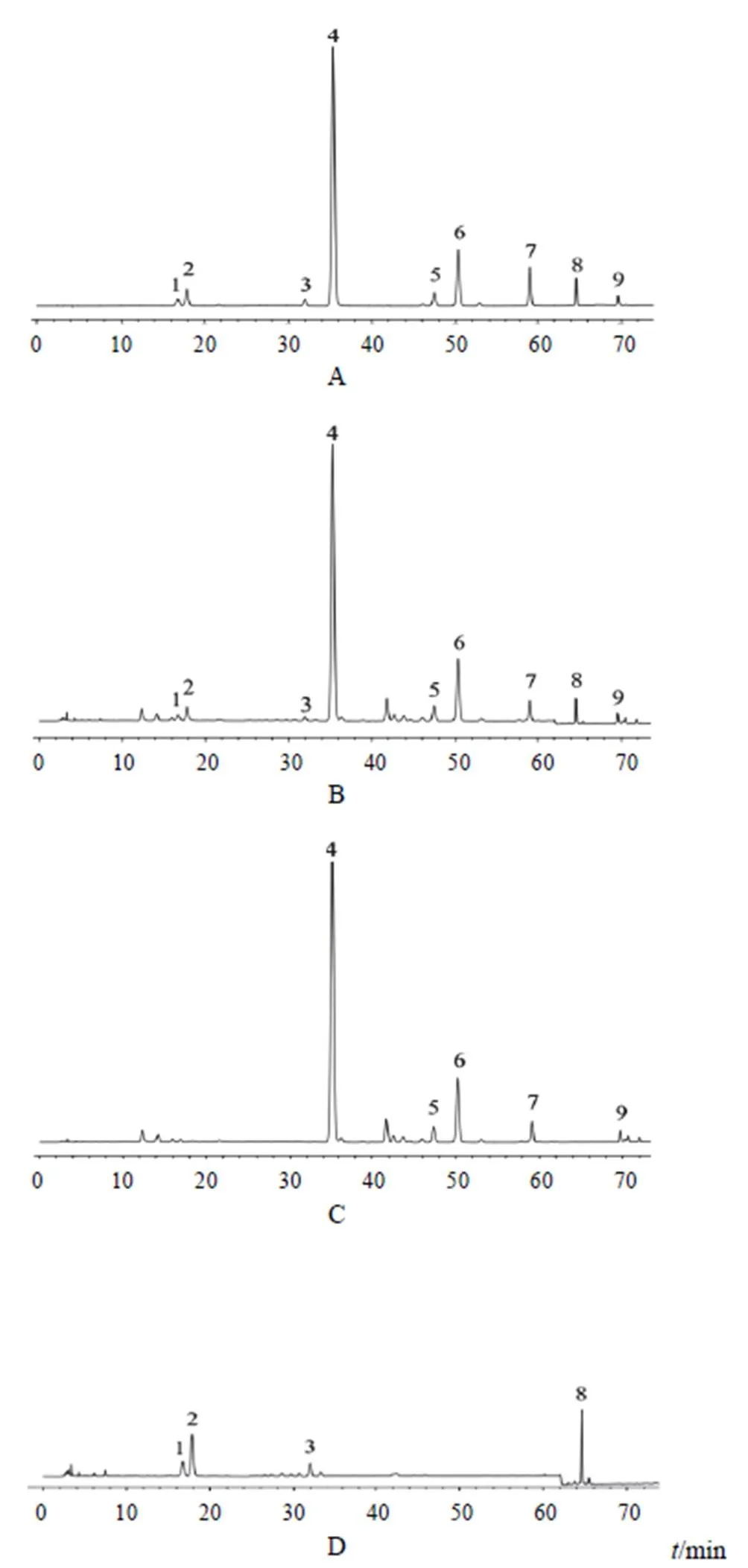
注:A.混合对照品;B.供试品;C.黄芩对照;D.甘草对照;1.芹糖甘草苷;2.甘草苷;3.异甘草苷;4.黄芩苷;5.千层纸素A-7-O-β-D-葡萄糖醛酸苷;6.汉黄芩苷;7.黄芩素;8.甘草酸;9.汉黄芩素
表2 9种成分线性关系考察结果
成分回归方程相关系数线性范围/μg 芹糖甘草苷Y=11.23X+5.8330.999 90.032 5~1.040 0 甘草苷Y=16.42X+17.990.999 90.050 9~1.630 0 异甘草苷Y=39.34X+7.1300.999 90.007 8~0.248 0 黄芩苷Y=30.16X+391.90.999 80.436 9~13.980 0 汉黄芩苷Y=38.06X+78.220.999 90.078 4~2.510 0 黄芩素Y=60.18X+29.710.999 90.025 4~0.812 0 甘草酸Y=5.999X+26.070.999 70.856 3~2.740 0 汉黄芩素Y=56.20X+9.6920.999 70.004 3~0.139 0 千层纸素A-7-O-β-D-葡萄糖醛酸苷Y=16.34X+17.960.999 90.040 3~1.290 0
2.3.4 稳定性试验
精密吸取同一供试品溶液,按“2.1”项下色谱条件,分别于0、2、4、6、8、12、24 h进样测定各成分峰面积值,结果供试品溶液中芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素的峰面积RSD分别为1.46%、1.55%、2.51%、0.08%、0.47%、0.28%、0.62%、0.13%和0.41%,表明供试品溶液在24 h内稳定。
2.3.5 重复性试验
精密称取同一批次黄芩(批号1805011)、甘草(批号1805022)粉末各6份,每份0.1 g,按“2.2.2”项下方法制备,按“2.1”项下色谱条件进行测定,经计算,样品中芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素的平均含量为8.724、10.01、1.560、140.6、14.59、27.29、3.630、22.95、1.407 mg/g,RSD分别为0.52%、2.48%、1.24%、1.23%、0.63%、0.75%、1.26%、0.62%和1.21%,表明该方法重复性良好。
2.3.6 加样回收率试验
取已知含量的同一批次黄芩(批号1805011)甘草(批号1805022)粉末6份,每份0.1 g,精密称定,分别精密加入与样品中各成分等量的对照品溶液,按“2.1”项下色谱条件进样测定,计算加样回收率及RSD。结果芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素的平均回收率分别为99.3%、101.3%、101.7%、101.7%、102.7%、103.1%、102.5%、98.9%和102.2%,RSD分别为2.89%、2.09%、2.18%、2.66%、2.72%、1.08%、2.75%、1.28%和1.31%,表明方法的准确度良好。
2.4 样品含量测定
取3批黄芩、甘草样品,按“2.1”项下色谱条件进行测定,并计算各样品中芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素的含量,见表3。应用检验对黄芩、甘草配伍前后上述9种成分的含量进行分析,结果显示芹糖甘草苷含量升高(<0.01),甘草苷含量降低(<0.01),其他成分含量无明显变化。
表3 3批黄芩、甘草样品配伍前后9种成分含量测定结果(mg/mL)
成分 1 2 3 黄芩甘草黄芩-甘草 黄芩甘草黄芩-甘草 黄芩甘草黄芩-甘草 芹糖甘草苷-0.031 80.039 6 -0.017 60.023 7 -0.027 50.034 6 甘草苷-0.069 50.065 2 -0.049 70.047 9 -0.048 50.040 0 异甘草苷-0.011 90.011 2 -0.005 50.005 2 -0.006 40.006 4 黄芩苷0.596 7-0.530 6 0.544 0-0.522 3 0.565 8-0.557 4 千层纸素 A-7-O-β-D-葡萄糖醛酸苷0.065 2-0.052 2 0.045 6-0.042 2 0.058 6-0.057 5 汉黄芩苷0.115 0-0.094 2 0.109 8-0.105 8 0.109 5-0.108 2 黄芩素0.014 8-0.012 7 0.015 2-0.015 4 0.014 1-0.014 3 甘草酸-0.103 60.103 7 -0.061 80.064 3 -0.092 70.091 5 汉黄芩素0.005 2-0.004 9 0.007 4-0.006 9 0.004 8-0.005 5
注:“-”为未检出
3 讨论
现代研究表明,黄芩具有抗菌、抗炎、抗病毒及抗癌等药理作用,黄酮类成分是其主要的药效活性成分[4]。黄芩苷是其中含量最高的黄酮类活性成分,在黄芩根部含量为10.11%[5]。黄芩苷、汉黄芩苷、黄芩素、汉黄芩素是黄芩的特征成分,是黄芩及其制剂的主要质量控制指标性成分[6]。甘草具有抗炎、抗肿瘤、抗氧化、降糖降压的作用,主要含有黄酮类、皂苷类和多糖类化合物[7-8]。甘草酸是甘草中含量最高的三萜皂苷类成分,占总三萜皂苷类化合物的2%以上,具有抗过敏、抗炎、保护肝脏的作用[9]。黄酮类成分在甘草中的含量仅次于三萜皂苷类成分,甘草苷和异甘草苷为其中含量较高的代表性成分。结合实际测定结果与对照品获得的难易程度,本研究最终确定以芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素9种成分作为指标性成分进行测定。
为保证提取效率,同时参考药典和文献[10-11]的提取方法,本试验应用单因素考察法比较了不同提取溶剂(30%、50%、70%乙醇,纯甲醇)、不同料液比(50、100、200、250倍),以及不同提取时间(30、45、50 min)对9种指标成分含量的影响,最终确定了提取方法。
本试验分别考察了甲醇-水、乙腈-水、乙腈-0.1%乙酸水溶液和乙腈-0.1%磷酸水溶液不同流动相系统,以各色谱峰的峰形和分离度为指标进行比较,结果发现,以乙腈-0.1%磷酸水溶液为流动相时,各色谱峰分离度和峰形良好,且基线平稳。经全波长扫描分析,芹糖甘草苷、甘草苷、异甘草苷、黄芩苷、千层纸素A-7-O-β-D-葡萄糖醛酸苷、汉黄芩苷、黄芩素、甘草酸和汉黄芩素的最大吸收波长分别为254、276、360、280、325、275、280、237、274 nm,由此确定了波长切换程序,确保每个成分均在其最大吸收波长测定,检测灵敏度更高。在色谱柱的选择上,考察了Phenomenex Synergi Polar-RP 80A(4.6 mm×250 mm,4 μm)和Agilent Eclipse XDB-C18(4.6 mm×250 mm,5 μm),发现前者各色谱峰分离度优于后者,且峰形更美观,故选用前者。
本试验通过波长切换技术,建立了HPLC同时测定黄芩-甘草药对中9种主要成分含量的方法。结果显示,黄芩-甘草配伍后,芹糖甘草苷含量有所增加,甘草苷含量有所降低,对黄芩的主要成分没有影响。推测黄芩和甘草配伍可能增加了芹糖甘草苷的溶出,而甘草苷减少可能由于提取过程中发生结构转化,或是与黄芩中的某些化学成分相互结合,具体机制有待进一步研究。本方法稳定准确,可为黄芩-甘草药对的内在质量评价提供参考,也可为含黄芩-甘草药对的中药制剂质量评价和控制提供依据。
[1] 魏佳明,朱俊平,刘瑞连,等.古代经典名方中的药对运用思维探讨[J].天津中医药,2019,36(7):659-661.
[2] 国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2015.
[3] 孟硕.麻荆颗粒制备工艺与质量标准研究[D].北京:中国中医科学院, 2016.
[4] 王慧,周红潮,张旭,等.黄芩苷药理作用研究进展[J].时珍国医国药, 2019,30(4):955-958.
[5] WEI F, WANG X, ZHANG X Y. Application of graphene oxide as a catalyst to accelerate extraction of total flavonoids and the hydrolysis of baicalin from Radix Scutellari[J]. Separation Purification Technology,2014,133:421-428.
[6] 付国辉,马香芹.黄芩的化学成分及药理作用研究进展[J].中国当代医药,2015,22(22):18-20.
[7] 邢国秀,李楠,王童,等.甘草中黄酮类化学成分的研究进展[J].中国中药杂志,2003,28(7):593-597.
[8] ZHANG Q, YE M. Chemical analysis of the Chinese herbal medicine Gan-Cao (licorice)[J]. Journal of Chromatography A,2009,1216(11):1954-1969.
[9] 张耀峰.甘草及其活性成分的药理活性研究进展[J].中医临床研究, 2019,11(9):141-142.
[10] 卫昊,郭玲玲,李柳柳,等.不同海拔和光照对黄芩中7种黄酮类有效成分含量的影响[J].中草药,2019,50(6):1472-1476.
[11] 刘香南,李明珠,尚晓娜,等.“一测多评”法测定甘草中6种有效成分含量[J].中国实验方剂学杂志,2013,19(24):56-59.
Simultaneous Determination of Nine Components in Scutellariae Radix-Glycyrrhizae Radix et Rhizoma Pair by HPLC Wavelength Switching Method
PENG Qing, MENG Shuo, MIAO Lan, LIN Li, LIU Guangyu, ZHANG Peng, LIU Jianxun
To establish an HPLC method for simultaneous determination of liquiritin apioside, liquiritin, isoliquiritin, baicalin, papylamine A-7-O-β-D-glucuronide, wogonoside, baicalein, glycyrrhizic acid and wogonin in Scutellariae Radix - Glycyrrhizae Radix et Rhizoma pair; To study the law of content changes of the 9 components after compatibility.The separation was performed on Phenomenex Synergi Polar-RP 80A (4.6 mm × 250 mm, 4 μm) with mobile phase composed of acetonitrile- 0.1% phosphoric acid solution for gradient elution and with switching detection wavelength at the flow rate of 1.0 mL/min; the column temperature was controlled at 35 ℃, so as to determine the contents of main 9 components in Scutellariae Radix - Glycyrrhizae Radix et Rhizoma pair before and after compatibility.The linear ranges of liquiritin apioside, liquiritin, isoliquiritin, baicalin, papylamine A-7-O-β-D-glucuronide, wogonoside, baicalein, glycyrrhizic acid and wogonin were 0.032 5‒ 1.040 0 μg (=0.999 9), 0.050 9‒1.630 0 μg (=0.999 9), 0.007 8‒0.248 0 μg (=0.999 9), 0.436 9‒13.980 0 μg (=0.999 8), 0.040 3‒1.290 0 μg (=0.999 9), 0.078 4‒2.510 0 μg (=0.999 9), 0.025 4‒0.812 0 μg (=0.999 9), 0.085 6‒ 2.740 0 μg (=0.999 7), 0.004 3‒0.139 0 μg (=0.999 7), respectively. After the compatibility, the content of liquiritin apioside increased (<0.01), and the content of liquiritin decreased (<0.01), while there was no significant change in the contents of other components.This method is stable and accurate, and can provide scientific basis for the quality evaluation and control of Scutellariae Radix - Glycyrrhizae Radix et Rhizoma pair and its preparations. The contents of some components changed in Scutellariae Radix - Glycyrrhizae Radix et Rhizoma pair after compatibility.
Scutellariae Radix; Glycyrrhizae Radix et Rhizoma; content determination; HPLC; wavelength switching

R284.1
A
1005-5304(2020)05-0065-05
10.3969/j.issn.1005-5304.201908413
北京市科技计划“十病十药”研发专项(Z171100001717007);国家自然科学基金面上项目(81872992);中国中医科学院基本科研业务费自主选题项目(ZZ11-068)
刘建勋,E-mail:liujx0324@sina.com
(2019-08-26)
(2019-09-23;编辑:陈静)

