总前列腺特异性抗原荧光免疫层析定量检测试剂的研究及应用
朱利国,刘 云,陈永伟,施龙顺,孙 萍,吴 国
(1.江苏省原子医学研究所附属江原医院,江苏 无锡 214063;2.江苏省原子医学研究所,江苏 无锡 214063;3.国药东风总医院,湖北 十堰 442000)
前列腺疾病是我国中老年男性泌尿系统中的一种常见疾病。目前,我国已经步入老龄化,前列腺疾病不仅在中老年中高发多见,而且有年轻化趋向。在临床上前列腺特异性抗原(tPSA)常常被用作早期发现、早期筛查前列腺癌的重要指标[1-2]。目前常见的tPSA方法学检测主要有ELISA、化学发光免疫分析(CLIA)、电化学发光免疫分析(ECLIA)、时间分辨荧光免疫分析(TRFIA)等。这几种方法都存在操作步骤繁琐且反应时间较长的共性问题,我们研发的tPSA荧光免疫层析定量检测方法,可以有效地缩短样本检测时间[3-4],以便更好地为临床服务。
1 材料与方法
1.1 研究对象 收集2018年1月—2019年5月于江苏省江原医院门诊、住院就诊患者和体检中心体检人群90 名,年龄38~83 岁,均为男性,晨起空腹抽取3 mL血液,分离血清后备用。
1.2 试剂与仪器 标记两株不同点位的抗tPSA抗体L1、检测抗体C1、质控抗体Q1(羊抗鼠IgG)、荧光微球、tPSA标准品、AFP标准品均来自无锡市江原实业技贸公司;ECLIA tPSA试剂盒、tPSA质控品均为罗氏公司产品;CA199标准品,为达安公司产品;硝酸纤维素膜来自美国Merck-Millipore公司;样品垫、聚酯膜、底板、吸水纸采购于上海杰一公司;其他试剂为国产分析纯;HG-98免疫荧光检测仪为上海互帼公司产品。
1.3 制备方法
1.3.1 抗体标记荧光微球:使用pH 7.2~7.6的MES活化缓冲液洗涤荧光微球,加入碳二亚胺(EDC)和N-羟基琥珀酰亚胺(NHS),室温反应20~30 min,洗涤荧光微球,用0.05 mol/L pH 7.2~7.6的磷酸盐缓冲液复溶后加入标记抗体L1,室温反应2 h,加入含有10% BSA的0.05 mol/L pH 7.2~7.6的磷酸盐缓冲液,室温反应30 min,洗涤荧光微球,用含有1% BSA,0.1% Tween-20,0.05 mol/L pH 7.2~7.6的磷酸盐缓冲液复溶至原体积,定量喷涂于聚酯膜上,避光35 ℃~38 ℃烘干1 h,加入干燥剂封存备用。
1.3.2 荧光免疫层析试纸条组装部件处理:(1)样品垫的处理:使用含1%BSA、0.1%Triton100的0.02 mol/L pH 7.4的磷酸盐缓冲液浸泡样品烘干。(2)包被膜的制备:使用含1%蔗糖的0.02 mol/L pH 7.4的磷酸盐缓冲液,分别将检测抗体C1和质控抗体Q1稀释到1 mg/mL,将二者以0.5 cm的间隔喷于硝酸纤维素膜上,烘干后加入干燥剂封存备用。
1.3.3 荧光免疫层析试纸条的组装:在湿度小于35%,稳定20 ℃~25 ℃的环境下,在PVC底板上黏贴上包被膜、结合了荧光微球标记的结合垫、样品垫和吸水纸形成微滤体系,切割成0.3 cm宽,装入卡壳中即制成试纸条(图1)。
1.4 检测方法 用加样器将20 μL血清标本或标准参考品加入测试卡加样孔中,同时加入50 μL样品稀释液,加样孔朝外放入孵育器中。连接电源,打开检测主机,膜层析反应15 min,运行仪器,仪器通过相应的分析软件自动计算出待测样本中的tPSA浓度。
标准曲线的绘制:将tPSA标准品制成6个不同的浓度,分别为0、2、4、10、50、100 ng/mL,每个浓度做5个平行样。膜层析反应15 min后,仪器读取T、C线信号。
与ECLIA检测试剂盒比较:按ECLIA试剂盒要求将90份血清标本与免疫层析法同时进行平行检测。
1.5 统计学处理 应用SPSS 12.0统计软件对数据进行分析。
2 结果
2.1 检测结果判读 检测时,液体在层析作用下前移动,若血清标本中tPSA的含量过少,试样中的tPSA与结合垫上标记抗体L1结合的荧光微球结合形成复合物C1则相应较少,结合垫中的标记抗体L1与C线上的质控抗体Q1大量结合,因此T线将比C线荧光值低很多,结果为阴性;若试样中tPSA的浓度较大,则复合物C1相应较多,与T线处的检测抗体C1结合并大量形成抗体-抗原-抗体复合物C2,而且试样中tPSA越高, T线荧光值越高,结果为阳性。无论是阳性还是阴性结果,因鼠源性抗体标记的荧光微球过量包被,因而总有未结合检测抗体C1的部分荧光微球与C线处的羊抗鼠IgG结合,在C线处出现荧光微球的聚集。如果C线没有出现荧光计数,无论T线有无荧光条带,结果均无效(图1)。
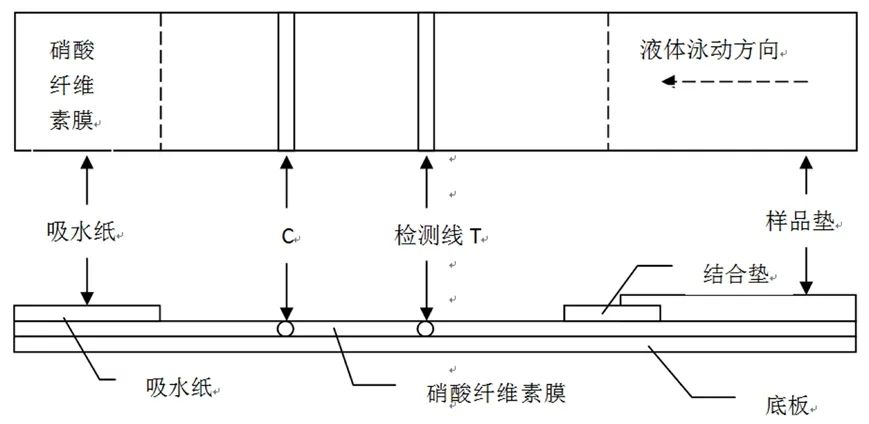
图1 tPSA荧光免疫层析检测试纸结构图
2.2 标准曲线绘制 按照统计学方法,以检测样品荧光值信号为纵坐标,tPSA标准品浓度为横坐标,建立方程并拟合成标准曲线(图2)。该标准曲线的R2为0.9779,线性较好,符合定量检测的要求。

图2 tPSA荧光免疫层析试纸条标准曲线
2.3 tPSA免疫层析荧光试纸条性能评价 (1)灵敏度:重复测定零剂量点(20 次),以±2s的荧光值在标准曲线上得到的相应值为检测低限,相对应的检测灵敏度平均值为0.02 ng/mL。(2)稳定性和精密度:免疫层析荧光试纸条法检测tPSA高、低两个质控品浓度(39.6 ng/mL,4.26 ng/mL)的批内和批间CV(n=10)。结果显示,批内CV为3.86%、4.68%,平均批内CV为4.27%,批间CV为6.22%、7.5%,平均批间CV为6.86%,均低于10%,表明免疫层析荧光试纸条法检测tPSA精密度良好。同一批试剂4 ℃放置6 个月后,荧光计数无明显变化(P>0.05),说明该方法稳定性较好。(3)准确度:用10 ng/mL的标准品分别加入到含量为1.980、4.58、15.66 ng/mL的血清中进行回收试验,回收率分别为105.2%、101.3%、98.1%;平均回收率为101.5%。(4)特异性:将1 000 U/mL的AFP、500 ng/mL的CEA高浓度标准品作为样品,用tPSA免疫荧光层析试纸条进行检测,各浓度点测定值分别为1.82 ng/mL、1.02ng/mL,说明两者无交叉反应,方法特异性好。
2.4 与ECLIA方法的比较 按ECLIA试剂盒要求将90 份血清标本与免疫层析法同时进行平行检测并对所有检测数据进行分析。结果表明,免疫层析试纸条与ECLIA试剂盒的相关系数为R2=0.9945(图3),平均相对偏倚为18.39%,两种方法高度相关;ECLIA试剂盒CUT-off值为4.0 ng/mL,其中ECLIA试剂盒检测出的阳性血清标本采用荧光免疫层析试纸检测均为阳性。

图3 荧光免疫检测试纸条-ECLIA试剂盒相关性
3 讨论
tPSA是一种蛋白酶[5],主要由前列腺腺泡、导管细胞分泌,具有提高精子活力和液化精液的效果。由于屏障隔离的原因,正常情况下tPSA在血液中含量极少,但当前列腺发生病变时可引起血液中tPSA含量增高,所以tPSA可作为一种有效标志物。tPSA具有前列腺器官的特异性,但tPSA非前列腺特异性抗原,不具有相应的肿瘤特异性[6-7],良性前列腺疾病和恶性前列腺疾病都可以让患者的tPSA水平升高,但tPSA仍然具有较好的临床应用价值,被临床作为一种稳定有效的早期筛查方法,在病变早期、疗效评价、预后判断等方面发挥重要作用。由于多数前列腺癌患者早期常无特异性的临床表现,仅在临床超声检查或外科直肠指检时偶然发现,经直肠穿刺活检是前列腺癌诊断的金标准,但有一定的漏诊率,患者临床检查的依从性相对较低。血清tPSA的检测操作简单,对病人而言没有痛苦,检查的依从性较好,建议45 岁以上的男性应当进行血清tPSA的常规普查,特别可以用于特定人群的筛查。
目前常见的tPSA方法学检测主要有ELISA、CLIA、ECLIA、TRFIA等,以上几种检测方法均具备较高的灵敏度和准确性,但对医疗机构而言都具有耗时长、操作相对繁琐等缺点,单项检测成本高昂,手工操作容易产生人为误差,仪器设备的高投入及对操作人员的高要求一定程度上限制了其在临床的应用。我们开发研制的tPSA荧光免疫层析试纸条能够符合床旁检测(point of care test, POCT)要求,具有较高的灵敏度,精密度良好(批内、批间误差小),与ECLIA法检测所得结果没有显著差异(R2=0.9945),但是操作简单,快速、灵敏。检测仪器体积小、便于携带,试剂易于保存,完全符合POCT的临床应用要求[8]。本方法采用双抗体夹心检测反应模式,将标记抗体的荧光纳米微球作为示踪物,喷涂在结合垫上,另一抗体固定于试纸的T线区,滴加样本后在层析作用下移至结合垫,形成荧光微球-抗抗体-抗体,继续层析至T线区,被固定在T线区的抗体捕获,形成荧光微球-抗抗体-抗体-抗抗体复合物,通过检测荧光强度比对标准曲线就可以得到相应的血清标本浓度。
采用该荧光免疫层析试纸条可实现简便、快速、单人份定量检测,更适应临床检验特别是基层医疗机构的临床筛查需求,同时实现检测仪器和试剂的产业化,达到较好的社会效益和经济效益,值得临床推广应用。

