基于磁性C12烷基壳聚糖硅胶复合材料磁固相萃取-高效液相色谱法测定双酚类化合物
黄琼兰,胡静荣,邢淇玮,胡晶晶,杨 珍,张慧娟*
(1.中南民族大学化学与材料科学学院,分析化学国家民委重点实验室,湖北武汉 430074;2.中南民族大学实验教学与实验室管理中心,湖北武汉 430074)
内分泌干扰化合物具有和内分泌激素类似的生理作用,长期接触即使是低剂量也会使人体代谢紊乱,进而可能引发糖尿病、肥胖、心血管疾病甚至癌症[1,2]。双酚A(BPA)作为塑料生产的重要原料,因其具有雌激素活性,成为近十年来最受关注的双酚类内分泌干扰物[3 - 5]。加拿大和欧盟都已经禁止在婴儿奶瓶材质中添加BPA,以减少其对婴幼儿健康的危害[6,7]。研究表明,具有与BPA类似结构的其它双酚类化合物(BPs),如双酚S(BPS)、双酚F(BPF)和双酚AF(BPAF)等,也具有雌激素活性,且已在地表水、沉积物、室内灰尘和人体尿液中被检出[8,9]。目前对于双酚类化合物的检测方法主要是各类色谱分离技术与高灵敏检测器联用,例如气相色谱-质谱法(GC-MS)[10]、液相色谱-串联质谱法(LC-MS/MS)[11]和电化学发光传感器法[12]。由于双酚类化合物在实际样品中的含量低且样品基质复杂,因此,建立高效,快速的样品前处理与色谱分离联用技术尤为重要。
磁固相萃取因其萃取效率高且易于分离回收的优点,在样品前处理技术中发挥着重要的作用[13]。壳聚糖是天然环境友好的高分子材料,其在重金属污染治理领域中有着不俗表现[14 - 17],此外对双酚类物质如BPAF有较好的去除效果[18]。但是壳聚糖材料机械强度差,极性基团过多且不易回收,我们课题组就此进行改善,制备了磁性C12烷基壳聚糖硅胶复合材料,其对BPA具有很好的富集性能[19]。本文以磁性C12烷基壳聚糖硅胶复合材料为分离富集材料,以高效液相色谱-二极管阵列检测器(HPLC-DAD)为分离检测手段,建立了同时测定包括BPA、BPS、BPF、BPAF以及四氯双酚A(TCBPA)5种双酚类化合物的分析方法。结果表明,磁性C12烷基壳聚糖硅胶复合材料对5种目标BPs均具有优良的富集能力。在最佳的富集条件下,5种BPs的检出限范围为2.34~15.6 μg/L,且方法的精密度好。方法用于茶饮样品中可能存在的双酚类化合物的检测,显示茶饮基质不会影响BPs的富集。我们所建立的分析方法准确性较好,可以用于检测茶饮品中的BPs。
1 实验部分
1.1 仪器与试剂
Agilent 1260高效液相色谱系统(美国,安捷伦科技有限公司),配二极管阵列检测器(DAD);50 μL微量进样器(上海高鸽工贸有限公司);XW-80A微型涡旋混合仪(上海沪西分析仪器有限公司)。
双酚S(BPS,99%),双酚F(BPF,99.0%),双酚A(BPA,99.0%),双酚AF(BPAF,98%),四氯双酚A(TCBPA,98%),均购于上海阿拉丁生化科技股份有限公司。采用甲醇配制BPF、BPA、BPAF和TCBPA标准储备液,各标液浓度为1.0 g/L。BPS的标准储备液为0.1 g/L。所有标准储备液4 ℃避光保存,实验时稀释成不同浓度。甲醇和乙腈均为色谱纯,购于美国Tedia公司。其它试剂均为分析纯,购于国药集团化学试剂有限公司。实验用水均为超纯水。
1.2 色谱条件
色谱柱:WondaSilTM C18柱(150 mm × 4.6 mm,5 μm;日本,Shimadzu公司);流动相A为乙腈,B为超纯水。梯度洗脱程序:0~5 min,40%~80%A;5~9 min,80%A;9~19 min,80%~100%A;19~20 min,100%~40%A;流速:1.0 mL/min。紫外检测波长为:225 nm;柱温:30 ℃;进样量:10 μL。每次进样前,采用40%A平衡10 min。
1.3 磁固相萃取流程
磁性C12烷基壳聚糖硅胶复合材料由本课题组自制[19]。磁固相萃取流程如下:准确称取一定量的磁性复合材料于PTFE离心管中,用5 mL水/甲醇混合溶液(体积比95/5)对材料进行清洗,然后用甲醇对其进行活化,N2气吹干。加入10.00 mL含有一定浓度的BPS、BPF、BPA、BPAF和TCBPA的标准混合液,在室温下用涡旋仪涡旋一段时间,待富集结束后进行磁性固液分离,用水清洗材料除去残液。N2气吹干后加入2 mL的洗脱剂,涡旋10 min进行洗脱,再次磁性分离,取清液10 μL进行HPLC分析检测。富集率(%)由(W/W0)×100计算,其中W0、W(mg)分别为富集前及洗脱后溶液中每种BPs的质量。
1.4 茶饮样品预处理
塑料瓶装品牌茶饮A和B均购于超市,规格均为500 mL。将瓶装茶饮连瓶置于90 ℃水浴锅中加热10 min后,取出自然冷却,待用。品牌C和D为茶包,分别放入装有250 mL的90 ℃水的烧杯中,浸泡10 min,取出茶包,自然冷却。冷却茶水均用高浓度且pH=6.0的磷酸盐缓冲溶液(PBS)稀释,最终茶饮样品中PBS的浓度为20 mmol/L。在最优条件下利用复合材料进行磁固相萃取,洗脱液待测。
2 结果与讨论
2.1 溶液pH值和盐浓度对富集率的影响
样品溶液的pH值可能会影响5种BPs的存在形式,以及磁性C12壳聚糖硅胶复合材料表面电荷的种类和密度,进而影响复合材料对BPs的富集。由于材料中SiO2成分于强酸强碱中不稳定,因此本实验在pH=4.0~9.0范围内考察了pH值对材料富集性能的影响,5种BPs的浓度均为0.5 mg/L(此浓度也是后续其它条件考察时所用浓度)。从图1(a)的结果来看,在pH=4.0~6.0之间,当pH=6.0时,5种BPs物质的富集量达到最大;当pH>6.0后,BPF、BPA和BPAF的富集量基本没有变化,TCBPA的富集量略下降,而BPS的富集量大幅度减小。究其原因可能是BPS的pKa为8.2[2],在碱性条件下易电离,pH越大,BPS离子化程度越高,从而导致材料与BPS之间的疏水作用力减小,富集效果变差。因此,实验选择pH=6.0为后续实验溶液的pH值。

图1 pH值(a)和盐浓度(b)对萃取性能的影响。磁性材料用量:50 mg;洗脱剂:2 mL的乙腈;误差棒为3次平行测定的标准偏差Fig.1 Influence of pH value (a) and salt concentration (b) on the extraction.A mass of magnetic composite:50 mg;Eluent:2 mL of acetonitrile;the error bars represent standard deviation of three parallel experiments
溶液盐浓度可以改变吸附剂表面的电荷密度和溶液的离子强度,可能会影响富集材料对5种BPs的吸附行为。实验中选择NaCl调节溶液盐浓度,考察盐浓度对磁固相萃取的影响。在考察的盐浓度范围(0~150 mmol/L)内,复合材料对5种BPs的富集基本不受盐浓度的影响(图1(b))。
2.2 材料用量及富集时间对萃取性能的影响
采用适量的吸附剂、提供足够的吸附位点才能保证每种BPs都达最佳的富集量。由图2(a)可知,随着吸附剂用量的增加,BPAF和TCBPA的富集量很快达到平衡,而BPS、BPF和BPA的富集量随磁性复合材料用量的增加而增大。当材料用量达到40 mg后,5种BPs的富集量基本保持不变。综合考虑,后续实验中采用50 mg磁性C12烷基壳聚糖硅胶复合材料。同时,我们对富集时间也进行了考察。从图2(b)可以看到,5种BPs富集20 min后均达到平衡。因此,选择20 min为后续实验需要的富集时间。

图2 材料用量(a)及富集时间(b)对萃取性能的影响。洗脱剂:2 mL的乙腈;误差棒为3次平行测定的标准偏差Fig.2 Influence of the amount of sorbent (a) and enrichment time (b) on the extraction.Eluent:2 mL of acetonitrile;the error bars represent standard deviation of three parallel experiments
2.3 洗脱条件的考察
以乙腈为洗脱剂,考察洗脱剂用量和洗脱时间对材料洗脱的影响。5种BPs的洗脱率随乙腈用量的增大而增大,当乙腈洗脱体积达到2 mL时,BPS、BPF、BPA、BPAF和TCBPA的洗脱率分别是98.1%、97.0%、97.9%、96.8%和96.6%(图3(a))。从环保和提高富集倍数考虑,2 mL是最合适的洗脱剂用量。随后考察了洗脱时间的影响,结果如图3(b)所示。洗脱时间为5 min时,5种BPs的洗脱率已超过96%,洗脱迅速。为了保证分析方法的重现性,最终选择10 min为最佳洗脱时间。

图3 洗脱体积(a)和洗脱时间(b)对萃取性能的影响。磁性材料用量:50 mg;样品体积:10 mL;误差棒为3次平行测定的标准偏差Fig.3 Influence of elution volume (a) and elution time (b) on the extraction.A mass of magnetic composite:50 mg;sample volume:10 mL;the error bars represent standard deviation of three parallel experiments
2.4 分析方法评价及样品分析
基于反相色谱分离机理,以乙腈和水的混合溶液作为二元流动相,优化了色谱分离条件并实现了5种BPs的基线分离。在最佳的色谱条件下,测定5种BPs的线性方程、线性范围和检出限(LODs)如表1所示。5种BPs在各自的线性范围内,峰面积与浓度的线性关系良好,线性相关系数R超过了0.99。BPS的线性范围略窄的原因可能是因为其极性较大,在高浓度时材料对其富集不完全造成的。
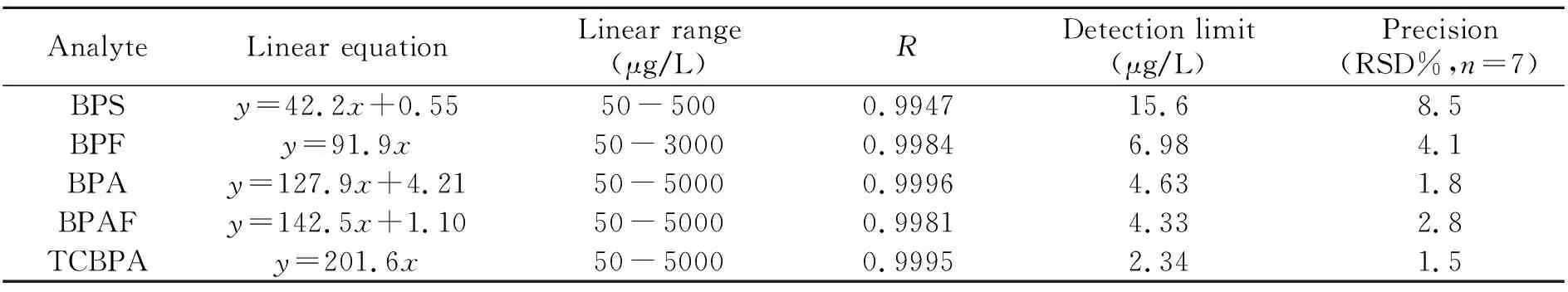
表1 分析方法的线性范围、线性相关性、精密度及检出限
平行分析7次BPs标准混合溶液(0.05 mg/L)后,计算结果的标准偏差S,以3S作为检出限,5种BPs的检出限为2.34~15.6 μg/L。方法的精密度用相对标准偏差(RSD)表示,RSDs在1.5%~8.5%之间。与类似的富集材料相比[20,21],基于磁性C12烷基壳聚糖硅胶复合材料建立的分析方法的检出限较低,灵敏度较高。
包装是保证食品质量和安全的屏障。而塑料包装的茶饮或茶包加热后,包装中的BPs可能迁移到茶饮中,从而被人体摄入,因此建立检测茶饮基质中的双酚类化合物含量具有一定的挑战。我们对4种茶饮进行了加标分析,两个不同加标浓度的回收率列于表2。通过图4的茶饮加标样品色谱分离图,可以看到茶饮基质对BPs色谱峰的定量没有干扰。在4种茶饮中,5种BPs的加标回收率在86.0%~112.3%之间,RSD不超过4.23%。4种茶饮中均未检测到BPs,考虑到瓶装茶饮加温时间和茶包冲泡时间可能过短,从而导致包装中存在的BPs未迁移至茶饮中。后续实验中会做进一步研究。

图4 茶饮A及其加标分析的色谱分离图。(a)茶饮A中添加BPS的浓度为0.4 mg/L,其它4种为2 mg/L;(b)茶饮A中5种BPs的浓度均为0.2 mg/L;(c)茶饮A的空白Fig.4 Chromatograms of blank and spiked tea drink A.(a) The spiked concentration of BPS was 0.4 mg/L and other BPs was 2 mg/L;(b) the spiked concentration of each BPs was 0.2 mg/L;(c) the blank of tea brink A
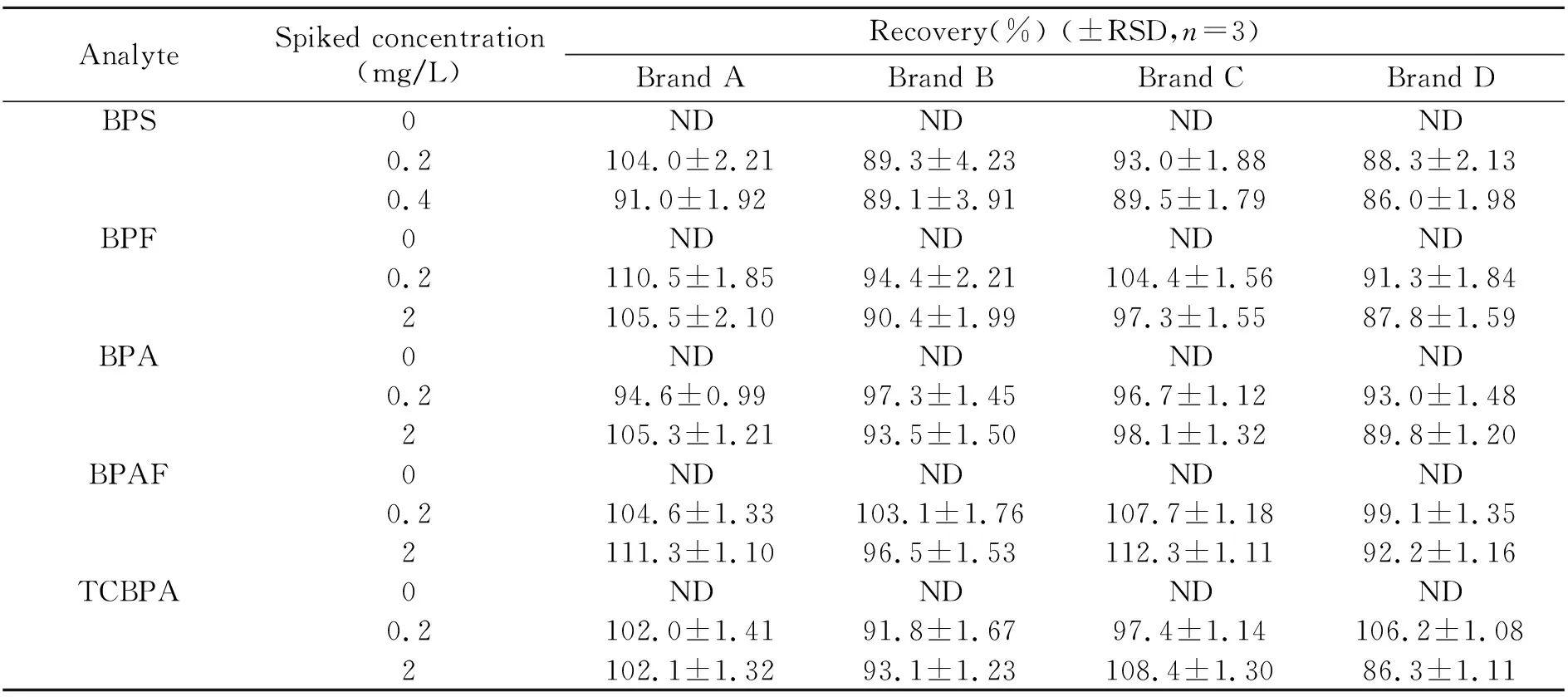
表2 4种市售茶饮中BPS、BPF、BPA、BPAF和TCBPA加标回收率的测定
3 结论
本文基于磁性C12烷基壳聚糖硅胶复合材料成功建立了以磁性固相萃取为富集方法,高效液相色谱-二极管阵列检测为分离检测手段,高效、准确测定5种BPs的分析方法。建立的分析方法应用于茶饮样品的分析,虽然在4种茶饮中均未检测到BPs,但分析方法的回收率在86.0%~112.3%之间,表明该方法准确性好。

