磷石膏气-液-固吸附制备纳米碳酸钙
周 静,李 锋
(贵州省都匀市黔南民族师范学院化学化工学院,贵州 都匀 558000)
磷石膏(PG)是湿法磷酸生产过程中产生的一种富钙废渣。它由接近90%的二水硫酸钙和8%以上的氧化硅以及少量的其它杂质组成,如五氧化二磷、氟化物和游离酸。在众多的CO2捕集技术中,Ca环(Ca-L)技术因其较大的化学计量捕集能力被认为是最有前途的高温脱碳工艺。但其捕集CO2的成本仍高于预期,相比之下,纳米氧化钙吸附剂表现出更高的吸附容量和更快的二氧化碳反应性吸附一直是人们关注的焦点。
利用PG作为钙源制备纳米CaO基CO2吸附剂,不仅可以起到资源化利用的作用,而且为Ca-L技术降低CaO基CO2吸附剂成本提供了一条新的途径。目前,对PG制备的CaCO3的研究已有报道。美国发明公开了一种可行的一步法制备纳米碳酸钙的方法,该方法是由废石膏与氨水在连续二氧化碳喷射下通过水相反应制备纳米碳酸钙。作用如式(1)所示。在方法学方面,如前所述,该工艺与沉淀碳酸钙(PCC)的制备有一些相似之处。然而,在制备过程中,只要优化CO2流量和反应时间,就很容易制备出纳米碳酸钙,而在表面活性剂的作用下,只有70%的PCC的粒径小于500nm。

本文以PG为原料制备纳米碳酸钙,系统研究了温度、CO2流量、反应时间、可溶性杂质等对碳酸钙成核及晶体生长的影响。对所得碳酸钙的粒径分布、晶相、组成、微观结构和CO2吸附性能进行了评价。
1 实验部分
1.1 气-液-固反应制备纳米碳酸钙
试剂和材料:磷石膏来自中国云南磷化工集团有限公司;氢氧化铵溶液(25%~28%,AR)购自中国国药化学试剂有限公司。
纳米碳酸钙制备:利用图1所示的实验装置从PG合成纳米碳酸钙。PG与去离子水混合,质量比为1∶9~1∶7。然后将所得浆液与一定量的氢氧化铵混合,氨与SO42-的物质的量比为2.3~2.5。在达到设定温度后,在连续搅拌下,用管道将给定流速的二氧化碳输送到浆液中。定期倒出约10 mL泥浆,分析其硫酸根离子浓度和pH值,以监测PG的转化率。过滤后,使用可见分光光度计(720N,INESA,中国)在420nm处借助BaCrO4溶液对硫酸根离子浓度进行定量,同时用pH测试仪测量pH值。当pH低于8时,反应终止。过滤并干燥浆液以获得碳酸钙粉末。通过改变反应温度、CO2流量、反应时间等,研究了上述实验条件对碳酸钙制备及性能的影响[1-3]。

图1 PG合成碳酸钙的实验装置及机理
1.2 材料性能测试
在0.04~2000μm范围内,用激光粒度分析仪(美国贝克曼库尔特LS-230 Coulter)测定了产物的粒度分布(PSD),并用场发射扫描电子显微镜(FE-SEM,SIRION,FEI,Netherland)对碳酸钙的形貌进行了表征。此外,还利用透射电子显微镜(TEM,JEM-1380EX,JEOL,Japan)和选区电子衍射(SAED)观察了样品的详细微观结构。
1.3 CO2吸附性能的评价
用热重分析仪(TGA,Pyris 1,Perkin Elmer,America)通过连续记录样品重量变化来评估制备的CaCO3的 CO2吸附性能。样品(2 mg)最初加热至800°C,并在纯氮气中保持10 min,以实现完全煅烧。随后,炉温降至600°C;在此温度下,在20%二氧化碳中碳化10 min。然后,再次加热至800℃进行煅烧。通过重复上述步骤,可以很容易地实现循环 CO2吸附性能[4-5]。
2 结果和讨论
2.1 反应结晶过程
PG中CaCO3的反应结晶是一个极其复杂的过程,涉及气相(CO2)、液相(NH3·H2O)和固相(PG)。在这项研究中,提出了一个可能的方案,并在图1中加以说明。它主要包括以下几个过程:①二氧化碳从气相扩散到水相并随后生成碳酸氢根离子;②氢氧化铵的电离;③碳酸氢根离子与氢氧化根离子反应生成碳酸根离子;④CaSO4在PG中的溶解;⑤碳酸盐离子与硫酸盐离子的快速反应及碳酸钙的后续结晶。在这些亚过程中,碳酸钙的结晶是最关键的一步,它直接决定了碳酸钙晶体的尺寸、分布和最终产品的收率,并受温度、过饱和度和反应时间的影响。
2.2 特征结果
PG衍生纳米碳酸钙的形态如图2所示。从图2可以看出,所得到的产物是由非晶纳米颗粒(约100nm)组成,具有聚集结构。SEM图像测量的颗粒直径与X射线衍射图计算的结果一致[6]。

图2 40°C下,138 mL/min二氧化碳流速下50min碳酸钙的扫描电镜图像
2.3 反应温度和CO2流量对CaCO3-PSD的协同效应
在138mL/min CO2流量下,CaCO3PSD随反应温度的变化如图3所示。可见,随着温度的升高,PSD从53~258nm转移到40~173nm,其中在30℃和40℃时达到的PSD几乎重叠,平均粒径也从156 nm减小到104 nm。

图3 制备温度对138mL/min CO2流量下CaCO3 PSD的影响
众所周知,当钙离子和碳酸盐离子的浓度超过临界过饱和时,碳酸钙的成核是自发的,然后随着晶体的生长而发生[7-8]。CO2流量与过饱和度直接相关,对结晶过程有重要影响。因此,当二氧化碳流量增加到251mL/min时,温度对PSD的影响结果如图4所示。
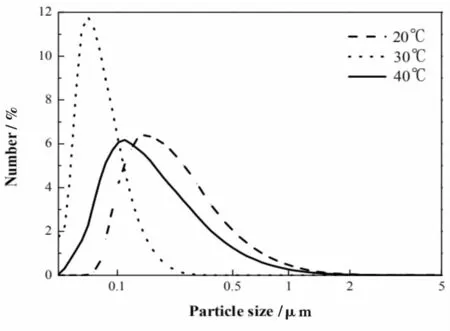
图4 制备温度对251 mL/min CO2流量下CaCO3 PSD的影响
与图3不同,在30℃下合成的碳酸钙具有最小的平均粒径,即86nm,而在20℃和40℃下获得的碳酸钙粒径分别为284nm和260nm。通常,提高CO2流量可以增加CO2的浓度,从而加速成核速率和晶体生长然而。如所揭示的,二氧化碳流速对碳酸钙结晶的影响也与反应温度有关;在这种情况下,对于这种二氧化碳流速,最佳反应温度是30℃。
综上所述,通过对上述结果的比较,可以得出反应温度不是决定碳酸钙PSD的唯一参数,温度与CO2流量之间存在协同作用。
2.4 其它反应条件对CaCO3 PSD的影响
在保证CaSO4完全转化的条件下,反应时间对CaCO3PSD的影响如图5所示。如图5所示,随着时间从50 min增加到160 min,碳酸钙的一次粒子密度从40~195nm增加到93~598 nm,平均粒径也从原来的104 nm增加到215nm。反应时间的延长为晶体生长提供了更多的时间,导致碳酸钙粒径增大。因此,要制备纳米碳酸钙,必须严格控制反应时间[9-10]。

图5 反应时间对40°C、138mL/min CO2流量下CaCO3 PSD的影响
2.5 二氧化碳吸附性能
二氧化碳吸附性能如图6所示。
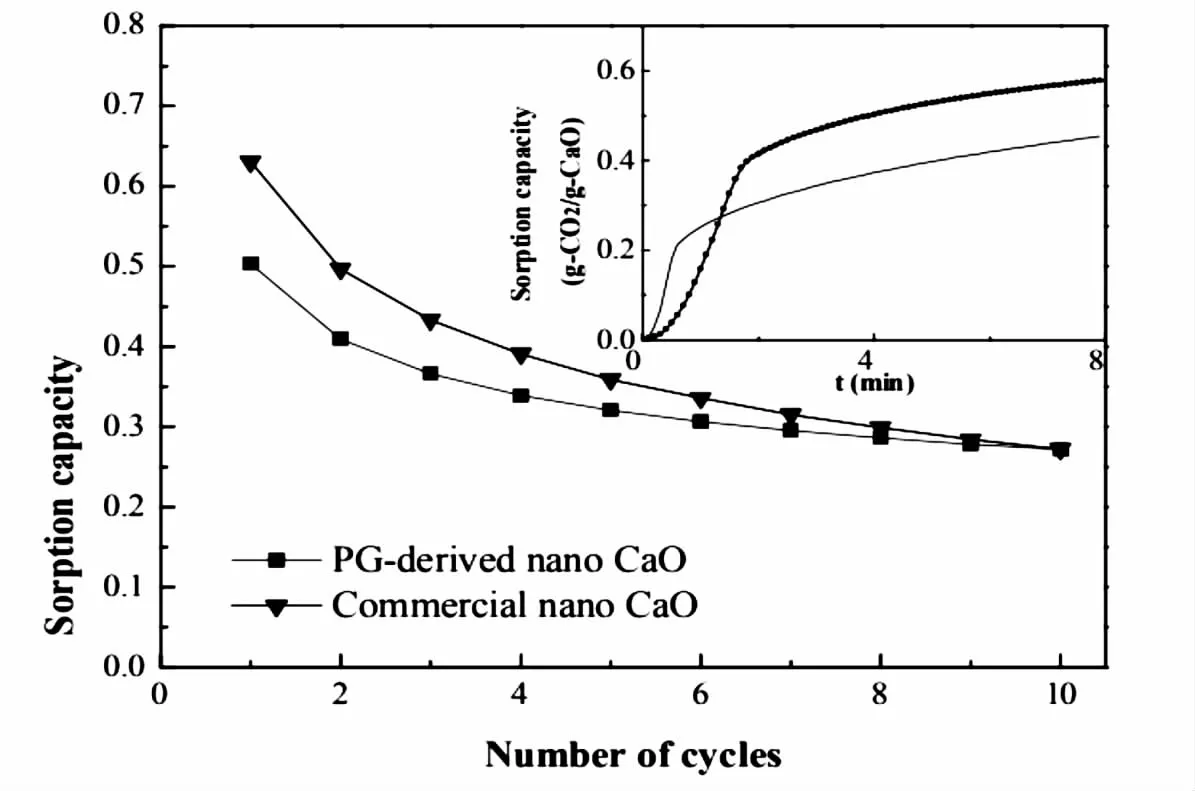
图6 40°C、138mL/min二氧化碳流速下,PG衍生纳米氧化钙对二氧化碳的吸附能力
为了在Ca-L技术中得到应用,有必要研究PG衍生纳米CaO的CO2捕获性能。图6显示了在40°C下以138mL/min的二氧化碳流速获得的样品的二氧化碳吸附能力。可见,合成固体的碳化曲线显示了一个典型的两步反应过程,具有快、慢的动力学过程,符合纳米材料的特点曹。PG衍生的纳米CaO由于含有氧化铝、二氧化硅等杂质,其初始CO2吸附量比商用纳米CaO低0.13g/g。但随着循环次数的增加,这两种吸附剂之间的吸附量差距逐渐减小,循环10次后吸附量基本相同。这是因为PG制备的纳米CaO中的杂质会延迟CaO在煅烧过程中的热烧结。
3 结论
在气-液-固体系中,通过一步反应结晶法从废PG中得到纳米碳酸钙。结果表明,制备温度和CO2流量对碳酸钙的PSD有显著影响。综合来看,随着温度的升高,保持较低的CO2流量有利于纳米碳酸钙的形成。其中,将温度控制在30~40℃,CO2流量控制在251~138mL/min,可以制备出平均粒径为86~104nm的纳米碳酸钙,反应时间短,PG中可溶性杂质少,有利于纳米碳酸钙的制备。此外,所得产物具有较好的循环CO2吸附稳定性,循环10次后其吸附容量与商用纳米CaO相同。

