基于网络药理学探索丹参饮治疗慢性萎缩性胃炎的机制研究
李昆阳 刘华一
慢性萎缩性胃炎(chronic atrophic gastritis,CAG)是以胃黏膜固有腺体萎缩、减少为主的一类疾病,甚至发展为伴肠上皮化生和(或)异型增生的癌前病变。CAG属Correa级联反应的中央阶段,对于疾病的发展和转归具有重要的承接作用,积极治疗对胃癌的防治具有重要临床意义。然而,目前西医尚未有统一、规范、有效的治疗方案,多采用抗炎、杀菌、抑酸、助消化、黏膜保护等方法缓解症状,对于萎缩病理状态的改变仍缺乏特效药,仅通过具有生物活性功能的维生素、叶酸及微量元素改善胃黏膜状态,以求延缓其进展。中医方剂具有“多成分、多靶点、多途径”的特点在治疗该疾病中具有巨大优势,不仅能够明显改善症状,及时阻断病程发展[1-3],甚至能够逆转萎缩[4]。究其症状,CAG类属中医“胃痞”范畴,病程缠绵,“久病必虚,久病必瘀”且“阳明为多气多血之腑”,“气虚血瘀”贯穿CAG的整个疾病过程,故在补脾、疏肝、消积、理气辨证治疗基础上加以活血、行气、祛瘀之法。
丹参饮载于《时方歌括》,由丹参、檀香、砂仁组成,“治心痛、胃脘诸痛多效”,为行气活血的代表方剂。方中重用丹参一两为君,取其“专入血分,活血行血,内达脏腑而化瘀滞”之功;檀、砂各用一钱为佐,檀香调脾胃、利胸膈,为理气之要药;砂仁理元气、通滞气,醒脾养胃;三药合用,行气活血而瘀自散,为行气化瘀止痛之良方。现代药理研究表明,丹参饮具有抗菌、抗炎、镇痛等多种作用,临床上广泛应用于CAG、消化性溃疡等多种脾胃病的治疗中,能够有效改善气虚血瘀症状[5-7]。但目前对其作用于疾病的活性物质和特定的分子机制知之甚少,值得进一步深入探究。
网络药理学是一种涵盖化学信息学、生物信息学、网络生物学和传统药理学的新方法,可更系统地揭示中药的活性成分和潜在机制,从整体探索中药和机体的相互作用[8]。本研究采用网络药理学的方法,探究丹参饮治疗CAG的有效成分、作用靶点及潜在机制,为后续深入研究提供参考和依据。
1 材料和方法
1.1 丹参饮化学成分的收集、筛选和靶点预测
通过检索TCMSP[9]获得丹参、檀香、砂仁已知的全部化学成分,以口服利用度(oral bioavailability,OB)≥30%和类药性(drug-likeness,DL)≥0.18为条件,筛选出丹参饮的主要活性成分;通过PubChem获得活性成分的SMILES;检索Swiss Target Prediction[10],获得相关靶点信息;与TCMSP获得成分靶点合并去重,即可获得丹参饮主要活性成分的相关靶点。
1.2 CAG靶点检索
本研究以“Gastritis、Atrophic”为关键词分别检索DrugBank、DisGeNET、Genetic Association Database(GAD)和Online Mendelian Inheritance in Man(OMIM)数据库,去除假阳性后合并去重,即为CAG相关靶点。
1.3 网络构建及分析
通过UniProt数据库将所有靶点进行标准化处理,得到其官方名称及UniProt ID,用于后续分析工作。将丹参饮活性成分相关靶点与CAG相关靶点相映射,可获得丹参饮治疗CAG的潜在作用靶点。根据上述靶点预测结果,采用Cytoscape3.2.1软件构建丹参饮“活性成分-作用靶点”关系网络,其中节点(node)代表活性成分、靶点;边(edge)连接活性成分与靶点,展现两者之间的关系。
1.4 富集分析
本研究利用 DAVID(Version 6.8)平台对共同靶点进行Gene ontology(GO)注释分析和Pathway分析,用于描述候选靶点特征; 运用Omicshare云平台将结果可视化。其中GO注释包括生物过程(biological process,BP)、细胞成分(cell component,CC)和分子功能(molecular functions,MF),KEGG通路分析结果以气泡图形势呈现富集结果的通路,以探究丹参饮治疗CAG可能的作用机制。
1.5 蛋白质相互作用网络的构建
蛋白质通常与脂质、核酸和其他蛋白质等共同发挥作用,蛋白质-蛋白质相互作用(PPI)网络有助于了解各种蛋白质在复杂疾病中的作用,运用Cytoscape软件中Bisogenet插件构建网络并将结果可视化。分别构建丹参饮活性成分相关靶点及CAG相关靶点PPI网络;Merge获取2个网络的交集,即为丹参饮治疗CAG的直接或间接靶点调控网络。
1.6 核心靶点筛选及聚类分析
网络中的每个节点均有自由度(degree centrality,DC)、中心中介性(betweenness centrality,BC)、紧密度(closeness centrality,CC)、特征向量中心性(eigenvector centrality,EC)、网络中心性(network centrality,NC)和局部边连通性(loal average connectivity,LAC)等参数信息,可通过network analyzer、CytNCA插件进行网络分析评估。先以“DC≥2中位数DC”为筛选条件,然后选择BC、CC、DC、EC、LAC、NC均大于中位数的节点为核心靶点。
人类机体复杂,由多个相对独立而又相互作用的功能模块组成,聚类分析作为一种重要的分类方法可以清楚展现PPI网络中的固有规律,MCODE算法生成的模块稳定可靠,将筛选出的核心靶点以K-core≥4为条件筛选出聚类较好的基因模块,从多角度解释丹参饮治疗CAG的机理。
2 结果
2.1 丹参饮活性成分
通过TCMSP数据库收集到437个丹参饮成分,筛选后得到78个主要活性成分;另纳入12种上述三种药物中含量较高的成分,剔除不含相关信息的化学成分后,最终确定丹参饮86个活性成分,其中丹参67个、檀香7个、砂仁14个,丹参与檀香、丹参与砂仁各有一个共同活性成分,具体成分信息见表1。

表1 丹参饮中潜在活性成分表
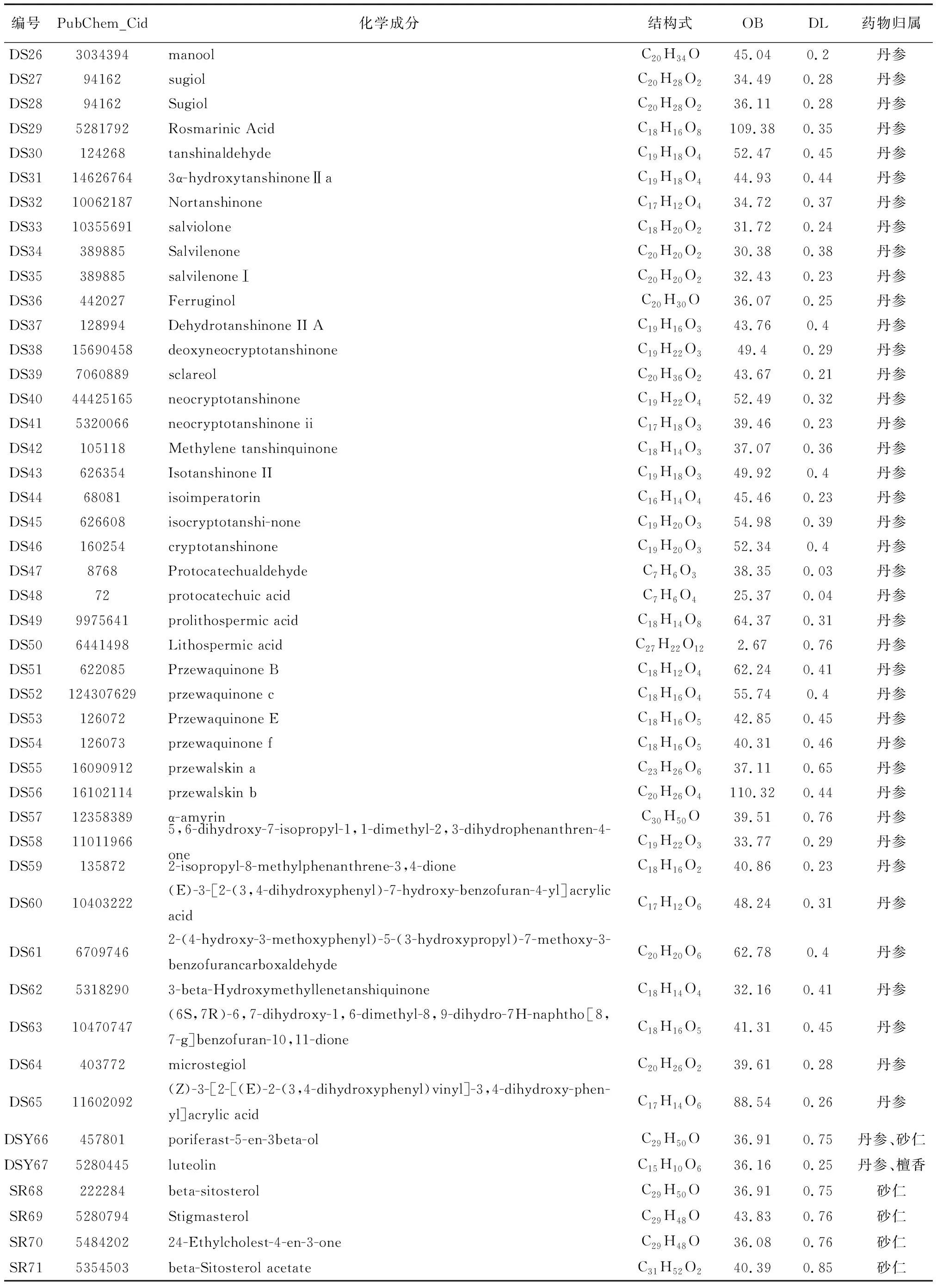
续表

续表
2.2 丹参饮作用靶点
检索、去重后共得到丹参饮有效靶点355个,其中丹参304个、砂仁147个、檀香123个,三味药共同作用靶点57个,占全部药物的16.1%,丹参、檀香共同靶点25个(7%),丹参、砂仁共同靶点51个(14.4%),砂仁、檀香共同靶点4个(1.1%),可见不同药物可通过相同的作用靶点共同发挥作用。degree值代表与该节点相连的边的条数,越大则表明在网络中越关键,图中节点颜色随着degree值的变大而逐渐加深,可直观看出相对主要活性成分和重要靶点(图1)。
2.3 丹参饮治疗CAG的潜在作用靶点
检索DrugBank、DisGeNET、GAD、OMIM分别得到14个、118个、46个和15个CAG相关靶点,去除重复后共得到165个CAG相关靶点。与丹参饮主要成分的作用靶点相映射,构建“丹参饮-作用靶点-CAG”网络,139条边连接99个节点(图2),75个丹参饮成分通过作用于24个靶点对CAG起到直接治疗作用,其中62个成分作用于PTGS2,29个成分作用于PPARG,NR1H2、DRD2、EGFR、TNF等靶点也被多个成分所调节,木犀草素、丹参酮IIA、丹参新醌D、β-谷甾醇、Glimepiride等活性成分调节多个靶点,由此可见中药治疗疾病多成分、多靶点的特点。
2.4 丹参饮治疗CAG的生物功能分析
为了深入了解丹参饮对CAG的药理作用机制,对24个共同靶点(PTGS2、PPARG、NR1H2、DRD2、EGFR、TNF、CYP1A2、BCL2、CYP2C19、TP53、ABCB1、AKT1、CYP2B6、CYP2C8、CYP2E1、CYP3A4、GSTP1、HSPA2、IL2、IL6、MIF、ODC1、SOD1、VEGFA)进行了GO和KEGG通路分析,得到235个GO注释结果和56条通路。其中16个BP、10个CC、8个MF具有重要意义(图3),其生物功能主要与物质代谢、细胞增殖与凋亡、信号转导、氧化还原等相关,这体现出丹参饮通过调控多个复杂的生物过程来治疗CAG。 以P<0.05为条件,共得到48条重要通路(图4),其中多与代谢、癌症、炎症相关,排名在前10的通路依次为:药物代谢细胞P450、化学致癌、亚油酸代谢、癌症通路、花生四烯酸代谢、细胞色素P450介导的异生素代谢、HIF-1信号通路、肌萎缩侧索硬化(amyotrophic lateral sclerosis,ALS)、PI3K-Akt信号通路、麻疹。
2.5 PPI网络的关键节点
为了全面探究丹参饮治疗CAG的核心药理机制,课题组采用拓扑方法评估核心网络,共得到关键节点156个,筛选策略示意图见图5。
2.6 聚类分析
将上述156个关键靶点,运用MCODE 插件进行聚类分析,得到5个聚类较好的模块,然后对各个模块进行富集分析,GO结果所涉及的生物过程依次为:物质代谢,基因表达、沉默和复制,DNA、RNA损伤修复和转录调控,蛋白质合成,细胞凋亡的负调控。KEGG通路共37条,多与癌症相关,不同模块富集到相同的通路有核糖体、细胞周期、泛素介导的蛋白质降解、PI3K-Akt信号通路、前列腺癌、病毒致癌、癌症通路。
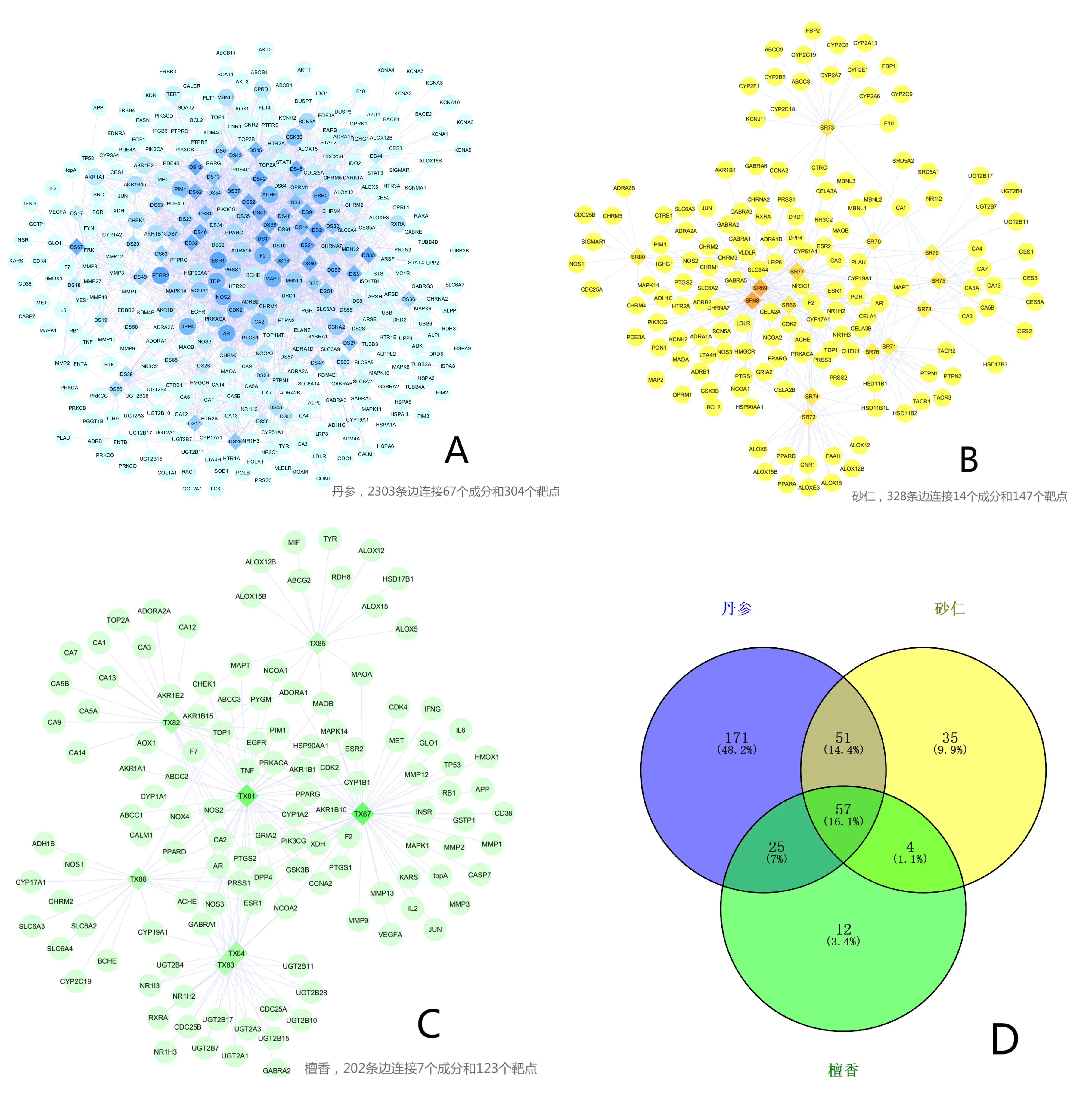
注:A为丹参的“成分—靶点”网络;B为砂仁的“成分—靶点”网络;C为檀香的“成分—靶点”网络;D为三味药“成分—靶点”的韦恩图。菱形—成分、圆形—靶点、蓝色—丹参、黄色—砂仁、绿色—檀香。
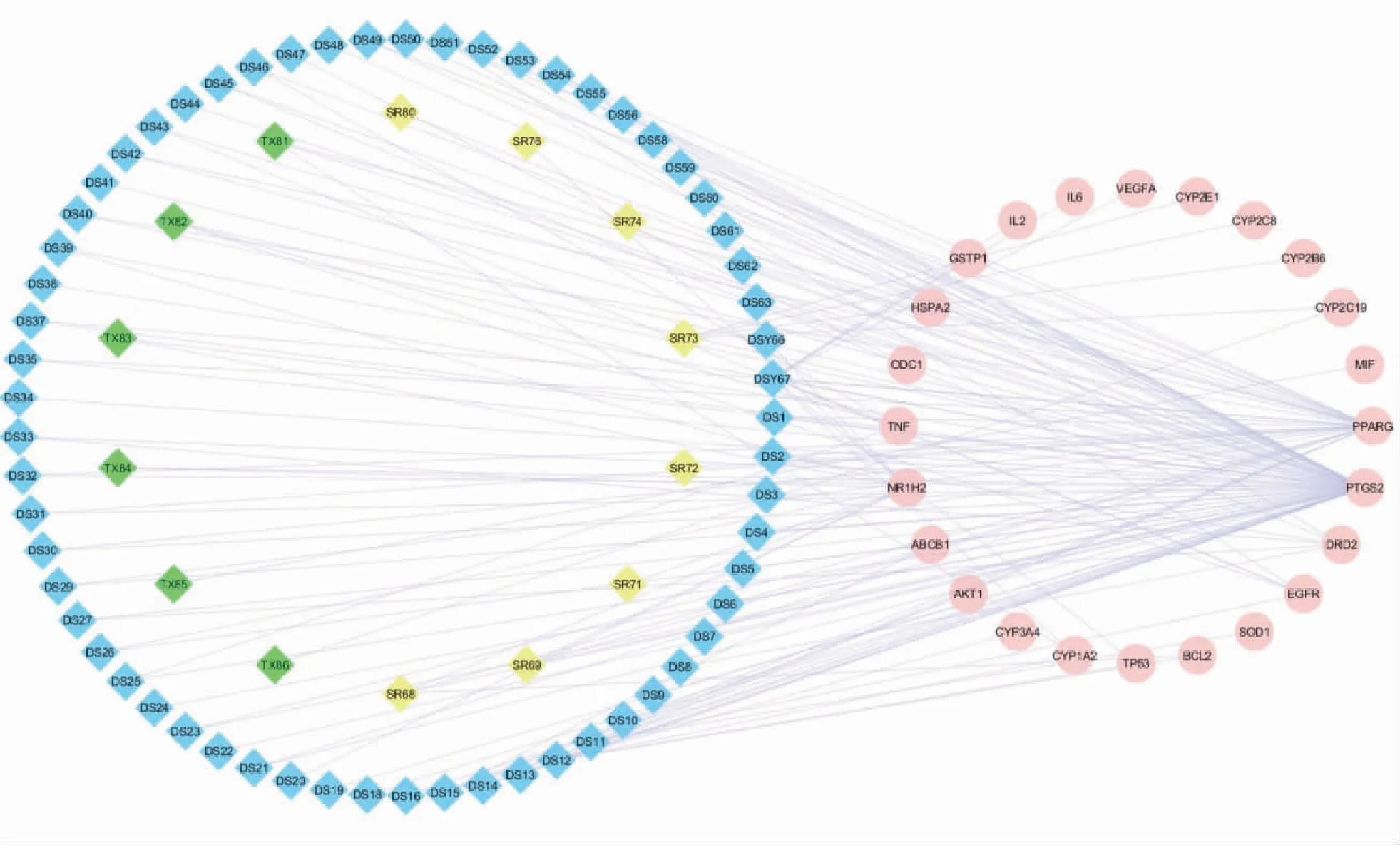
注:菱形—成分、圆形—靶点、蓝色—丹参、黄色—砂仁、绿色—檀香。

图3 丹参饮活性成分治疗CAG潜在靶点的GO生物学过程
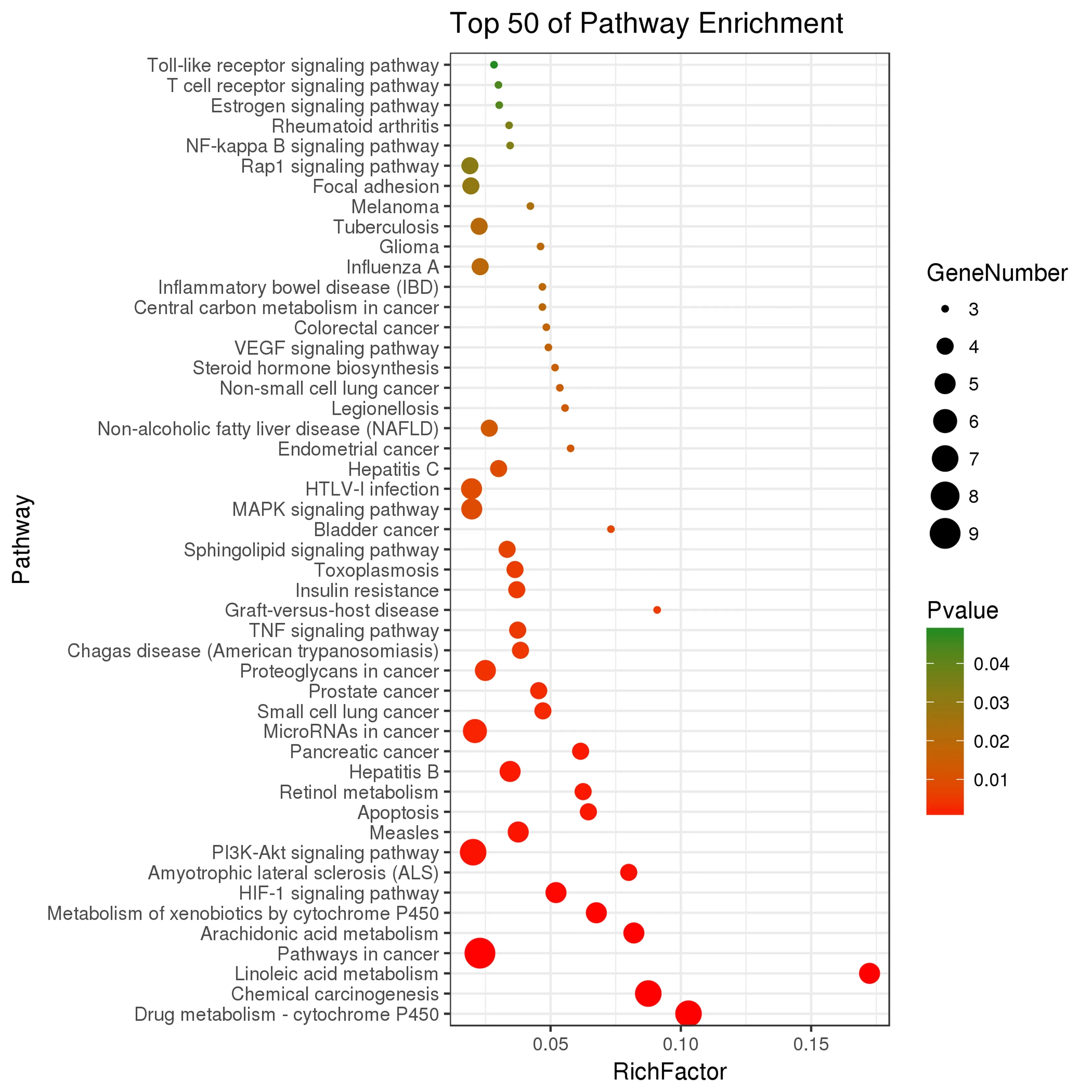
图4 丹参饮活性成分治疗CAG潜在靶点的KEGG通路分析结果示意图

图5 丹参饮治疗CAG的PPI网络关键节点筛选示意图
3 讨论
本研究筛选出丹参饮86个活性成分、355个潜在靶点,与165个CAG靶点相映射,得到24个共同靶点,包括多种功能酶、信号分子、转录因子等物质;富集分析得到生物功能235个、信号通路56条,发现丹参饮的75个有效成分主要通过调控PTGS2、PPARG、NR1H2、DRD2、EGFR、TNF等相关靶点蛋白,干预机体的氧化还原、物质代谢、炎症反应、细胞增殖凋亡等生物途径,并可能通过缺氧诱导因子-1(hypoxia inducible factor-1,HIF-1)、PI3K-Akt等信号通路来治疗CAG,并抑制其发展为胃癌。
CAG作为一个临床复杂疾病,为更全面探讨其机理,本研究又构建了PPI网络并进行拓扑分析,将拓扑得到的156个关键靶点进行聚类分析,得到5个模块,并对这5个模块进行富集分析。结果显示,GO生物过程除了之前得出的物质代谢、细胞增殖凋亡外,还增加了基因表达、沉默和复制,DNA、RNA损伤修复和转录调控,以及蛋白质合成。KEGG通路仍主要富集在癌症及与癌症发生发展密切相关的细胞周期、泛素介导的蛋白质降解、PI3K-Akt等信号通路上。
CAG萎缩分布不均匀,胃黏膜同时存在多种病理状态,其发生发展是一个多阶段、多因素、受多基因作用的复杂过程,而丹参饮可从多层次、多角度参与到胃黏膜的组织修复,这与其他研究结果所显示的丹参饮能够提高机体抗氧化能力,减轻细胞坏死及凋亡,改善胃黏膜微环境缺血缺氧状态等作用也具有一致性[11-12]。丹参饮通过调节多个生物过程来治疗CAG,与中医通过辨证论治,治病求本,调节“体质”的观点也不谋而合。
本研究发现丹参饮治疗CAG的作用机制主要体现在控制炎症反应和调节细胞的增殖和凋亡。(1)核心靶点均与炎症反应及细胞的增殖和凋亡密切相关。其中PTGS2催化花生四烯酸产生多种炎性前列腺素,介导机体炎症反应,并与细胞粘附增加、表型变化、细胞凋亡和肿瘤血管生成密切相关[13-14];PPARG是脂肪代谢和葡萄糖稳态的关键调节因子,能调节MAPK p38、IL-6的磷酸化,其活化能促进细胞凋亡、抑制细胞迁移和增殖,并抑制NF-κB介导的促炎反应[15-16];核受体NR1H2可监测内源性甾醇水平以维持全身胆固醇水平,并调节炎症反应,并能够抑制细胞增殖[17-18];多巴胺受体DRD2参与自主运动、情绪及激素调节、多巴胺诱导的免疫效应和肿瘤等众多生物过程,并与肿瘤细胞的增殖、侵袭、转移、自噬、凋亡都密切相关[19-20];受体酪氨酸激酶EGFR编码表皮生长因子受体,通过其多种配体结合促发关键细胞磷酸化,激活至少4个下游信号级联,包括RAS/RAF/MEK/ERK、PI3K/AKT、PLCγ/PKC、STATs,也可以激活NF-κB信号级联反应,还可直接磷酸化其他蛋白质、酶及受体,导致细胞增殖、迁移和分化[21-23];TNF主要由活化的巨噬细胞产生,可诱导某些肿瘤细胞系的细胞死亡,在特定条件下可以刺激细胞增殖并诱导细胞分化,是重要的炎症介质,并参与某些自身免疫病的病理损伤[24-26]。(2)富集分析结果中多种生物过程和通路都与炎症反应及细胞的增殖和凋亡密切相关。除了各种疾病通路外,显著富集于HIF-1、PI3K/Akt、TNF、MAPK、VEGF等通路上。缺氧是肿瘤微环境中驱动肿瘤发生的最常见原因之一,HIF-1对维持氧稳态起主要调节作用,其过表达与STAT3、NF-κB、TLR4、Myc、mTOR、AP-1、IGF-1、Wnt、TGF-β、Notch1等的激活都密切相关,进而影响炎症反应、血管生成、细胞增殖凋亡、迁移和侵袭、物质代谢而在肿瘤进程中发挥重要作用[27-28]。PI3K-Akt信号通路经常在各种人类癌症中被激活,PI3K催化PIP3的产生,PIP3作为第二个信使激活Akt,活化的AKT通过磷酸化多种酶、激酶和转录因子等下游因子,进而调节细胞的功能;PI3K/Akt/NF-κB/BMP-2-Smad轴、PTEN/PI3K/Akt轴、PI3K/Akt-mTOR等多种途径均可调节全身炎症反应,肿瘤细胞的增殖与凋亡、侵袭转移、存活和自噬[29-30]。机体内各种反应错综复杂,通路之间互相关联影响,丹参饮通过调节多个靶点和通路,共同发挥抗炎和抗氧化作用,进而调节细胞的增殖和凋亡。而CAG作为一种慢性炎症,或(已)发展为胃癌前病变,抑制炎症反应及细胞的增殖和凋亡对防止该病转变为胃癌具有重要意义。
中医药符合现代精准医学中个体化治疗的理念,但在分子生物学水平上证明其治疗效果仍然是一个巨大的挑战。“多成分、多靶点”既是中医药的优势,同时也为基础研究带来了不便,网络药理学通过整合各数据库结果,建立“药物—成分—靶点—疾病”关系预测模型,系统而整体地去探究药物治疗疾病的作用关系,符合中医的整体观念,有利于中医药的现代研究和临床推广。但是,该方法仍具有一些缺陷,目前现有的中医药相关数据库存在积累不足、质量不高、现有数据重复性不强的局限性,而中医药成分信息的正确性对于网络构建与分析结果至关重要;另外该方法仅是通过计算机模拟得到活性成分与相关靶基因,但不能明确活性成分对靶基因调控关系,仍需进一步通过实验研究加以验证。
综上,本研究通过网络药理学初步阐明丹参饮治疗CAG的作用机制,科学地体现出了中医整体观和系统性,为中医药多成分、多靶点、多途径的治疗优势提供了有力证据,为中医药治疗多因素导致的复杂疾病提供了新途径,同时为后续分子机制研究提供了一定方向。

