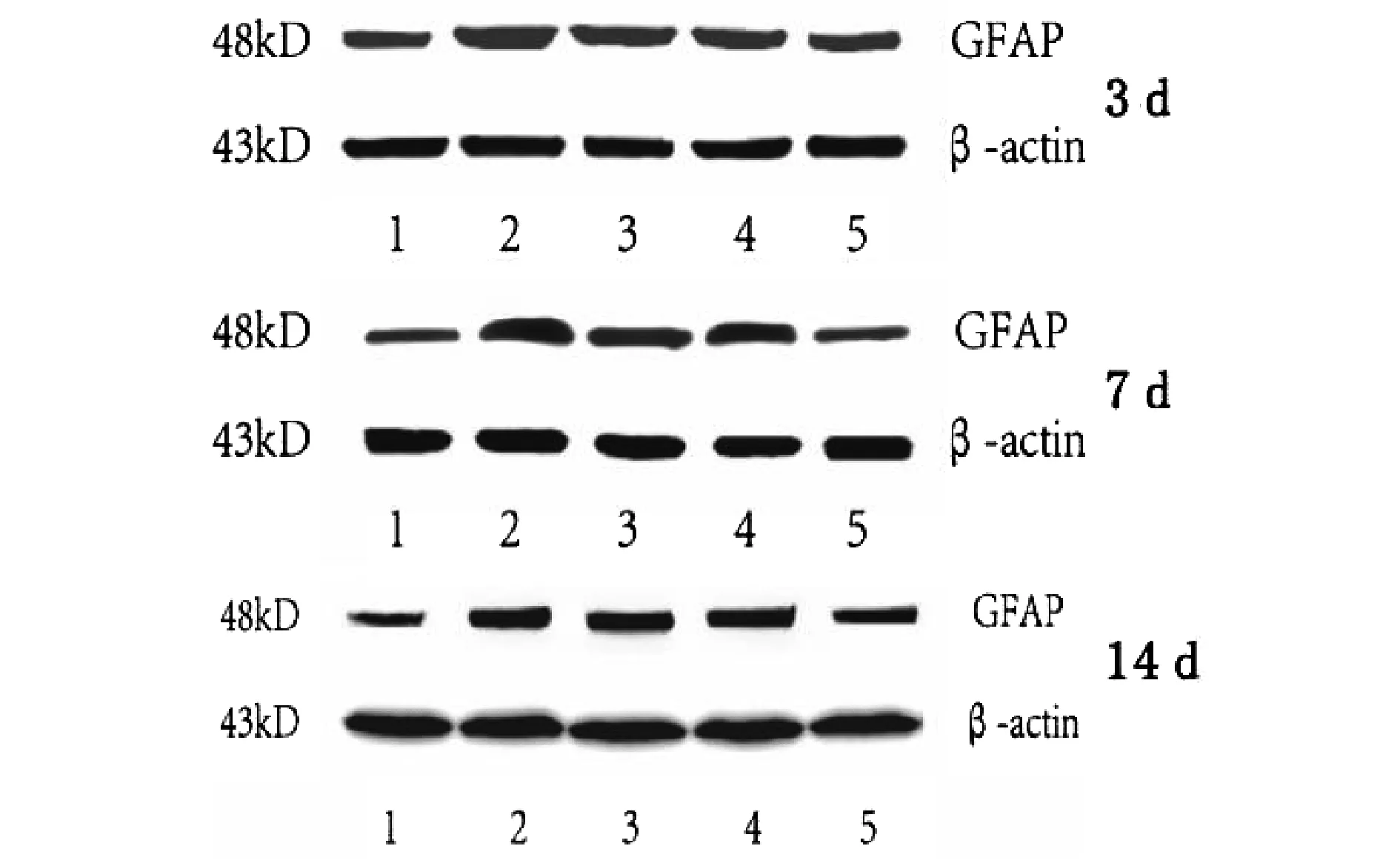
电针联合身痛逐瘀胶囊改善慢性坐骨神经损伤模型大鼠疼痛及对GFAP/p38MAPK信号通路的影响*
金 弘,刘婷婷,刘树民,陈英华,孙晓伟,祝鹏宇
(1.黑龙江中医药大学附属第一医院,黑龙江 哈尔滨 150040; 2.黑龙江中医药大学,黑龙江 哈尔滨 150040;3.黑龙江中医药大学附属第二医院,黑龙江 哈尔滨 150001)
神经病理性疼痛(Neuropathic pain, NP)主要临床特征为痛觉过敏、自发性疼痛和痛觉超敏,多是由于疾病引起躯体感觉神经系统受损而发病[1]。临床常见于脊髓损伤等中枢神经系统损伤和坐骨神经急慢性压迫、糖尿病等引起的周围神经损伤[2]。神经病理性疼痛目前被普遍认为是一种难治性的疼痛状态,严重影响了患者的生活质量,并且给社会造成了沉重的经济负担。
神经病理性疼痛发病机制较为复杂,目前有报道外周及中枢敏化、痛觉受体表达上调、促炎因子释放和胶质细胞活化等机制均可能直接或者间接参与了其疼痛的发生和发展[3]。其中,神经胶质细胞活化被认为占据重要地位,当神经细胞受损时,神经胶质细胞通过相关受体表达而被激活,神经胶质纤维酸性蛋白(GFAP)过度释放,进而介导了神经活性物质及多种促炎细胞因子过度表达[4]。而p38MAPK信号通路被认为是神经病理性疼痛发病机制的关键因子之一,其活化后能够抑制痛觉信号传导,并且促进神经胶质细胞活化[5]。在前期研究中发现,电针联合身痛逐瘀胶囊能够显著改善神经病理性疼痛患者疼痛症状[6],为进一步观察GFAP/p38MAPK信号通路在电针联合身痛逐瘀胶囊镇痛作用中的机制,本研究拟建立慢性坐骨神经损伤(CCI)模型大鼠,观察不同治疗方法对大鼠疼痛及GFAP/p38MAPK信号通路相关因子表达的影响,为本疗法的临床应用提供坚实的理论依据。
1 材料与方法
1.1 实验动物与分组
采用随机数字表法将90只购自黑龙江中医药大学动物实验中心[动物合格许可证号:SCXK(黑)2008004]的健康清洁级雄性SDSD(Sprague Dawley)大鼠随机分为假手术组、模型组、电针组、中药组和针药组,大鼠体质量(250±30)g,每组根据干预时间点不同分为3个亚组,分别为3 d、7 d和14 d组,每个亚组共6只大鼠。大鼠购买后适应性饲养1周后开始实验,保证室温21~24℃,相对湿度50%~70%,室内12 h交替照明,除手术前禁食24 h外,其余时间大鼠自由进食和水。实验过程中对大鼠的处置均按照国际最新的实验动物使用和关怀指南进行。
1.2 主要实验仪器和试剂
1.2.1 仪器 大鼠热痛刺激仪(BME-410A型,中国医学科学院生物工程研究所,北京);电泳系统(042BR14167,BIO-RAD,美国);数码凝胶图像处理系统(Tanon-4100,天能科技,中国);华佗针灸针(苏州医疗设备厂,中国);电针仪(KWD-801,英迪,中国)。
1.2.2 试剂 GFAP(bs-0199R,北京博奥森);p-p38 MAPK(bs-0636R,北京博奥森);身痛逐瘀胶囊(规格:0.35 g/粒,黑龙江中医药大学中医药研究院,批号:20110513)。
1.3 动物模型制备
本研究所选择的模型是慢性坐骨神经损伤模型(CCI),参照Bennett等[7]的方法,大鼠术前禁食不禁水24 h,称重后按照0.35 mL/100 g的剂量用水合氯醛腹腔注射麻醉,待大鼠完全麻醉后,将其固定到自制的木板上,手术部位选择为左侧后肢大腿部,局部剃毛、备皮后用碘伏消毒,在大鼠股骨中上约1/3处切开,然后用眼科镊钝性分离肌肉及皮下筋膜,暴露坐骨神经主干后,用事先备好并消毒完成的铬制羊肠线(规格为4-0号)结扎坐骨神经干,以1.0 mm间距均匀结扎4道。术后缝合肌肉及皮肤,其中,假手术组仅暴露坐骨神经而不用羊肠线结扎,其余各组均按照上述方法结扎。术后待动物完全苏醒后观察其自发性疼痛行为学,观察其是否有过度的舔足、缩足、跛行和损伤侧后肢负重能力降低等自发性疼痛的表现;术后3 d对其进行机械缩足反射潜伏期测定,以上述结果较术前均显著且稳定的下降超过30%为模型建立成功的标志。
1.4 治疗方法
1.4.1 假手术组 手术仅暴露坐骨神经但不结扎,术后大鼠常规饲养,给予与中药组同体积的生理盐水灌胃,每日1次,未经其他任何治疗。
1.4.2 模型组 术后大鼠常规饲养,给予与中药组同体积的生理盐水灌胃,每日1次,未经其他任何治疗。
1.4.3 电针组 选穴:选择模型大鼠损伤侧环跳穴和阳陵泉穴。操作方法:将大鼠用自制的木板捆绑后,上述穴位局部及针具常规消毒,选择规格为0.25 mm×25 mm一次性无菌针灸针,快速将针刺入皮下,进针深度为5 mm[8]。然后将电针仪的正极和负极分别接到环跳穴和阳陵泉穴上,波形选择参照前期研究结果,选择疏密波,电针频率为2 Hz/100 Hz,然后调节控制电流的旋钮,以调节电针电流,直至大鼠下肢针刺局部肌肉轻微颤动,并且大鼠未剧烈挣扎,即为针刺电流大小,每次针灸治疗时间为30 min,每日针刺治疗1次。
1.4.4 中药组 中药给药的剂量参照前期研究结果[9],实验开始前制备身痛逐瘀胶囊药物混悬液,具体方法是取药粉1.64 g,加入0.9%氯化钠注射液并定容至100 mL,置于4℃冷藏保存备用。灌胃时,根据查阅文献及预实验结果,给予15 mL/kg给药容积灌胃,以确保疗效及实验动物能够耐受。每日灌胃1次。
1.4.5 针药组 给予电针和中药联合治疗,方法及疗程同电针组和中药组。
1.5 观察指标及检测方法
1.5.1 热缩足反射潜伏期的检查方法 本研究检测大鼠热缩足反射潜伏期(Thermal withdrawal latency,TWL)的方法是利用BME-410A型热辐射刺激仪对被检查大鼠足底进行照射[10],记录各组大鼠热缩足反射潜伏期,计算方法是以仪器开始照射至大鼠出现回避所用时间即为其TWL,实验过程中,事先将大鼠置于箱内适应30 min,确保箱内温度保持恒定,以免影响实验结果。为了减少误差,研究过程中对每只大鼠TWL检测3次,每次照射间隔时间为25 s,计算每只大鼠3次数据的平均值,即为其热缩足反射潜伏期。
1.5.2 动物取材及检测 实验动物在各时间点检查完机械缩足反射阈值后,称重后按照0.35 mL/100 g的剂量用水合氯醛腹腔注射麻醉,暴露左心室,用20 mL注射器插入左心室,剪开左心耳,多聚甲醛灌注至肺脏变白后取出长度约为1.5 cm的L4~L6段脊髓组织,置于1.5 mL冻存管中,液氮冻存后置于-80℃冰箱备用。Western blot检测时称取100 mg置于-80 ℃冻存的脊髓组织,经裂解、研磨和离心等步骤提取总蛋白,BCA法测定蛋白浓度,制备蛋白质上样样品,电泳电压和时间分别为浓缩胶80 V,30 min;分离胶120 V,60 min;转膜后37℃水浴震荡1 h封闭,根据各抗体说明书按比例将一抗稀释,将膜放入一抗中,在4 ℃条件下孵育过夜;取出膜后,用TBST清洗5 min×3次,加入HRP标记的二抗,稀释比例为1∶2 000,在37 ℃条件下孵育1 h,然后以TBST清洗10 min×3次。最后经ECL发光液曝光,并采用quantity one分析软件分别测量目的蛋白和内参蛋白的灰度值,以两者的比值即为目的蛋白的相对表达量。
1.6 统计学处理
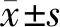
2 实验结果
2.1 各组大鼠热缩足反射潜伏期检测结果
结果表明,模型组大鼠TWL明显低于手术之前,术后3 d、7 d和14 d 3个时间点均较假手术组显著降低,差异具有统计学意义(P<0.05);电针组、中药组及针药组给予相应治疗后,坐骨神经慢性压迫模型大鼠TWL显著升高,术后3 d、7 d和14 d 3个时间点均较模型组显著升高,差异具有统计学意义(P<0.05);针药组大鼠TWL显著升高,术后3 d、7 d和14 d 3个时间点均较电针组和中药组显著升高,差异具有统计学意义(P<0.05)。详见表1。
2.2 各组大鼠脊髓组织GFAP蛋白表达
结果可见,模型组大鼠GFAP在脊髓组织中的表达在术后3 d、7 d和14 d 3个时间点均较假手术组降低,差异具有统计学意义(P<0.05);电针组、中药组及针药组给予相应治疗后,坐骨神经慢性压迫模型大鼠GFAP在脊髓组织中的表达各时间点均较模型组显著升高,差异具有统计学意义(P<0.05);针药组大鼠GFAP在脊髓组织中的表达各时间点均较电针组及中药组显著升高,差异具有统计学意义(P<0.05)。详见表2、图1。
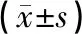
表1 各组大鼠TWL检测结果
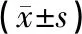
表2 各组大鼠GFAP相对表达量检测结果
注:1.假手术组;2.模型组;3.电针组;4.中药组;5.针药组。图1 各组CCI模型大鼠脊髓组织GFAP蛋白表达
2.3 各组大鼠脊髓组织p-p38蛋白表达
结果可见,模型组大鼠p-p38在脊髓组织中的表达在术后3 d、7 d和14 d 3个时间点均较假手术组显著降低,差异具有统计学意义(P<0.05);电针组、中药组及针药组给予相应治疗后,坐骨神经慢性压迫模型大鼠p-p38在脊髓组织中的表达各时间点均较模型组显著升高,差异具有统计学意义(P<0.05);针药组大鼠p-p38在脊髓组织中的表达各时间点均较电针组及中药组显著升高,差异具有统计学意义(P<0.05)。详见表3、图2。

注:1.假手术组;2.模型组;3.电针组;4.中药组;5.针药组。图2 各组CCI模型大鼠脊髓组织p-p38蛋白表达

表3 各组大鼠脊髓组织p-p38蛋白表达量检测结果
3 讨论
CCI模型是目前用于研究神经病理性疼痛较为常用的模型之一,大鼠造模成功后,其病理改变与坐骨神经痛较为相似,因此是研究中医学中“痹症”“腰腿痛”[11]等疾病理想的动物模型。该类疾病在中医学典籍中有记载,对其症状的描述与现在临床所见也较为一致,针灸疗法是医籍记载中治疗“腰腿痛”的重要方法之一,可追溯到《黄帝内经》中。由坐骨神经慢性压迫所导致的神经病理性疼痛,临床表现为腰部压痛或不自主疼痛,并常伴有沿着坐骨神经分布区域的放射性疼痛为主,最典型的表现就是臀部、大腿以及小腿后外侧疼痛。《灵枢·经脉》篇记载,足太阳膀胱经循行过程中,支脉经过髀枢后,沿着髀外后廉到达腘中,下贯踹内;而足少阳胆经直行的经脉下合髀厌中,向下经过髀阳,出于膝外廉,下行至外辅骨之前,向下到达绝骨之端,下出外踝之前。因此,中医学理论认识到可以选择足太阳膀胱经和足少阳胆经的穴位治疗该病。至现代,越来越多的研究采用数据挖掘的方法探讨临床常见疾病针灸选穴及处方规律,结果也提示足太阳膀胱经和足少阳胆经的穴位使用频率较高[12]。现代医学一直致力于经络实质的研究,其中,经络系统与神经系统相似性较高的理论占有重要地位,在人体足太阳膀胱经和足少阳胆经巡行部位下可见坐骨神经主干及其分支分布,而足太阳膀胱经和足少阳胆经的穴位较多分布在上述神经的体表投影之上[13]。在上述两经的穴位中,环跳穴与阳陵泉穴不论是从中医临床还是现代解剖学研究角度看均为治疗本病重要穴位,环跳穴为足少阳和足太阳经交会穴,定位于臀外侧部,针刺能疏通两经经气,其深部正当坐骨神经,主治腰腿疼痛,《针灸甲乙经》云:“腰胁相引痛急……胫痛不可屈伸……环跳主之。”环跳穴解剖结构依次经皮肤、皮下组织和臀大肌到达深部坐骨神经,针刺能够调节坐骨神经功能,减轻疼痛症状。阳陵泉穴为合穴、胆经下合穴及八会穴之筋会,其下为腓总神经分支,针刺能调节足少阳经经气。
GFAP是仅存在于中枢神经系统星形胶质细胞中的一种中间丝蛋白,可以作为星形胶质细胞活化的标志物。而星形胶质细胞活化又会引起机体炎症因子等一系列反应,有研究发现,神经病理性疼痛模型中GFAP表达升高能够诱发TNF-α等炎症因子表达上调[14-15]。因此,本研究选择GFAP作为观察电针联合身痛逐瘀胶囊镇痛作用的观察指标。p38MAPK 信号通路激活通过外周机制参与神经病理性疼痛主要是通过与受损神经细胞进行直接或者间接耦联,使受损神经细胞的传入神经元异常放电被抑制,从而降低受损神经纤维末梢伤害性感受器异常升高的兴奋性[16]。而p38MAPK信号通路激活通过中枢机制参与神经病理性疼痛主要是能够抑制痛觉信号的传导、神经胶质细胞的活化以及异常兴奋的神经元的可塑性。主要通过减少脊髓背角兴奋性神经递质的释放、增强对受损神经纤维相应节段脊髓背角神经元的抑制等发挥作用。由此可见,p38MAPK/GFAP信号通路相关指标可能是神经病理性疼痛发生过程中的关键因子。
本研究结果显示,模型组大鼠各时间点TWL值较假手术组显著降低(P<0.05);电针组、中药组及针药组各时间点TWL较模型组显著升高(P<0.05);针药组大鼠各时间点TWL较电针组和中药组显著升高(P<0.05)。Western blot检测结果表明,模型组大鼠各时间点GFAP、p-p38MAPK蛋白表达较假手术组显著降低(P<0.05);电针组、中药组及针药组各时间点GFAP、p-p38MAPK蛋白表达较模型组显著升高(P<0.05);针药组大鼠各时间点GFAP、p-p38MAPK蛋白表达较电针组和中药组显著升高(P<0.05)。上述结果表明,慢性坐骨神经损伤后脊髓组织中GFAP、p-p38蛋白表达升高,可能参与了神经病理性疼痛的发生过程;给予电针、中药以及针药联合治疗均能显著抑制脊髓组织GFAP、p-p38蛋白表达,其中,尤以针药组疗效更为显著。综上所述,电针联合身痛逐瘀胶囊能够减轻CCI模型大鼠疼痛反应,其机制可能与下调脊髓组织中GFAP和p-p38MAPK蛋白表达有关。

