氮杂环丙烷参与的1,3-偶极环加成反应研究进展
赵 森
(荆州职业技术学院 湖北 荆州 434020)
氮杂环丙烷的参与的环加成反应是在许多生物活性天然产物和药物中获得作为核心结构骨架的各种含氮杂环的有力策略。适用于各种含氮环状化合物的合成,因为它很容易作为1,3-偶极合成子与各种亲偶极物反应,氮杂环丙烷的高反应性归因于它易于形成1,3-偶极子由路易斯酸介导的中间体。氮杂环丙烷是最小的环状应变含N杂环化合物,在有机合成中得到了广泛的研究。
一、路易斯酸催化的氮杂环丙烷环加成反应
(一)路易斯酸催化的氮杂环丙烷环加成反应合成咪唑类化合物
1991年,Jin-Ook Baeg和Howard Alper报道了,双(苄腈)二氯化钯是氮杂环丙烷与碳二亚胺的环加成反应形成咪唑啉亚胺的有效催化剂,产率为40-94%[1]。该方法是区域特异性的,涉及更多取代的环碳-氮键的裂解。其中一个咪唑啉基亚胺的X射线结构确定,以及所有环加成反应产物的光谱和分析数据,为结构分配提供了基础。

图1
2017年,Pinaki Bhusan De等人报道了铜催化的2-烷基-/2-芳基氮杂环丙烷与苯并咪唑的交叉偶联[2]。该反应涉及氮杂环丙烷与苯并咪唑的区域特异性开环,得到苯并咪唑基乙胺衍生物,其导致C(sp2)-H和N-H键之间的脱氢交叉偶联,产生二氢咪唑并咪唑。光学活性的2-芳基氮杂环丙烷可以立体可逆地交叉偶联,具有高对映体纯度(77-97%ee)。这些需氧催化体系在中等温度下包含廉价的Cu(II)盐和PCy3配体。

图2
(二)路易斯酸催化的氮杂环丙烷环加成反应合成吡咯类化合物
2009年Paul A.Wender和Daniel Strand报道了由路易斯(AgSbF6)或布朗斯台德酸催化的氮杂环丙烷和非活化的炔之间的正式[3+2]环加成反应,得到了2,3-二氢吡咯[3]。该反应温和条件下进行,可扩展多种底物,使用缓慢的催化剂负载,高度区域选择性,得到提供多种多取代的二氢吡咯。

图3
2009年,Jinmin Fan等人通过使用FeCl3催化的氮杂环丙烷与芳基炔的反应,构建了一系列新的高官能化的2-吡咯啉,其中涉及芳基取代的链烯基阳离子[4]。
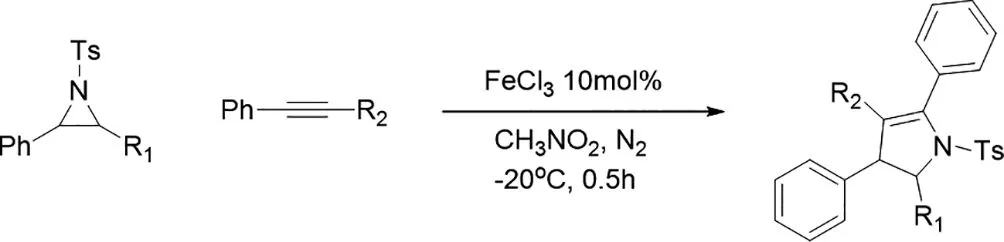
图4
2010年,Matthew Brichacek等人报道了铜催化剂催化的手性乙烯基氮杂环丙烷可以立体特异性地环扩展的反应[5]。该合成方法以具有适当几何形状的氮杂环丙烷作为起始材料,控制获得手性2,5-顺式-或2,5-反式-3-吡咯啉产物。得到了二十三个环扩展实例,其中大多数具有立体特异性环化。

图5
2015年Linqing Wang等人通过原位产生的镁催化剂介导内消旋-氮杂环丙烷和C3-烷基吲哚之间的不对称形式[3+2]-环加成,合成不对称吡咯并吲哚啉的衍生物。通过在易于制备的非手性配体的帮助下使用市售的配体,可以获得多种吡咯并吲哚啉[6]。
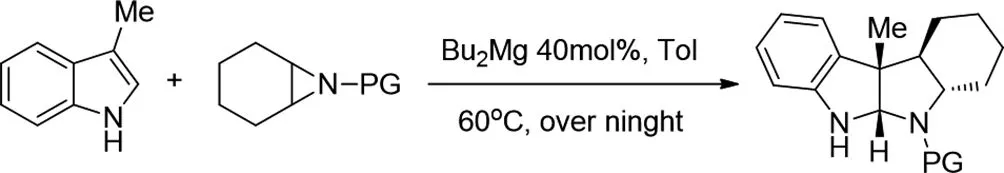
图6
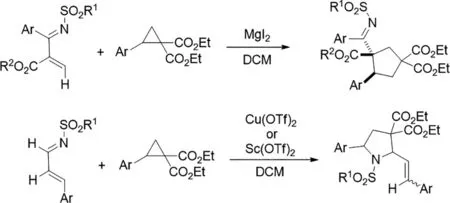
图7
2018年,Pei-Jun Yang等人提出了第一路易斯酸([(CH3CN)4Cu]PF6)催化的外消旋2-(杂)芳基-N-磺酰基氮杂环丙烷经C-N键与亲核试剂裂解的立体聚合转化[8]。这包括[异]芳香醛和1,3-二取代吲哚的[3+2]环加成反应,与富电子(杂)芳烃的不对称Friedel-Crafts型反应,以及与胺的不对称氨解反应,为手性1,3-异恶唑烷,吡咯并吲哚啉,2-(杂)芳基苯乙胺和邻位二胺的合成提供了可靠途径。基于对照实验的结果,提出了涉及外消旋氮杂环丙烷的I型动态动力学不对称转化(DyKAT)的机理。
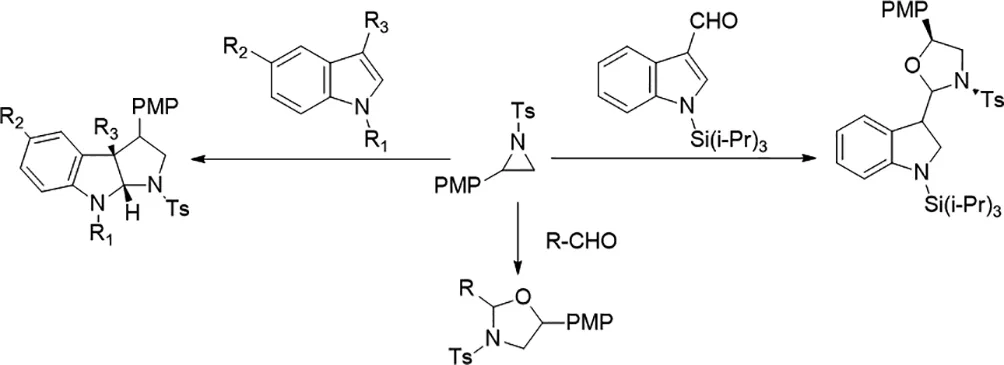
图8
2018年,Mateo Alajarin等人通过相应的Yb(OTf)3和Y(OTf)3产生的N-芳基-C,C-二苯基乙烯亚胺与金属羰基和金属-甲亚胺叶立德的有效[3+2]环化促进了碳-碳键杂化[9]。已经完成了供体-受体环氧乙烷和氮杂环丙烷在温和条件下进行反应,得到了结构上复杂的恶唑烷和吡咯烷衍生物,这是一种区域选择性构建该化合物的方法。此外,加热N-芳基-C,C-二苯基乙烯亚胺和2,3-二羧酸二乙基己酯的混合物得到咪唑烷衍生物。通过计算研究这些[3+2]环加成的反应机理。
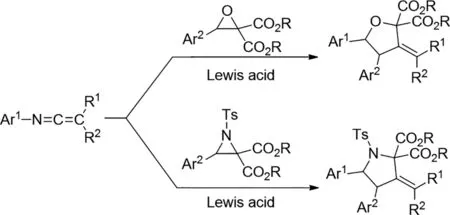
图9
(三)路易斯酸催化的氮杂环丙烷环加成反应合成苯胺类化合物
2014年,Ke Gao等人发现发现钴-N-杂环卡宾催化剂通过开环烷基化促进2-芳基吡啶与1,2-二芳基氮杂环丙烷的邻C-H官能化[10]。该反应在温和的室温条件下产率良好,得到了带有2-氨基官能团的1,1-二-芳基甲烷。
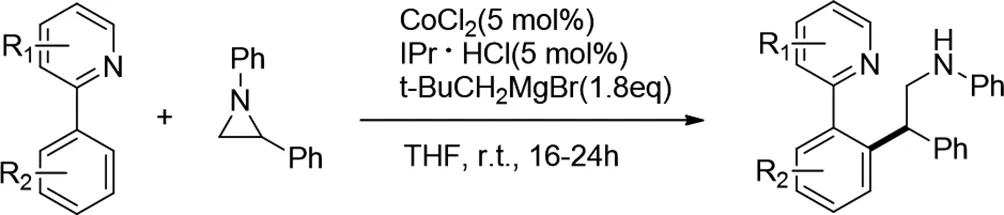
图10
(四)路易斯酸催化的氮杂环丙烷环加成反应合成恶唑类化合物
1995年,Jin-Ook Baeg等人发现了含有适当取代基的1,2,3-三取代的氮杂环丙烷,可以与杂环戊烯在Pd(II)的催化下反应,得到五元环杂环[11]。该反应具有较高的区域选择性和立体特异性,保留了氮杂环丙烷环中取代基的立体化学结构。1,2-二取代的氮杂环丙烷与杂环戊烯反应,得到相应的手性五元环杂环,反应在保持构型的情况下进行。
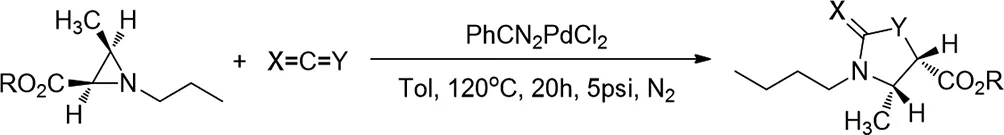
图11
2005年,Takeshi Munegumi等人发现,在镍催化剂存在下,氮杂环丙烷与异氰酸酯进行环加成反应,并分离出五种亚氨基恶唑烷衍生物[12]。在NiI2存在下反应时最佳。加长反应的时间,NiI2催化亚氨基恶唑烷异构化,生成相应的咪唑烷酮衍生物。

图12
2017年,Xingxing Wu等人报导了由Ni(II)-二恶唑啉络合物催化的N-甲苯磺酰亚胺和醛的非对映和对映选择性形式[3+2]环加成反应。获得的1,3-恶唑烷产物具有高非对映选择性,良好的收率(高达99%)[13]。通过手性转移方法实现具有挑战性的远距离立体声中心控制。
换油周期的延长,对润滑油的剪切稳定性提出了挑战。此次展会,阿朗新科还将介绍其针对这一市场变化推出的Keltan OCP极强稳定性的牌号K0500R。该牌号是无定形OCP黏指剂,具有优异的低温性能,其剪切稳定指数(SSI)为18,符合当前市场的最新技术发展要求。目前,阿朗新科正在积极与润滑油行业内的标杆企业选用K0500R开展长寿命柴油机油行车实验。
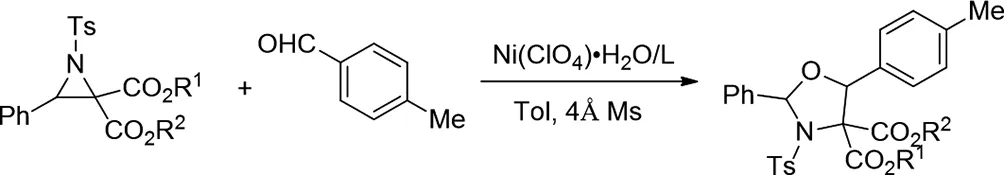
图13
2017年,Sunatda Arayachukiat等人使用过渡金属配位化合物作为路易斯酸和亲核助催化剂的双催化体系,开发了从相应的N-甲苯磺酰基嘧啶和CO2区域选择性合成N-甲苯磺唑烷酮的有效方法[14]。在筛选的路易斯酸时,无卤素的五乙醇铌(Nb(OEt)5在四丁基碘化铵(TBAI)存在下显示出最佳的催化活性。由催化实验支持的系统DFT计算表明,CO2插入是该过程的速率决定步骤,并且它高度依赖于铌中心的空间位阻。
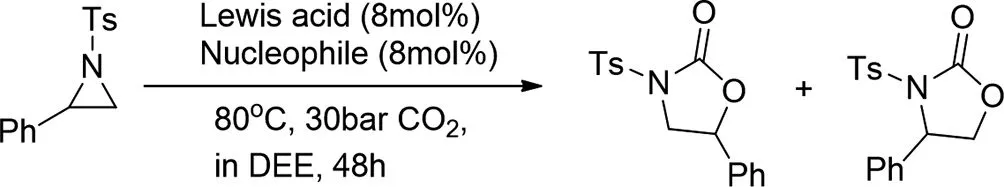
图14
(五)路易斯酸催化的氮杂环丙烷环加成反应合成恶嗪类化合物
2018年,Honglei Liu等人报道了Ni-催化的[8+3]环加成的庚三烯酮与2-芳基-N-甲苯磺酰胺在温和的反应条件下顺利进行,得到各种4-甲苯磺酰基-2,3,4,4a-四氢环庚[b]-[1,4]恶嗪衍生物,产率适中至优异[15]。

图15
2018年,Abhijit Mal等人通过路易斯酸催化的Sn2型开环活化的氮杂环丙烷与2-卤代苯酚,然后在一锅条件下以逐步方式进行Cu(I)催化的分子内C-N环化,得到3,4-二氢-1,4-苯并恶嗪衍生物,产率高(高达95%)[16]。该策略为(S)-3甲基-1,4-苯并恶嗪(S)-3v提供短而有效的合成,后者是左氧氟沙星合成中的后期中间体。该方法有效且简单,具有优异的对映和非对映特异性(ee>99%,de>99%)。
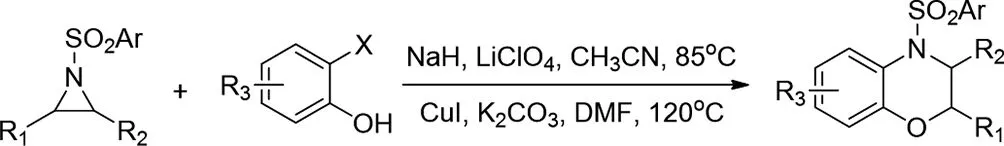
图16
(六)路易斯酸催化的氮杂环丙烷环加成反应合成恶二嗪类化合物
2015年,Stalin R.Pathipati等人报道了高选择性路易斯酸催化的三元杂环与硝酮的环加成反应[17]。使用Al或In催化剂,使用环氧乙烷,氮杂环丙烷和硫杂环丁烷作为底物用于合成各种六元杂环。该催化方案显示出广泛的底物范围,并且在温和的反应条件下以高产率和优异的选择性提供了获得新结构基序的途径。
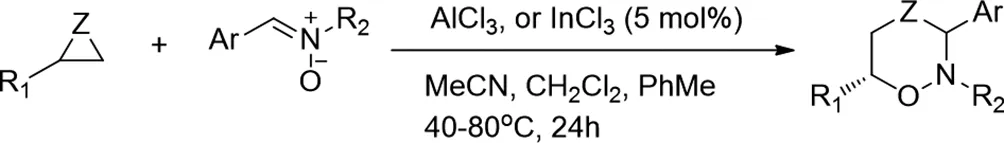
图17
(七)路易斯酸催化的氮杂环丙烷环加成反应合成哒嗪类化合物
2018年,Alexey O.Chagarovskiy等人报道了两种不同三元环的(3+3)-环化的第一个实例。发现与二氮杂环丙烷反应的供体-受体环丙烷在温和路易斯酸(Ni)催化下以高产率和非对映选择性提供全氢哒嗪衍生物[18]。该反应适用的底物范围广泛,并表现出优异的官能团耐受性。
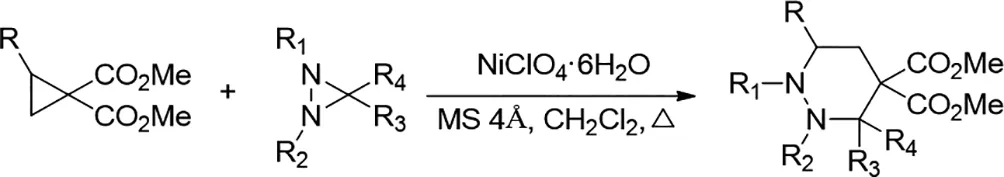
图18
(八)路易斯酸催化的氮杂环丙烷环加成反应合成吡嗪类化合物
2018年,Bijay Ketan Das等人报道了,具有炔丙基胺的立体特异性Cu催化的N-磺酰基氮杂环丙烷开环,亲核加氢胺化得到哌嗪,双键异构化以提供四氢吡嗪[19]。光学活性的氮杂环丙烷可以与高对映体纯度(>98%ee)交叉偶联。
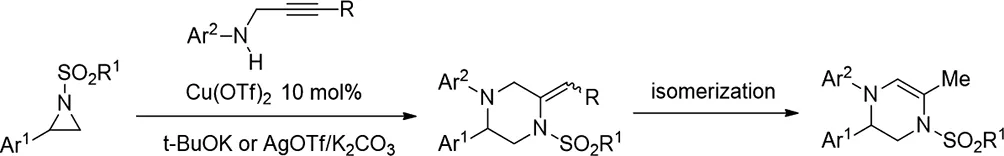
图19
(九)路易斯酸催化的氮杂环丙烷环加成反应合成氮杂卓类化合物
2014年,Ming-Bo Zhou开发了一种合成氮杂环庚烷衍生物(一种典型的七元杂环系统)的实用方法,该方法涉及使用六氟锑酸催化氮杂环丙烷与两个炔的正式[3+2+2]环加成反应[20]。该方法适用于两种相同或不同的末端炔烃,用于[3+2+2]环加成与未活化的氮杂环丙烷,并提供相应的吖庚因衍生物,产率高,具有良好的化学和区域选择性。

图20
(十)路易斯酸催化的氮杂环丙烷环加成反应合成哌嗪类化合物
2012年,Piera Trinchera等人报道了通过在催化量的路易斯酸(MgBr2)使未活化的N-烷基芳基氮杂环丙烷反应,直接合成顺式和反式2,5-二取代的N,N-二烷基哌嗪对映体的反应。并经立体化学和核磁共振研究揭示这一过程的机制[21]。

图21
(十一)路易斯酸催化的氮杂环丙烷环加成反应合成噻唑烷类化合物
2016年,Mani Sengoden等人报道了,Al(salen)Cl有效地催化未活化的手性氮杂环丙烷与异硫氰酸酯的对映特异性(3+2)环加成,在室温下提供94-99%ee的官能化亚氨基噻唑烷。使用铝路易斯酸作为催化剂,高对映体纯度,温和的反应条件,宽的底物范围和高原子经济性是重要的实用特征[22]。

图22
(十二)路易斯酸催化的氮杂环丙烷环加成反应合成噻嗪类化合物
2017年,Rohit Kumar Varshnaya和Prabal Banerjee报道了路易斯酸(MgI2)催化N-甲苯磺酰基二羧酸酯和环氧乙烷的[3+3]环化,原位生成的巯基醛用于合成官能化的噻嗪和氧杂噻吩衍生物的方法[23]。另外,该方法通过去甲基化和Krapcho单羧化促进噻嗪的衍生化。
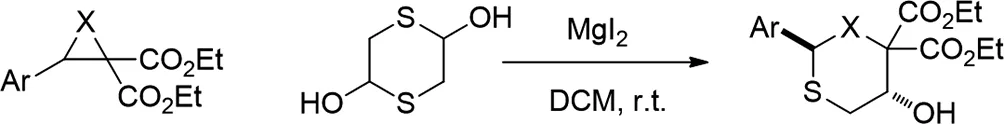
图23
2018年,Murugan Vijay等人用1,4-二噻烷-2,5-二醇制备了N-磺酰基氮杂环丙烷的多米诺双催化C-N/C-S键,在室温下得到3,4-二氢-1,4-噻嗪[24]。使用Bi(OTf)3作为催化剂,原子经济性和区域选择性是重要的实用特征。

图24
(十三)路易斯酸催化的氮杂环丙烷环加成反应合成异喹啉类化合物
2018年,Sang Gyu Lee和Sung-Gon Kim报道了供体受体氮杂环丙烷与N,N-二烷基-3-乙烯基苯胺的路易斯酸催化的[3+3]环加成反应,用于立体选择性合成四氢异喹啉(THIQ)[25]。使用Gd(OTf)3作为路易斯酸催化剂进行的反应对各种N-甲苯磺酰氮杂环丙烷和N,N-二烷基-3-乙烯基苯胺底物具有耐受性,并且通常以高产率获得高官能化THIQ,具有好的非对映选择性。
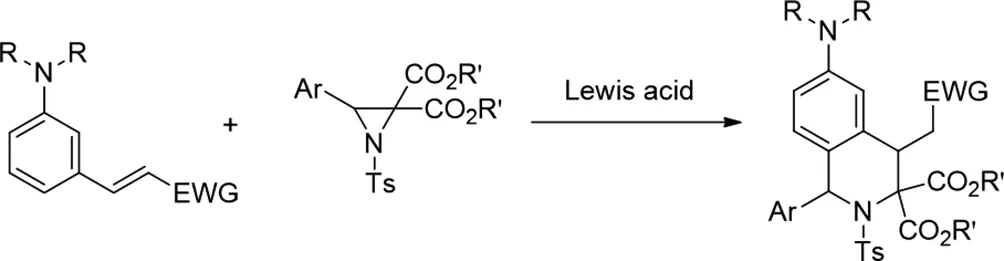
图25
2019年Seungyeon Kim和Sung-Gon Kim使用Mg(OTf)2/双恶唑啉催化剂建立了供体-受体氮杂环丙烷与N,N-二烷基-3-乙烯基苯胺的非对映体和对映体选择性[3+3]环加成反应[26],得到了高官能化的四氢异喹啉。各种N,N-二烷基-3-乙烯基苯胺,如m-N,N-二甲基氨基苯基α,β-不饱和苯基酮和3-(mN,N-二甲基氨基苯基)丙烯酸酯,以及供体受体N-甲苯磺酰基嘧啶,已应用于这种不对称催化方案。

图26
(十四)路易斯酸催化的氮杂环丙烷环加成反应合成咔啉类化合物
2017年,Masthanvali Sayyad等人报道了,通过激活的氮杂环丙烷开环化(DROC)与2-乙烯基吲哚环合成具有优异立体选择性(de,ee至>99%)的各种1,4-二取代四氢-β-咔啉衍生物[27]。该反应通过LiClO4催化的Friedel-Crafts型烷基化2-乙烯基吲哚与活化的氮杂环丙烷,然后以多米诺骨牌方式进行分子内氮杂-迈克尔反应。

图27
(十五)路易斯酸催化的氮杂环丙烷环加成反应合成哌啶类化合物
2017年,Yizhou Zhan等人报道了在氮杂环丙烷2,2-二酯和共轭二烯之间的新型路易斯酸(三氟甲磺酸钪)催化的[3+2]分子内交叉环加成(IMCC)[28]。这是第一个具有碳=碳双键的偶氮甲碱叶立德分子内1,3-偶极环加成的区域特异性IMCC,并为构建结构复杂和多样化的氮杂[n.2.1]骨架提供了一种通用且有效的策略。[3+2]IMCC可在温和条件下以克规模进行。更重要的是,3-烷基取代的氮杂环丙烷也是成功的。优异的结构多样性,简便的操作和多样化的后修饰将支持[3+2]IMCC在天然产物合成和药物发现中的应用。
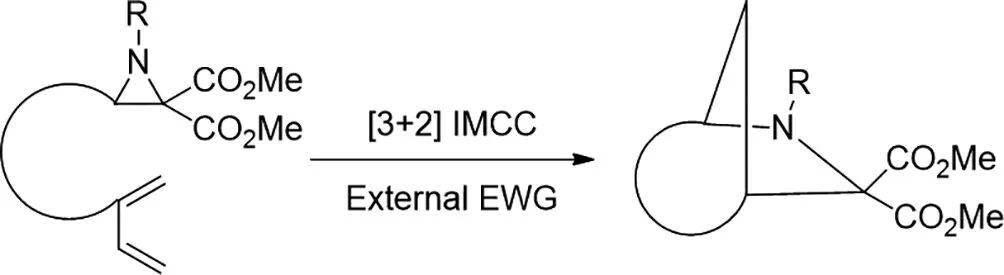
图28
二、金属卟啉配合物催化的氮杂环丙烷的偶极环加成反应
2017年,Xun Wang等人报道了一种新的多孔金属-金属卟啉骨架MMPF-10,由一种八角形卟啉配体构成,该配体连接铜桨轮单元,形成具有强渗透力的拓扑结构的骨架[29]。卟啉配体的原位金属化为MMPF-10提供了两个独特的可接近的Cu(II)中心。这使得它在首次报道的CO2与氮杂环丙烷的反应中表现为有效的路易斯酸催化剂,以合成由MMPF催化的恶唑烷酮。
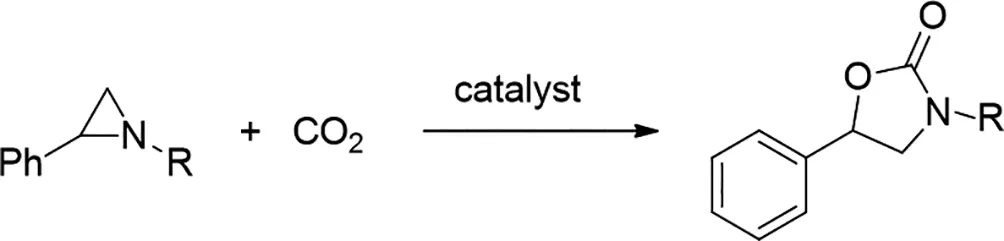
图29
2019年,Satoru Teranishi等人报道了有效的铁卟啉路易斯酸催化的氮杂环丙烷与醛的环加成反应[30],以提供具有高区域和非对映选择性的恶唑烷。该反应在25℃下,甲苯中与1mol%的铁催化剂一起进行。基于理论研究和基于同步加速器的X射线吸收精细结构测量提供了对氮杂环丙烷-铁卟啉络合物的基本见解,该络合物是产生1,3-偶极合成子的关键中间体。
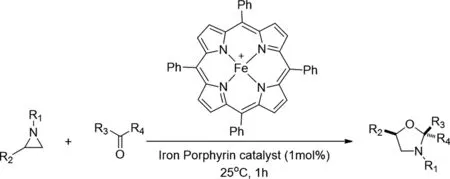
图30
三、热反应导致氮杂环丙烷开环发生的环加成反应
氮杂环丙烷的骨架结构为键角接近60o的三元环,这种结构的环张力非常大,在加热的条件下即可开环,得到甲亚胺叶立得离子,从而与其他化合物进行反应。很多科学家基于这种理论对氮杂环丙烷的环加成反应进行了探索。
(一)热反应氮杂环丙烷环加成合成吡咯类化合物
1986年,Wayne K.Anderson等人报道了由甲硅烷基亚胺盐或氮杂环丙烷或2H-氮杂环丙烷经1,3-偶极环加成反应,合成了一系列双[(氨基甲酰氧基)甲基]吡咯啉衍生物[31]。将吡咯啉的抗肿瘤活性与相应的吡咯进行比较。除C-2-偕二甲基取代的吡咯啉外,其他几种衍生物均具有抗癌活性。
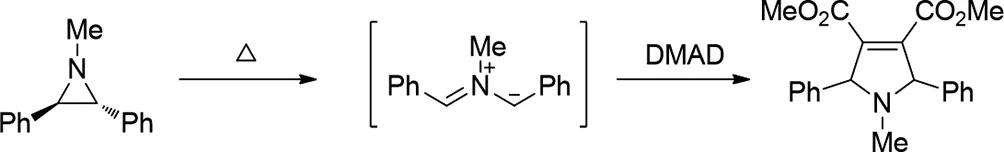
图31
2014年,Alexander F.Khlebnikov等人报道了,量子化学计算1-甲基-2,3-二苯基-和1,2,3-三苯基氮杂环丙烷的热开环,形成相应的S-,U-和W-型甲亚胺叶立德以及使用PCM溶剂化模型,在DFT B3LYP/6-31G(d)理论水平下进行它们对乙炔二甲酸二甲酯(DMAD)和2,3-二氰基-2-丁二酸二Jinmin Fan甲酯的环加成反应。计算完全符合实验结果,并解释了根据亲偶极子和内鎓盐中的取代基从协同路径到非协同路径的转换。发现在亲偶极物中,例如在二氰基丁二酸二烷基酯中,强吸电子取代基显着降低了偶氮甲碱叶立德与这种偶极子反应中形成两性离子中间体的阻隔性。这可以使逐步循环加载与协同循环加速竞争。然而,甚至对具有几个吸电子取代基的亲偶极物的环加成的一致性受到叶立德和亲偶极物对应物中电子和空间效应的精细平衡的支配。假设在偶氮甲炔叶立德中引入取代基使相应两性离子中的正电荷不稳定将有利于协同环加成,即使用二烷基二氰基丁二酸酯也在理论上和实验上进行了测试[32]。

图32
(二)热反应氮杂环丙烷环加成合成噻唑烷类化合物
2009年,Grzegorz Mloston′等人报道了,反式-1-甲基-2,3-二苯基氮杂环丙烷(反式-1a)与芳族和环脂族硫代酮2,在沸腾的甲苯中,得到相应的顺式-2,4-二苯基-1,3-噻唑烷顺式-4,该反应是通过反式-1a的开环旋转得到中间体(E,E)-配位的甲亚胺叶立德3a的[2+3]-环加成反应(方案1)。顺式-1a与乙炔二羧酸二甲酯(5)的类似反应得到反式-2,5-二氢-1-甲基2,5-二苯基吡咯-3,4-二甲酸酯(反式-6)。另外,顺式-1a和反式-1a与二氰基富马酸二甲酯(7a)以及顺式-1a和二氰基马来酸二甲酯(7b)的反应产生相同的两种立体异构体二甲基3,4-二氰基的混合物。3,4-二氰基-1-甲基-2,5-二苯基吡咯烷-3,4-二羧酸酯8a和8b。相反,顺式-1,2,3-三苯基氮杂环丙烷(顺式-1b)和7a仅得到一个立体异构的吡咯烷-3,4-二羧酸酯10,具有基于轨道对称性控制预期的构型,即通过协同反应步骤[33]。
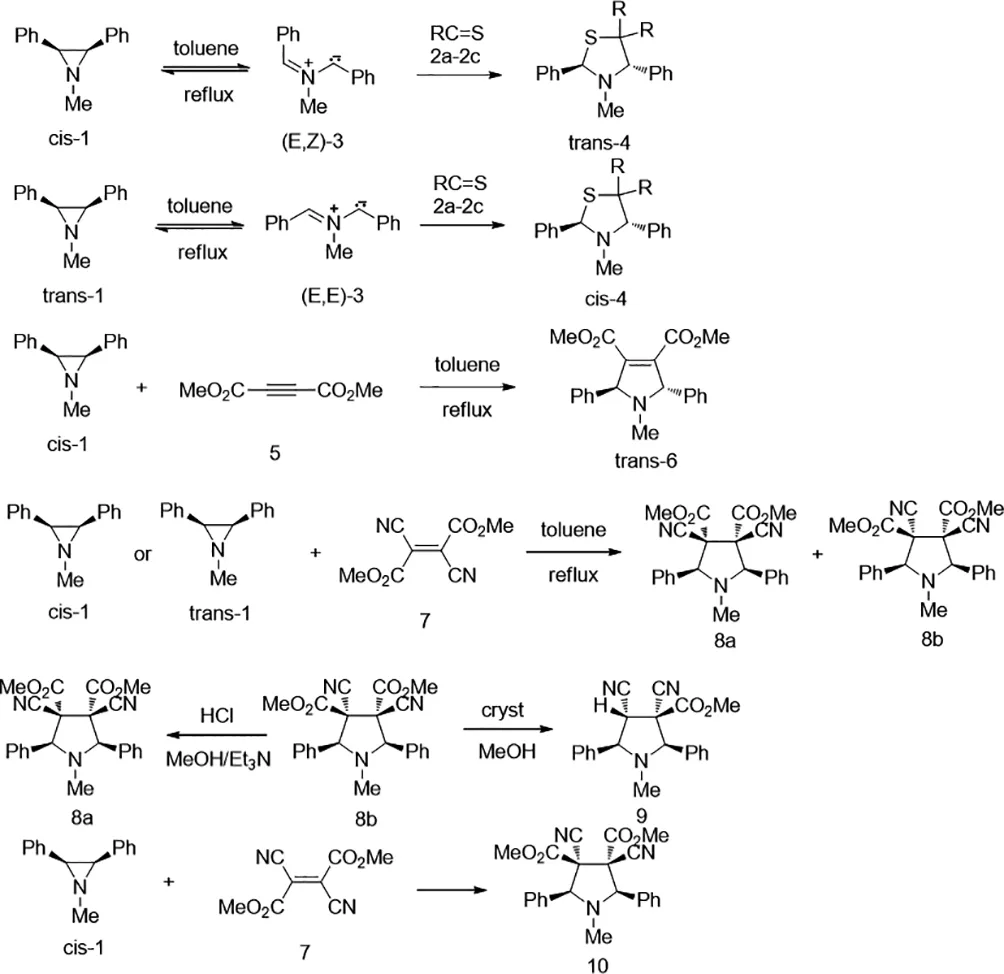
图33
(三)热反应氮杂环丙烷环加成合成1,3-二氧戊环-2-酮类化合物
2011年,Hui Zhou等人报道了使用3-巯基丙基三甲氧基硅烷作为硅烷偶联剂,使1,3-双-(4-烯丙基-2,6-二异丙基苯基)咪唑氯化物与MCM-41反应,合成N-杂环卡宾(NHC)官能化MCM-41及其CO2。通过与CO2的反应进一步合成2加合物(称为MCM-41-IPr-CO2)。原位漫反射红外傅立叶变换光谱(DRIFTS)用于研究MCM-41-NHC的可逆CO2捕获释放能力。MCM-41-IPr-CO2加合物被证明是一种有效的非均相催化剂,用于将CO2环加成到环氧化物或氮杂环丙烷中,在温和条件下具有优异的区域选择性。此外,由于CO2作为有效稳定在MCM-41上的NHC的保护基团,使得催化剂可以通过简单的过滤方法回收并重复使用多次而没有明显的活性损失[34]。

图34
(四)热反应氮杂环丙烷环加成合成恶唑烷类化合物
2011年,Jakob Danielsson等人描述了甲亚胺叶立德与醛的1,3-偶极环加成反应[35]。通过氮杂环丙烷的热电环开环产生的偶氮甲碱叶立德与醛发生1,3-偶极环加成反应得到了恶唑烷。随后将恶唑烷水解成相应的氨基醇,得到抗非对映异构体作为主要产物。

图35
(五)热反应氮杂环丙烷环加成合成咪唑烷类化合物
2016年,Mohamed Ali Tabarki和Rafaa Besbes报道了通过多种N-取代的异硫氰酸酯用于合成咪唑烷-2-硫酮的环加成反应,涉及N-烷基氮杂环丙烷-2-羧酸酯的环扩展[36]。后者通过完全区域和立体选择性过程进行开环和环化,得到目标反式-咪唑烷-2-硫酮,这取决于N-取代基对氮杂环丙烷和异硫氰酸酯的空间和电子效应。

图36

