中药血竭UPLC指纹图谱与主成分分析研究
魏荷琳 肖隆祥 封家福 吴亮


【摘要】血揭是传统中药,有进口血竭和国产血揭之分,但两者外观相似。为了准确鉴定两种血竭,以保证用药安全,本研究采用超高效液相色谱(UPLC)方法对5批进口血竭样品和5批国产血竭样品进行了分析,计算共有峰的相对保留时间(RRT)和相对峰面积(EPA)。通过中药色谱指纹图谱相似度评价系统对色谱数据进行相似度和主成分分析。结果证明,该UPLC方法具有良好的准确度、重现性和稳定性。进口血竭RRT的相对标准偏差(RSD)小于0.17%,国产血竭RRT的RSD小于0.06%,证明UPLC指纹图谱方法准确。进口血竭EPA的RSD为32.78-70.43%,国产血竭RPA的RSD为22.30-60.31%,说明血竭的化学成分的含量差异较大。相似度分析的结果显示,相同产地血竭的相似度较高,不同产地血竭的指纹图谱有明显差异;主成分分析能明显区分两种不同产地的血竭。本研究有助于不同来源血竭的准确鉴定,并为其质量评价与安全用药提供实验依据。
【关键词】血竭 超高效液相色谱 指纹图谱 主成分分析
血竭为传统中医活血化瘀名贵药,《本草纲目》以“麒鳞竭”为其正名。《纲目》云:“骐麟竭,木之脂液,如人之膏血,其味甘咸而走血;血竭除血痛,为活血之圣药是矣。”。《中国药典》(2015年版,1部)记载,血竭具有活由定痛,化疲生肌之功效,内服主要用于心腹瘀痛,外用主治跌打損伤等病症。目前,中国市售血竭有进口血竭和国产血竭两种:进口血竭来源于棕榈科黄藤属植物麒麟竭(Dae-monorops draco,RDD)果实渗出的树脂,国产血竭来源于百合科龙血树属植物剑叶龙血树(Dracaena cochinchinensis,RDC)茎干提取的树脂[。很显然,进口血竭和国产血竭的植物来源不同,两者化学组成是否具有差异,以及能否相互替代使用目前也还有诸多疑问。
中药指纹图谱技术是评价中药优劣、鉴别真伪、区分物种和确保其一致性和稳定性的有效方法。中药指纹图谱技术的理论体系和方法是解析中药的主导技术和实现中药现代化的核心力量,该体系理论和技术的成熟及完善可为现代中药创制提供强有力的理论和日支术支撑。随着现代分析技术的发展,中药指纹图谱技术在研究中药有效成分、控制中药质量以及鉴别方面越来越成熟,已得到国际上广泛的认可。
为明确区分两种不同植物来源的血竭,探索其活性成分,本研究应用超高效液相色谱(UPLC)对进口血竭及国产血竭的指纹图谱技术,通过中药色谱指纹图谱相似度评价系统对色谱数据对进口血竭和国产血竭进行相似度评价和主成分分析。
1 材料与方法
1.1 药材与试剂
5批进口血竭和5批国产血竭为市场收集,经乐山师范学院陈封政教授鉴定为麒麟竭Daemonorops draco果实以及剑叶龙血树Dracaena cochinchinensis茎干的树脂。
乙腈,甲醇和甲酸从Lab-scan (Bangkok,Thailand)购得,去离子水由Milli-Q水净化系统(Millipore,Bedford,MA,USA)获得。
1.2 仪器
1875HTAG TRU-SWEEP型超声波清洗机(Crest,New York,USA)、5810离心机(Eppendorf,Hamburg,Germany)、粉碎机(RT-04,Fargo,Taiwan)和Adventurer电子秤(OHAUS,USA)。 Waters AcquityUPLC超高效液相色谱仪配备真空脱气器、四级泵、自动取样器、柱温箱和紫外检测器。EPOWER PRO色谱工作站用于数据采集和处理。BEH C18柱(2.1mm×100mm,1.8μm)用于样品分离。
1.3 色谱条件
以0.1甲酸水溶液(A)和1%甲酸乙腈(B)为流动相,用UPLC梯度洗脱分离。流速为0.3mL/min;柱温设定为40oC,检测波民为280nm,进样量为1μL。梯度洗脱条件如下:0-8min,15-20% B;8-30min,20-68% B;30-30.5min,100% B;30.5-35min,100% B;35-35.5min,100-15% B;35.5-40min,15% B。
1.4 供试品溶液的制备
粉碎10批血竭样品,将粉末通过20目筛,在室温下真空干燥至恒重。取样品0.1g,精密称定置25mL离心管中,精密加入100%甲醇10mL,拧紧瓶盖混匀,在室温下超声萃取(功率270kw,频率40k Hz)30分钟,放冷,转移至离心机,于3500r/min条件下离心10min,冷却后,将上清液过滤转移到25mL容量瓶中,药渣再加10mL100%甲醇按上述重复萃取1次,两次得到的上清液用100%甲醇定容至25mL,摇匀静置30min。提取液用孔径为0.22μm的滤膜过滤后,进行UPLC分析。
1.5 方法学考察
1.5.1 精密度试验
分别取进口血竭和国产血竭供试品各一批,按“1.4”项下方法制备供试品溶液,按“1.3”项下色谱条件进样分析6次,记录色谱图,将数据导入“中药色谱指纹图谱相似度评价系统(2012版)”,以各自活险成分为参照峰,计算各共有峰阳对峰面积的RSD和相对保留时间的RSD。
1.5.2 重复性试验
分别取进口血竭和国产血竭供试品各一批,按“1.4”项下方法平行制备6份供试品溶液,按“1.3”项下色谱条件进样分析,记录色谱图,以各自活胜成分为参照峰,计算各共有峰相对峰面积的RSD和相对保留时间的RSD。
1.5.3 稳定性试验
分别取进口血竭和国产血竭供试品各一批,按“1.4”项下方法制备供试品溶液,在0、2、4、8、16、24 h按“1.3”项下色谱条件进样分析,记录色谱图,以各自活性成分为参照峰,计算各共有峰相对峰面积的RSD和相对保留时间的RSDo
1.6 指纹图谱建立及相似度评价
1.6.1 共有峰及参照峰的选择
根据5批进口血竭和5批国产血竭的UPLC色谱图,进口血竭发现9个共有峰,选择,号峰作为参照峰。国产血竭发现7个共有峰,选择7号峰作为参照峰,构建进口血竭和国产血竭UPLC色谱图特征指纹图谱,以此作为它们鉴别的依据。
1.6.2 相似度计算及对照指纹图谱的生成
经UPLC检测得到5批进口血竭和5批国产血竭指纹图谱,见图1。将5批进口血竭和5批国产血竭样品指纹图谱分别导入中药色谱指纹图谱相似度评价系统,分别设置样品RDD-1、RDC-1图谱为参照图谱,对照图谱生成方法采用中位数法,时间窗宽度为0.1,自动匹配,生成对照指纹图谱,与5批进口血竭和5批国产血竭图谱进行比较,进行相似度计算。
1.7 聚类分析和主成分分析
将标准化的数据聚类分析和主成分分析前将。选择第一和第二个主分量绘制主成分分析的散点图。聚类分析采用组间平均连接方法,用平方欧式距离来测量观测距离矩阵。使用SPSS软件(IBM SPSS Statistics 25,Armonk,USA!对所有样本进行聚类分析和主成分分析。
2 结果
2.1 检测波长的选择
紫外波长扫描用光电二极管阵列(PDA)探测器在280nm波长下对目标峰具有较高的信噪比,选择其作为检测波长。
2.2 流动相的选择
本研究采用0.1%甲酸乙腈-0.1%甲酸水溶液作为流动相,具有良好的分辨率、适中的停留时间和平滑的基线。
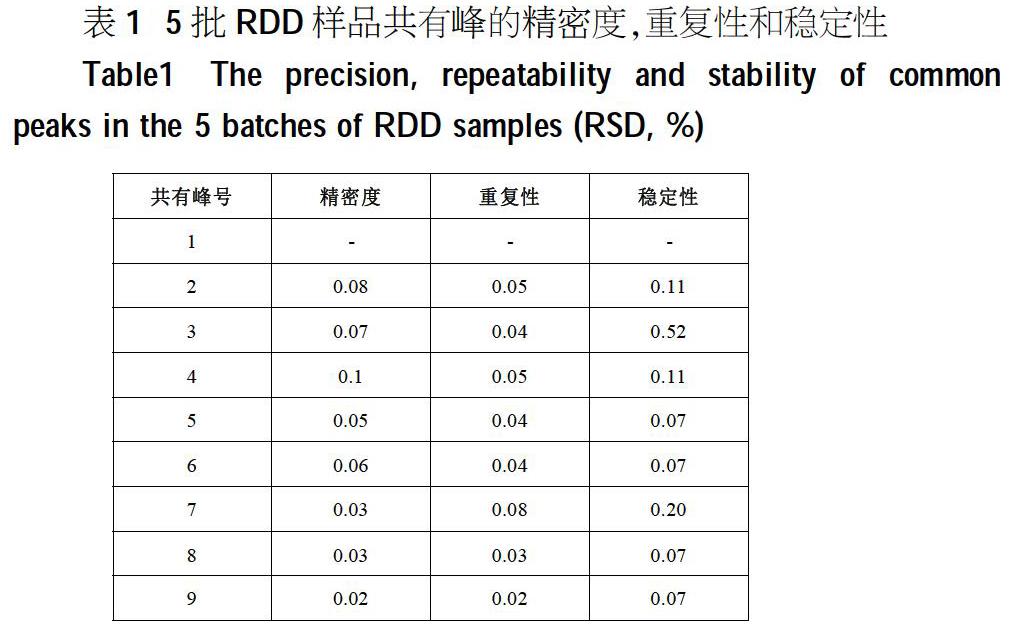
2.3 精密度、重复性和稳定性
运用稳定性、精密度和重复性试验,对本方法的进行综合验证,结果为表1和表2。通过在仪器中用相同样品注射六次来评估该方法的精确度。相对保留时间RRT为单个峰的保留时间与参考峰的保留时间之比。相对峰面积(RPA)为单个峰的保留峰面积与参考峰的保留峰面积之比。进口血竭RRT的RSD小于0.10%;国产血竭RRT的RSD小于0.02%。该方法可认为是可靠的。对同一个样品进行提取6次,来评估该方法的重复性。进口血竭RRT的RSD值小于0.09%,国产血竭RR丁的RSD值分别为小于0.07%,表明该方法具有较高的重现性。在24小时稳定性试验中,将相同的样品分别在0、2、4、8、16和24小时进行分析。进口血竭RRT的RSD值小于0.08%,国产血竭RRT的RSD值小于0.17%。结果表明,样品溶液在24小时内稳定。这些数据表明UPLC方法适用于血竭的定性和定量分析。
2.4 相似度分析
采用所建立的方法对10批血竭样品进行了分析,得到了U-PLC指纹图谱。在所有分析的进口血竭样品中发现9个共有峰,国产血竭样品中发现7个共有峰。用中药色谱指纹图谱相似度评价系统(2012年版)分别计算进口血竭9个共有峰和国产血竭7个共有峰的相对保留时间(RRT)和相对保留面积(RPA),结果总结在表3和表4。进口血竭RRT的RSD值略微波动在0.04-0.17%的范围内,RSD值小于0.17%;而国产血竭RRT的RSD值略微波动在0.02-0.06%的范围,RSD值小于0.06%,证明了两者指纹图谱分析的准确性。进口血竭RPA的RSD值在32.78-79.43%范围,国产血竭RPA的RSD值在22.39-66.31%范围,两者波动均较大,说明不同产地的进口血竭樣品里面的化学成分含量相差较大,国产血喝亦然。
图1为10批血竭样品的指纹图谱,表5是进口血竭和国产血竭的相似度分析。进口血竭5个样本的相似度为0.919-0.987范围内,国产血竭5个样本的相似度为0.886-0.984范围内,表明各批次进口血竭和国产血竭质量相对稳定。
2.5 主成分分析
将相似度评价系统计算的共有峰的相对峰面积代入主成分分析,进口血竭样品和国产血竭样品通过散点图进行区分(图2)。RDD-1、2、5和RDD-3、4各自分布得比较相近,而RDC-1、2、5和RDC-3、4各自分布得比较靠近,原因可能是不同来源的同种血竭的成分不同而导致的。
而且进口血竭主要分布在散点图的左上相限区域(RDD-1~RDD-5),国产血竭主要分布在右下相限区域(RDC-1~RDC-5),因此可以明显得出进口血蝎和国产血竭的成分具有明显差异,分成两组。
3 讨论
5批进口血竭样品和5批国产血竭样品的相似度都比较相近,所以能分别体现出5批血竭是同种血竭。
而进口血竭和国产血竭的RRT的RSD值都比较小,能表现不同批次的同种血竭具有大部分相同的化学成分,它们的指纹图谱均比较准确。进口血竭和国产血竭的RPA的RSD值分别的差异比较大,所以不同来源的同种血竭含有化学成分的含量明显不同。因此,本研究提出的指纹图谱方法适用于两种药物的种间鉴定和种内一致性评价。进口血竭和国产血竭具有的药理作用有相同也有不同,而且对于相同的药理作用药效也有差异,况且它们的外观相近,难以鉴别,所以开发一种中药指纹图谱方法来鉴定这两种药物不可或缺。中药指纹图谱技术是符合中医理论及现状的较好的质量控制技术,它以指标性成份峰作为标记,结台非指标成份进行比对,用来综合评价药物质量,既符合中医药理论的整体观点,也满足了对中药质量的可控、保证其疗效的要求。因此,中药指纹图谱不仅是一种中药质量控制模式和技术,更可以发展成为一种采用各种指纹图语来进行中药理论(复杂系统)和新药开发的研究体系和研究模式。
本研究UPLC指纹图谱方法的建立为进口血竭和国产血竭的质量控制奠定了坚实的基础,为血竭质量评价和标准化提供有价值的参考。
参考文献:
[1]李枫,张蓓蕾。活血圣药—血揭研究综述[J].上海医药,1998,19(8):33-34.
[2]中国药典委员会,2015.中国药典,I部[M],化学出版社,北京,pp.133.
[3]中华本草编委会,1999.中华本草,第8卷[M],上海科技出版社,上海,pp.455-458.
[4]王兰珍,王继永,张燕,于海群,刘勇.血竭植物资源开发利用现状[J].时珍国医国药,2007,18(4):1017-1019.
[5]GuPta D,Bleekley B,Gapta RK.Dragons Blood:Botany,chemistry and therapeutic uses[J].Journalof Ethnopharmacology,2008,115:361-380.
[6]吴平,杜青云.血竭的化学成分与临床应用研究进展[J].海峡药学,2000,12(2):1-2.
[7]Xie PS,Chen SB,Liang YZ,Wang XH,Tian RT,UptondR,2016.Chromatographic fingerprint analysis-arational approach for quality assessment oftraditional Chinese herbal medicine[J].Journal ofChromatography n,1112:171-180.
[8]姚令文,刘燕,郑笑为,戴忠,汪棋,马双成.指纹图谱、特征图谱技术在中药材和中成药中的应用[J].中国新药杂志,2018,27(8):934-939.
[8]孙国祥,孙万阳,张晶,侯志飞,杨方良,李显林,胡延雷,王述东,吴莎.中药质量一致性评价体系-基于定量指紋图谱检查的中药标准制剂控制模式的解析[J].中南药学,2018,16(1):2-13.
[10]Coviadarajaa R,Tejas V,Pushpangadan P.High-performance liquid chromatography(HPLC)as atool for standardization of complex herbal drugs[J].Journal of AOAC International,2019,102(4):986-992.
[1]]崔建蓉.血竭的药理作用、临床作用研究.四川生理科学杂志,2004,26(3):136-137.
[12]付梅红,方婧,王祝举,唐力英,杨洪军,李文,杨雪燕,黄璐琦.血揭药理研究与临床应用概述[J].时珍国医国药,2010,21(6):1498-1500.
[13]王俊,刘霞,孙伟,汪波,李丹平,樊佳佳,张晓存,陈士林.名贵中药材血揭的DNA条形码鉴定研究[J].中国药学杂志,2015,50(15):1261-1265.
[14]邹纯才,鄢海燕.我国中药色谱指纹图谱相似度评价方法30年(1988—2017年)研究进展与展望[J].中国中药杂志,2018,43(10):1969-1977.
[15]Coodarzi M,Russell PJ,Vender Heyden Y.Similarity analyses of chromatographicherbal fingerprints:a review[J].Anal ChimActa.2013,804:16-28.
[16]余一鸣,胡永慧,韩立云,刘素香,陈常青.中药质量控制的研究进展[J].中草药,2017,48(12):2557-2563.
基金项目:本课题为四川省科技计划项目应用基础研究项目(2018JC0445),药食同源植物资源开发四川省高校重点实验室开放基金重点项目(10Y201810),乐山市科技局产学研合作项目(15CXY0012)和2018年乐山职业技术学院院级课题(KY2018005)阶段性成果。
作者简介:魏荷琳(1987.01-),女,汉族,讲师,硕士研究生,现从事中药相关专业教学、科研工作。

