水铝钙石吸附水中F-影响因素及动力学研究
许昶雯, 何孟杰, 张 进, 张 磊
(1.滁州学院土木与建筑工程学院;2.中国人民解放军66220部队,安徽滁州 239000)
0 引言
水资源短缺是目前人类面临的重大问题,其中水质型缺水问题是导致水资源短缺的关键原因.2016年,国家环保部门针对地下水、地表水等进行水质监测,评价结果显示:氟化物为主要超标物质之一[1],远超《生活饮用水卫生标准》(GB5749-2006)[2]中对氟化物规定的1 mg/L的限制.氟作为人体内不可缺少的微量元素,对人体的生长发育有一定的促进作用[3],但当人体摄入过量的氟时,会引起氟斑牙或氟骨病,甚至导致氟中毒[4].而人体内的氟离子80%来自日常饮用水中[5],因此保证饮用水氟离子达标是人体健康的重要防线.
目前,在针对去除F-的方法中,化学吸附法因操作简便、不会二次污染而广受应用[6,7].类水滑石(HTLCs)作为常用的阴离子吸附剂,得到了广泛研究与应用[8-10],作为同是阴离子黏土的水铝钙石相比类水滑石是一种新型无机吸附材料[11],其在水处理领域中逐渐成为研究热点.因此本文将利用水铝钙石作为吸附剂,围绕其对水中F-的影响因素展开研究,并进行动力学拟合分析,探究其对F-的吸附性能,为阴离子黏土作为吸附剂在控制离子型污染应用方面拓宽道路.
1 材料与方法
1.1 试剂与仪器
1.1.1 实验试剂
水铝钙石(邵阳天堂助剂化工有限公司)、纯氟化钠(天津市北辰方正试剂厂)、冰乙酸、氢氧化钠(天津市恒兴化学试剂制造有限公司)、氯化钠(天津市化学试剂批发公司)、环己二胺四乙酸(天津市大茂化学试剂厂).
1.1.2 实验仪器
FA1004型电子天平(上海舜宇恒平科学仪器有限公司)、HJ-3型恒温磁力加热搅拌器(天津滨海新区大港红杉实验设备厂)、THZ-C型恒温振荡器(太仓市实验设备厂)、PF-1C型氟离子选择电极(上海越磁电子科技有限公司)、SX2-4-10型马弗炉(天津市中环实验电炉有限公司).
1.2 实验前期准备
1.2.1 F-标准曲线
参考《水和废水监测分析方法(第四版)》中的离子选择电极法[12]进行F-标准曲线的测定,绘制E(mV)-lgCF-(mg/L)标准曲线如图1所示.
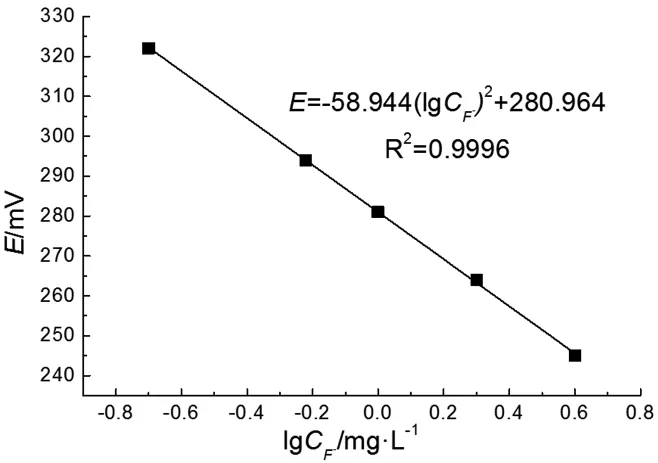
图1 氟离子标准曲线
1.2.2 模拟含氟废水的配制
用NaF试剂配制含氟废水,其中F-浓度为10 mg/L.
1.3 实验及分析方法
1.3.1 焙烧温度对F-吸附率的影响
投加12 g·L-1的经不同温度焙烧后的水铝钙石至配置好的50 mL含氟废水中,保持温度20℃,转速200 r·min-1,放置恒温振荡器中反应3 h.反应结束后固液分离,测定上清液中F-浓度,计算F-吸附率,研究焙烧温度对F-吸附率的影响.
1.3.2 吸附剂投加量对F-吸附率的影响
分别投加不同质量的经500℃焙烧后的水铝钙石至配置好的50 mL含氟废水中,保持温度20℃,转速200 r·min-1,放置恒温振荡器中反应3 h.反应结束后固液分离,测定上清液中F-浓度,计算F-吸附率,研究吸附剂投加量对F-吸附率的影响.
1.3.3 反应时间对F-吸附率的影响
投加12 g·L-1经500℃焙烧后的水铝钙石至配置好的50mL含氟废水中,保持温度20℃,转速200r·min-1,放置恒温振荡器中反应3 h,分别记录不同反应时间下上清液F-浓度,计算F-吸附率,研究反应时间对F-吸附率的影响.
1.3.4 转速对F-吸附率的影响
投加12 g·L-1经500℃焙烧后的水铝钙石至配置好的50 mL含氟废水中,保持温度20℃,放置恒温振荡器中在不同转速下反应3 h,反应结束后固液分离,测定上清液中F-浓度,计算F-吸附率,研究转速对F-吸附率的影响.
1.3.5 分析方法
实验结束后混合液经0.45 μm滤膜过滤进行固液分离,采用氟离子选择电极法测定F-浓度,依据下列公式计算吸附率和吸附量:
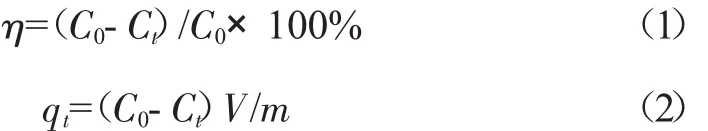
式中:η为吸附效率,%;qt为吸附反应t时刻时吸附量,mg/g;C0为 F-初始浓度,mg/L;Ct为吸附反应 t时刻时F-浓度,mg/L;V为溶液体积,L;m为水铝钙石质量,g.
2 结果与分析
2.1 水铝钙石焙烧温度对F-吸附率的影响
水铝钙石焙烧温度对F-吸附率的影响如图2所示.由图2可知,当焙烧温度从100℃升至500℃时,F-吸附率由82.37%提高到91.75%.这是由于随着焙烧温度的提高,水铝钙石层状结构逐渐形成,对F-吸附率不断提高,当焙烧温度达到500℃左右时,层状结构较为稳定,吸附效果最好.然而当焙烧温度进一步升高至700℃时,F-吸附率下降至78.67%,水铝钙石层状结构被破坏而形成尖晶石,稳定性变弱,吸附能力下降.本实验结果与相关文献[13]的报道是一致的.

图2 焙烧温度对吸附率的影响
2.2 水铝钙石投加量对F-吸附率的影响
水铝钙石投加量对F-吸附率的影响如图3所示.由图3可知,当水铝钙石投加量由0.2 g·L-1增加到2 g·L-1时,F-吸附率由42.37%提高至88.76%.之后,随着水铝钙石的继续投加,F-吸附率上升缓慢,当投加量达到6 g·L-1后,F-吸附率趋于平缓.这是由于当水铝钙石投加量较小时,F-被吸附进入吸附剂层间,层间吸附位点较多,吸附率增长较快,当投加量大于6 g·L-1后,空白吸附位点减少,吸附反应逐渐达到饱和.

图3 投加量对吸附率的影响
2.3 反应时间对F-吸附率的影响
反应时间对F-吸附率的影响如图4所示.由图4可知,当反应开始10 min时,吸附率已经达到82.57%,说明该反应为快速反应.此后在反应60 min内,吸附率快速上升,达到93.25%.60 min之后,由于溶质在吸附剂表面的吸附和脱附是同时进行,F-吸附率随时间增加趋缓,逐渐趋于平稳.

图4 反应时间对吸附率的影响
2.4 转速对F-吸附率的影响
转速对F-吸附率的影响图5所示.由图5可知,转速对F-吸附率基本没有影响,在不同转速下,F-吸附率维持在95%左右.因此,可判断出转速并不是影响F-吸附率的关键因素.

图5 转速对吸附率的影响
2.5 吸附动力学
吸附动力学是对吸附量随反应时间变化的深入研究,通过吸附动力学模型拟合可以得知整个反应的吸附速率,反映材料的吸附性能,据此研究吸附材料的吸附机理[14].动力学方程是表示吸附速率与吸附质浓度等参数之间的关系,本文采用拟一级、拟二级和层间扩散模型对水铝钙石吸附F-过程进行动力学描述.其中,拟一级动力学模型描述的是吸附速率与吸附质浓度变化值之间的正比例关系[15],表达式如式(3)所示;拟二级动力学模型是假设吸附为化学吸附过程,涉及化学共价键和氢键的构建过程[16],表达式如式(4)所示;层间扩散模型方程如式(5)所示.

式中:qt为t时刻水铝钙石对F-的吸附量(mg/g);k1为拟一级动力学速率常数(min-1);k2为拟二级动力学速率常数(g/(mg·min));kF为层间扩散速率常数(mg/(g·min1/2)).

图6 水铝钙石吸附F-拟一级和拟二级动力学模型
水铝钙石吸附F-拟一级和拟二级动力学模型如图6所示,模型拟合参数如表1所示.由图6和表1拟一级和拟二级动力学参数对比分析可知,水铝钙石吸附F-过程与拟二级动力学模型更加拟合,表明整个吸附过程主要表现为化学吸附,吸附反应主要为F-进入水铝钙石层间,发生化学反应形成化学键,恢复水铝钙石的层状结构.

表1 拟一级和拟二级动力学模型参数
层间扩散动力学模型如图7所示.由图7可知,水铝钙石吸附F-过程并非直线,表明整体反应过程由多个阶段组成,基本分为两个阶段进行.第一个阶段直线比较陡,反应较快,表现为F-从溶液中扩散到水铝钙石表面的过程;第二个阶段直线较缓,反应较慢,表现为吸附剂内部扩散阶段,最终逐渐趋于平衡.
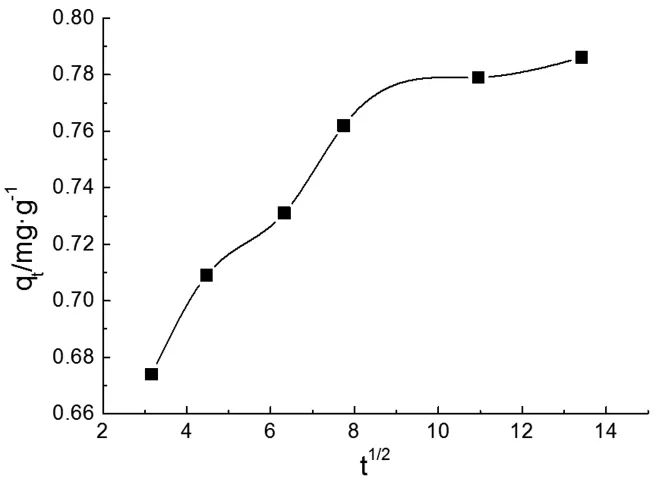
图7 水铝钙石吸附F-的层间扩散动力学模型
3 结论
3.1 随水铝钙石焙烧温度的升高,F-吸附率先提高后降低,当焙烧温度为500℃时,F-吸附率达到最高.表明在一定温度范围内,随着焙烧温度的升高,水铝钙石层状结构生成并逐步稳定,有助于吸附过程,吸附效果达到最好;但随着焙烧温度的继续升高,层状结构破坏,吸附效果下降.
3.2 F-吸附率随水铝钙石投加量和反应时间的增加而增大,直至达到平衡;而转速对F-吸附率影响不大.
3.3 经动力学拟合得知:水铝钙石吸附F-过程更加符合拟二级动力学模型,吸附过程主要为化学吸附,主要表现为F-进入水铝钙石层间构成化学键.

