肠壁囊样积气症的多层螺旋CT表现及其诊断价值
荣冰水,张 莉
肠壁囊样积气症(pneumatosis cystoides intestinalis,PCI),又称肠道气囊肿症、囊性淋巴积气症,是一种临床少见的与各种胃肠和非胃肠疾病相关的消化道疾病,其影像学特征为分布于消化道肠壁肌层或黏膜下和(或)浆膜下多发积气影[1]。由于其临床表现及体征缺乏明显特异性,容易被漏诊或误诊。多层螺旋CT(multisliecs helieal CT,MSCT)薄层扫描对病变定位、定性诊断有较高价值,并且能够清晰显示邻近脏器及周围脂肪间隙的变化,对PCI的诊断具有很高的准确率[2]。本研究回顾性分析21例PCI的临床表现及MSCT资料,探讨PCI的MSCT临床价值,以提高对该疾病的认识,减少误诊、误治。
1 对象与方法
1.1 对象 收集2008-01至2020-01于我院诊治的PCI患者共21例,均经肠镜诊断证实。患者年龄44~85岁,平均67.4岁,其中男13例,女8例。病程2.0 d~1.5个月。临床表现:7例腹胀不适、间断隐痛且自行缓解就诊;2例因恶心、呕吐就诊;8例停止排气、排便,肠梗阻就诊;结肠多发息肉结肠镜切除术后和输尿管结石碎石后出现隐痛各2例就诊。8例伴有高血压、高血脂病,6例伴有糖尿病,1例合并慢性支气管炎,3例合并胆囊结石,2例合并输尿管结石,2例结肠多发息肉。
1.2 方法 21例中,单纯MSCT平扫8例,MSCT平扫+增强13例,均使用Discovery CT GS(美国GE公司)行腹部扫描。患者取仰卧位,足先进,深吸气后屏气扫描,范围为膈顶至耻骨联合上缘。对比剂碘海醇(300 mgI/ml),采用高压注射器经肘前静脉团注对比剂,触发扫描模式(腹主动脉近端阈值100 Hu)启动动脉期扫描。参数选择:平均管电压120 kV,自动管电流调制,螺距1.375 ∶1,扫描视野50 cm,显示视野25 cm。重建采用标准算法,重建层厚、层间距均为1.25 mm,常规窗位/窗宽(40 Hu/250 Hu),腹膜窗窗位/窗宽(-10 Hu/300 Hu),对比剂流速3.0 ml/s,剂量1.5 ml/kg。获得图像传至工作站,进行MRP及MIP重建对图像分析。
1.3 纳入及排除标准 所有纳入病例的MSCT及结肠镜检查资料均由高级职称影像医师和消化科医师进行分析,MSCT采用腹膜窗或肺窗观察病变,分析病变累及肠段范围、发生部位、形态、数量、密度、有无腹腔游离气体。MSCT随访检查肠曲周围含气多房性透亮区和(或)游离气体消失,患者临床症状消失。排除消化道穿孔、缺血性肠病壁内积气、结肠多发憩室等疾病。
2 结 果
2.1 一般情况 21例均有腹部不适症状,4例有过结肠息肉切除或碎石病史。肠壁周围积气及腹腔游离气体均被MSCT检出,MSCT明确诊断肠壁囊样积气症7例(33.3%,图1),均经非手术治疗后治愈。13例伴有腹腔游离气体,其中10例误诊为消化道穿孔(图2),余4例被误诊为盲肠憩室炎伴感染穿孔、末端回肠炎伴穿孔等,可能与放射科医生对该病认识不足,没有认真结合临床及体征进行影像全面分析有关,其中3例进行剖腹探查手术。

图1 肠壁积气症典型CT影像(女,81岁)

图2 肠壁积气症误诊为消化道穿孔(女,68岁)
2.2 PCI发作部位及分布 病变位于小肠5例,升结肠及盲肠4例,升结肠及横结肠3例,横结肠2例,乙状结肠7例, 浆膜下型6例,黏膜下型5例,混合型10例。
2.3 主要CT表现 混合型肠腔内外可见多个含气低密度影(图1B),浆膜下型均表现肠腔外单个、多个类圆形空泡影,部分呈簇状,大小不一(图3)。黏膜下型表现肠腔内沿肠壁单个、多个呈“串珠样”排列、条带状或环形的低密度气体影,部分可见肠壁分离,呈“双层征”(图4)。合并游离气体的腹腔脂肪间隙清晰,内可见点、片状低密度影。可合并肝内静脉、门静脉、肠系膜上静脉、脾静脉内积气。
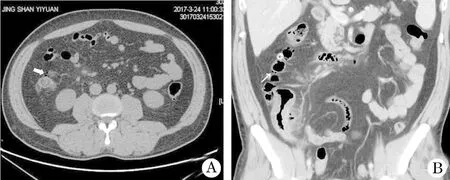
图3 肠壁积气症浆膜下型CT影像

图4 肠壁积气症黏膜下型CT影像
3 讨 论
3.1 一般特征 PCI最早在尸解标本中被描述,分为原发性与继发性,原发性(15%)少见,绝大多数为继发性(85%),病变可累及部分或全部消化道,可出现在肠系膜、网膜和肝胃韧带中,主要发生于小肠和结肠,以结肠多见[3]。本组病例结肠受累占76.2%(16/21),1例累及肠系膜上静脉、脾静脉、门静脉。PCI根据肠壁积气分布不同可分为3型:Ⅰ型(浆膜下型)、Ⅱ型(黏膜下型)和Ⅲ型(混合型)[4]。该疾病可发生于新生儿到老年人任何年龄阶段,以30~60 岁较为多见,男性多于女性[1],本组病例男性占61.8%(13/21)。我国甘肃、青海、新疆等地报道病例数最多,其他为全国散在病例,提示可能与地理环境及饮食习惯有关[5,6],近几年报道病例增多,可能与CT机及结肠镜普及应用、放射科和临床医师对本病认识提高有关。
3.2 发病机制 PCI的发病机制尚不清楚,但一些原因已形成学说,如机械损伤学说、肺源性学说、细菌学说、生化性学说等。没有一种学说能够独立解释PCI发生的所有病理过程,如肺源性学说无法解释气囊肿中氢气的来源,细菌学说不能解释患者为什么少有腹膜炎、发热等炎性反应,生化性学说缺乏理论说明何原因导致淋巴管扩张[7]。目前机械损伤学说被多数研究者接受,即在幽门及肠道梗阻、严重便秘、肠胃溃疡、胃肠道准备、手术及胃结肠镜检查等损伤肠黏膜或肠腔内压力增高的情况下,气体通过受损黏膜,引起肠壁黏膜内积气。
3.3 临床症状 有研究者认为,PCI不是一种单独的疾病而是一种症状,它和全身的临床疾病状态息息相关,本组病例腹胀不适7例,恶心呕吐2例,停止排便排气8例,肠镜及碎石后腹痛各2例,均可造成肠腔压力增高和(或)黏膜受损。继发性PCI主要表现为原发病症状,常见的疾病有消化道疾病、慢性肺部疾病、自身免疫性疾病。PCI临床缺乏特异性,本身无特殊症状,可表现为腹胀、腹痛、呕吐、腹泻、便秘、血便、里急后重、吸收不良等[1],约3%可出现严重并发症肠梗阻、肠扭转、肠套叠、肠穿孔等,病死率约为85%[8,9]。本组1例合并肝静脉、门静脉、肠系膜上静脉、脾静脉积气,报道罕见,可能是肠黏膜损伤,气体进入门脉系统所致。
3.4 影像学诊断 目前,PCI诊断主要依靠影像学及结肠镜、超声肠镜等检查,X线平片、X线钡餐、内镜可以检测在肠壁黏膜下气体囊肿,具有局限性,不能很好显示病变全貌,不能全面评估病变。MSCT的空间及密度分辨率较高,利用多层面重建后处理技术,即使扫描前没有做肠道准备,在显示肠腔、肠壁及壁外系膜、淋巴结、周围脂肪间隙方面,以及显示病变的大小、形态及累及范围,区分腹腔游离气体与PCI病变内气体等均有较大优势,对定位、定性具有更大价值。MSCT被认为是PCI检查的首选方法[10,11]。
典型的CT表现:沿肠曲轮廓散在分布的含气多房性透亮区,形态不一,可呈“串珠样”“簇状”“蜂窝状”气体影,凸向腔内或腔外,气体较多时,在黏膜下和(或)浆膜下可见条形、线样及环形气体影,肠内容物位于肠道中央呈悬浮样,可见肠壁分离征。破裂时,腹腔脂肪间隙清晰,可见散在气体影,即出现无痛性气腹征象。CT不仅能够准确判断肠壁积气分型,发现腹腔游离气体,还能提示邻近肠壁及腹膜是否增厚、周围脂肪间隙清晰程度、肠管扩张、腹腔积液、门静脉气栓等征象,对判断病因、鉴别诊断、严重并发症,甚至对患者潜在危险程度进行综合评估。
发现肠壁积气和(或)腹腔游离气体需要排除消化道穿孔、缺血性肠病壁内积气、结肠多发憩室等疾病。消化道穿孔,常伴随肠液外溢,周围脂肪间隙模糊,腹膜炎症状明显,局部胃肠壁增厚、水肿;PCI游离气腹时,无肠液外渗,无腹膜刺激征,而且游离气体明显多于消化道穿孔[12]。多发结肠憩室,多表现为突出肠道轮廓外密度不均的软组织密度影/肠壁外凸的小圆形含气影,合并感染时周围脂肪间隙密度增高,可见索条影,局限肠壁增厚,部分憩室内可见钙化灶/粪石。缺血性肠病肠壁积气,为肠壁坏死的特异征象,往往发生于晚期,肠壁内点状或细线样气体密度影,无明确囊壁,急腹症表现明显,常伴有胃肠壁节段性增厚、门静脉系统积气及栓塞,必要时增强扫描进行全面观察[13]。
3.5 治疗及预后 PCI属于良性自限性罕见疾病,诊断明确无特殊治疗[1,14,15],无症状者可临床观察,出现腹痛、肠胃胀气、食欲不振、梗阻、腹泻等症状,可行吸入性或高压氧治疗。
本组21例中7例结合临床及典型影像表现明确诊断后,经非手术治疗后治愈。本组误诊率高达66.7%(14/21),与文献[16]报道基本一致,可能因本病少见,放射科及临床医师对本病缺乏认识,诊断思维局限于常见病,是造成误诊漏诊主要原因;未认真分析病史、体征是造成误诊漏诊的次要原因。

